Главное
«Вьюити» (Vuity, пилокарпин) — новый лекарственный препарат, предназначенный для терапии пресбиопии у взрослых.
«Вьюити», разработанный «Аллерган» (Allergan), принадлежащей «ЭббВи» (AbbVie), одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA).
30-дневный курс глазных капель «Вьюити» обойдется американскому пациенту в 86 долларов. Расходы придется возмещать из собственного кармана, поскольку «Вьюити» вряд ли получит страховое покрытие, так как в нем нет медицинской необходимости ввиду более дешевой альтернативы в виде очков.
«Вьюити» окажется востребованным среди людей, которых не устраивает, что приходится целый день то надевать очки для чтения, то снимать их, если, к примеру, по работе необходимо постоянно переключаться между ближним и дальним зрением.
«Вьюити» справляется с легко-умеренной тяжестью пресбиопии, препарат менее эффективне при возрасте после 65 лет. «Вьюити» следует использовать с осторожностью при вождении автомобиля ночью или выполнении опасных работ при плохом освещении. Могут также возникнуть некоторые проблемы со сменой фокуса между ближним и дальним зрением. Контактные линзы должны быть сняты перед применением «Вьюити», а затем вновь надеты по истечении 10 минут после закапывания препарата.

Что такое пресбиопия
Пресбиопия («старческое зрение», возрастная дальнозоркость, старческая дальнозоркость) — это физиологическая недостаточность аккомодации, связанная со старением глаза, которая приводит к постепенному ухудшению способности четко фокусироваться на близких объектах. Пресбиопия, с которой сталкиваются люди старше 40 лет, настигает каждого четвертого жителя Земли. Состояние похоже на дальнозоркость (гиперметропию), которая начинается в детстве и проявляется симптомами размытости зрения на близком расстоянии.
Пресбиопия, будучи нормальной частью процесса старения, возникает из-за возрастных изменений хрусталика (снижение эластичности и повышение твердости) и силы ресничной мышцы глаза, в результате чего глаз, когда смотрит на близкие предметы, фокусирует свет позади, а не на сетчатке. Пресбиопия — один из видов аномалий рефракции наряду с близорукостью, дальнозоркостью и астигматизмом.
Пресбиопия может быть скорректирована при помощи очков, контактных линз, мультифокальных интраокулярных линз (искусственный хрусталик), а также рефракционной хирургии, изменяющей кривизну роговицы для более точной фокусировки света на сетчатке: кондуктивная кератопластика, лазерный кератомилёз in situ (LASIK), лазерная субэпителиальная кератэктомия (LASEK), фоторефракционная кератэктомия (PRK), линзы-вкладыши.
«Вьюити»: механизм действия пилокарпина при пресбиопии
Пилокарпин (pilocarpine, AGN-190584), реализованный в рецептуре глазных капель, — холинергический агонист мускаринового ряда, активирующий мускариновые рецепторы, расположенные на гладких мышцах, таких как круговая мышца радужной оболочки (сфинктер зрачка) и цилиарная (ресничная) мышца. Сокращение первой приводит к сужению зрачка, что улучшает остроту зрения вблизи и на среднем расстоянии при сохранении некоторой зрачковой реакции на свет. Сокращение второй переводит глаз в более близорукое состояние.
Ноу-хау «Вьюити» представлено оптимизированной рецептурой пилокарпина гидрохлорида (1,25%), доставляемого по технологии pHast, которая позволяет офтальмологическому раствору быстро адаптироваться к физиологическому pH слезной пленки в целях улучшения комфорта пациента, усиления лекарственной переносимости, минимизации затуманивания зрения.
Эффект «Вьюити», который начинает действовать уже через 15 минут после закапывания в глаза, продолжается до 6 часов, улучшая зрение вблизи и на среднее расстояние без влияния на зрение вдаль.
«Вьюити» и обычный пилокарпин: есть ли различия?
Пилокарпина гидрохлорид (pilocarpine hydrochloride) в виде офтальмологического раствора традиционно используется для лечения глаукомы. [1] Это один из самых старых методов лечения глаукомы, но из-за своих побочных эффектов пилокарпин не всегда хорошо переносится и в настоящее время не часто назначается при данном терапевтическом показании. [2] [3] [4]
Пилокарпин, будучи циклическим эфиром, весьма подвержен гидролизу при физиологическом pH. Для стабилизации пилокарпина в офтальмологическом растворе необходим низкий pH (~4). [5] Однако при низком pH пилокарпин протонирован или ионизирован, и потому плохо проникает через роговицу, [6] что ограничивает его биодоступность. [7]
Известно, что существующие лекарственные препараты, содержащие пилокарпин, при инстилляции капель вызывают боль в области бровей, головную боль, глазной дискомфорт, гиперемию и затуманивание зрения. Примеры дискомфорта, связанного с глазной поверхностью, который могут испытывать пациенты, включают жжение, щипание и раздражение. [3] [8] [9] [10] [11] [12] Исследования показали, что пилокарпин вызывал больше нежелательных явлений и чаще приводил к прекращению терапии по сравнению с другими вариантами лечения глаукомы. [9] [13] [14]. Пациенты также сообщали о более низком качестве жизни при использовании пилокарпина и более высоком предпочтении иного варианта лечения глаукомы. [13] Низкий рН офтальмологического раствора может быть причиной некоторых из этих побочных эффектов. [5]
Офтальмологический раствор пилокарпина в форме препарата «Вьюити» (Vuity) разработан с учетом вопросов с переносимостью пилокарпина так, чтобы быстро уравновешивать рН глазной поверхности, что, в свою очередь, увеличивает содержание неионизированного пилокарпина, улучшая его биодоступность [7] и снижая побочные эффекты, такие как глазной дискомфорт и помутнение зрения.
Пилотное клиническое испытание сравнило «Вьюити» с генерическим пилокарпином среди 5 пациентов с пресбиопией. Участникам закапывали «Вьюити» в один глаз, генерический пилокарпин во второй. Установлено, что среднее значение оценки нечеткого зрения при назначении «Вьюити» получилось статистически значимо ниже, чем при применении генерического пилокарпина.
Зафиксированы такие нежелательные явления, как глазное давление и/или боль, боль в области бровей, затуманивание зрения, жжение, зуд, повышенная светочувствительность. При этом все они, кроме одного случая давления и/или боли в глазу и одного случая боли в области бровей, были зарегистрированы при применении генерического пилокарпина. Согласно биомикроскопическому исследованию, средний показатель гиперимии конъюнктивы были ниже при назначении «Вьюити», чем генерического пилокарпина.
Анализ in vitro показал, что pH «Вьюити» быстрее достигает равновесия с физиологическим pH слезной пленки (~6,5), тем самым не нарушая ее целостности. Это объясняет лучшую переносимость, меньший офтальмологический дискомфорт и сниженное число нежелательных явлений.
За счет мгновенного повышения pH, быстро увеличивающего неионизированную долю пилокарпина на глазной поверхности, офтальмологическая биодоступность «Вьюити» существенно выше, чем у генерического пилокарпина. Это приводит к эффективной доставке препарата в передний сегмент глаза и способствует его длительному действию.
«Вьюити»: эффективность и безопасность пилокарпина при пресбиопии
Основные результаты
Эффективность и безопасность «Вьюити» были проверены в двух клинических испытаниях GEMINI 1 (NCT03804268) и GEMINI 2 (NCT03857542) фазы III (рандомизированных, двойных слепых, плацебо-контролируемых, многоцентровых), которые пригласили взрослых (40–55 лет) пациентов (n=750) с пресбиопией.
Участникам назначали плацебо или пилокарпин — по одной капле в каждый глаз один раз в день на протяжении 30 дней.
В обоих исследованиях доля пациентов, у которых мезопическая (при тусклом освещении) высококонтрастная бинокулярная скорректированная с учетом расстояния острота зрения вблизи (DCNVA) улучшилась на 3 и более строчки (по таблице LogMAR), причем без потери более чем 1 строчки (5 букв) скорректированной остроты зрения вдали (CDVA) при той же рефракционной коррекции, оказалась статистически значимо больше в группе пилокапина в сравнении с группой плацебо: 31% и 26% — против 8% и 11% (p<0,01). Оценка была проведена на 30-й день лечения по прошествии 3 часов после применения препарата.

- Следует понимать, что улучшение DCNVA минимум на 2 строчки указывает на значимое для пациента изменение остроты зрения, если исходить из ряда психометрических методов оценки, всесторонне учитывающих индивидуальное восприятие таких улучшений.
Среди наиболее распространенных побочных реакций на назначение пилокарпина, впрочем, редких: головная боль, гиперемия конъюнктивы, затуманенное зрение, боль в глазах, нарушение зрения, раздражение глаз, повышенное слезотечение.
Функциональное зрение на ближнем расстоянии
Назначение «Вьюити» привело к тому, что больше пациентов, чем в группе плацебо, вышли к статусу функционального зрения вблизи (DCNVA 20/40 или лучше). При этом пик эффективности лечения повышался по ходу терапии, а тахифилаксии (быстрое снижение терапевтического эффекта при повторном применении лекарственного средства, то есть развитие толерантности) не наблюдалось.
Так, в 1-й день лечения в группе «Вьюити» 73,9%, 82,4%, 87,5%, 77,7%, 71,0%, 72,1% и 66,5% пациентов достигли данного статуса — соответственно по прошествии 0,25, 0,5, 1, 3, 6, 8 и 10 часов после закапывания пилокарпина. В группе плацебо пропорции следующие: 58,6% (p<0,0001), 63,8% (p<0,0001), 68,0% (p<0,0001), 64,6% (p=0,0001), 63,3% (p=0,0264), 66,0% и 64,8%.
На 30-й день лечения в группе «Вьюити» 80,9%, 86,6%, 92,7%, 87,6%, 79,6%, 78,2% и 74,9% пациентов засвидетельствовали статус функционального зрения вблизи — соответственно по прошествии 0,25, 0,5, 1, 3, 6, 8 и 10 часов после закапывания пилокарпина. В группе плацебо пропорции следующие: 74,5% (p=0,0415), 77,1% (p=0,0011), 78,9% (p<0,0001), 75,2% (p<0,0001), 76,3%, 74,0% и 73,8%.
Тяжесть пресбиопии
Терапевтическая эффективность «Вьюити» коррелировала с исходной тяжестью пресбиопии. Так, при лечении препаратом «Вьюити» пациенты с более тяжелой формой пресбиопии с большей вероятностью начинали видеть большее число строчек, тогда как пациенты с менее тяжелой формой пресбиопии с большей вероятностью достигали функционального зрения вблизи (DCNVA 20/40 или лучше).
К примеру, по прошествии 1 часа после закапывания пилокарпина, когда терапевтическая эффективность достигала своего пика, пропорция испытуемых в подгруппе с исходной тяжестью пресбиопии 20/40 или лучше, показавших улучшение DCNVA на 1 и более строчек, составила 75,0%, тогда как при исходной тяжести 20/80 или хуже данная пропорция составила 93,2%. Улучшение DCNVA на 3 и более строчек оказалось справедливым для 24,7% и 59,6% пациентов — в подгруппах 20/50 и 20/100 соответственно.
По прошествии 1 часа после закапывания пилокарпина к статусу функционального зрения вблизи вышли 85,4%, 69,5% и 46,6% человек в подгруппах 20/50, 20/63 и 20/80 исходной тяжести пресбиопии. После 3 часов — 75,3%, 46,3% и 35,2%, после 6 часов — 62,9%, 37,8% и 20,5%.
Зрение на среднем расстоянии
«Вьюити» обеспечил улучшение зрения на среднем расстоянии, если исходить из дистанции в 66 см — той, на которой обычно происходит работа за компьютером.
Так, согласно показателю скорректированной с учетом расстояния остроты зрения на среднем расстоянии (DCIVA), которое было оценено на 30-й день лечения, назначение «Вьюити» привело к улучшению зрения на 7,7, 6,5, 4,8, 4,3 и 4,0 буквы (5 букв — 1 строчка) — соответственно по прошествии 1, 3, 6, 8 и 10 часов после закапывания пилокарпина. В группе плацебо результаты следующие: 3,3 (p<0,0001), 3,0 (p<0,0001), 2,9 (p<0,0001), 2,8 (p=0,0001) и 2,4 буквы (p<0,0001).
LASIK
«Вьюити» справился с улучшением остроты зрения вблизи у пациентов с пресбиопией, которые ранее прошли лазерную рефракционную хирургическую процедуру LASIK.
Так, на 30-й день лечения показатель DCNVA улучшился на 3 и более строчки у 16,7%, 38,9%, 41,7%, 37,8%, 16,2%, 13,9% и 8,3% пациентов в группе «Вьюити» — соответственно по прошествии 0,25, 0,5, 1, 3, 6, 8 и 10 часов после закапывания пилокарпина. В группе плацебо пропорции участников были следующими: 0,0% (p=0,0087), 2,6% (p=0,0001), 10,5% (p=0,0022), 5,1% (p=0,0005), 7,7%, 2,6% и 0,0%.
Указанное улучшение остроты зрения вблизи статистически значимо не различалось между лечившимися препаратом «Вьюити» подгруппами пациентов, ранее прошедших LASIK и не проходивших эту процедуру: 16,8%, 32,7%, 39,0%, 28,0%, 17,4%, 12,6% и 10,5%.
Опыт пациентов
В ходе опроса участников (n=125) клинических испытаний GEMINI выяснилось, что 76% получавших «Вьюити» прекратили пользоваться очками для чтения в пределах 10-часового терапевтического периода; 84% выразили уверенность, что будут применять «Вьюити», когда он поступит в продажу; 83% сообщили, что собираются закапывать пилокарпин не реже 5 дней в неделю.
Дополнительные материалы
Инструкция по медицинскому применению лекарственного препарата «Вьюити» (Vuity, пилокарпин) в США. [PDF]
Package insert / product label
Generic name: pilocarpine hydrochloride
Dosage form: ophthalmic solution
1. Indications and Usage for Vuity Eye Drops
VUITY® is indicated for the treatment of presbyopia in adults.
2. Vuity Eye Drops Dosage and Administration
The recommended dosage of VUITY is one drop in each eye once daily. A second dose (one additional drop in each eye) may be administered 3-6 hours after the first dose.
If more than one topical ophthalmic product is being used, the products should be administered at least 5 minutes apart.
3. Dosage Forms and Strengths
VUITY (pilocarpine hydrochloride ophthalmic solution) is a clear, colorless, sterile ophthalmic solution containing 1.25% (12.5 mg/mL) of pilocarpine hydrochloride.
4. Contraindications
VUITY is contraindicated in patients with known hypersensitivity to the active ingredient or to any of the excipients.
5. Warnings and Precautions
5.1 Blurred Vision
Miotics, including VUITY, may cause accommodative spasm. Patients should be advised not to drive or operate machinery if vision is not clear (e.g., blurred vision).
In addition, patients may experience temporary dim or dark vision with miotics, including VUITY. Patients should be advised to exercise caution in night driving and other hazardous activities in poor illumination.
5.2 Risk of Retinal Detachment
Rare cases of retinal detachment and retinal tear have been reported with miotics, including VUITY.
Individuals with pre-existing retinal disease are at increased risk. Therefore, examination of the retina is advised in all patients prior to the initiation of therapy.
Patients should be advised to seek immediate medical care with sudden onset of flashing lights, floaters, or vision loss.
5.3 Iritis
VUITY is not recommended to be used when iritis is present because adhesions (synechiae) may form between the iris and the lens.
5.4 Use with Contact Lenses
Contact lens wearers should be advised to remove their lenses prior to the instillation of VUITY and to wait 10 minutes after dosing before reinserting their contact lenses.
5.5 Potential for Eye Injury or Contamination
To prevent eye injury or contamination, care should be taken to avoid touching the dispensing bottle to the eye or to any other surface.
6. Adverse Reactions/Side Effects
The following clinically significant adverse reactions are described elsewhere in labeling:
- Hypersensitivity [see Contraindications (4)]
6.1 Clinical Trials Experience
Because clinical trials are conducted under widely varying conditions, adverse reaction rates observed in the clinical trials of a drug cannot be directly compared to rates in the clinical trials of another drug and may not reflect the rates observed in practice.
VUITY dosed once daily was evaluated in 375 participants with presbyopia in two randomized, double-masked, vehicle-controlled studies (GEMINI 1 and GEMINI 2) of 30 days duration. The most common adverse reactions reported in >5% of participants were headache and conjunctival hyperemia. Ocular adverse reactions reported in 1-5% of participants were blurred vision, eye pain, visual impairment, eye irritation, and increased lacrimation.
VUITY was also evaluated in 114 participants with presbyopia in a randomized, double-masked, vehicle-controlled 14-day study (VIRGO) in which participants received two doses of VUITY in each eye, 6 hours apart daily. The most common adverse reactions reported in >5 % of participants were headache and eye irritation. Ocular adverse reactions reported in 1-5% of participants were visual impairment, eye pain, blurred vision, and vitreous floaters.
6.2 Postmarketing Experience
The following adverse reactions have been identified during postapproval use of VUITY. Because these reactions are reported voluntarily from a population of uncertain size, it is not always possible to reliably estimate their frequency or establish a causal relationship to VUITY exposure.
Eye disorders: vitreous detachment, vitreomacular traction, retinal tear, retinal detachment.
8. Use In Specific Populations
8.1 Pregnancy
Risk Summary
There are no adequate and well-controlled studies of VUITY administration in pregnant women to inform a drug-associated risk. Oral administration of pilocarpine to pregnant rats throughout organogenesis and lactation did not produce adverse effects at clinically relevant doses.
Data
Human Data
No adequate and well-controlled trials of VUITY have been conducted in pregnant women. In a retrospective case series of 15 women with glaucoma, 4 patients used ophthalmic pilocarpine either pre-pregnancy, during pregnancy or postpartum. There were no adverse effects observed in patients or in their infants.
Animal Data
In embryofetal development studies, oral administration of pilocarpine to pregnant rats throughout organogenesis produced maternal toxicity, skeletal anomalies and reduction in fetal body weight at 90 mg/kg/day (approximately 485-fold higher than the maximum human ophthalmic dose [MHOD] of 0.03 mg/kg/day assuming administration of 2 drops/eye/day, on a mg/m2 basis).
In a peri-/postnatal study in rats, oral administration of pilocarpine during late gestation through lactation increased stillbirths at a dose of 36 mg/kg/day (approximately 195-fold higher than the MHOD). Decreased neonatal survival and reduced mean body weight of pups were observed at ≥18 mg/kg/day (approximately 100 times the maximum human ophthalmic dose of VUITY).
8.2 Lactation
Risk Summary
There is no information regarding the presence of pilocarpine in human milk, the effects on the breastfed infants, or the effects on milk production to inform risk of VUITY to an infant during lactation.
Pilocarpine and/or its metabolites are excreted in the milk of lactating rats. Systemic levels of pilocarpine following topical ocular administration are low [see Clinical Pharmacology (12.3)], and it is not known whether measurable levels of pilocarpine would be present in maternal milk following topical ocular administration.
The developmental and health benefits of breastfeeding should be considered along with the mother’s clinical need for VUITY and any potential adverse effects on the breastfed child from VUITY.
Data
Animal Data
Following a single oral administration of 14C-pilocarpine to lactating rats, the radioactivity concentrations in milk were similar to those in plasma.
8.4 Pediatric Use
Presbyopia does not occur in the pediatric population.
8.5 Geriatric Use
Clinical studies of VUITY did not include participants aged 65 and over to determine whether they respond differently from younger participants. Other reported clinical experience with ophthalmic pilocarpine solutions have not identified overall differences in safety between elderly and younger participants.
10. Overdosage
Systemic toxicity following topical ocular administration of pilocarpine is rare, but occasionally patients who are sensitive may develop sweating and gastrointestinal overactivity. Accidental ingestion can produce sweating, salivation, nausea, tremors and slowing of the pulse and a decrease in blood pressure. In moderate overdosage, spontaneous recovery is to be expected and is aided by intravenous fluids to compensate for dehydration. For patients demonstrating severe poisoning, atropine, the pharmacologic antagonist to pilocarpine, should be used.
11. Vuity Eye Drops Description
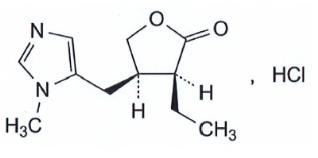
VUITY (pilocarpine hydrochloride ophthalmic solution) 1.25% is a cholinergic muscarinic receptor agonist prepared as an isotonic, clear, colorless, sterile ophthalmic solution containing 1.25% of pilocarpine hydrochloride. The chemical name for pilocarpine hydrochloride is (3S,4R)-3-ethyl-4-[(1-methyl-1H-imidazol-5-yl)methyl]oxolan-2-one hydrochloride. Its molecular weight is 244.72 and its molecular formula is C11H16N2O2 · HCl. Its structural formula is:
Each mL of VUITY contains pilocarpine hydrochloride 1.25% (12.5 mg) as the active ingredient, equivalent to 1.06% (10.6 mg) pilocarpine free-base. Preservative is: benzalkonium chloride 0.0075%. Inactive ingredients in the ophthalmic solution are: boric acid, sodium citrate dihydrate, sodium chloride, purified water, and may also include hydrochloric acid and/or sodium hydroxide for pH adjustment to between 3.5 and 5.5, if necessary.
12. Vuity Eye Drops — Clinical Pharmacology
12.1 Mechanism of Action
Pilocarpine hydrochloride is a cholinergic muscarinic agonist which activates muscarinic receptors located at smooth muscles such as the iris sphincter muscle and ciliary muscle. VUITY contracts the iris sphincter muscle, constricting the pupil to improve near and intermediate visual acuity while maintaining some pupillary response to light. VUITY also contracts the ciliary muscle and may shift the eye to a more myopic state.
12.3 Pharmacokinetics
Systemic exposure to pilocarpine was evaluated in 22 participants with presbyopia who were administered 1 drop of VUITY in each eye once daily for 30 days (GEMINI 1). The mean (SD) Cmax and AUC values from time 0 to last measurable concentration over 10-hour period post-last dose on Day 30 were 1.95 (0.98) ng/mL and 4.14 (2.16) ng·hr/mL, respectively. The median Tmax value on Day 30 was 0.3 hours postdose with a range from 0.2 to 0.5 hours postdose.
Systemic exposure to pilocarpine was also evaluated in 8 participants with presbyopia who were administered 1 drop of VUITY in each eye twice daily for 14 days (VIRGO). The Day 14 mean (SD) Cmax following first daily dosing was 1.81 (0.51) ng/mL and following second daily dosing was 2.12 (1.75) ng/mL. The Day 14 mean (SD) AUC over 6-hour post-dose following first daily dose was 4.35 (1.50) ng·hr/mL and following second daily dose was 4.22 (3.14) ng·hr/mL. There was no significant systemic drug accumulation over time, with accumulation index ratios between Day 1 and Day 14 based on AUC as 1.42 and 1.03 for the first and second daily dose, respectively.
13. Nonclinical Toxicology
13.1 Carcinogenesis, Mutagenesis, Impairment of Fertility
Carcinogenesis
Pilocarpine did not induce tumors in mice at any dosage level studied (up to 30 mg/kg/day; approximately 80-times the MHOD). In rats, an oral dose of 18 mg/kg/day (approximately 100 times the MHOD), resulted in a statistically significant increase in the incidence of benign pheochromocytomas in both male and female rats, and a statistically significant increase in the incidence of hepatocellular adenomas in female rats.
Mutagenesis
Pilocarpine did not show any potential to cause genetic toxicity in a series of studies that included: 1) bacterial assays (Salmonella and E. coli) for reverse gene mutations; 2) an in vitro chromosome aberration assay in a Chinese hamster ovary cell line; 3) an in vivo chromosome aberration assay (micronucleus test) in mice; and 4) a primary DNA damage assay (unscheduled DNA synthesis) in rat hepatocyte primary cultures.
Impairment of Fertility
Pilocarpine oral administration to male and female rats at a dosage of 18 mg/kg/day (100 times the MHOD) resulted in impaired reproductive function, including reduced fertility, decreased sperm motility, and morphologic evidence of abnormal sperm. It is unclear whether the reduction in fertility was due to effects on males, females, or both. In dogs, exposure to pilocarpine at a dosage of 3 mg/kg/day for 6 months resulted in evidence of impaired spermatogenesis (approximately 55 times the MHOD).
14. Clinical Studies
The efficacy of VUITY dosed once daily for the treatment of presbyopia was demonstrated in two 30‐Day Phase 3, randomized, double‐masked, vehicle‐controlled studies, namely GEMINI 1 (NCT03804268) and GEMINI 2 (NCT03857542). A total of 750 participants aged 40 to 55 years old with presbyopia were randomized (375 to VUITY group) in two studies and participants were instructed to administer one drop of VUITY or vehicle once daily in each eye.
In both studies, the proportion of participants gaining 3 lines or more in mesopic, high contrast, binocular distance corrected near visual acuity (DCNVA), without losing more than 1 line (5 letters) of corrected distance visual acuity (CDVA) with the same refractive correction was statistically significantly greater in the VUITY group compared to the vehicle group at Day 30, Hour 3 (see Table 1).
| GEMINI 1 | GEMINI 2 | |||||
| VUITY N=163 |
Vehicle N=160 |
p-value | VUITY N=212 |
Vehicle N=215 |
p-value | |
| Proportion of participants gaining 3-lines or more in mesopic DCNVA, without losing more than 1 line (5 letters) of CDVA at Day 30, Hour 3 | 31% | 8% | p<0.01 | 26% | 11% | p<0.01 |
Figures 1 and 2 present the proportion of participants who gained 3-lines or more in mesopic DCNVA at Day 30.
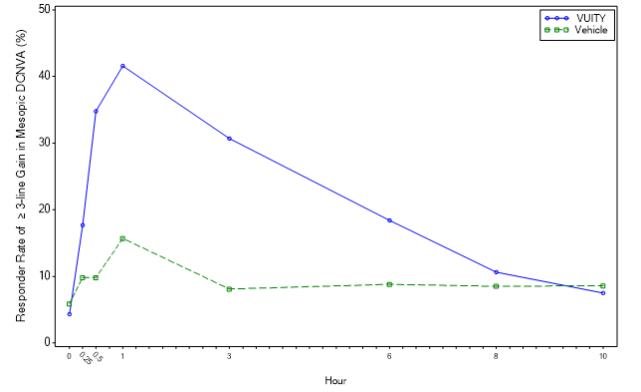
Figure 1: Proportion of Participants Achieving 3-Lines or More Improvement in Mesopic, High Contrast, Binocular DCNVA at Day 30 in GEMINI 1 (Intent-to-Treat Population)
| Timepoint | Hour 0 | Hour 0.25 | Hour 0.5 | Hour 1 | Hour 3 | Hour 6 | Hour 8 | Hour 10 |
| VUITY (%) | 4.3 | 17.7 | 34.8 | 41.6 | 30.7 | 18.4 | 10.6 | 7.5 |
| Vehicle (%) | 5.9 | 9.8 | 9.8 | 15.7 | 8.1 | 8.8 | 8.5 | 8.6 |
| Difference (95% CI) | -1.5 (-6.4, 3.3) | 7.9 (0.3, 15.5) | 25.0 (16.2, 33.8) | 25.9 (16.4, 35.5) | 22.5 (14.3, 30.8) | 9.7 (2.3, 17.0) | 2.1 (-4.4, 8.5) | -1.1 (-7.1, 5.0) |
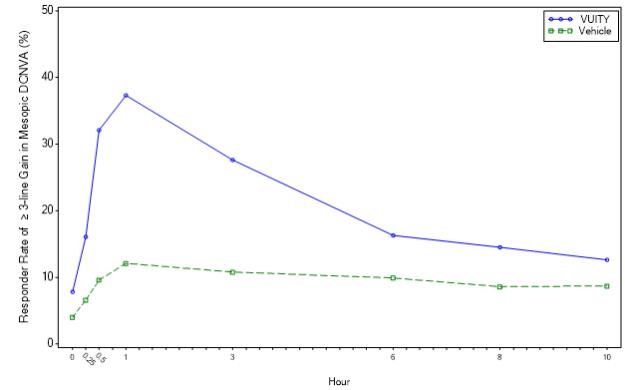
Figure 2: Proportion of Participants Achieving 3-lines or More Improvement in Mesopic, High Contrast, Binocular DCNVA at Day 30 in GEMINI 2 (Intent-to-Treat Population)
| Timepoint | Hour 0 | Hour 0.25 | Hour 0.5 | Hour 1 | Hour 3 | Hour 6 | Hour 8 | Hour 10 |
| VUITY (%) | 7.8 | 16.1 | 32.1 | 37.3 | 27.6 | 16.3 | 14.5 | 12.6 |
| Vehicle (%) | 4.0 | 6.6 | 9.6 | 12.1 | 10.8 | 9.9 | 8.6 | 8.7 |
| Difference (95% CI) | 3.8 (-0.9, 8.4) | 9.4 (3.2, 15.7) | 22.5 (14.7, 30.3) | 25.2 (17.0, 33.4) | 16.7 (9.1, 24.3) | 6.5 (-0.1, 13.1) | 5.9 (-0.5, 12.2) | 3.8 (-2.3, 10.0) |
The efficacy of VUITY dosed twice daily for the treatment of presbyopia was also demonstrated in a 14-Day, randomized, double-masked, vehicle-controlled study, namely VIRGO (NCT04983589). A total of 230 participants aged 40 to 55 years old with presbyopia were randomized (114 to VUITY group) and participants were instructed to administer one drop of VUITY or vehicle twice daily in each eye, with each dose administered 6 hours apart.
In this study, the proportion of participants gaining 3 lines or more in mesopic, high contrast, binocular distance corrected near visual acuity (DCNVA), without losing more than 1 line (5 letters) of corrected distance visual acuity (CDVA) with the same refractive correction was statistically significantly greater in the VUITY group compared to the vehicle group at Day 14, Hour 9 (3 hours after the second dose) (see Table 2).
| VIRGO | |||
| VUITY BID N=114 |
Vehicle BID N=116 |
p-value | |
| Proportion of participants gaining 3-lines or more in mesopic DCNVA, without losing more than 1 line (5 letters) of CDVA at Day 14, Hour 9 (3 hours after the second dose) | 35% | 8% | p< 0.01 |
Figure 3 presents the proportion of participants who gained 3-lines or more in mesopic DCNVA at Day 14.
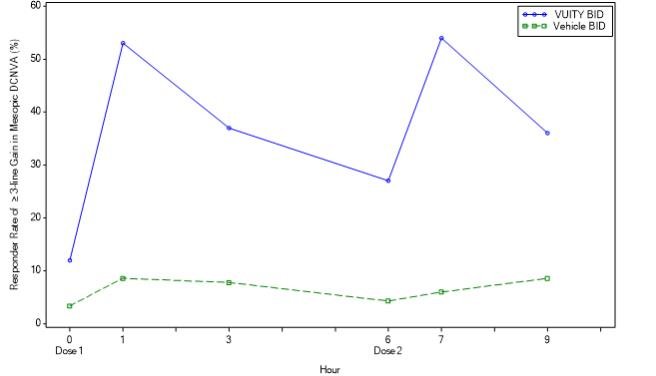
Figure 3: Proportion of Participants Achieving 3-lines or More Improvement in Mesopic, High Contrast, Binocular DCNVA at Day 14 in VIRGO (Intent-to-Treat Population)
| Timepoint | Hour 0 | Hour 1 | Hour 3 | Hour 6 | Hour 7 | Hour 9 |
| VUITY BID (%) | 12.3 | 53.5 | 37.7 | 27.2 | 54.4 | 36.8 |
| Vehicle BID (%) | 3.4 | 8.6 | 7.8 | 4.3 | 6.0 | 8.6 |
| Difference (95% CI) | 8.8 (2.0, 15.7) | 44.9 (34.4, 55.4) | 30.0 (19.8, 40.1) | 22.9 (13.9, 31.8) | 48.4 (38.2, 58.5) | 28.2 (18.0, 38.4) |
16. How is Vuity Eye Drops supplied
VUITY is supplied as an isotonic, clear, colorless sterile ophthalmic solution in colorless low density polyethylene (LDPE) ophthalmic dispenser bottles and tips, with dark green high impact polystyrene caps as follows:
| 2.5 mL fill in 5 mL bottle (Box containing 1 bottle) | NDC 0074-7098-01 |
| 2.5 mL fill in 5 mL bottle (Box containing 3 bottles) | NDC 0074-7098-03 |
| 2.5 mL fill in 5 mL bottle (Carton containing 1 bottle) | NDC 0074-7098-04 |
| 5 mL fill in 5 mL bottle (Carton) | NDC 0074-7098-06 |
Storage
Store at 15°C to 25°C (59°F to 77°F). After opening, VUITY can be used until the expiration date on the bottle.
17. Patient Counseling Information
Night Driving
VUITY may cause temporary dim or dark vision. Advise patients to exercise caution with night driving and when hazardous activities are undertaken in poor illumination [see Warnings and Precautions (5.1)].
Accommodative Spasm
Temporary problems when changing focus between near and distant objects may occur. Advise patients not to drive or use machinery if vision is not clear (e.g., blurred vision) [see Warnings and Precautions (5.1)].
When to Seek Physician Advice
Advise patients to seek immediate medical care with sudden onset of flashing lights, floaters, or vision loss [see Warnings and Precautions (5.2)].
Contact Lens Wear
Contact lens should be removed prior to the instillation of VUITY. Wait 10 minutes after dosing before reinserting contact lenses [see Warnings and Precautions (5.4)].
Avoiding Contamination of the Product
Do not touch dropper tip to any surface, as this may contaminate the contents [see Warnings and Precautions (5.5)].
Concomitant Topical Ocular Therapy
If more than one topical ophthalmic medication is being used, the medicines must be administered at least 5 minutes apart.
Distributed by: Allergan, an AbbVie company
Manufactured for:
AbbVie Inc.
North Chicago, IL 60064 USA
© 2023 AbbVie. All rights reserved.
VUITY and its design are trademarks of Allergan Sales, LLC, an AbbVie company.
v5.0USPI7098
PRINCIPAL DISPLAY PANEL
NDC 0074-7098-01
Vuity™
(pilocarpine HCI ophthalmic solution) 1.25%
Contains one
2.5 mL bottle
Rx Only
Sterile
For topical
application
in the eye
1 x 2.5 mL
Allergan™
An AbbVie company
PRINCIPAL DISPLAY PANEL
NDC 0074-7098-03
Vuity™
(pilocarpine HCI ophthalmic solution) 1.25%
Contains three
2.5 mL bottles
Rx Only
Sterile
For topical
application
in the eye
3 x 2.5 mL
Allergan™
An AbbVie company
PRINCIPAL DISPLAY PANEL
NDC 0074-7098-04
Vuity™
(pilocarpine HCI ophthalmic
solution) 1.25%
Rx Only
Sterile
2.5 mL
For Topical Application in the Eye
Allergan™
An AbbVie company
PRINCIPAL DISPLAY PANEL
NDC 0074-7098-05
Professional Sample
Not for Resale
Vuity™
(pilocarpine HCI ophthalmic
solution) 1.25%
Rx Only
Sterile
1.5 mL
For Topical Application in the Eye
Allergan™
An AbbVie company
PRINCIPAL DISPLAY PANEL
NDC: 0074-7098-06
Vuity®
(pilocarpine HCI ophthalmic
solution) 1.25%
Rx Only
Sterile
5 mL
For Topical Application in the Eye
Allergan™
An AbbVie company
Первый препарат для лечения старческой дальнозоркости
FDA одобрило препарат компании Allergan для лечения старческой дальнозоркости. Препарат в форме глазных капель безопасен и может существенно улучшить зрение на срок до шести часов.
Препарат VUIT эффективен при пресбиопии. Глазные капли начинают действовать через 15 минут. Они используют специальную формулу, которая содержит пилокарпин, с собственной технологией Allergan pHast. В ходе клинических исследований III фазы GEMINI1 и GEMINI 2 у пациентов, которые самостоятельно применяли VUITY один раз в день, на 30-й день фиксировалось улучшение зрения на срок до шести часов.
Кроме того, ни в одном из исследований у пациентов не было выявлено серьезных побочных эффектов. Наиболее часто возникали головная боль и покраснение глаз, которые наблюдались менее чем у 5% участников исследования. VUITY не оказывал отрицательного влияния на зрение.
Источник: https://www.pharmalive.com/fda-approval-of-abbvie-eye-drop-a-new-moment-in-presbyopia/
31.10.2021
В России впервые выявили миллион заболевших ковидом за месяц
Заболеваемость коронавирусной инфекцией в России в октябре достигла максимума с начала пандемии — в стране впервые выявили больше миллиона заразившихся за месяц, следует из подсчетов ТАСС на основе данных федерального оперативного штаба.
Данный информационный сайт предназначен исключительно для медицинских, фармацевтических и иных работников системы здравоохранения.
Вся информация сайта www.rmj.ru (далее — Информация) может быть доступна исключительно для специалистов системы здравоохранения. В связи с этим для доступа к такой Информации от Вас требуется подтверждение Вашего статуса и факта наличия у Вас профессионального медицинского образования, а также того, что Вы являетесь действующим медицинским, фармацевтическим работником или иным соответствующим профессионалом, обладающим соответствующими знаниями и навыками в области медицины, фармацевтики, диагностики и здравоохранения РФ. Информация, содержащаяся на настоящем сайте, предназначена исключительно для ознакомления, носит научно-информационный характер и не должна расцениваться в качестве Информации рекламного характера для широкого круга лиц.
Информация не должна быть использована для замены непосредственной консультации с врачом и для принятия решения о применении продукции самостоятельно.
На основании вышесказанного, пожалуйста, подтвердите, что Вы являетесь действующим медицинским или фармацевтическим работником, либо иным работником системы здравоохранения.
Читать дальше
Первые и единственные глазные капли Vuity компании Allergan одобрены FDA для коррекции пресбиопии с 28 октября 2021 г. Глазные капли Vuity представляют собой оптимизированную формулу пилокарпина pHast (1,25%), специально разработанную для лечения пресбиопии. Технология pHast позволяет Vuity адаптироваться к физиологическому pH слезной пленки.
Vuity улучшает зрение вблизи за счет уменьшения размера зрачка. При этом зрение вдаль не ухудшается. Препарат начинает работать через 15 минут после закапывания, его эффект длится до 6 часов.
Глазные капли Vuity получили одобрение FDA на основании результатов двух основных клинических исследований фазы 3, GEMINI 1 и GEMINI 2, в которых оценивалась эффективность, безопасность и переносимость Vuity при лечении пресбиопии. В обоих исследованиях приняли участие 750 человек в возрасте от 40 до 55 лет с пресбиопией. Они были рандомизированы на группу Vuity и группу плацебо в соотношении один к одному. Участники закапывали по одной капле Vuity или плацебо один раз в день в оба глаза.
Результаты обоих исследований свидетельствовали в пользу Vuity: у статистически значимой части участников, получавших Vuity, острота зрения вблизи в мезопических условиях (при низкой освещенности) улучшилась на три строки по сравнению с плацебо без потери остроты зрения вдаль. Ни в одном из клинических исследований у субъектов, получавших Vuity, серьезных побочных эффектов не наблюдалось. Наиболее частыми несерьезными побочными эффектами Vuity, которые наблюдались с частотой > 5%, были головная боль и покраснение глаз.
Глазные капли Vuity могут использоваться для коррекции пресбиопии вплоть до момента проведения хирургического лечения.
Christie W.C., Tauber J., Fangqiu Z., et al. GEMINI 1 Phase 3: AGN-190584 improves intermediate vision in participants with presbyopia. ASCRS. 2021.
What Is Vuity?
Vuity (pilocarpine hydrochloride ophthalmic solution) is a cholinergic muscarinic receptor agonist indicated for the treatment of presbyopia in adults.
What Are Side Effects of Vuity?
Vuity may cause serious side effects including:
- hives,
- difficulty breathing,
- swelling of your face, lips, tongue, or throat,
- blurred vision,
- eye pain,
- visual impairment,
- eye irritation, and
- excessive tearing or watering of the eye
Get medical help right away, if you have any of the symptoms listed above.
Side effects of Vuity include:
- headache and
- eye redness.
Seek medical care or call 911 at once if you have the following serious side effects:
- Serious eye symptoms such as sudden vision loss, blurred vision, tunnel vision, eye pain or swelling, or seeing halos around lights;
- Serious heart symptoms such as fast, irregular, or pounding heartbeats; fluttering in your chest; shortness of breath; and sudden dizziness, lightheartedness, or passing out;
- Severe headache, confusion, slurred speech, arm or leg weakness, trouble walking, loss of coordination, feeling unsteady, very stiff muscles, high fever, profuse sweating, or tremors.
This document does not contain all possible side effects and others may occur. Check with your physician for additional information about side effects.
Dosage for Vuity
The dose of Vuity is one drop instilled in each eye once daily. If more than one topical ophthalmic product is being used, the products should be administered at least 5 minutes apart.
Vuity In Children
Presbyopia does not occur in the pediatric population.
What Drugs, Substances, or Supplements Interact with Vuity?
Vuity may interact with other medicines.
Tell your doctor all medications and supplements you use.
Vuity During Pregnancy and Breastfeeding
Tell your doctor if you are pregnant or plan to become pregnant before using Vuity; it is unknown how it might affect a fetus. It is unknown if Vuity passes into breast milk. Consult your doctor before breastfeeding.
Additional Information
Our Vuity (pilocarpine hydrochloride ophthalmic solution) 1.25%, for Topical Ophthalmic Use Side Effects Drug Center provides a comprehensive view of available drug information on the potential side effects when taking this medication.
DESCRIPTION
VUITY (pilocarpine hydrochloride ophthalmic solution) 1.25% is a cholinergic muscarinic receptor agonist prepared as an isotonic, colorless, sterile ophthalmic solution containing 1.25% of pilocarpine hydrochloride. The chemical name for pilocarpine hydrochloride is (3S,4R)-3-ethyl-4-[(1-methyl-1H-imidazol-5-yl)methyl]oxolan-2-one hydrochloride. Its molecular weight is 244.72 and its molecular formula is C11H16N2O2 •HCl. Its structural formula is:
Each mL of VUITY contains pilocarpine hydrochloride 1.25% (12.5 mg) as the active ingredient, equivalent to 1.06% (10.6 mg) pilocarpine free-base. Preservative is: benzalkonium chloride 0.0075%. Inactive ingredients in the ophthalmic solution are: boric acid, sodium citrate dihydrate, sodium chloride, purified water, and may also include hydrochloric acid and/or sodium hydroxide for pH adjustment to between 3.5 and 5.5, if necessary.
INDICATIONS
VUITY® is indicated for the treatment of presbyopia in adults.
DOSAGE AND ADMINISTRATION
The recommended dosage of VUITY is one drop in each eye once daily. A second dose (one additional drop in each eye) may be administered 3-6 hours after the first dose.
If more than one topical ophthalmic product is being used, the products should be administered at least 5 minutes apart.
HOW SUPPLIED
Dosage Forms And Strengths
VUITY (pilocarpine hydrochloride ophthalmic solution) is a clear, colorless, sterile ophthalmic solution containing 1.25% (12.5 mg/mL) of pilocarpine hydrochloride.
Storage And Handling
VUITY is supplied as an isotonic, clear, colorless sterile ophthalmic solution in colorless low density polyethylene (LDPE) ophthalmic dispenser bottles and tips, with dark green high impact polystyrene caps as follows:
| 2.5 mL fill in 5 mL bottle (Box containing 1 bottle) | NDC 0074-7098-01 |
| 2.5 mL fill in 5 mL bottle (Box containing 3 bottles) | NDC 0074-7098-03 |
| 2.5 mL fill in 5 mL bottle (Carton containing 1 bottle) | NDC 0074-7098-04 |
| 5 mL fill in 5 mL bottle (Carton) | NDC 0074-7098-06 |
Storage
Store at 15°C to 25°C (59°F to 77°F). After opening, VUITY can be used until the expiration date on the bottle.
Distributed by: Allergan, an AbbVie company. Manufactured for: AbbVie Inc., North Chicago, IL 60064 USA. Revised: Mar 2023
Side Effects & Drug Interactions
SIDE EFFECTS
The following clinically significant adverse reactions are described elsewhere in labeling:
- Hypersensitivity [see CONTRAINDICATIONS]
Clinical Trials Experience
Because clinical trials are conducted under widely varying conditions, adverse reaction rates observed in the clinical trials of a drug cannot be directly compared to rates in the clinical trials of another drug and may not reflect the rates observed in practice.
VUITY dosed once daily was evaluated in 375 participants with presbyopia in two randomized, double-masked, vehicle-controlled studies (GEMINI 1 and GEMINI 2) of 30 days duration. The most common adverse reactions reported in >5% of participants were headache and conjunctival hyperemia. Ocular adverse reactions reported in 1-5% of participants were blurred vision, eye pain, visual impairment, eye irritation, and increased lacrimation.
VUITY was also evaluated in 114 participants with presbyopia in a randomized, double-masked, vehicle-controlled 14-day study (VIRGO) in which participants received two doses of VUITY in each eye, 6 hours apart daily. The most common adverse reactions reported in >5 % of participants were headache and eye irritation. Ocular adverse reactions reported in 1-5% of participants were visual impairment, eye pain, blurred vision, and vitreous floaters.
Postmarketing Experience
The following adverse reactions have been identified during postapproval use of VUITY. Because these reactions are reported voluntarily from a population of uncertain size, it is not always possible to reliably estimate their frequency or establish a causal relationship to VUITY exposure.
Eye disorders: vitreous detachment, vitreomacular traction, retinal tear, retinal detachment.
DRUG INTERACTIONS
No Information provided
WARNINGS
Included as part of the PRECAUTIONS section.
PRECAUTIONS
Blurred Vision
Miotics, including VUITY, may cause accommodative spasm. Patients should be advised not to drive or operate machinery if vision is not clear (e.g., blurred vision).
In addition, patients may experience temporary dim or dark vision with miotics, including VUITY. Patients should be advised to exercise caution in night driving and other hazardous activities in poor illumination.
Risk Of Retinal Detachment
Rare cases of retinal detachment and retinal tear have been reported with miotics, including VUITY.
Individuals with pre-existing retinal disease are at increased risk. Therefore, examination of the retina is advised in all patients prior to the initiation of therapy.
Patients should be advised to seek immediate medical care with sudden onset of flashing lights, floaters, or vision loss.
Iritis
VUITY is not recommended to be used when iritis is present because adhesions (synechiae) may form between the iris and the lens.
Use With Contact Lenses
Contact lens wearers should be advised to remove their lenses prior to the instillation of VUITY and to wait 10 minutes after dosing before reinserting their contact lenses.
Potential For Eye Injury Or Contamination
To prevent eye injury or contamination, care should be taken to avoid touching the dispensing bottle to the eye or to any other surface.
Nonclinical Toxicology
Carcinogenesis, Mutagenesis, Impairment Of Fertility
Carcinogenesis
Pilocarpine did not induce tumors in mice at any dosage level studied (up to 30 mg/kg/day; approximately 80-times the MHOD). In rats, an oral dose of 18 mg/kg/day (approximately 100 times the MHOD), resulted in a statistically significant increase in the incidence of benign pheochromocytomas in both male and female rats, and a statistically significant increase in the incidence of hepatocellular adenomas in female rats.
Mutagenesis
Pilocarpine did not show any potential to cause genetic toxicity in a series of studies that included: 1) bacterial assays (Salmonella and E. coli) for reverse gene mutations; 2) an in vitro chromosome aberration assay in a Chinese hamster ovary cell line; 3) an in vivo chromosome aberration assay (micronucleus test) in mice; and 4) a primary DNA damage assay (unscheduled DNA synthesis) in rat hepatocyte primary cultures.
Impairment Of Fertility
Pilocarpine oral administration to male and female rats at a dosage of 18 mg/kg/day (100 times the MHOD) resulted in impaired reproductive function, including reduced fertility, decreased sperm motility, and morphologic evidence of abnormal sperm. It is unclear whether the reduction in fertility was due to effects on males, females, or both. In dogs, exposure to pilocarpine at a dosage of 3 mg/kg/day for 6 months resulted in evidence of impaired spermatogenesis (approximately 55 times the MHOD).
Use In Specific Populations
Pregnancy
Risk Summary
There are no adequate and well-controlled studies of VUITY administration in pregnant women to inform a drug-associated risk. Oral administration of pilocarpine to pregnant rats throughout organogenesis and lactation did not produce adverse effects at clinically relevant doses.
Data
Human Data
No adequate and well-controlled trials of VUITY have been conducted in pregnant women. In a retrospective case series of 15 women with glaucoma, 4 patients used ophthalmic pilocarpine either pre-pregnancy, during pregnancy or postpartum. There were no adverse effects observed in patients or in their infants.
Animal Data
In embryofetal development studies, oral administration of pilocarpine to pregnant rats throughout organogenesis produced maternal toxicity, skeletal anomalies and reduction in fetal body weight at 90 mg/kg/day (approximately 485-fold higher than the maximum human ophthalmic dose [MHOD] of 0.03 mg/kg/day assuming administration of 2 drops/eye/day, on a mg/m² basis).
In a peri-/postnatal study in rats, oral administration of pilocarpine during late gestation through lactation increased stillbirths at a dose of 36 mg/kg/day (approximately 195-fold higher than the MHOD). Decreased neonatal survival and reduced mean body weight of pups were observed at ≥18 mg/kg/day (approximately 100 times the maximum human ophthalmic dose of VUITY).
Lactation
Risk Summary
There is no information regarding the presence of pilocarpine in human milk, the effects on the breastfed infants, or the effects on milk production to inform risk of VUITY to an infant during lactation.
Pilocarpine and/or its metabolites are excreted in the milk of lactating rats. Systemic levels of pilocarpine following topical ocular administration are low [see CLINICAL PHARMACOLOGY], and it is not known whether measurable levels of pilocarpine would be present in maternal milk following topical ocular administration.
The developmental and health benefits of breastfeeding should be considered along with the mother’s clinical need for VUITY and any potential adverse effects on the breastfed child from VUITY.
Data
Animal Data
Following a single oral administration of 14C-pilocarpine to lactating rats, the radioactivity concentrations in milk were similar to those in plasma.
Pediatric Use
Presbyopia does not occur in the pediatric population.
Geriatric Use
Clinical studies of VUITY did not include participants aged 65 and over to determine whether they respond differently from younger participants. Other reported clinical experience with ophthalmic pilocarpine solutions have not identified overall differences in safety between elderly and younger participants.
Overdose & Contraindications
OVERDOSE
Systemic toxicity following topical ocular administration of pilocarpine is rare, but occasionally patients who are sensitive may develop sweating and gastrointestinal overactivity. Accidental ingestion can produce sweating, salivation, nausea, tremors and slowing of the pulse and a decrease in blood pressure. In moderate overdosage, spontaneous recovery is to be expected and is aided by intravenous fluids to compensate for dehydration. For patients demonstrating severe poisoning, atropine, the pharmacologic antagonist to pilocarpine, should be used.
CONTRAINDICATIONS
VUITY is contraindicated in patients with known hypersensitivity to the active ingredient or to any of the excipients.
CLINICAL PHARMACOLOGY
Mechanism Of Action
Pilocarpine hydrochloride is a cholinergic muscarinic agonist which activates muscarinic receptors located at smooth muscles such as the iris sphincter muscle and ciliary muscle. VUITY contracts the iris sphincter muscle, constricting the pupil to improve near and intermediate visual acuity while maintaining some pupillary response to light. VUITY also contracts the ciliary muscle and may shift the eye to a more myopic state.
Pharmacokinetics
Systemic exposure to pilocarpine was evaluated in 22 participants with presbyopia who were administered 1 drop of VUITY in each eye once daily for 30 days (GEMINI 1). The mean (SD) Cmax and AUC values from time 0 to last measurable concentration over 10-hour period post-last dose on Day 30 were 1.95 (0.98) ng/mL and 4.14 (2.16) ng•hr/mL, respectively. The median Tmax value on Day 30 was 0.3 hours postdose with a range from 0.2 to 0.5 hours postdose.
Systemic exposure to pilocarpine was also evaluated in 8 participants with presbyopia who were administered 1 drop of VUITY in each eye twice daily for 14 days (VIRGO). The Day 14 mean (SD) Cmax following first daily dosing was 1.81 (0.51) ng/mL and following second daily dosing was 2.12 (1.75) ng/mL. The Day 14 mean (SD) AUC over 6-hour postdose following first daily dose was 4.35 (1.50) ng•hr/mL and following second daily dose was 4.22 (3.14) ng•hr/mL. There was no significant systemic drug accumulation over time, with accumulation index ratios between Day 1 and Day 14 based on AUC as 1.42 and 1.03 for the first and second daily dose, respectively.
Clinical Studies
The efficacy of VUITY dosed once daily for the treatment of presbyopia was demonstrated in two 30-Day Phase 3, randomized, double-masked, vehicle-controlled studies, namely GEMINI 1 (NCT03804268) and GEMINI 2 (NCT03857542). A total of 750 participants aged 40 to 55 years old with presbyopia were randomized (375 to VUITY group) in two studies and participants were instructed to administer one drop of VUITY or vehicle once daily in each eye.
In both studies, the proportion of participants gaining 3 lines or more in mesopic, high contrast, binocular distance corrected near visual acuity (DCNVA), without losing more than 1 line (5 letters) of corrected distance visual acuity (CDVA) with the same refractive correction was statistically significantly greater in the VUITY group compared to the vehicle group at Day 30, Hour 3 (see Table 1).
Table 1: Primary Efficacy Results from GEMINI 1 and GEMINI 2 Studies (Intent-to-Treat Population)
| GEMINI 1 | GEMINI 2 | |||||
| VUITY N=163 |
Vehicle N=160 |
p-value | VUITY N=212 |
Vehicle N=215 |
p-value | |
| Proportion of participants gaining 3-lines or more in mesopic DCNVA, without losing more than 1 line (5 letters) of CDVA at Day 30, Hour 3 | 31% | 8% | p<0.01 | 26% | 11% | p<0.01 |
Figures 1 and 2 present the proportion of participants who gained 3-lines or more in mesopic DCNVA at Day 30.
Figure 1: Proportion of Participants Achieving 3-Lines or More Improvement in Mesopic, High Contrast, Binocular DCNVA at Day 30 in GEMINI 1 (Intent-to-Treat Population)
| Timepoint | Hour | |||||||
| Hour 0 | Hour 0.25 | 0.5 | Hour 1 | Hour 3 | Hour 6 | Hour 8 | Hour 10 | |
| VUITY (%) | 4.3 | 17.7 | 34.8 | 41.6 | 30.7 | 18.4 | 10.6 | 7.5 |
| Vehicle (%) | 5.9 | 9.8 | 9.8 | 15.7 | 8.1 | 8.8 | 8.5 | 8.6 |
| Difference (95% CI) | -1.5 (-6.4, 3.3) |
7.9 (0.3, 15.5) |
25.0 (16.2, 33.8) |
25.9 (16.4, 35.5) |
22.5 (14.3, 30.8) |
9.7 (2.3, 17.0) |
2.1 (-4.4, 8.5) |
-1.1 (-7.1, 5.0) |
Figure 2: Proportion of Participants Achieving 3-lines or More Improvement in Mesopic, High Contrast, Binocular DCNVA at Day 30 in GEMINI 2 (Intent-to-Treat Population)
| Timepoint | Hour | |||||||
| Hour 0 | Hour 0.25 | Hour 0.5 | Hour 1 | Hour 3 | Hour 6 | Hour 8 | Hour 10 | |
| VUITY (%) | 7.8 | 16.1 | 32.1 | 37.3 | 27.6 | 16.3 | 14.5 | 12.6 |
| Vehicle (%) | 4.0 | 6.6 | 9.6 | 12.1 | 10.8 | 9.9 | 8.6 | 8.7 |
| Difference (95% CI) | 3.8 (-0.9, 8.4) |
9.4 (3.2, 15.7) |
22.5 (14.7, 30.3) |
25.2 (17.0, 33.4) |
16.7 (9.1, 24.3) |
6.5 (-0.1, 13.1) |
5.9 (-0.5, 12.2) |
3.8 (-2.3, 10.0) |
The efficacy of VUITY dosed twice daily for the treatment of presbyopia was also demonstrated in a 14-Day, randomized, double-masked, vehicle-controlled study, namely VIRGO (NCT04983589). A total of 230 participants aged 40 to 55 years old with presbyopia were randomized (114 to VUITY group) and participants were instructed to administer one drop of VUITY or vehicle twice daily in each eye, with each dose administered 6 hours apart.
In this study, the proportion of participants gaining 3 lines or more in mesopic, high contrast, binocular distance corrected near visual acuity (DCNVA), without losing more than 1 line (5 letters) of corrected distance visual acuity (CDVA) with the same refractive correction was statistically significantly greater in the VUITY group compared to the vehicle group at Day 14, Hour 9 (3 hours after the second dose) (see Table 2).
Table 2: Primary Efficacy Results from VIRGO (Intent-to-Treat Population)
| VIRGO | |||
| VUITY BID N=114 | Vehicle BID N=116 |
p-value | |
| Proportion of participants gaining 3-lines or more in mesopic DCNVA, without losing more than 1 line (5 letters) of CDVA at Day 14, Hour 9 (3 hours after the second dose) | 35% | 8% | p< 0.01 |
Figure 3 presents the proportion of participants who gained 3-lines or more in mesopic DCNVA at Day 14.
Figure 3: Proportion of Participants Achieving 3-lines or More Improvement in Mesopic, High Contrast, Binocular DCNVA at Day 14 in VIRGO (Intent-to-Treat Population)
| Timepoint | Hour | |||||
| Hour 0 | Hour 1 | Hour 3 | Hour 6 | Hour 7 | Hour 9 | |
| VUITY BID (%) | 12.3 | 53.5 | 37.7 | 27.2 | 54.4 | 36.8 |
| Vehicle BID (%) | 3.4 | 8.6 | 7.8 | 4.3 | 6.0 | 8.6 |
| Difference (95% CI) | 8.8 (2.0, 15.7) |
44.9 (34.4, 55.4) |
30.0 (19.8, 40.1) |
22.9 (13.9, 31.8) |
48.4 (38.2, 58.5) |
28.2 (18.0, 38.4) |
PATIENT INFORMATION
Night Driving
VUITY may cause temporary dim or dark vision. Advise patients to exercise caution with night driving and when hazardous activities are undertaken in poor illumination [see WARNINGS AND PRECAUTIONS].
Accommodative Spasm
Temporary problems when changing focus between near and distant objects may occur. Advise patients not to drive or use machinery if vision is not clear (e.g., blurred vision) [see WARNINGS AND PRECAUTIONS].
When To Seek Physician Advice
Advise patients to seek immediate medical care with sudden onset of flashing lights, floaters, or vision loss [see WARNINGS AND PRECAUTIONS].
Contact Lens Wear
Contact lens should be removed prior to the instillation of VUITY. Wait 10 minutes after dosing before reinserting contact lenses [see WARNINGS AND PRECAUTIONS].
Avoiding Contamination Of The Product
Do not touch dropper tip to any surface, as this may contaminate the contents [see WARNINGS AND PRECAUTIONS].
Concomitant Topical Ocular Therapy
If more than one topical ophthalmic medication is being used, the medicines must be administered at least 5 minutes apart.
From 
Health Solutions From Our Sponsors
Report Problems to the Food and Drug Administration
You are encouraged to report negative side effects of prescription drugs to the FDA. Visit the FDA MedWatch website or call 1-800-FDA-1088.