Содержание
-
Структурная формула
-
Русское название
-
Английское название
-
Латинское название
-
Химическое название
-
Брутто формула
-
Фармакологическая группа вещества Тиболон
-
Нозологическая классификация
-
Код CAS
-
Фармакологическое действие
-
Фармакология
-
Применение вещества Тиболон
-
Противопоказания
-
Ограничения к применению
-
Применение при беременности и кормлении грудью
-
Побочные действия вещества Тиболон
-
Взаимодействие
-
Передозировка
-
Способ применения и дозы
-
Меры предосторожности
-
Торговые названия с действующим веществом Тиболон
Структурная формула
Русское название
Тиболон
Английское название
Tibolone
Латинское название
Tibolonum (род. Tiboloni)
Химическое название
(7альфа,17альфа)-17-Гидрокси-7-метил-19-норпрегн-5(10)-ен-20-ин-3-он
Брутто формула
C21H28O2
Фармакологическая группа вещества Тиболон
Нозологическая классификация
Код CAS
5630-53-5
Фармакологическое действие
—
эстроген-гестагенное.
Фармакология
Обладает также слабовыраженной андрогенной и анаболической активностью. Нивелирует климактерические изменения гипоталамо-гипофизарной системы. Снижает уровень ФСГ и ЛГ у женщин в менопаузе. У фертильных женщин подавляет овуляцию.
Оказывает стимулирующее действие на слизистую оболочку влагалища. Предотвращает остеопороз, снижает уровень фосфатов и кальция в сыворотке крови. Снижает выраженность климактерической вегетативной дисфункции (приливы, повышенное потоотделение, головные боли), улучшает либидо и психоэмоциональное состояние (повышает уровень центральных и периферических опиоидов).
После приема внутрь быстро и полностью всасывается из ЖКТ. Биотрансформируется с образованием трех фармакологически активных метаболитов: 3-альфа-ОН-тиболон и 3-бета-ОН-тиболон обладают преимущественно эстрогенной активностью, дельта −4-изомер тиболона обладает прогестагенной и слабой андрогенной активностью. Cmax 3-альфа-ОН- и 3-бета-ОН-метаболитов достигаются через 1–1,5 ч, T1/2 — около 7 ч, не накапливаются. Выводится главным образом в виде метаболитов, преимущественно с фекалиями, небольшое количество — с мочой.
Применение вещества Тиболон
Менопауза (естественная и хирургическая), остеопороз при эстрогенной недостаточности (профилактика).
Противопоказания
Гиперчувствительность, гормонозависимые опухоли (или подозрение на них), влагалищное кровотечение неясной этиологии, тромбофлебит и тромбоэмболия (в т.ч. в анамнезе), тяжелое нарушение функций печени, сердечно-сосудистая недостаточность, цереброваскулярные расстройства; отосклероз, возникший во время беременности или при лечении стероидами; в период менее 1 года после последней менструации, нелеченная гиперплазия эндометрия, порфирия, беременность, кормление грудью.
Ограничения к применению
Лейомиома, эндометриоз, гиперплазия эндометрия в анамнезе, почечная недостаточность, нарушение углеводного обмена, гиперхолестеринемия, эпилепсия, мигрень или сильные головные боли, системная красная волчанка, бронхиальная астма.
Применение при беременности и кормлении грудью
Применение при беременности противопоказано. В случае возникновения беременности во время применения препарата лечение необходимо немедленно прекратить.
Применение в период грудного вскармливания не рекомендуется.
Побочные действия вещества Тиболон
Со стороны нервной системы и органов чувств: головная боль, головокружение, нарушение зрения, депрессия.
Со стороны органов ЖКТ: тошнота, диарея, повышение активности печеночных трансаминаз.
Со стороны мочеполовой системы: метроррагия, пролиферация эндометрия.
Прочие: отек голеней, боль в спине, руках и ногах, изменение массы тела, усиление роста волос на лице, кожный зуд, сыпь, себорейный дерматит.
Взаимодействие
Усиливает действие антикоагулянтов, повышает потребность в гипогликемических средствах (снижает толерантность к глюкозе). Активность снижается при одновременном применении рифампицина, карбамазепина.
Передозировка
Симптомы: нарушение функции ЖКТ.
Лечение: симптоматическое.
Способ применения и дозы
Внутрь, не разжевывая, по 2,5 мг один раз в день (в одно и то же время суток). Первой принимается таблетка из верхнего, обведенного в рамку ряда, которая помечена днем, соответствующим дню начала приема, последующие — в направлении, указанном стрелкой. Не следует принимать удвоенную дозу для восполнения пропущенной. Улучшение достигается в течение нескольких недель, оптимальный курс лечения 3 мес и более.
Меры предосторожности
Не следует принимать препарат в период до истечения 12 мес после последней естественной менструации. Если препарат начать принимать раньше указанного срока, то увеличивается вероятность нерегулярных кровянистых выделений/кровотечений из влагалища.
Необходим регулярный контроль соответствующих лабораторных показателей у больных с гиперхолестеринемией, нарушением функции почек и сахарным диабетом. Следует иметь в виду, что на фоне тиболона возможно снижение уровней общего и свободного тироксина и тироксинсвязывающего глобулина.
При появлении симптомов тромбоэмболии, желтухи или стойких патологических изменений функциональных печеночных тестов лечение прекращают.
Торговые названия с действующим веществом Тиболон
| Торговое название | Цена за упаковку, руб. |
|---|---|
| Велледиен |
1229.00 |
| Ливиал® |
от 2543.00 до 2805.00 |
Изменение демографической структуры общества в последние десятилетия привело к увеличению в популяции доли женщин старшей возрастной группы. В настоящее время развитые страны мира стоят перед серьезной социальной и медицинской проблемой — инверсией возрастной «пирамиды», что связано с увеличением продолжительности жизни. Более трети своей жизни современная женщина проводит в состоянии дефицита женских половых гормонов. По данным ВОЗ с каждым годом возрастает число женщин, вступающих в период постменопаузы (к 2030 г. их количество достигнет 1,2 млрд человек). Менопауза, не являясь заболеванием, приводит к нарушению эндокринного равновесия в организме женщины, вызывая приливы, раздражительность, бессонницу, а в последующем — возможные урогенитальные расстройства, повышение риска развития остеопороза и сердечно-сосудистых заболеваний. Все эти данные свидетельствуют о необходимости разработки целого ряда медицинских и социальных мер по защите здоровья, сохранению работоспособности и достойного качества жизни женщин пери- и постменопаузального периода.
Новым этапом в развитии менопаузальной гормональной терапии (МГТ) стали данные о возможности эффективного использования особых групп препаратов как альтернативы традиционной эстрадиолсодержащей заместительной гормональной терапии (ЗГТ) [1]. Одним из таких препаратов является тиболон, относящийся к категории G3H — другие половые гормоны и препараты, применяющиеся для лечения менопаузальных нарушений. Тиболон — синтетический стероид, тканеселективный регулятор эстрогенной активности. В организме человека он метаболизируется в три изомера: 3 альфа-гидрокситиболон, 3 бета-гидрокситиболон и 4 дельта-метаболит, обладающие тканеселективным сродством к эстрогенным рецепторам. Гидроксиметаболиты циркулируют в плазме крови в связанном неактивном состоянии в виде сульфатированных форм. Попадая в ткани-мишени (кости, центральная нервная система, мочеполовые органы, сердечно-сосудистая система), метаболиты тиболона реактивируются под воздействием сульфатазы, что обеспечивает их эстрогеноподобный эффект. В молочной железе и эндометрии 4 дельта-изомер блокирует сульфатазу, препятствуя формированию активных метаболитов, способных взаимодействовать с эстрогенными рецепторами. Этот изомер обладает также гестагенными и слабыми андрогенными свойствами. В результате достигаются благоприятные эстрогенные эффекты в центральной нервной системе, костях и мочеполовом тракте при отсутствии нежелательных влияний в эндометрии и молочных железах.
Тиболон появился на фармацевтическом рынке с 1988 г. Зарегистрирован в 89 странах для лечения климактерического синдрома, в 45 странах — для профилактики остеопороза. В РФ зарегистрирован препарат Ледибон — тиболон 2,5 мг, который применяется один раз в сутки, желательно в одно и то же время. Показания к применению: лечение симптомов эстрогенной недостаточности у женщин спустя 1 год после последней естественной менструации; профилактика остеопороза у женщин в постменопаузе, имеющих высокий риск возникновения переломов, и при непереносимости других препаратов, применяемых для профилактики остеопороза. Начало лечения: естественная менопауза — лечение можно начать через 12 месяцев после последней естественной менструации; хирургическая менопауза — лечение начинают немедленно. Пропуск приема таблетки: менее 12 часов — принять немедленно; более 12 часов — пропустить прием таблетки, следующую таблетку принять в обычное время. Общая переносимость: Ледибон хорошо переносится, нет существенного влияния на массу тела.
В рандомизированных плацебо-контролируемых исследованиях было показано, что тиболон позволяет контролировать приливы жара, потливость и другие типичные симптомы, такие как бессонница, головная боль и утомляемость. В плане облегчения климактерических симптомов он оказался настолько же эффективным, как и многочисленные схемы эстроген-прогестагенной комбинированной и только эстрогенной терапии (ЭПТ/ЭТ) [8–10], хотя, возможно, он и характеризуется несколько более медленным началом действия, но может также использоваться в качестве «терапии прикрытия» для облегчения симптомов дефицита эстрогенов у женщин, получающих лечение агонистами гонадотропин-рилизинг-гормона (аГнРГ) по поводу миомы матки и эндометриоза [11, 12].
Показано, что тиболон способствует обратному развитию атрофии влагалища (увеличивает кариопикнотический индекс и индекс созревания клеток) и улучшает качество цервикальной слизи [13]. Женщины, получающие лечение тиболоном, отмечают значительное уменьшение сухости во влагалище, выраженности диспареунии и мочевых симптомов.
Эффекты тиболона в отношении циркулирующих андрогенов отличаются от действия стандартных пероральных схем МГТ (ЭПТ/ЭТ). При использовании тиболона уровень глобулина, связывающего половые стероиды (ГСПС), снижается, а не увеличивается, в связи с этим концентрация свободного тестостерона повышается, в то время как при стандартной МГТ (ЭПТ/ЭТ) наблюдается ее снижение. Показано, что увеличивается также концентрация дегидроэпиандростеронсульфата (ДЭАС) [14]. Кроме этого, 4 дельта-изомер тиболона также оказывает некоторое андрогенное действие. Эти свойства тиболона способствуют его благоприятному влиянию на сексуальное благополучие, которое заключается в повышении сексуального влечения, возбуждения, стимуляции сексуальных фантазий и повышении увлажненности влагалища [15–17]. В сравнении со стандартными схемами ЭПТ, тиболон в значительно большей степени способствует увеличению частоты коитусов, повышает степень наслаждения и удовлетворенности половым актом [18]. Что касается частоты оргазма и сексуальной чувствительности, то при применении тиболона или комбинации эстрогенов и андрогенов наблюдается более выраженный эффект, нежели при использовании ЭТ или в контрольной группе [19].
Предполагается, что существенное благоприятное воздействие тиболона на уровень настроения обусловлен нормализацией уровня эндорфинов и его андрогенными свойствами [15, 20]. В сравнительном исследовании с использованием ЭПТ тиболон оказался более эффективным в плане уменьшения выраженности расстройств настроения [21]. Кроме того, его эффект может осуществляться синергистически с эффектами психоактивных препаратов, что сопровождается более быстрым достижением улучшения у женщин, страдающих депрессией и психозами. Поскольку применение антидепрессантов часто ассоциируется с сексуальной дисфункцией, влияние тиболона на сексуальность у таких женщин сопровождается дополнительными преимуществами.
В рандомизированных контролируемых исследованиях показано, что тиболон вызывает увеличение минеральной плотности костной ткани (МПК) и предотвращает потерю костного вещества [23, 24]. Благоприятные эффекты тиболона наблюдались как в шейке бедра, так и в позвоночнике. Эти благоприятные эффекты отмечались при длительном (10-летнем) лечении [25] как в ранней, так и в поздней постменопаузе у женщин с установленным диагнозом остеопороза и у женщин, получавших лечение агонистами ГнРГ [11, 12, 26–28].
Терапия тиболоном значительно реже вызывает болезненность молочных желез и масталгию, нежели ЭПТ; эта причина гораздо реже, чем в случае ЭПТ, приводит к прекращению лечения тиболоном [8, 9, 23, 29]. Женщины с болезненностью молочных желез или масталгией на фоне ЭПТ, по-видимому, могут воспользоваться благоприятным эффектом при переходе на тиболон [30].
Тиболон не вызывает увеличения плотности ткани на маммограмме [29, 31]. Самопроизвольно возникшая повышенная рентгенографическая плотность молочных желез рассматривается как независимый фактор риска рака молочной железы. В настоящее время неясно, является ли индуцированная ЭПТ плотность молочных желез суррогатным маркером повышенного риска рака молочной железы, однако повышенная маммографическая плотность может маскировать опухоли молочных желез при скрининговой маммографии, что приводит к поздней диагностике [32]. Кроме того, повышенная маммографическая плотность приводит к увеличению частоты повторных вызовов пациенток, что вызывает страх женщин [33, 34]. Действие тиболона на молочные железы отличается от эффектов ЭПТ. В отличие от ЭПТ, тиболон не повышает риск пролиферации ткани молочной железы, но стимулирует апоптоз [31, 35]. Согласно объединенным данным всех исследований тиболона III/IV фазы, тиболон не вызывал увеличения риска рака молочной железы, в сравнении с плацебо (относительный риск (ОР) 0,50; 95% доверительный интервал 0,11–2,54) [36]. Исследование «Миллион женщин» (MWS) сообщает о повышении ОР рака молочной железы на фоне лечения тиболоном (ОР 1,45; 95% доверительный интервал 1,25–1,67), хотя это увеличение и достоверно (p < 0,0001) меньше, чем на фоне ЭПТ [5]. В другом эпидемиологическом исследовании, где использовалась база данных исследований общей практики Великобритании (GPRD), не обнаружено повышения риска при использовании тиболона (ОР 1,02; 95% доверительный интервал 0,78–1,33) [37]. Однако данные этого исследования были опубликованы только в виде тезисов, а не в виде полнотекстовой статьи.
Хотя лучшие доказательства влияния тиболона на развитие рака молочной железы, имеющиеся в настоящее время, получены от MWS, риски, описанные в этом обсервационном исследовании, вероятно, переоценены [3, 4]. Данные проведенных проспективных исследований [2, 33] свидетельствуют о том, что абсолютное увеличение риска рака молочной железы ниже, чем описано в исследовании MWS, и что риск применения тиболона и ЭТ, вероятно, ниже, чем риск использования ЭПТ.
В итоге: для кого Ледибон?
Пациентки в постменопаузе, имеющие вазомоторные симптомы, у которых Ледибон может иметь особое значение:
- женщины с низким уровнем сексуального влечения или так называемой женской сексуальной дисфункцией;
- женщины с расстройствами настроения и женщины, получающие психоактивные препараты;
- женщины с риском ускоренной потери костной ткани;
- женщины с менопаузальной масталгией;
- женщины с повышенной рентгенологической плотностью молочных желез;
- женщины с миомой матки;
- женщины с урогенитальными жалобами.
Пациентки, у которых может оказаться благоприятным переход с ЭПТ/ЭТ на Ледибон:
- женщины, у которых имеет место усиление боли в молочных железах;
- женщины, у которых наблюдается увеличение плотности молочных желез, что приводит к частым ложным вызовам на осмотр или получению нечитаемых маммограмм;
- женщины с низким сексуальным влечением;
- женщины с колебаниями настроения;
- женщины с кровотечениями (при условии отсутствия гистопатологических причин для кровотечения).
Пациентки без климактерических симптомов, которых следует иметь в виду (некоторые постменопаузальные женщины без климактерических симптомов или со слабо выраженной симптоматикой могут получить преимущество от лечения Ледибоном):
- женщины с низким сексуальным влечением;
- женщины с колебаниями настроения;
- женщины с остеопенией.
Литература
- Smith C. L., O’Malley B. W. Coregulator function: a key to understanding tissue specificity of selective receptor modulators // Endocr Rev. 2004; 25: 45–71.
- Anderson G. L., Limacher M., Assaf A. R. et al. Effects of conjugated equine estrogen in postmenopausalwomen with hysterectomy: the Women’s Health Initiative randomized controlled trial // J Am Med Assoc. 2004; 291: 1701–1712.
- Shapiro S. The Million Women Study: potential biases do not allowuncritical acceptance of the data // Climacteric. 2004; 7: 3–7.1
- Whitehead M., Farmer R. The MillionWomen Study: a critique // Endocrine. 2004; 24: 187–194.
- Million Women Study Collaborators. Breast cancer and hormone replacement therapy in the MillionWomen Study // Lancet. 2003; 362: 419–427.
- EMAS Revised Statement // Maturitas. 2005; 51: 8–14.
- IMS Revised Position Paper // Climacteric. 2004; 7: 333–337.
- Hammar M., Christau S., Nathorst-B¨o¨os J., Rud T., Garre K. A double-blind randomised trial comparing the effects of tibolone and continuous combined hormone replacement therapy in postmenopausal women with menopausal symptoms // Br J Obstet Gynaecol. 1998; 105: 904–911.
- Huber J., Palacios S., Berglund L. et al. The effect of tibolone compared with conjugated equine oestrogens continuously combined with medroxyprogesterone acetate on bleeding rates, quality of life and tolerability in postmenopausal women // Br J Obstet Gynaecol. 2002; 109: 886–893.
- Baracat E. C., Barbosa I. C., Giordano M. G. et al. A randomized, open-label study of conjugated equine estrogens plus medroxyprogesterone acetate versus tibolone: effects on symptom control, bleeding pattern, lipid profile and tolerability // Climacteric. 2002; 5: 60–69.
- Lindsay P. C., Shaw R. W., Coelingh Bennink H. J., Kovic P. The effect of add back treatment with tibolone (Livial®) on patients treated with the gonadotrophin-releasing hormone agonist triptorelin (Decapeptyl) // Fertil Steril. 1996; 65: 342–348.
- Palomba S., Affinito P., Di Carlo C., Bifulco G., Nappi C. Longterm administration of tibolone plus gonadotrophin-releasing hormone agonist for the treatment of uterine leiomyomas: effectiveness and effects on vasomotor symptoms, bone mass and lipid profile // Fertil Steril. 1999; 72: 889–895.
- Morris E. P., Wilson P. O. G., Robinson J., Rymer J. M. Long-term effects of tibolone on the genital tract in postmenopausal women // Br J Obstet Gynaecol. 1999; 106: 954–959.
- Doren M., Rubig A., Coelingh Bennink H. J., Holzgreve W. Differential effects on the androgen status of postmenopausal women treated with tibolone and continuous combined estradiol and norethindrone acetate replacement therapy // Fertil Steril. 2001; 75: 554–559.
- Davis S. R. The effects of tibolone on mood and libido // Menopause. 2002; 9: 162–170.
- Palacios S., Menendez C., Jurado R., Castano J. C., Vargas J. C. Changes in sex behaviour after menopause: effects of tibolone // Maturitas. 1995; 22: 155–161.
- Laan E., van Lunsen R. H. W., Everaerd W. The effects of tibolone on vaginal blood flow, sexual desire and arousability in postmenopausal women // Climacteric. 2001; 4: 28–41.
- Nathorst-Boos J., Hammar M. Effect on sexual life–a comparison between tibolone and a continuous estradiol-norethisterone acetate regimen // Maturitas. 1997; 26: 15–20.
- Castelo-Branco C., Vicente J., Figueras F. et al. Comparative effects of estrogens plus androgens and tibolone on bone, lipid pattern and sexuality in postmenopausal women // Maturitas. 2000; 34: 161–168.
- Genazzani A. R., Petraglia F., Facchinetti F. et al. Effects of Org OD 14 on pituitary and peripheral-endorphin in castrated rats and in postmenopausalwomen // Maturitas. 1987; 1: 35–48.
- Egarter Ch., Huber J., Leikermoser R. et al. Tibolone versus conjugated estrogens and sequential progestogen in the treatment of climacteric complaints // Maturitas. 1996; 23: 55–62.
- Meeuwsen I. B., Samson M. M., Duursma S. A., Verhaar H. J. The influence of tibolone on quality of life in postmenopausal women // Maturitas. 2002; 41: 35–43.
- Roux C., Pelissier C., Fechtenbaum J., Loiseau-Peres S., Benhamou C. L. Randomized, double-blind, 2-year comparison of tibolone with 17-estradiol and norethindrone acetate in preventing postmenopausal bone loss // Osteoporosis Int. 2002; 13: 241–248.
- Lippuner K., Haenggi W., Birkhauser M. H., Casez J.-P., Jaeger P. Prevention of postmenopausal bone loss using tibolone or conventional peroral or transdermal hormone replacement therapy with 17-oestradiol and dydrogesterone // J Bone Min Res. 1997; 12: 806–812.
- Rymer J., Robinson J., Fogelman I. Ten years of treatment with tibolone 2.5 mg daily: effects on bone loss in postmenopausal women // Climacteric. 2002; 5: 390–398.
- Berning B., Kuijk C. V., Kuiper J. W., Coelingh Bennink H. J. T., Kicovic P. M., Fauser B. C. J. M. Effects of two doses of tibolone on trabecular and cortical bone loss in early postmenopausal women: a two-year randomized, placebo-controlled study // Bone. 1996; 19: 395–399.
- Bjarnason N. H., Bjarnason K., Haarbo J., Rosenquist C., Christiansen C. Tibolone: prevention of bone loss in late postmenopausal women // J Clin Endocrinol Metab. 1996; 81: 2419–2422.
- Pavlov P. W., Ginsburg J., Kicovic P. M., van der Schaaf D. B., Prelevic G., Coelingh Bennink H. J. T. Double-blind, placebo controlled study of the effects of tibolone on bone mineral density in postmenopausal osteoporotic women with and without previous fractures // Gynecol Endocrinol. 1999; 13: 230–237.
- Lundstrom E., Christow A., Svane G. et al. Effects of tibolone and a continuous combined HRT regimen on mammographic breast density // Am J Obstet Gynecol. 2002; 186: 717–722.
- Palomba S., Di Carlo C., Morelli M. et al. Effect of tibolone on breast symptoms resulting from postmenopausal hormone replacement therapy // Maturitas. 2003; 45: 267–273.
- Valdivia I., Campodonico I., Tapia A. et al. Effects of tibolone and continuous combined hormone therapy on mammographic breast density and breast histochemical markers in postmenopausal women // Fertil Steril. 2004; 81: 617–623.
- Thurfjell E. Breast density and the risk of breast cancer // N Engl J Med. 2002; 347: 866.
- Chlebowski R. T., Hendrix S. L., Langer R. D. et al. Influence of estrogen plus progestin on breast cancer and mammography in healthy postmenopausal women: theWomen’s Health Initiative Randomized Trial // J Am Med Assoc. 2003; 289: 3243–3253.
- Banks E., Reeves G., Beral V. et al. Impact of use of hormone replacement therapy on false positive recall in the NHS breast screening programme: results from the Million Women Study // Br Med J. 2004; 328: 1291–1292.
- Conner P., ChristowA., Kersemaekerc W. Acomparative study of breast cell proliferation during hormone replacement therapy: effect of tibolone and continuous combined estrogen progestogen therapy // Climacteric. 2004; 7: 50–58.
- Helmond F. A., Kloosterboer H. J. Safety and tolerability profile of Livial. In: Genazzani AR, editor. Hormone replacement therapy and cancer. The current status of research and practice. Boca Raton: The Parthenon Publishing Group; 2002. P. 252–256.
- Allen D. S., de Vries C. S., Farmer R. D. T. Pharmaceutical content and regimen of hormone replacement therapy and risk of breast cancer // Pharmacoepidemiol Drug Saf. 2002; 11 (Suppl 1): 296.
А. Л. Тихомиров1, доктор медицинских наук, профессор
И. Б. Манухин, доктор медицинских наук, профессор
Е. И. Манухина, доктор медицинских наук, профессор
В. В. Казенашев, кандидат медицинских наук
ГБОУ ВПО МГМСУ им. А. И. Евдокимова МЗ РФ, Москва
1 Контактная информация: pacificoff@mail.ru
Rec.INN
зарегистрированное ВОЗ
Лекарственное взаимодействие
Входит в состав препаратов:
список
Фармакологическое действие
Анаболический стероид. Обладает эстрогенной, гестагенной и слабой андрогенной активностью, стабилизирует гипоталамо-гипофизарную систему после прекращения функционирования яичников, вызывает снижение секреции гонадотропных гормонов. Тормозит резорбцию костной ткани в постменопаузном периоде, смягчает такие проявления климактерического синдрома, как «приливы» крови к коже лица, повышенное потоотделение, головные боли. Положительно влияет на либидо и настроение (повышает концентрацию центральных и периферических опиоидов). Оказывает стимулирующее действие на слизистую оболочку влагалища, не стимулируя пролиферацию эндометрия. У фертильных женщин подавляет овуляцию.
Предотвращает развитие остеопороза, снижает концентрацию фосфатов и кальция в сыворотке крови.
Фармакокинетика
Абсорбция — высокая. Метаболизируется в печени с образованием гидрофильных продуктов, часть из которых фармакологически активна. Выводится почками (в т.ч. в форме метаболитов), через кишечник.
Показания активного вещества
ТИБОЛОН
Климакс (естественный или вследствие овариэктомии).
Профилактика климактерического остеопороза.
Режим дозирования
Внутрь в дозе 2.5 мг/сут (в одно и то же время); минимальная длительность лечения — 3 мес. Прием препарата начинают через 1 год после последней менструации или сразу же после хирургической менопаузы.
Побочное действие
Со стороны ЦНС: головокружение, головная боль.
Со стороны пищеварительной системы: диарея, повышение активности печеночных трансаминаз, изменение массы тела.
Со стороны эндокринной системы: усиление роста волос на лице, метроррагия, пролиферация эндометрия.
Прочие: отеки голеней, себорейный дерматоз, боли в спине, руках и ногах.
Противопоказания к применению
Беременность, гормонозависимые опухоли (в т.ч. подозрение на них), тромбофлебит, тромбоэмболия (в т.ч. в анамнезе), влагалищное кровотечение неясной этиологии, печеночная недостаточность, сердечно-сосудистая недостаточность, цереброваскулярные расстройства, отосклероз, возникший при беременности или при лечении стероидами, период менее 1 года после последней менструации.
Применение при беременности и кормлении грудью
Противопоказан при беременности.
Применение при нарушениях функции печени
Противопоказан при печеночной недостаточности.
Применение при нарушениях функции почек
C осторожностью применять при почечной недостаточности.
Особые указания
C осторожностью применять при почечной недостаточности, нарушениях углеводного обмена, гиперхолестеринемии, эпилепсии.
Не предназначен для использования в качестве контрацептива. В процессе лечения возможно повышение чувствительности больных к антикоагулянтам вследствие повышения фибринолитической активности крови.
При появлении симптомов тромбоэмболии, желтухи или стойких патологических изменений функциональных печеночных тестов лечение прекращают.
В период лечения необходим регулярный контроль соответствующих лабораторных показателей у больных с гиперхолестеринемией, почечной недостаточностью, сахарным диабетом. На фоне лечения возможно снижение концентраций общего и свободного Т4 и тироксинсвязывающего глобулина.
Лекарственное взаимодействие
Усиливает действие антикоагулянтов.
Велледиен — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер
ЛП-001739
Торговое наименование препарата
Велледиен
Международное непатентованное наименование:
Тиболон
Лекарственная форма
таблетки
Состав
Каждая таблетка содержит:
Действующее вещество:
Тиболон — 2,50 мг;
Вспомогательные вещества:
лактозы моногидрат — 69,44 мг, целлюлоза микрокристаллическая — 17,36 мг, аскорбил пальмитат — 0,20 мг, крахмал кукурузный — 10,00 мг, магния стеарат- 0,50 мг.
Описание:
Круглые, плоскоцилиндрические таблетки белого цвета.
Фармакотерапевтическая группа
прочие эстрогены.
Код АТХ: G03CX01
Фармакологические свойства
Фармакодинамика
Препарат избирательно регулирует эстрогеноподобную активность в тканях и является тканеселективным регулятором. Его фармакодинамические свойства определяются действием трех фармакологически активных метаболитов тиболона: 3-альфа- гидрокситиболон и 3-бета-гидрокситиболон обладают эстрогеноподобной активностью, дельта-4-изомеру свойственна прогестагеноподобная и слабая андрогеноподобная активность. Препарат восполняет дефицит эстрогенов в постменопаузальном периоде, облегчая связанные с их дефицитом симптомы — «приливы», депрессия, повышенное потоотделение ночью, головная боль. Положительно влияет на либидо и настроение (повышает концентрацию центральных и периферических опиоидов). Оказывает трофическое действие на слизистую оболочку влагалища, не вызывая пролиферацию эндометрия. Предотвращает потерю костной массы после наступления менопаузы или удаления яичников. Снижает концентрацию фосфатов и кальция в плазме крови.
Фармакокинетика
После приема внутрь тиболон быстро и интенсивно всасывается. Прием пищи не оказывает заметного влияния на всасывание препарата.
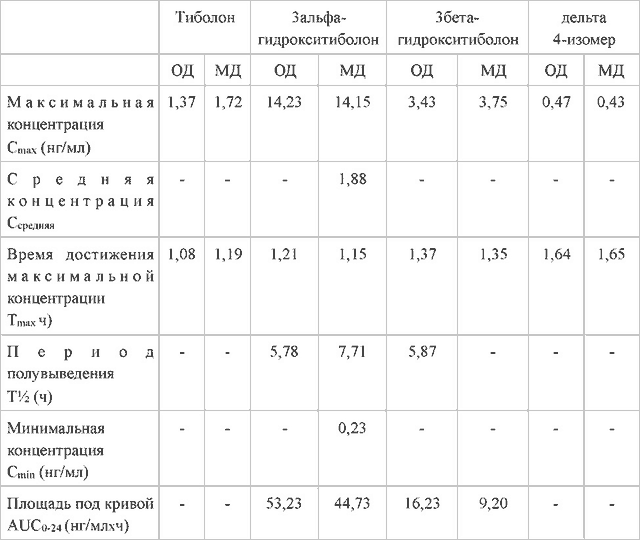
В результате быстрого метаболизма тиболона его концентрация в плазме крови очень низкая. Концентрация дельта 4-изомера в плазме крови также очень низкая, поэтому ряд фармакокинетических параметров невозможно определить. Максимальные концентрации в плазме крови метаболитов 3 альфа-гидрокситиболона (3а-ОН) и Збета-гидрокситиболона (3-в-ОН) выше, но кумуляции не происходит.
Таблица 1. Фармакокинетические параметры тиболона (доза 2,5 мг)
ОД — однократная доза; МД — многократная доза.
Выведение тиболона в основном происходит в форме конъюгированных метаболитов (в основном сульфатированных). Часть принятого тиболона выводится почками, большая часть — через кишечник.
Фармакокинетические параметры тиболона не зависят от функции почек.
Показания к применению
• Лечение симптомов эстрогенной недостаточности у женщин в постменопаузальном периоде (не ранее чем через 1 год после последней менструации при наступлении естественной менопаузы или сразу после хирургической менопаузы);
• профилактика постменопаузального остеопороза у женщин с высоким риском переломов при непереносимости или противопоказаниях к применению других лекарственных препаратов, предназначенных для лечения остеопороза.
Противопоказания
- Беременность и период грудного вскармливания;
- диагностированный (в том числе, в анамнезе) рак молочной железы или подозрение на него и диагностированные (в том числе, в анамнезе) эстрогензависимые злокачественные опухоли (например, рак эндометрия) или подозрение на них;
- кровотечение из влагалища неясной этиологии;
- тромбозы (венозные и артериальные) и тромбоэмболии в настоящее время или в анамнезе (в том числе тромбоз и тромбофлебит глубоких вен, тромбоэмболия легочной артерии), ишемическая болезнь сердца, инфаркт миокарда, ишемические и геморрагические цереброваскулярные нарушения;
- состояния, предшествующие тромбозу (в том числе, транзиторные ишемические атаки, стенокардия в настоящее время или в анамнезе);
- выявленная предрасположенность к венозному или артериальному тромбозу, включая резистентность к активированному протеину С, дефицит протеина С, дефицит протеина S или антитромбина III, антитела к фосфолипидам (антитела к кардиолипину, волчаночный антикоагулянт);
- множественные или выраженные факторы риска венозного или артериального тромбоза, в том числе осложненные поражения клапанного аппарата сердца, фибрилляция предсердий, заболевания сосудов головного мозга или коронарных артерий; неконтролируемая артериальная гипертензия;
- расширенно е оперативное вмешательство с длительной иммобилизацией,
- обширная травма, курение в возрасте старше 35 лет, ожирение с индексом массы тела >30 кг/м2;
- • злокачественные или доброкачественные опухоли (в том числе — аденома печени); в настоящее время или в анамнезе;
- печеночная недостаточность, острое заболевание печени или заболевание печени в анамнезе, после которого показатели функциональных проб печени не нормализовались;
- повышенная чувствительность к препарату или любому из его компонентов;
- порфирия;
- отосклероз, возникший во время предыдущей беременности или при применении гормональных контрацептивных препаратов в анамнезе;
- хроническая сердечная недостаточность (III-IV ФК), цереброваскулярные расстройства;
- период менее 1 года после последней менструации;
- нелеченая гиперплазия эндометрия;
- редкие наследственные заболевания: непереносимость галактозы, недостаточность лактазы или глюкозо-галактозная мальабсорбция.
С осторожностью
Если какое-либо из приведенных ниже состояний/заболеваний имеется в настоящее время, наблюдалось ранее и/или обострялось во время беременности или предыдущей гормонотерапии, пациентка должна находиться под тщательным наблюдением врача. Следует принимать во внимание, что эти состояния/заболевания могут рецидивировать или обостряться во время лечения препаратом Велледиен, в частности:
- лейомиома (фиброма матки) или эндометриоз;
- сердечно-сосудистая недостаточность без признаков декомпенсации;
- наличие факторов риска эстрогензависимых опухолей (например, рак молочной железы у родственников первой степени родства);
- контролируемая артериальная гипертензия ;
- гиперхолестеринемия;
- нарушения углеводного обмена , сахарный диабет, как при наличии , так и при отсутствии осложнений;
- желчнокаменная болезнь ;
- мигрень или сильная головная боль ;
- системная красная волчанка ;
- гиперплазия эндометрия в анамнезе;
- эпилепсия ;
- бронхиальная астма;
- почечная недостаточность;
- отосклероз, не связанный с беременностью или предшествующим применением гормональных контрацептивных препаратов.
Применение в период беременности и грудного вскармливания
Прием препарата противопоказан при беременности и в период грудного вскармливания.
Способ применения и дозы
Препарат Велледиен принимают внутрь по 1 таблетке в сутки, не разжевывая, запивая водой, желательно в одно и то же время, непрерывно. Первой принимается таблетка из ячейки верхнего ряда, отмеченной днем недели, соответствующим дню начала приема. Все остальные таблетки принимаются последовательно из ячеек в направлении стрелки на календарной упаковке, до тех пор, пока не будут приняты все таблетки.
Начало приема препарата Велледиен
Для лечения постменопаузальных симптомов препарат Велледиен необходимо применять только в отношении симптомов, неблагоприятно влияющих на качество жизни женщины. Прием препарата Велледиен начинают не ранее, чем через 12 месяцев после последней менструации при наступлении естественной менопаузы. Пациентки с менопаузой, обусловленной оперативным вмешательством, могут начинать прием препарата сразу же. Во всех случаях, не менее 1 раза в 6 месяцев необходимо проводить тщательную оценку риска и пользы лечения и продолжать применение препарата в период времени, когда польза от терапии превышает риск.
Переход на прием препарата Велледиен после Другого препарата Для заместительной гормональной терапии (ЗГТ)
Женщинам с интактной маткой, при переходе на прием препарата Велледиен после применения другого препарата ЗГТ, содержащего только эстрогены, рекомендуется сначала вызвать менструальноподобное кровотечение «отмены» путем применения прогестагена для устранения вероятно существующей гиперплазии эндометрия.
При переходе с препарата для ЗГТ с циклическим режимом приема, прием препарата Велледиен должен быть начат на следующий день после завершения применения прогестагена.
Если переход осуществляется с комбинированного препарата ЗГТ с непрерывным режимом приема, прием препарата Велледиен можно начинать в любое время.
Нарушение схемы приема препарата
Пропущенную таблетку, если с момента пропуска прошло менее 12 ч, женщина должна принять как можно скорее в тот же день. Следующая таблетка принимается в обычное время суток.
Если опоздание в приеме таблетки составило более 12 ч (интервал с момента приема последней таблетки более 36 ч), принимать пропущенную таблетку не нужно, а следующую таблетку необходимо выпить в обычное время.
Побочное действие
Для определения частоты возникновения побочных эффектов препарата применяют следующую классификацию:
- Очень часто (>1/10)
- Часто (>1/100 и <1/10)
- Нечасто (>1/1 000 и <1/100)
- Редко (>1/10 000 и <1/1 000)
- Очень редко (> 1/10 000).
Нарушения со стороны .желудочно-кишечного тракта: часто — боль внизу живота.
Нарушения со стороны кожи и подкожных тканей: часто — усиление роста волос, в том числе на лице; нечасто — акне.
Нарушения со стороны репродуктивной системы и молочных желез: часто — выделения из влагалища, увеличение толщины эндометрия, кровянистые выделения или кровотечение из влагалища, боль в молочных железах, генитальный зуд, кандидозный вульвовагинит, боль в области таза, дисплазия шейки матки, вульвовагинит; нечасто -микоз, нагрубание молочных желез, болезненность сосков.
Лабораторные и инструментальные данные: нечасто — увеличение массы тела; отклонения результатов мазка из шейки матки (отклонение от нормальных значений цитологических характеристик цервикального эпителия).
Большинство побочных эффектов носило слабовыраженный характер. Число случаев патологии шейки матки (рак шейки матки) не увеличивалось при приеме тиболона по сравнению с плацебо.
Другими возможными побочными эффектами могут быть (частота не установлена):
- головокружение , головная боль , мигрень ;
- депрессия;
- кожные высыпания, зуд кожи, себорейный дерматит;
- нарушения зрения (включая нечеткость зрения);
- желудочно — кишечные расстройства ( диарея , метеоризм );
- задержка жидкости в организме, периферические отеки;
- боль в суставах и мышцах ;
- нарушения функции печени (включая повышение активности трансаминаз).
Риск развития рака молочной железы
У женщин, получающих терапию комбинированными (эстроген/гестаген) препаратами более 5 лет, отмечалось двукратное увеличение частоты диагностирования рака молочной железы.
Любой повышенный риск у пациенток, получающих только эстроген или тиболон, существенно ниже, чем риск, наблюдаемый у пациенток, получающих терапию комбинированными (эстроген/гестаген) препаратами.
Уровень риска зависит от продолжительности применения (см. раздел «Особые указания»).
Таблица 2. Предполагаемый дополнительный риск развития рака молочной железы после 5лет применения (по данным «Исследования миллиона женщин»).
|
Возрастная группа (годы) |
Дополнительные случаи на 1000 пациенток, ранее не получавших ЗГТ, за период 5 лет |
Отношение риска* (95 % ДИ) |
Дополнительные случаи на 1000 пациенток, ранее получавших ЗГТ, за период свыше 5 лет (95 % ДИ) |
|
ЗГТ только эстрогеном |
|||
|
50-65 |
9-12 |
1,2 |
1-2 (0-3) |
|
Терапия комбинированными (эстроген/гестаген) препаратами |
|||
|
50-65 |
9-12 |
1,7 |
6 (5-7) |
|
Тиболон |
|||
|
50-65 |
9-12 |
1,3 |
3 (0-6) |
ДИ — доверительный интервал;
* суммарное отношение рисков. Отношение рисков не является постоянным, оно возрастает с увеличением продолжительности применения.
Риск развития рака эндометрия
Риск развития рака эндометрия составляет около 5 случаев на 1000 женщин с неудаленной маткой, не получающих ЗГТ или тиболон.
Самый высокий риск развития рака эндометрия наблюдался в рандомизированном плацебо-контролируемом исследовании, включавшем женщин, которые на начальном этапе не были обследованы на наличие патологии эндометрия, таким образом, дизайн исследования был приближен к условиям клинической практики (исследование LIFT, средний возраст 68 лет). В данном исследовании не было выявлено случаев рака эндометрия, диагностированного в группе плацебо (n = 1746) после наблюдения в течение 2,9 лет, по сравнению с 4 случаями рака эндометрия в группе, получавшей тиболон (n = 1746), что соответствует диагностике 0,8 дополнительного случая рака эндометрия на 1000 женщин, получавших тиболон в течение 1 года в данном исследовании (см. раздел «Особые указания»).
Риск развития ишемического инсульта
Относительный риск развития ишемического инсульта не зависит от возраста или длительности приема препарата, но абсолютный риск сильно зависит от возраста. Общий риск развития ишемического инсульта у женщин, принимающих тиболон, будет увеличиваться с возрастом (см. радел «Особые указания»).
Рандомизированное контролируемое исследование в течение 2,9 лет установило 2,2-кратное увеличение риска развития инсульта у женщин (средний возраст 68 лет), принимавших тиболон в дозе 1,25 мг (28/2249) по сравнению с плацебо (13/2257). Большинство (80 %) инсультов были ишемическими.
Абсолютный риск развития инсульта сильно зависит от возраста. Так абсолютный риск за 5 лет составляет 3 случая на 1000 женщин в возрасте 50-59 лет и 11 случаев на 1000 женщин в возрасте 60-69 лет.
Для женщин, принимающих тиболон в течение 5 лет, можно ожидать около 4 дополнительных случаев на 1000 пациенток в возрасте 50-59 лет и 13 дополнительных случаев на 1000 пациенток в возрасте 60-69 лет.
Были отмечены и другие нежелательные явления, связанные с применением препаратов для ЗГТ, содержащих только эстроген, и ЗГТ комбинированными (эстроген/гестаген) препаратами для ЗГТ:
• Продолжительное применение препаратов для ЗГТ, содержащих только эстроген, и комбинированные (эстроген/ге стагеные) препараты было связано с незначительным повышением риска развития рака яичников. По данным «Исследования миллиона женщин» ЗГТ в течение 5 лет приводила к 1 дополнительному случаю рака на 2500 пациенток. Это исследование показало, что относительный риск возникновения рака яичников при приеме тиболона аналогичен риску при применении других препаратов для ЗГТ.
• Прием тиболона связан с увеличением относительного риска развития венозной тромбоэмболии (ВТЭ), т.е. тромбоза глубоких вен и тромбоэмболии легочной артерии, в 1,3-3 раза. Подобное явление чаще происходит во время первого года применения препарата (см. раздел «Особые указания»).
Таблица 3. Дополнительный риск развития ВТЭ при применении свыше 5 лет по результатам исследования «Инициатива здоровья женщин»
|
Возрастная группа (годы) |
Частота заболеваний на 1000 женщин, в группе плацебо свыше 5 лет |
Отношение рисков (95 % ДИ) |
Дополнительные случаи на 1000 пациенток, ранее получающих ЗГТ |
|
Только эстроген перорально* |
|||
|
50-59 |
7 |
1,2 (0,6-2,4) |
1 (3-10) |
|
Комбинация эстроген/прогестаген перорально |
|||
|
50-59 |
4 |
2,3 (1,2-4,3) |
5 (1-13) |
|
*У женщин с удаленной маткой |
ДИ — доверительный интервал;
• Отмечается незначительное увеличение риска развития ишемической болезни сердца (ИБС) у пациенток старше 60 лет, получающих ЗГТ комбинированные (эстроген/гестаген) препараты. Нет никаких оснований полагать, что риск развития инфаркта миокарда при приеме тиболона отличается от риска применения других видов ЗГТ.
• Заболевания желчного пузыря (желчнокаменная болезнь, холецистит).
• Кожные заболевания: хлоазма, многоформная эритема, узловатая эритема,
сосудистая пурпура.
• Деменция при начале терапии в возрасте старше 65 лет (см. радел «Особые указания»).
• Панкреатит.
• Повышение артериального давления.
Передозировка
Острая токсичность тиболона у животных очень низкая, поэтому токсических симптомов можно не ожидать, даже если пациентка приняла несколько таблеток одновременно. В случаях острой передозировки могут развиться тошнота, рвота и влагалищное кровотечение. Антидот неизвестен. Рекомендована симптоматическая терапия.
Взаимодействие с другими лекарственными препаратами
Тиболон усиливает фибринолитическую активность крови, что может привести к усилению противосвертывающего действия антикоагулянтов, в частности варфарина, поэтому доза варфарина должна быть соответствующим образом откорректирована по МНО (международное нормализованное отношение).
Одновременное применение тиболона и антикоагулянтов необходимо контролировать, особенно в начале и в конце лечения тиболоном.
Существует лишь ограниченная информация относительно фармакокинетического взаимодействия при лечении тиболоном. Исследование in vivo продемонстрировало, что совместное применение с тиболоном в небольшой степени влияет на фармакокинетику субстрата цитохрома Р450 3А4 мидазолама. Исходя из этого, возможно наличие лекарственного взаимодействия с другими субстратами CYP3A4. Лекарственные препараты-индукторы CYP3A4 (барбитураты, карбамазепин, производные гидантоина, рифампицин) при одновременном применении могут повышать метаболизм тиболона и, следовательно, повлиять на его терапевтический эффект.
Препараты, содержащие зверобой продырявленный (Hypericum perforatum) могут усиливать метаболизм эстрогенов и прогестагенов посредством индукции изофермента CYP3A4. Повышенный метаболизм эстрогенов и прогестагенов может привести к снижению их клинического эффекта и изменению профиля маточных кровотечений.
Особые указания
Препарат Велледиен не предназначен для применения в качестве контрацептивного средства и не защищает от нежелательной беременности.
Решение о начале приема препарата Велледиен должно быть основано на соотношении «польза/риск» с учетом всех индивидуальных факторов риска, а у женщин старше 60 лет следует также принять во внимание повышение риска развития инсультов.
Для лечения постменопаузальных симптомов препарат Велледиен необходимо назначать только в отношении симптомов, которые неблагоприятно влияют на качество жизни. Во всех случаях необходимо не менее одного раза в год проводить тщательную оценку риска и пользы терапии, и следует продолжать прием препарата Велледиен только в случае, когда польза от терапии превышает риск.
Необходимо тщательно оценить риск развития инсульта, риск развития рака молочной железы и рака эндометрия у каждой женщины с интактной маткой (см. раздел «Побочное действие»), учитывая все индивидуальные факторы риска, частоту возникновения и особенности обоих видов рака и инсульта с точки зрения излечиваемости, заболеваемости и смертности.
Доказательства относительного риска, связанного с заместительной гормонотерапией (ЗГТ) или применением тиболона для лечения преждевременной менопаузы ограничены. Вместе с тем, соотношение польза/риск у женщин с преждевременной менопаузой может быть более благоприятным, чем у женщин старшего возраста, из-за низкого уровня абсолютного риска у более молодых женщин.
Медицинское обследование/наблюдение
До начала или возобновления приема Велледиена следует собрать индивидуальный и семейный медицинский анамнез.
Физикальное обследование (включая обследование органов малого таза и молочных желез) должно проводиться с учетом данных анамнеза, абсолютных и относительных противопоказаний. Во время приема препарата рекомендованы профилактические повторные осмотры, частота и характер которых определяются индивидуальными особенностями пациентки, но не реже 1 раза в 6 месяцев. В частности, женщина должна быть информирована о необходимости сообщения врачу об изменениях в молочных железах.
Обследования, включая соответствующие методы визуализации, например, маммографию, необходимо проводить в соответствии с принятой в настоящее время схемой обследования, адаптированной к клиническим потребностям каждой пациентки, но не реже 1 раза в 6месяцев.
Причины для немедленной отмены приема препарата и незамедлительного обращения к врачу
Прием препарата следует прекратить в случае выявления противопоказания и/или при следующих состояниях/заболеваниях:
• желтуха или ухудшение функции печени;
• внезапное повышение артериального давления, отличающееся от обычных показателей артериального давления, характерных для пациентки;
• возникновение головной боли типа мигрени.
Гиперплазия и рак эндометрия
Данные наблюдательных исследований показали увеличение риска развития гиперплазии или рака эндометрия у женщин, принимающих тиболон. Риск развития рака эндометрия повышается с увеличением продолжительности применения препарата.
Тиболон может увеличивать толщину эндометрия, измеряемую с помощью трансвагинального ультразвукового исследования.
В течение первых месяцев приема тиболона могут наблюдаться «прорывные» кровотечения и кровянистые выделения.
При появлении кровянистых выделений/кровотечения на фоне приема препарата Велледиен, которые
— продолжаются более 6 месяцев от начала приема препарата, — начинаются через 6 месяцев после начала приема препарата и продолжаются даже после
его отмены,
женщине необходимо обратиться к врачу — это может быть признаком гиперплазии эндометрия.
Рак молочной железы
Данные разных клинических исследований с точки зрения доказательной медицины в
отношении риска развития рака молочной железы при приеме тиболона противоречивы и требуется проведение дальнейших исследований.
По данным «Исследования миллиона женщин» было выявлено значимое увеличение риска развития рака молочной железы при применении тиболона в дозе 2,5 мг (см. раздел «
Побочное действие
»). Этот риск становился явным через несколько лет применения препарата и возрастал с увеличением продолжительности применения, возвращаясь к исходному уровню через несколько лет (чаще через 5 лет) после прекращения применения препарата.
Эти результаты не были подтверждены в ходе исследования с использованием Базы Данных Общей (врачебной) Практики (GPRD).
Рак яичников
Рак яичников распространен значительно меньше, чем рак молочной железы. Длительная (не менее 5-10 лет) заместительная монотерапия эстрогенами связывалась с незначительным повышением риска развития рака яичников.
Некоторые исследования, включая исследование «Инициатива здоровья женщин» (WHI) свидетельствуют о том, что длительная терапия комбинированными препаратами для ЗГТ может обладать аналогичным или несколько более низким риском.
В «Исследовании миллиона женщин» было показано, что относительный риск развития рака яичников при применении тиболона был аналогичен риску, связанному с применением других видов ЗГТ.
Венозная тромбоэмболия
Препараты для ЗГТ, содержащие только эстрогены, или комбинированные препараты для ЗГТ, содержащие эстроген и гестаген, могут увеличивать риск возникновения ВТЭ (тромбоза глубоких вен или тромбоэмболии легочной артерии) в 1,3 — 3 раза, особенно в течение первого года применения препаратов для ЗГТ (см. раздел «
Побочное действие
»).
Данные об увеличении риска развития ВТЭ при применении тиболона недостаточны, однако нельзя исключить незначительное увеличение риска по сравнению с женщинами, не принимавшими тиболон.
Пациентки с известными тромбофилическими состояниями имеют повышенный риск развития ВТЭ и прием препарата Велледиен может увеличить этот риск, поэтому применение препарата данной популяцией пациенток противопоказано (см. раздел «
Противопоказания
»).
Факторами риска развития ВТЭ являются применение эстрогенов, пожилой возраст, обширное оперативное вмешательство, длительная иммобилизация, ожирение (индекс массы тела (ИМТ) >30 кг/м2), беременность и послеродовой период, системная красная волчанка и рак.
Особое внимание следует уделить мерам профилактики, предотвращающим развитие тромбоза, ВТЭ в послеоперационном периоде. Рекомендуется прекращение терапии препаратом Велледиен за 4-6 недель перед хирургическим вмешательством, если в дальнейшем предполагается длительное соблюдение постельного режима. Лечение не должно возобновляться, пока у женщины не восстановится двигательная активность.
Женщинам, у которых ВТЭ в анамнезе отсутствует, но которые имеют родственников первой степени родства, имеющих в анамнезе тромбоз в молодом возрасте, может быть предложен скрининг (следует информировать женщину, что при скрининге выявляется лишь часть тромбофилических состояний). Если выявлено тромбофилическое состояние, которое обособлено от тромбоза у родственников, или серьезное нарушение (например, дефицит антитромбина III, протеина S, протеина C или комбинация нарушений), прием препарата Велледиен противопоказан.
Перед назначением тиболона женщинам, получающим антикоагулянты, врач должен тщательно оценить соотношение польза/риск применения ЗГТ или тиболона.
Если после начала лечения развивается ВТЭ прием препарата необходимо прекратить. Женщина должна быть информирована о необходимости немедленного обращения к врачу, если появятся симптомы потенциальной тромбоэмболии (боль и односторонний отек нижней конечности, внезапная боль в груди, одышка).
Ишемическая болезнь сердца
В рандомизированных контролируемых исследованиях не получено доказательств защиты от инфаркта миокарда у женщин с наличием или отсутствием ИБС, которые получали ЗГТ комбинированными препаратами (эстроген/гестаген) или препаратами для ЗГТ, содержащими только эстроген. В эпидемиологических исследованиях с использованием базы GPRD не было получено доказательств защиты от инфаркта миокарда у женщин в постменопаузе, которые получали тиболон.
Велледиен или какие-либо другие препараты для ЗГТ не должны применяться для профилактики сердечно-сосудистых заболеваний.
Ишемический инсульт
Прием тиболона увеличивает риск возникновения ишемического инсульта, начиная с первого года применения (см. раздел «
Побочное действие
»). Абсолютный риск возникновения инсульта строго зависит от возраста, и, следовательно, данный эффект тиболона тем больше, чем больше возраст.
При возникновении необъяснимых мигренеподобных головных болей с или без нарушения зрения необходимо как можно быстрее обратиться к врачу. В этом случае нельзя принимать препарат до тех пор, пока врач не подтвердит безопасность продолжения ЗГТ, поскольку такие головные боли могут быть ранним диагностическим признаком возможного инсульта.
Другие состояния
• По имеющимся данным применение тиболона приводило к значительному
дозозависимому снижению холестерина ЛПВП (липопротеинов высокой плотности) (с 16,7 % при дозе 1,25 мг до 21,8 % при дозе 2,5 мг после двух лет
применения).
• Снижалась общая концентрация триглицеридов и липопротеинов. Снижение концентрации общего холестерина и холестерина ЛПОНП (липопротеинов очень низкой плотности) не являлось дозозависимым. Концентрация холестерина ЛПНП (липопротеинов низкой плотности) не изменялась. Клиническое значение этих данных пока неизвестно.
• Эстрогены могут вызывать задержку жидкости, поэтому пациентки с сердечной или почечной недостаточностью должны находиться под тщательным наблюдением
врача.
• Женщины с уже имеющейся гипертриглицеридемией должны находиться под
тщательным наблюдением врача во время терапии тиболоном, так как редкие
случаи значительного повышения концентрации триглицеридов в плазме крови, способствующие развитию панкреатита, отмечались во время терапии эстрогенами при данном состоянии.
• Прием тиболона может вызвать незначительное снижение концентрации в плазме крови тироксинсвязывающего глобулина (ТСГ) и общего Т4. Концентрация общего Т3 не изменяется. Тиболон снижает концентрацию глобулина, связывающего половые гормоны (ГСПГ), но не влияет на концентрацию кортикостероидсвязывающего глобулина (КГС) и свободного кортизола.
• Применение препаратов для ЗГТ не улучшает когнитивную функцию. Имеются данные о повышенном риске возможного развития деменции у женщин при начале непрерывной терапии препаратами для ЗГТ, содержащими только эстрогены, в возрасте после 65 лет (см. раздел «
Побочное действие
»).
Влияние на способность управления транспортными средствами, механизмами
Не отмечено какого-либо действия тиболона на концентрацию внимания и способность управлять транспортными средствами и другими механизмами.
Форма выпуска
Таблетки 2,5 мг. По 28 таблеток в блистере из ПВХ/Ал фольги. По 1 блистеру вместе с
инструкцией по применению помещают в пачку картонную.
Условия хранения
Хранить при температуре не выше 25 °С.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять препарат по истечении срока годности.
Условия отпуска
Отпускают по рецепту.
Владелец (держатель) Регистрационного удостоверения
Эксэлтис Хелскеа С.Л.
Авенида Миралкампо, 7, Полигоно Индустриаль Миралкампо,
19200 Асукека-де-Энарес, Гвадалахара, Испания.
Производитель
Лабораториос Леон Фарма С.А.,
Провинция Леон, г. Виллаквиламбре 24008, ул. Ла-Валлина, индустриальный полигон Наватехэра, Испания
Получить дополнительную информацию о препарате, а также направить свои претензии и информацию о нежелательных явлениях можно по следующему адресу в России:
Московское Представительство компании с ограниченной ответственностью
«Эксэлтис Хелскеа С.Л.»
119435, Москва, Большой Саввинский пер., д.11, офис II.
Тел./факс:+7 (495) 648 39 47, +7 (495) 648 63 54.
Данная версия инструкции действует с 27.09.2017 г
Купить Велледиен в planetazdorovo.ru
*Цена в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
-
Архив журнала
/ -
2003
/ - №11
Тиболон как альтернатива заместительной гормональной терапии
Е.А. Ушкалова
Заместительная гормональная терапия (ЗГТ), наряду с положительными эффектами, не лишена и ряда недостатков. Это диктует необходимость поиска эффективных и безопасных альтернатив ЗГТ при постменопаузальных нарушениях, одной из которых является тиболон — синтетический стероид, обладающий андрогенными, гестагенными и эстрогенными свойствами. Рассматривается влияние тиболона на климактерические симптомы и качество жизни женщин в постменопаузе. Обсуждаются эффекты этого препарата на нервно-психическое состояние и когнитивные функции, факторы риска сердечно-сосудистых заболеваний, костную ткань и эндометрий. Отмечается возможное протективное влияние тиболона в отношении рака молочной железы.
Заместительная гормональная терапия (ЗГТ) за последние десятилетия получила широкое распространение, особенно за рубежом. Например, в США в настоящее время ее получают около 6 млн. женщин [1]. Это обусловлено тем, что те или иные климактерические симптомы имеют место более чем у 75% женщин в постменопаузе, причем, примерно, у 25% из них они оцениваются как тяжелые [2]. Наряду с положительными эффектами, ЗГТ не лишена и ряда недостатков, поэтому поиск эффективных и безопасных альтернатив продолжается. В качестве одной из них рассматривается тиболон – синтетический стероид, обладающий андрогенными, гестагенными и эстрогенными свойствами [3]. Препарат находится на мировом фармацевтическом рынке более двух десятилетий и зарегистрирован примерно в 70 странах мира. Он был разработан специально для лечения остеопороза, однако, благодаря уникальным фармакологическим свойствам, вскоре был также зарегистрирован для лечения климактерического синдрома и профилактики остеопороза.
Фармакологические эффекты тиболона преимущественно обусловлены его метаболитами, воздействующими на разные органы и ткани [4]. Тиболон- синтетический стероид, при попадании внутрь метаболизируется с образованием трех метаболитов: 3альфа-OH-тиболон, 3бета-OH-тиболон и 4сигма-изомер, которые обладают различным сродством к стероидным рецепторам. Исследования in vitro показали, что гидроксиметаболиты тиболона имеют высокое сродство к эстрогенным рецепторам (преимущественно к a-рецепторам), а 4сигма-изомер – обладает высоким аффинитетом к рецепторам прогестерона и слабым сродством к андрогенным рецепторам [5]. Концентрация различных метаболитов тиболона варьирует в разных органах и тканях [4], в связи с чем препарат проявляет тканеселективное действие [7]. На костную ткань и влагалище тиболон оказывает эстрогенный эффект. В эндометрии проявляется гестагенное действие 4сигма-изомера, а в головном мозге и печени этот изомер оказывает андрогенные эффекты. В молочной железе тиболон вызывает мощное угнетение сульфатазы и ингибирование 17бета-гидроксистероиддегидрогеназы (тип I), что приводит к блокаде превращения эстрона сульфата в эстрон и затем, в эстрадиол.
Оказывая селективное гормональное действие на разные органы-мишени, тиболон вызывает различные эффекты у женщин в постменопаузе, которые были изучены более чем в 20 рандомизированных контролируемых двойных слепых исследованиях [8].
В связи с уникальным механизмом действия, тиболон выделен в отдельный класс терапии – STEAR (selective tissue estrogenic activity regulator; тканеселективный регулятор эстрогенной активности). Официальное представление тиболона как нового класса терапии состоялось в мае 2003 года на шестом европейском конгрессе по менопаузе.
В настоящее время, с учетом нерандомизированных и открытых исследований, а также клинических испытаний и ретроспективных анализов, изучению тиболона у женщин посвящено более 400 работ [8].
Влияние тиболона на климактерические симптомы и качество жизни женщин в постменопаузе
Влияние тиболона на климактерические симптомы было изучено не менее чем в 8 рандомизированных двойных слепых клинических исследованиях, 4 из которых были плацебо-контролируемыми [9-13]. В одном исследовании проводилось сравнение тиболона с эстрадиола валератом [13], еще в одном – с комбинацией конъюгированных эстрогенов и медрокспрогестерона ацетата [14], в двух – с комбинацией эстрадиола и норэтистерона ацетата [15,16].
Эти исследования показали, что тиболон в дозе 2,5 мг по эффективности ослабления приливов не уступает стандартным режимам ЗГТ. Препарат также эффективен при лечении приливов, развивающихся при терапии агонистами гонадотропин-рилизинг гормона [17].
Во многих исследованиях продемонстрированы благоприятные эффекты тиболона и в отношении других симптомов менопаузы, включая повышенную утомляемость, психологическую нестабильность, головные боли и бессонницу [9,12,14].
В работе Genazzani и соавт. показано, что ослабление приливов жара при лечении тиболоном ассоциируется с улучшением сна и настроения [11]. Исследователи высказали предположение, что последний эффект обусловлен бета-эндорфинами, концентрация которых под влиянием тиболона повышается. В небольшом исследовании, включавшем молодых женщин с удаленной маткой и яичниками, тиболон проявлял одинаковую эффективность в отношении ослабления приливов и улучшения настроения с эстрадиола валератом [13].
Благодаря наличию эстрогенного действия, тиболон нормализует созревание клеток влагалища, уменьшает его сухость и диспареунию у женщин в менопаузе [18,19]. По данным ряда исследований, он не уступает эстрогенам по эффективности устранения этих симптомов. Более того, в проспективных рандомизированных исследованиях показано, что сексуальность женщин при применении тиболона повышается в большей степени, чем при использовании эстрогенов или их комбинаций с прогестинами [15,20-24].
В плацебо-контролируемых исследованиях доказано, что тиболон увеличивает либидо и сексуальную активность [25]. Под влиянием препарата особенно усиливались сексуальные фантазии, половое возбуждение и оргазм. Открытое многоцентровое исследование с участием 184 женщин, впервые получавших тиболон в течение 4 месяцев, продемонстрировало значительное повышение степени их удовлетворенности разными аспектами половой жизни [25]. В основе этих эффектов лежат 2 механизма: прямое андрогенное действие 4сигма-изомера и увеличение циркуляции свободного тестостерона. Под влиянием тиболона количество циркулирующего гормоносвязывающего глобулина снижается примерно на 50% [26,27]. Вследствие этого уменьшается концентрация общего тестостерона, но значительно возрастает уровень его свободной активной фракции. Изменения уровня гормонов, вызываемые тиболоном, благоприятно отличаются от таковых, вызываемых эстрогеном (повышение уровня гормоносвязывающего глобулина и снижение уровней общего и свободного тестостерона). Слабое андрогенноподобное действие при приеме тиболона клинически обусловливает, главным образом, улучшение качества жизни, в виде благоприятного влияния на настроение и улучшение либидо. Некоторые авторы даже рекомендуют применение тиболона для усиления полового влечения у женщин с персистирующим, несмотря на адекватную комбинированную ЗГТ, снижением либидо [30]. При этом важно, что тиболон не вызывает андрогенных побочных эффектов, таких как акне и гирсутизм [3].
В отличие от эстрогенов тиболон не оказывает эстрогенного действия на миометрий, напротив, его 4сигма-изомер вызывает гестагенный эффект. В результате, при применении тиболона не происходит стимуляции эндометрия и, соответственно, нет необходимости в дополнительном назначении гестагена для защиты миометрия [7,28,29].
В сравнительных исследованиях с комбинацией эстрадиола и норэтистерона ацетата количество эпизодов вагинальных кровотечений у женщин, получавших тиболон, было примерно в 2 раза меньшим, чем у женщин, получавших комбинированную терапию [31,32]. По результатам двойного слепого многоцентрового европейского исследования, тиболон вызывал кровотечения существенно реже, чем при использовании комбинированной монофазной терапии (конъюгированные эстрогены с медроксипрогестероном ацетатом) [23]. Еще в одном рандомизированном исследовании пероральное применение тиболона (2,5 мг/сут) было сопряжено с меньшей частотой кровотечений, чем циклическая трансдермальная комбинированная терапия (пластырь 17бета-эстрадиола 50 мкг/сут в течение 14 дней, затем пластырь 17бета-эстрадиола 50 мкг/сут + норэтистерона ацетат 0,25 мг/сут в течение последующих 14 дней) [33]. Кровотечения, вызванные тиболоном, чаще наблюдаются в раннем постменопаузальном периоде, в связи с чем в настоящее время назначение препарата рекомендуют женщинам, которые находятся в менопаузе не менее 1 года [3].
В целом, ослабление климактерических и урогенитальных симптомов под влиянием тиболона ассоциируется с улучшением качества жизни женщин [36].
Влияние тиболона на нервно-психическое состояние и когнитивные функции
Тиболон оказывает умеренный положительный эффект на настроение [27,31]. В небольшом открытом исследовании длительное применение тиболона (10 лет) приводило к уменьшению нервозности в ответ на небольшой стресс [35]. Эти данные были подтверждены в другом рандомизированном исследовании [36].
Эффекты препарата на когнитивные функции изучены недостаточно, что обусловлено сложностью проведения подобных исследований, требующих соответствия основной и контрольной групп по множеству параметров (уровень интеллекта, возраст, образование, занимаемая должность, психический статус и др.), и отсутствием стандартизованных определений ряда понятий и стандартизованных методов их измерения. Результаты небольшого исследования позволяют предположить, что при кратковременном применении (3-6 месяцев) тиболон может способствовать сохранению когнитивной функции у женщин в постменопаузе [37]. Однако все эти данные требуют подтверждения в хорошо спланированных больших исследованиях.
Влияние тиболона на факторы риска сердечно-сосудистых заболеваний
Под влиянием тиболона происходят отличные от традиционной ЗГТ (чистые эстрогены и комбинированные эстроген-гестагенные комбинации) изменения концентраций липидов в крови. Изучению влияния тиболона на липидный профиль и факторы свертывания крови было посвящено 7 плацебо-контролируемых, двойных слепых исследований и 2 сравнительных двойных слепых исследования с комбинацией эстрадиола и норэтистерона ацетата. В краткосрочных исследованиях тиболон в дозе 2,5 мг/сут снижал уровень холестерина липопротеидов высокой плотности (ЛПВП) примерно на 20%, общего холестерина – на 10% и триглицеридов – на 20%. Он также вызывал небольшое снижение концентрации холестерина липопротеидов низкой плотности (ЛПНП) или не влиял на него [25,26,32,38]. В других плацебо-контролируемых исследованиях снижение уровней холестерина ЛПВП и триглицеридов под влиянием препарата было более выраженным, однако концентрации холестерина ЛПНП и липопротеина (альфа) не изменялись [11,28,29]. В некоторых исследованиях снижение уровня ЛПВП под влиянием тиболона имело недостоверный характер [40,41].
Снижение уровня холестерина ЛПВП при применении тиболона ассоциировалось с повышением активности липазы в печени (андрогенный эффект), однако в исследовании показано, что при этом способность плазмы пациенток высвобождать холестерин из артериальных стенок оставалась неизменной [42]. В исследовании на обезьянах значительное снижение уровня холестерина ЛПВП не сопровождалось обострением атеросклероза подвздошной артерии, что связывают с благоприятным влиянием препарата на функцию сосудов или печеночный метаболизм [43].
В рандомизированном клиническом исследовании показано, что существенное снижение уровня ЛПВП (в среднем на 27%) при лечении тиболоном было обусловлено его влиянием лишь на один подкласс ЛПВП, в связи с чем антиатерогенные функции (обратный транспорт холестерина и угнетение окисления ЛПНП) оставались неизмененными [43]. Недостатком данного исследования является его небольшая продолжительность (12 недель), однако полученные результаты полностью совпадают с данными 2-летних экспериментальных исследований на обезьянах. Они были подтверждены еще в одном рандомизированном, плацебо-контролируемом исследовании, продолжавшемся 3 месяца [44].
Потенциально неблагоприятные эффекты, связанные со снижением уровня холестерина ЛПВП, уравновешиваются влиянием тиболона на эндотелин и липопротеин (альфа), антиишемическими эффектами, обнаруженными у женщин со стенокардией, и повышением чувствительности к инсулину [45-49]. В длительных исследованиях уровень холестерина ЛПВП возвращался к исходному через 3 года лечения этим препаратом [46-49]. Недавно была показана способность тиболона снижать концентрации тромбоксана B2, что может приводить к улучшению метаболизма простагландинов и снижать риск сердечно-сосудистых заболеваний [50].
В отличие от эстрогенов тиболон не оказывает выраженного действия на повышение свертываемости крови, но стимулирует фибринолитическую активность. В плацебо-контролируемых исследованиях показано, что длительное применение тиболона приводит к повышению уровней гемоглобина, антитромбина III, плазминогена и числа тромбоцитов [51,52]. В многоцентровом рандомизированном двойном слепом исследовании не удалось выявить существенного влияния препарата на свертываемость крови [32].
По мнению исследователей, клиническое значение эффектов тиболона на метаболизм липидов и гемостаз остается неясным и требует дальнейшего изучения.
При лечении тиболоном наблюдалось 3-4-кратное увеличение уровня С-реактивного белка, что сопоставимо с таковым при применении стандартной ЗГТ [53]. Однако, значение изменений уровня С-реактивного белка для клинических проявлений сердечно-сосудистых заболеваний у женщин в менопаузе остается не до конца ясным [8]. Тиболон не влияет на уровень гомоцистеина – другого вещества, с которым связывают риск коронарной болезни [54].
Тиболон снижает уровень свободных жирных кислот в плазме крови, что приводит к нормализации соотношения симпатических и парасимпатических влияний на сердце и, по мнению исследователей, может способствовать предупреждению инфаркта миокарда и сердечной недостаточности [55]. Еще одним благоприятным эффектом тиболона на сердечно-сосудистую систему является прямое влияние на эндотелиальные клетки, обусловливающее снижение адгезии лейкоцитов к эндотелию [56].
Тромбоэмболических осложнений в клинических исследованиях препарата не наблюдалось [57]. Повышенного риска венозной тромбоэмболии не удалось выявить и по результатам широкого медицинского применения тиболона в течение более 15 лет во многих странах мира [3]. Данные, полученные на 4537 женщинах, участвовавших в III и IV фазах клинических испытаний тиболона, показали, что относительный риск для всех сердечно-сосудистых заболеваний, составил: RR=0,58 (0,31-1,10).
Данные экспериментальных исследований у обезьян дают основание предполагать, что тиболон не оказывает существенного влияния на сердечно-сосудистую систему, по-видимому, вследствие того, что его негативные эффекты уравновешиваются позитивными. Длительное (в среднем 7,5 лет) наблюдение за женщинами, получавшими тиболон, также не позволило выявить повышение толщины интимы сонной артерии и увеличение числа атеросклеротических бляшек [58]. Однако, окончательно вопрос о безопасности тиболона в отношении сердечно-сосудистой системы может быть решен только в хорошо спланированных крупномасштабных клинических исследованиях.
Влияние тиболона на костную ткань
Влияние тиболона на костную ткань является следствием его эстрогенной активности [8]. Оно было изучено в 8 рандомизированных двойных слепых исследованиях, 7 из которых были плацебо-контролируемыми и одно – сравнительным с эстрогенами [59-66]. Во всех исследованиях было продемонстрировано значительное повышение минеральной плотности кости в поясничном отделе позвоночника и шейке бедра под влиянием тиболона по сравнению с плацебо [67]. Наиболее выраженным благоприятное влияние тиболона на костную ткань было у женщин с остеопорозом. Оно проявлялось уже при кратковременном приеме препарата (3 месяца) [65] и сохранялось при длительном применении (10 лет) [68].
По эффективности предотвращения потери костной ткани у женщин в постменопаузе тиболон в клинических исследованиях не уступал эстрогенам и комбинированной ЗГТ [41,59,69,70]. Сходная эффективность тиболона и эстрогенов подтверждена результатами мета-анализа, включавшего 39 рандомизированных контролируемых 2-летних исследований [71]. Преимуществом тиболона перед стандартной ЗГТ является и лучшая переносимость, которая позволяет применять его на протяжении длительного времени (10 лет и более) [68,72]. Препарат также предотвращает потерю костной ткани, вызванную агонистами гонадотропин-рилизинг гормона [73].
Результаты измерения минеральной плотности кости при лечении тиболоном позволяют предположить наличие у него протективного эффекта в отношении переломов, обусловленных остеопорозом, однако это предположение должно быть подтверждено в целенаправленных клинических исследованиях.
Влияние тиболона на эндометрий
Несмотря на отдельные сообщения о пролиферации эндометрия у женщин, получавших тиболон [74,75], в длительных (до 8 лет) исследованиях показано наличие у препарата протективного эффекта в отношении эндометрия [29,76-78]. Он обусловлен тем, что преобладающим (если не единственным) метаболитом тиболона в эндометрии является 4сигма-изомер, связывающийся с рецептором прогестерона и, таким образом, защищающий его от агонистических эффектов двух метаболитов с эстрогенной активностью [79]. Данные, полученные в III и IV фазах клинических испытаний тиболона, показали, что относительный риск рака эндометрия составил RR=0,37 (0,03-0,59).
В открытом проспективном многоцентровом исследовании не было отмечено стимулирующего влияния тиболона на эндометрий через 12 и 24 месяцев лечения соответственно у 98,2% и 91,9% обследованных женщин [81].
Частота прорывных кровотечений при применении тиболона значительно ниже, чем при применении комбинированной ЗГТ [20,26,31,81]. Аменорея при приеме тиболона достигается быстрее: у 90% женщин она наступает в течение 6 месяцев лечения [31,74,75]. Кровотечения реже отмечаются у женщин более старшего возраста [82]. Наблюдение в течение 3 лет за женщинами с фибромами матки, получавшими тиболон, не позволило выявить роста миом [83].
Тиболон и рак молочной железы
Влияние тиболона на клетки молочной железы изучалось особенно тщательно. В ткани молочной железы тиболон и его метаболиты оказывают ингибирующее влияние на ферменты, способствующие локальному синтезу эстрадиола (сульфатаза и 17сигма-гидроксистероид дегидрогеназа (тип I)) и напротив, активирует ферменты (сульфотрансфераза и 17сигма-гидроксистероид дегидрогеназа (тип II)), преобразующие активный эстрадиол в менее активный эстрон и неактивные сульфатированные формы, которые выводятся из организма с мочой. Таким образом, тиболон отличается уникальным механизмом действия, который обусловливает не только отсутствие стимуляции эстрогенных рецепторов в молочной железе эстрогенными метаболитами тиболона, но и благодаря специфической «ферментной регуляции», способствует снижению локальной концентрации активного эстрадиола [84]. Помимо этого в исследованиях in vitro у тиболона была выявлена антипролиферативная активность, способность усиливать клеточную дифференциацию и вызывать апоптоз раковых клеток молочной железы [85].
В клинических исследованиях доказано, что тиболон значительно реже приводит к увеличению плотности молочной железы при маммографии и реже вызывает масталгию, чем эстрогены и комбинированная ЗГТ [31,85-87]. Положительные эффекты тиболона связывают с его влиянием на ферменты, принимающие участие в локальной продукции эстрогенов в тканях молочной железы. В III и IV фазах клинических испытаний препарата с участием 4537 женщин, задокументированная частота рака молочной железы составила 1,59 на 1000 человеко-лет в основной группе против 3,15 в группе плацебо. Относительный риск рака молочной железы при приеме тиболона составил: RR=0,50 (0,11-2,54) [80].
Вышеизложенное позволило высказать предположение о том, что тиболон обладает протективным действием в отношении рака молочной железы [3].
Тиболон и сахарный диабет
У пожилых женщин с сахарным диабетом 2 типа при применении тиболона в дозе 2,5 мг/сут не было выявлено значительных изменений липидного профиля [88]. Препарат повышал чувствительность к инсулину в случае резистентности к гормону [88]. Он не оказывал отрицательного влияния на артериальное давление у женщин с сахарным диабетом и гипертензией [38]. Вышеприведенные эффекты позволяют рекомендовать тиболон для применения больным диабетом в постменопаузе [38,89].
Заключение
На сегодняшний день тиболон может рассматриваться в качестве достойной альтернативы стандартной ЗГТ для большинства женщин в постменопаузе [89]. Тиболон проявляет сходную клиническую эффективность с эстрогенами при симптомах менопаузы, как приливы и различные урогенитальные нарушения, но превосходит последние по влиянию на сексуальность. Его безопасность в отношении эндометрия и способность предотвращать потерю костной ткани сопоставимы с таковыми комбинированной ЗГТ, однако тиболон реже вызывает прорывные кровотечения. Суммарный эффект тиболона и его метаболитов на сердечно-сосудистую систему в настоящее время рассматривают как нейтральное действие. Дальнейшие рандомизированные исследования позволят сделать окончательные выводы. Подтверждения требует и наличие у тиболона протективного эффекта в отношении рака молочной железы.
Такого рода исследования уже начаты. Это крупные многоцентровые рандомизированные слепые плацебо-контролируемые исследования:
- исследование LIFT (Long-term Interventional Fracture study in osteoporotic patients), направленное на выявление частоты переломов;
- исследование OPAL (Osteoporosis Prevention and Antiatherosclerosis effects of TiboLone), оценивающее влияние препарата на костную ткань и сердечно-сосудистую систему;
- исследование LIBERATE (Livial Intervention following Breast Cancer; Efficacy, Recurrence, and Tolerability Endpoints), посвященное безопасности тиболона в отношении молочной железы;
- исследование THEBES (Tibolone Histology of the Endometrium and Breast Endpoints Study), оценивающее ответ эндометрия на лечение [21].
Результаты этих исследований позволят окончательно определить место тиболона в терапии и профилактике постменопаузальных нарушений.
Литература
- Hamdy RC: Hormonal replacement therapy. South Med J 2001; 94:1141-2
- Porter M, Penney GC, Russell D, et al. A population based survey of women’s experience of the menopause. Br J Obstet Gynaecol 2002;103:1025-8.
- Speroff L, Clarkson ThB. Is tibolone a Viable Alternative to HT? Obstet Gynecol 2003;48:54-68.
- Vos RM, Krebbers SF, Verhoeven CH, et al. The in vivo human metabolism of tibolone. Drug Metab Dispos 2002;30:106-12.
- Blok LJ, De Ruiter PE, Kuhne EC, et al. Progestogenic effects of tibolone on human endometrial cancer cells. Clin Endocrinol Metab 2003;88:2327-34.
- Bodine PV, Harris HA, Lyttle CR, Komm BS. Estrogenic effects of 7alpha-methyl-17alpha-ethynylestradiol: a newly discovered tibolone metabolite. Steroids 2002;67:681-6.
- Kloosterboer HJ. Tibolone: a steroid with a tissue-specific mode of action. J Steroid Biochem Mol Biol 2001;76:231-8.
- Modelska K, Cummings S. Tibolone for Postmenopausal Women: Systematic Review of Randomized Trials. J Clin Endocrinol Metab 2002;87:16-23.
- Kicovic PJL, Cort_s-Prieto M, Milojevic S, Franchi F. Placebo-controlled cross-over study of effects of Org OD 14 in menopausal women. Reproduction 1982;6:81-91.
- Cittadini JB, Ben AR, Denari HJ, et al. Use of a new steroid (Org OD 14) in the climacteric syndrome. Reproduccion 1982;6:69-79.
- Genazzani AR, Petraglia F, Genazzani AD, et al. Effects of Org OD 14 on pituitary and peripheral _-endorphin in castrated rats and post-menopausal women. Maturitas 1987;Suppl. 1:35-48.
- Nevinny-Stickel J. Double-blind cross-over study with Org OD 14 and placebo in postmenopausal patients. Arch Gynecol 1983;234:27-31.
- Crona NGL, Samsioe UB, Silfverstolpe G. Treatment of climacteric complaints with Org OD 14: a comparative study with oestradiol valerate and placebo. Maturitas 1988;9:303-8.
- Bedenek-Jaszmann LJ Long-term placebo-controlled efficacy and safety study of ORG OD 14 in climacteric women. Maturitas 1987;Suppl. 1:25-33.
- Nathorst-Boos J, Hammar M. Effect on sexual life-a comparison between tibolone and a continuous estradiol-norethisterone acetate regimen. Maturitas 1997;26:15-20.
- Doren M, Ruebig A, Holzgreve W. Defferential effects on the androgen status of postmenopausal women treated with tibolone and continuous combined estradiol and norethindrone acetate replacement therapy. Fertil Steril 2001;75:554-8.
- Taskin O, Yalcinoglu AI, Kucuk S, et al. Effectiveness of tibolone on hypoestrogenic symptoms induced by goserelin treatment in patients with endometriosis. Fertil Steril 1997;67:40-45.
- Botsis D, Kassanos D, Kalogirou D, et al. Vaginal ultrasound of the endometrium in postmenopausal women with symptoms of urogenital atrophy on low dose oestrogen or tibolone treatment: a comparison. Maturitas 1997;26:57-62.
- Morris E, Wilson P, Robinson J, Rymer J. Long term effects of tibolone on the genital tract in postmenopausal women. Br J Obstet Gynaecol 1999;106: 954-9.
- Kokcu A, Cetinkaya MB, Yanik F, et al. The comparison of effects of tibolone and conjugated estrogen-medroxyprogesterone acetate therapy on sexual performance in postmenopausal women. Maturitas 2000;36:75-80.
- Mendoza N, Suarez AM, Alamo F, et al. Lipid effects, effectiveness and acceptability of tibolone versus transdermic 17 beta-estradiol for hormonal replacement therapy in women with surgical menopause. Maturitas 2000;37:37-43.
- Castelo-Branco C, Vicente JJ, Figueras F, et al. Comparative effects of estrogens plus androgens and tibolone on bone, lipid pattern and sexuality in postmenopausal women. Maturitas 2000;34:161-8.
- Huber J, Palacios S, Berglund L, et al. Effects of tibolone and continuous combined hormone replacement therapy on bleeding rates, quality of life and tolerability in postmenopausal women. BJOG 2002;109:886-93.
- Egarter C, Topcuoglu A, Vogl S, et al. Hormone replacement therapy with tibolone: effects on sexual functioning in postmenopausal women. Acta Obstet Gynecol Scand 2002;81:649-53.
- Davis S, Burger H. Use of androgens in postmenopausal women. Curr Opin Obstet Gynecol 1997; 9:177-80.
- Laan E, van Lunsen RH, Everaerd W. The effects of tibolone on vaginal blood flow, sexual desire and arousability in postmenopausal women. Climacteric 2001;4:28-41.
- Doren M, Rubig A, Coelingh Bennink HJ, et al. Differential effects on the androgen status of postmenopausal women treated with tibolone and continuous combined estradiol and norethindrone acetate replacement therapy. Fertil Steril 2001;75:554-9.
- Tang BLK, Markiewicz HJ, Gurpide E. Human endometrial 3_-hydroxysteroid dehydrogenase/isomerase can locally reduce intrinsic estrogenic/progestagenic activity ratios of a steroidal drug (Org OD 14). J Steroid Biochem Mol Biol 1993;45:345-51.
- Genazzani A, Benedek-Jaszmann DM, Andolsek L, et al. Org OD 14 and the endometrium. Maturitas 1991;13:243-51.
- Davis SR.The effects of tibolone on mood and libido. Menopause 2002;9:162-70.
- Hammar M, Christau J, Rud T, Garre K. A double-blind, randomised trial comparing the effects of tibolone and continuous combined hormone replacement therapy in postmenopausal women with menopausal symptoms. Br J Obstet Gynaecol 1998;105:904-11.
- Winkler U, Altkemper B, Helmond FA, et al. Effects of tibolone and continuous combined hormone replacement therapy on parameters in the clotting cascade: a multicenter, double-blind, randomized study. Fertil Steril 2000;74:10-9.
- Mendoza N, Pison JA, Fernandez M, et al. Prospective, randomised study with three HRT regimens in postmenopausal women with an intact uterus. Maturitas 2002;4:289-98.
- Bukulmez O, Al A, Gurdal H, et al. Short-term effects of three continuous hormone replacement therapy regimens on platelet tritiated imipramine binding and mood scores: a prospective randomized trial. Fertil Steril 2001;75:737-43.
- Fluck E, File SE, Rymer J. Cognitive effects of 10 years of hormone-replacement therapy with tibolone. J Clin Psychopharmacol 2002;22:62-7.
- Yazici K, Pata O, Yazici A, et al. [The effects of hormone replacement therapy in menopause on symptoms of anxiety and depression]. Turk Psikiyatri Derg 2003;14:101-5.
- Pan HA, Wang ST, Pai MC, et al. Cognitive function variations in postmenopausal women treated with continuous, combined HRT or tibolone. A comparison. J Reprod Med.2003;48:375-80.
- Lloyd G, McGing A, Patel N, et al. A randomised placebo controlled trial of the effects of tibolone on blood pressure and lipids in hypertensive women. J Hum Hypertension 2000;14:99-104.
- D_ren M, R_big HJ, Holzgreve W. Resistance of pelvic arteries and plasma lipids in postmenopausal women: comparative study of tibolone and continuous combined estradiol and norethindrone acetate replacement therapy. Am J Obstet Gynecol 2000 183:575-82.
- Bjarnason N, Bjarnason KH, Bennink HJ, Christiansen C. Tibolone: influence on markers of cardiovascular disease. J Clin Endocrinol Metab 1997;82:1752-6.
- Castelo-Branco C, Casals E, Figueras F, et al. Two-year prospective and comparative study on the effects of tibolone on lipid pattern, behavior of apolipoproteins AI and B. Menopause. 1999;6:92-7.
- von Eckardstein A, Crook D, Elbers J, et al. Tibolone lowers high density lipoprotein cholesterol by increasing hepatic lipase activity but does not impair cholesterol efflux. Clin Endocrinol (Oxf) 2003;58:49-58.
- Ginsburg J, Prelevic GM. Antiatherosclerotic effects of tibolone. Menopause 2001;8:79-80.
- Pan HA, Wang ST, Chen CH, et al. Flow resistance in carotid and middle cerebral arteries in postmenopausal women: a comparative study of tibolone and continuous combined hormone replacement therapy. Climacteric 2002;5:259-265.
- Register TC, Wagner JD, Zhang L, et al. Effects of tibolone and conventional hormone replacement therapies on arterial and hepatic cholesterol accumulation and on circulating endothelin-1, vascular cell adhesion molecule-1, and E-selectin in surgically menopausal monkeys. Menopause 2002;9:411-21.
- Cagnacci A, Mallus E, Tuveri F, et al. Effect of tibolone on glucose and lipid metabolism in postmenopausal women. J Clin Endocrinol Metab 1997;82:251-3.
- Haenggi W, Bersinger NA, Mueller MD, et al. Decrease of serum endothelin levels with postmenopausal hormone replacement therapy or tibolone. Gynecol Endocrinol 1999;13:202-5.
- Farish E, Barnes JF, Rolton HA, et al. Effects of tibolone on lipoprotein(a) and HDL subfractions. Maturitas 1994;20:215-9.
- Lloyd GW, Patel NR, McGing EA, et al. Acute effects of hormone replacement with tibolone on myocardial ischaemia in women with angina. Int J Clin Pract 1998;52:155-7.
- Canbaz M, Vural P, Akgul C. Effects of tibolone on thromboxane B(2) levels in postmenopausal women. Gynecol Obstet Invest 2002;53:13-5.
- Parkin D, Smith F, Lindsay R, Hart DM. Effects of long-term Org OD 14 administration on blood coagulation in climacteric women. Maturitas 1989;11:95-101.
- Cortes-Prieto J. Coagulation and fibrinolysis in post-menopausal women treated with Org OD 14. Maturitas 1987;Suppl. 1:67-72.
- Garnero P, Jamin C, Benhamou CL, et al. Effects of tibolone and combined 17bet-estradiol and norethisterone acetate on serum C-reactive protein in healthy post-menopausal women: a randomized trial. Hum Reprod 2002;17:2748-53.
- Celik H, Ayar A, Tug N, et al. Effects of tibolone on plasma homocysteine levels in postmenopausal women. Fertil Steril 2002;78:347-350.
- Manzella D, Fornaro F, Carbonella M, et al. Effect of tibolone administration on heart rate variability and free fatty acid levels in postmenopausal women. Fertil Steri. 2002;78:1005-9.
- de Kleijn MJ, Wilmink HW, Bots ML, et al. Hormone replacement therapy and endothelial function. Results of a randomized controlled trial in healthy postmenopausal women. Atherosclerosis 2001;159:357-65.
- Davis SR Menopause: new therapies. MJA 2003;178:634-7.
- Prelevic GM, Kwong P, Byrne DJ, et al. A cross-sectional study of the effects of hormone replacement therapy on the cardiovascular disease risk profile in healthy postmenopausal women. Fertil Steril 2002;77:945-51.
- Berning B, Kuijk JW, Bennink HJ, et al. Effects of two doses of tibolone on trabecular and cortical bone loss in early postmenopausal women: a two-year randomized, placebo-controlled study. Bone 1996;19:395-9.
- Bjarnason N, Bjarnason J, Rosenquist C, Christiansen C. Tibolone: prevention of bone loss in late postmenopausal women. J Clin Endocrinol Metab 1996;81:2419-22.
- Bjarnason N, Bjarnason C, Christiansen C. The response in spinal bone mass to tibolone treatment is related to bone turnover in elderly women. Bone 1997;20:151-5.
- Studd J, Arnala I, Kicovic PM, et al. A randomized study of tibolone on bone mineral density in osteoporotic postmenopausal women with previous fractures. Obstet Gynecol 1998;92:574-9.
- Milner M, Harrison RF, Gilligan, et al. Bone density changes during two years treatment with tibolone or conjugated estrogens and norgestrel, compared with untreated controls in postmenopausal women. Menopause 2000;7:327-33.
- Rymer J, Robinson J, Fogelman I. Effects of 8 years of treatment with tibolone 2.5 mg daily on postmenopausal bone loss. Osteoporos Int 2001;12:478-83.
- Fenkci V, Yilmazer M, Fenkci S. Effects of short-time (3 months) tibolone treatment on bone turnover in postmenopausal women. Arch Gynecol Obstet 2003;268:85-7.
- Lippuner K, Haenggi W, Birkhaeuser MH, et al. Prevention of postmenopausal bone loss using tibolone or conventional peroral or transdermal hormone replacement therapy with 17beta-estradiol and dydrogesterone. J Bone Miner Res 1997;12:806-12.
- Lamy O, Krieg MA. [Hormone replacement therapy and its derivatives in the prevention and treatment of osteoporosis]. Rev Med Suisse Romande 2002;122:377-81.
- Rymer J, Robinson J, Fogelman I. Ten years of treatment with tibolone 2.5 mg daily: effects on bone loss in postmenopausal women. Climacteric 2002;5:390-8.
- Gambacciani M, Ciaponi M. Postmenopausal osteoporosis management. Curr Opin Obstet Gynecol 2000;12:189-97.
- Lippuner K, Haenggi W, Birkhaeuser MH, et al. Prevention of postmenopausal bone loss using tibolone or conventional peroral or transdermal hormone replacement therapy with 17bet-estradiol and dydrogesterone. J Bone Miner Res 1997;12:806-12.
- Doren M, Nilsson J-A, Johnell O. Effects of specific post-menopausal hormone therapies on bone mineral density in post-menopausal women: a meta-analysis. Human Reproduction 2003;18:1737-46.
- Kloosterboer HJ, Ederveen AG. Pros and cons of existing treatment modalities in osteoporosis: a comparison between tibolone, SERMs and estrogen (+/-progestogen) treatments. J Steroid Biochem Mol Biol 2002;83:157-65.
- Fedele L, Bianchi S, Raffaelli R, et al. A randomized study of the effects of tibolone and transdermal estrogen replacement therapy in postmenopausal women with uterine myomas. Eur J Obstet Gynecol Reprod Biol 2000;88:91-4.
- Ginsburg J, Prelevic G, Butler D, et al. Clinical experience with tibolone (Livial) over 8 years. Maturitas 1995;21:71-76.
- Meuwissen JH, Wiegerinck MA, Haverkorn MJ. Regression of endometrial thickness in combination with reduced withdrawal bleeding as a progestational effect of tibolone in postmenopausal women on oestrogen replacement therapy. Maturitas 1995;21:121-5.
- Siseles NO, Halperin H, Benencia HJ, et al. A comparative study of two hormone replacement therapy regimens on safety and efficacy variables. Maturitas 1995;21:201-10.
- Rymer J, Chapman MG, Fogelman I, et al. A study of the effect of tibolone on the vagina in postmenopausal women. Maturitas 1994;18:127-33.
- Botsis D, Kassanos D, Kalogirou D, et al. Vaginal ultrasound of the endometrium in postmenopausal women with symptoms of urogenital atrophy on low-dose estrogen or tibolone treatment: a comparison. Maturitas 1997;26:57-62.
- Markiewicz L, Gurpide E. In vitro evaluation of estrogenic, estrogen antagonistic and progestagenic effects of a steroidal drug (Org OD-14) and its metabolites on human endometrium. J Steroid Biochem 1990;35:535-41.
- Egarter C, Sator M, Berghammer P, et al. Efficacy, tolerability, and rare side effects of tibolone treatment in postmenopausal women. Int J Gynaecol Obstet 1999;64:281-6.
- Volker W, Coelingh Bennink HJ, Helmond FA. Effects of tibolone on the endometrium. Climacteric 2001;4:203-8.
- Landgren MB, Bennink HJ, Helmond FA, et al. Dose-response analysis of effects of tibolone on climacteric symptoms. BJOG 2002;109:1109-14.
- Berning B, van Kuijk C, Benink HJ, et al. Absent correlation between vaginal bleeding and oestradiol levels or endometrial morphology during tibolone use in early postmenopausal women. Maturitas 2000;35:81-8.
- Chetrite G, Kloosterboer JR. Effect of tibolone (Org OD14) and its metabolites on estrone sulphatase activity in MCF-7 and T-47D mammary cancer cells. Anticancer Res 1997;17:135-40.
- Gompel A, Siromachkova A, Kloosterboer HJ, Rostene W. Tibolone actions on normal and breast cancer cells. Eur J Cancer 2000;36:S76-S77.
- Kloosterboer HJ. Endocrine prevention of breast: any role for tibolone? Eur J Cancer 2002;38(suppl 6):S24-S25.
- Bulbul NH, Ozden S, Dayicioglu V. Effects of hormone replacement therapy on mammographic findings. Arch Gynecol Obstet 2003;268:5-8.
- Prelevic GM, Beljic T, Balint-Peric L, et al. Metabolic effects of tibolone in postmenopausal women with non-insulin dependent diabetes mellitus. Maturitas 1998;28:271-6.
- Szanto F. [Tibolone therapy in postmenopausal women with a history of many risk factors]. Orv Hetil 2003;144:701-4.