Язвенный колит
Версия: Клинические рекомендации РФ 2018-2020 (Россия)
Категории МКБ:
Язвенный колит (K51)
Разделы медицины:
Гастроэнтерология, Проктология
Общая информация
Краткое описание
Разработчик клинической рекомендации
Российская Гастроэнтерологическая Ассоциация
Общероссийская общественная организация «Ассоциация колопроктологов России»
Одобрено Научно-практическим Советом Минздрава РФ
В соответствии с Правилами поэтапного перехода медицинских организаций к оказанию медицинской помощи на основе клинических рекомендаций, разработанных и утвержденных в соответствии с частями 3, 4, 6 –9 и 11 статьи 37 Федерального закона «Об основах охраны здоровья граждан в Российской Федерации», утвержденных постановлением Правительства Российской Федерации от 19.11.2021 № 1968, клинические рекомендации применяются следующим образом:
– размещенные в Рубрикаторе до 1 сентября 2021 года – с 1 января 2022 года;
– размещенные в Рубрикаторе до 1 июня 2022 года – с 1 января 2023 года;
– размещенные в Рубрикаторе после 1 июня 2022 года – с 1 января 2024 года.
Клинические рекомендации
Язвенный колит
Год утверждения (частота пересмотра): 2020
Возрастная категория: Взрослые
Пересмотр не позднее: 2022
Дата размещения: 21.07.2020
ID: 193
Определение заболевания или состояния (группы заболеваний или состояний)
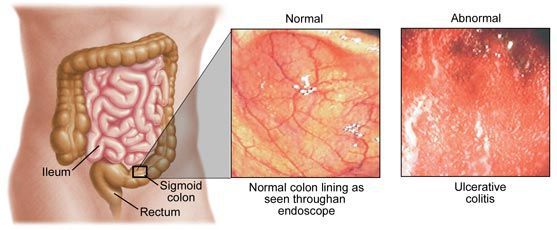
Язвенный колит (ЯК) – хроническое заболевание толстой кишки, характеризующееся иммунным воспалением ее слизистой оболочки.
Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
K51.0 – Язвенный (хронический) энтероколит
K51.1 – Язвенный (хронический) илеоколит
K51.2 – Язвенный (хронический) проктит
K51.3 – Язвенный (хронический) ректосигмоидит
K51.4 – Псевдополипоз ободочной кишки
K51.5 – Мукозный проктоколит
K51.8 – Другие язвенные колиты
K51.9 – Язвенный колит неуточненный
Облачная МИС «МедЭлемент»
Классификация
Классификация заболевания или состояния (группы заболеваний или состояний)
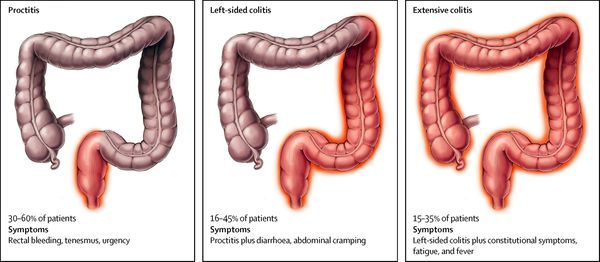
Надлежащая классификация ЯК по протяженности поражения, характеру течения, тяжести атаки и наличию осложнений определяет вид и форму введения лекарственных препаратов, а также периодичность скрининга на колоректальный рак [5].
Для описания протяженности поражения применяется Монреальская классификация (табл. 1), оценивающая протяженность макроскопических изменений при эндоскопическом исследовании толстой кишки.
Таблица 1. Монреальская классификация ЯК по протяженности поражения [6].
По характеру течения выделяют:
1. Острое течение (менее 6 месяцев от дебюта заболевания):
2. Хроническое непрерывное течение (длительность ремиссии менее 6 мес на фоне адекватной терапии).
3. Хроническое рецидивирующее течение (длительность ремиссии более 6 мес).
Для правильного формулирования диагноза и определения тактики лечения следует оценивать тяжесть текущего обострения (атаки), для чего используются простые критерии Truelove-Witts, как правило, применяемые в повседневной клинической практике, и индекс активности ЯК (индекс Мейо; DAI), как правило, применяемый в клинических испытаниях. Однако, для определения социального статуса пациента, получения инвалидности, льготного лекарственного обеспечения, бесплатного санаторно-курортного лечения и других социальных льгот необходимо учитывать тяжесть заболевания в целом, что определяется тяжестью текущей атаки, наличием внекишечных проявлений и осложнений, рефрактерностью к лечению, в частности, развитием гормональной зависимости и резистентности. Выделяют легкую, среднетяжелую и тяжелую атаки ЯК (табл. 2 и 3).
Таблица 2. Тяжесть атаки ЯК согласно критериям Truelove-Witts [7].
В клинической практике нередко встречается так называемая «сверхтяжелая или крайне тяжелая атака» ЯК, характеризующаяся диареей более 10-15 раз в сутки, нарастающим падением гемоглобина, лихорадкой выше 38°С, тяжелой гипопротеинемией и электролитными сдвигами, высоким уровнем С-реактивного белка (СРБ) [8,9]. Подходы к лечению такого колита отличаются от обычных. В англоязычной литературе такое состояние называется «острый тяжелый ЯК» (acute severe UC) [10].
Таблица 3. Тяжесть атаки согласно индексу активности ЯК (индекс Мейо).
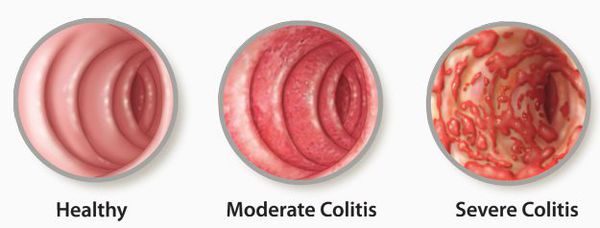
Тяжесть атаки язвенного колита устанавливается по сумме баллов: 0–2 — ремиссия (при этом оценка параметров ректального кровотечения и эндоскопического состояния слизистой = 0 баллов); 3–5 — легкая атака ЯК; 6–9 — среднетяжелая атака ЯК; 10–12 — тяжелая атака ЯК.
Парциальный индекс (или неполная шакала Мейо) без данных эндоскопии: 0–1 балл –клиническая ремиссия (при этом параметр «ректальное кровотечение» = 0 баллов; 1–2 балла –легкая атака; 3–5 баллов – среднетяжелая атака; ≥ 6 баллов – тяжелая атака ЯК.
Используемая в индексе Мейо шкала оценки состояния слизистой оболочки по Schroeder приведена в Таблице 4. и применяется для оценки эндоскопической активности ЯК.
Таблица 4. Классификация ЯК в зависимости от эндоскопической активности (по Schroeder)[11].
Классификация ЯК в зависимости от ответа на гормональную терапию облегчает выбор рациональной лечебной тактики, поскольку целью консервативного лечения является достижение стойкой ремиссии с прекращением терапии глюкокортикостероидами (ГКС). Для этих целей выделяются:
1. Гормональная резистентность:
- В случае тяжелой атаки – отсутствие положительной динамики со стороны клинических и лабораторных показателей, несмотря на применение системных ГКС в дозе, эквивалентной 2мг/кг массы тела преднизолона** в сутки, в течение более чем 7 дней;
- В случае среднетяжелой атаки – сохранение активности заболевания при пероральном приеме ГКС в дозе, эквивалентной 1 мг/кг массы тела преднизолона**, в течение 2 недель.
2. Гормональная зависимость:
- Увеличение активности болезни, возникшее при уменьшении дозы ГКС после достижения исходного улучшения в течение 3 месяцев от начала лечения;
- Возникновение рецидива болезни в течение 3 месяцев после окончания лечения ГКС.
При формулировании диагноза следует отразить характер течения заболевания, протяженность поражения, тяжесть текущей атаки или наличие ремиссии, наличие гормональной зависимости или резистентности, а также наличие внекишечных или кишечных осложнений ЯК. Ниже приведены примеры формулировок диагноза:
1. «Язвенный колит, хроническое рецидивирующее течение, проктит, среднетяжелая атака».
2. «Язвенный колит, хроническое непрерывное течение, левостороннее поражение, среднетяжелая атака. Гормональная зависимость. Внекишечные проявления (периферическая артропатия)».
3. «Язвенный колит, хроническое рецидивирующее течение, тотальное поражение, тяжелая атака. Гормональная резистентность. Токсический мегаколон».
Этиология и патогенез
Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Этиология воспалительных заболеваний кишечника (ВЗК), в том числе ЯК, не установлена. Заболевание развивается в результате сочетания нескольких факторов, включающих генетическую предрасположенность, дефекты врожденного и приобретенного иммунитета, нарушения кишечной микрофлоры и влияние факторов окружающей среды. Описано около 100 генетических полиморфизмов, ассоциированных с ЯК. Генетическая детерминированность приводит к изменениям врожденного иммунного ответа, аутофагии, нарушению механизмов распознавания микроорганизмов, нарушению эпителиального барьера и, как результат, извращению адаптивного иммунитета. Ключевым дефектом, предрасполагающим к развитию ВЗК является нарушения распознавания бактериальных молекулярных маркеров (паттернов) дендритными клетками, что приводит к гиперактивации сигнальных провоспалительных путей.Также при ВЗК отмечается уменьшение разнообразия кишечной микрофлоры за счет снижения доли анаэробных бактерий, преимущественно Bacteroidetes и Firmicutes. На этом фоне развитие ВЗК происходит под действием пусковых факторов, к которым относят курение, нервный стресс, дефицит витамина D, питание с пониженным содержанием пищевых волокон и повышенным содержанием животного белка, кишечные инфекции, особенно, инфекция Clostridioides difficile.
Результатом взаимного влияния факторов риска является активация лимфоцитов-Т-хелперов 2 типа, гиперэкспрессия провоспалительных цитокинов, в первую очередь, фактора некроза опухоли-альфа и молекул клеточной адгезии. Вследствие этих нарушений формируется воспалительная лимфоплазмоцитарная инфильтрация и деструкция слизистой оболочки толстой кишки с характерными макроскопическими изменениями и развивается клиническая картина ЯК.
При ЯК поражается только толстая кишка (за исключением ретроградного илеита), в процесс обязательно вовлекается прямая кишка, воспаление чаще всего ограничивается слизистой оболочкой (за исключением острого тяжелого колита) и носит диффузный характер.
Эпидемиология
Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Согласно зарубежным данным, заболеваемость ЯК составляет от 0,6 до 24,3 на 100 000 человек, распространенность достигает 505 на 100 000 человек [3]. Данные о распространенности ЯК в Российской Федерации ограничены [4]. Распространенность ЯК выше в северных широтах и в западных регионах. Заболеваемость и распространенность ЯК в Азии ниже, однако, в настоящее время увеличивается. Европеоиды страдают заболеванием чаще, чем представители негроидной и монголоидной рас. Пик заболеваемости отмечается между 20 и 30 годами жизни, а второй пик заболеваемости описан в возрасте 60-70 лет. Заболеваемость приблизительно одинакова у мужчин и женщин.
Клиническая картина
Cимптомы, течение
Клиническая картина заболевания или состояния (группы заболеваний или состояний)
ЯК включает четыре клинических синдрома:
Кишечный синдром. Типичные кишечные симптомы включают диарею, преимущественно в ночное время (65 % случаев), кровь в стуле (95-100% случаев), тенезмы (чаще при проктитах и проктосигмоидитах), иногда тенезмы в сочетании с запором при дистальном ограниченном поражении. При проктитах и проктосигмоидитах диарея может отсутствовать, в клинической картине преобладают тенезмы. Для ЯК, в отличие от БК, боль в животе не характерна. Может быть умеренно выраженный болевой абдоминальный синдром спастического характера, чаще перед стулом.
Эндотоксемия — признаки системного воспаления, обусловленные высокой активностью воспалительного процесса в толстой кишке. Эндотоксемия в разной степени сопутствует среднетяжелым и тяжелым формам ЯК. Основные симптомы – общая интоксикация, лихорадка, тахикардия, анемия, увеличение СОЭ, лейкоцитоз, тромбоцитоз, повышение уровня острофазных белков: СРБ, фибриногена.
Метаболические расстройства являются следствием диареи, токсемии, избыточной потери белка с калом вследствие экссудации и нарушением всасывания воды и электролитов. Клинические симптомы типичны: потеря массы тела (иногда до степени истощения), обезвоживание, гипопротеинемия, гипоальбуминемия с развитием отечного синдрома, гипокалиемия и другие электролитные нарушения, гиповитаминоз
Внекишечные системные проявления (ВКП) встречаются в 20-25% случаев ЯК и обычно сопровождают тяжелые формы болезни [12] (табл. 5).
Таблица 5. Основные внекишечные (системные) проявления язвенного колита.
Аутоиммунные проявления, связанные с активностью воспалительного процесса, появляются вместе с основными кишечными симптомами обострения и исчезают вместе с ними на фоне лечения. Аутоиммунные проявления, не связанные с активностью процесса (в англоязычной литературе их часто называют «сопутствующими аутоиммунными заболеваниями»), имеют тенденцию к прогрессированию независимо от фазы основного заболевания (обострение или ремиссия) и часто определяют негативный прогноз болезни.
Кишечные осложнения ЯК включают кишечное кровотечение, токсическую дилатацию и перфорацию толстой кишки, а также колоректальный рак. Поскольку эти осложнения в большей степени требуют хирургического лечения, подробно они рассматриваются в Разделе 3.2 «Хирургическое лечение».
Диагностика
Диагностика
Критерии установления диагноза/состояния на основании патогномоничных данных:
1) анамнестических данных,
2) физикального обследования,
3) лабораторных исследований,
4) инструментального обследования.
Однозначных диагностических критериев ЯК не существует. Диагноз выставляется на основании сочетания данных анамнеза, клинической картины и типичных эндоскопических и гистологических изменений.
Жалобы и анамнез
- У всех пациентов при подозрении на ЯК рекомендуется сбор анамнеза и жалоб для верификации диагноза [13-16].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4)
- В том числе при сборе анамнеза рекомендуется уточнить наличие факта курения для сужения круга диагностического поиска и верификации диагноза [17].
Уровень убедительности рекомендаций – А (уровень достоверности доказательств – 2)
Комментарий: обращается внимание на частоту и характер стула, длительность данных симптомов, наличие примеси крови, характер болей в животе; поездки в южные страны; принимаемые лекарства (в частности, антибиотики и нестероидные противовоспалительные средства (НПВП)); курение; наличие воспалительных и злокачественных заболеваний кишечника у родственников [18,19].
Физикальное обследование
- У всех пациентов с подозрением на ЯК в обязательном порядке рекомендуется физикальное обследование с целью сужения круга диагностического поиска и верификации диагноза:
— осмотр перианальной области;
— пальцевое исследование прямой кишки (трансректальное пальцевое исследование) [20, 197].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5)
Комментарий: при физикальном осмотре могут быть обнаружены различные проявления ЯК, включая лихорадку, периферические отеки, дефицит питания, наличие признаков перфорации или токсической дилатации толстой кишки, а также внекишечных проявлений.
Лабораторные диагностические исследования
- Рекомендуется всем пациентам при подозрении на ЯК развернутый общий (клинический) анализ крови для диагностики анемии, сопутствующей патологии, а также определения степени активности ЯК [21-26].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4)
Комментарий: при общем (клиническом) анализе крови могут быть диагностированы анемии (железодефицитная, анемия хронического заболевания), лейкоцитоз (на фоне хронического воспаления или на фоне стероидной терапии), тромбоцитоз.
- Рекомендуется всем пациентам при подозрении на ЯК анализ крови биохимический общетерапевтический (общий белок, альбумин, АЛТ, АСТ, общий билирубин, гамма-ГТ,ЛДГ, К+, Na+, Сl—, С-реактивный белок, щелочная фосфатаза, фибриноген) для диагностики сопутствующей патологии [23,26-30].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4)
Комментарий: биохимическое исследование позволяет выявить электролитные нарушения, гипопротеинемию (в частности, гипоальбуминемию), а также повышение щелочной фосфатазы, что является возможным проявлением ассоциированного с ЯК первичного склерозирующего холангита.
- Рекомендуется пациентам с острым течением ЯК (первой атаке заболевания) проводить дифференциальную диагностику с острой кишечной инфекцией [188].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4)
- Рекомендуется пациентам с обострением ЯК выполнить иммунохроматографическое экспресс-исследование кала на токсины A и B клостридии (Clostridium difficile) исключения клостридиальной инфекции [31-34].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4)
- Рекомендуется всем пациентам при подозрении на ЯК, среднетяжелой и тяжелой атаках ЯК, гормональной резистентности или резистентности к биологической терапии молекулярно-биологическое исследование биоптатов и пунктатов из очагов поражения (толстой кишки) органов и тканей на цитомегаловирус (Cytomegalovirus) [37,38].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4)
Инструментальные диагностические исследования
- Рекомендуется всем пациентам с легкой и умеренной активностью ЯК проведение колоноскопии для верификации диагноза. Пациентам с выраженной активностью ЯК рекомендуется проведение ректосигмоидоскопии [u1] [19,39].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4)
Комментарий: колоноскопия обязательна для установления диагноза ЯК, а также для решения вопроса о колэктомии. Эндоскопическое исследование толстой кишки является основным методом диагностики ЯК, однако, специфичные эндоскопические признаки отсутствуют. Наиболее характерными являются непрерывное воспаление, ограниченное слизистой оболочкой, начинающееся в прямой кишке и распространяющееся проксимальнее, с четкой границей воспаления. Эндоскопическую активность ЯК наилучшим образом отражают контактная ранимость (выделение крови при контакте с эндоскопом), отсутствие сосудистого рисунка и наличие эрозий и изъязвлений. Обнаружение стойкого сужения кишки на фоне ЯК требует обязательного исключения колоректального рака.
- Рекомендуется пациентам с тяжелой атакой ЯК обзорная рентгенография органов брюшной полости для исключения:
— перфорации толстой кишки [40];
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4)
— токсической дилатации толстой кишки [19].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5)
- Всем пациентам с подозрением на ЯК при первичной постановке диагноза, при сомнениях в правильности ранее выставленного диагноза, рекомендуется выполнение биопсии толстой кишки с целью верификации диагноза [42,43].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5)
Комментарий: при длительном анамнезе ЯК (более 7-10 лет) – хромоэндоскопия с прицельной биопсией или ступенчатая биопсия (из каждого отдела толстой кишки) для исключения дисплазии эпителия. Рекомендуемым стандартом биопсии при постановке диагноза является взятие биоптатов слизистой оболочки прямой кишки и не менее чем из 4 других участков толстой кишки, а также слизистой оболочки подвздошной кишки.
К микроскопическим признакам ЯК относятся деформация крипт (разветвленность, разнонаправленность, появление крипт разного диаметра, уменьшение плотности крипт, «укорочение крипт», крипты не достигают подлежащего слоя мышечной пластинки слизистой оболочки), «неровная» поверхность слизистой в биоптате слизистой оболочки, уменьшение числа бокаловидных клеток, базальный плазмоцитоз, инфильтрация собственной пластинки слизистой оболочки, наличие крипт-абсцессов и базальных лимфоидных скоплений. Степень воспалительной инфильтрации обычно уменьшается по мере удаления от прямой кишки.
- Рекомендуется всем пациентам с подозрением на ЯК при первичной постановке диагноза, при сомнениях в правильности ранее выставленного диагноза, при длительном анамнезе ЯК, при подозрении на осложнения ЯК, а также для исключения патологии других органов брюшной полости — ультразвуковое исследование органов брюшной полости, забрюшинного пространства, малого таза [44-45].
Уровень убедительности рекомендаций – А (уровень достоверности доказательств – 2)
- Рекомендуется всем пациентам с подозрением на ЯК при необходимости дифференциальной диагностики или при невозможности проведения полноценной илеоколоноскопии одно из следующих визуализирующих методов исследования:
— магнитно-резонансная томография (МРТ) органов брюшной полости [47];
Уровень убедительности рекомендаций – B (уровень достоверности доказательств – 3)
— компьютерная томография (КТ) органов брюшной полости с контрастированием кишечника (в случае недоступности экспертной оценки или невозможности выполнения МРТ) [48,49].
Уровень убедительности рекомендаций – B (уровень достоверности доказательств – 3)
- Рекомендуется пациентам с подозрением на ЯК при необходимости дифференциальной диагностики или при невозможности проведения полноценной колоноскопии, МРТ и КТ проведение ирригоскопии с двойным контрастированием для оценки протяженности поражения в толстой кишке, уточнения наличия образований, стриктур и др. [20,50,189].
Уровень убедительности рекомендаций – В (уровень достоверности доказательств – 2)
Комментарий: пациентам с подозрением на ЯК также возможно выполнение дополнительных исследований в зависимости от клинической ситуации.
Иная диагностика
Дополнительные инструментальные и лабораторные исследования выполняются преимущественно с целью проведения дифференциальной диагностики с рядом заболеваний. Это инфекционные, сосудистые, медикаментозные, токсические и радиационные поражения, а также дивертикулит и др. На следующем этапе дифференциальной диагностики проводится верификация клинических диагнозов ЯК и БК, относящихся к группе ВЗК. Таким образом, дифференциальный диагноз ЯК проводится с болезнью Крона толстой кишки, острыми кишечными инфекциями (дизентерия, сальмонеллез, кампилобактериоз, иерсиниоз, амебиаз), паразитозами, антибиотико-ассоциированными поражениями кишечника (псевдомембранозный колит, вызываемый C.Difficile) [52], туберкулезом кишечника, системными васкулитами, раком толстой кишки, дивертикулитом, микроскопическими колитами (коллагеновым и лимфоцитарным) [52], радиационным проктитом.
С целью дифференциальной диагностики и подбора терапии при внекишечных проявлениях ЯК и сопутствующих состояниях может потребоваться консультация:
- врача-психотерапевта или медицинского психолога (невроз, планируемая операция с наличием стомы и т.п.);
- врача-эндокринолога (стероидный сахарный диабет, надпочечниковая недостаточность у пациентов на длительной гормональной терапии);
- врача-дерматовенеролога (дифференциальный диагноз узловатой эритемы, пиодермии ит.п.);
- врача-ревматолога (артропатии, сакроилеит и т.п.);
- врача-акушера-гинеколога (беременность).
Лечение
Лечение
1. Консервативное лечение
Лечебные мероприятия при ЯК включают в себя назначение лекарственных препаратов, хирургическое лечение, психосоциальную поддержку и диетические рекомендации.
Выбор вида консервативного или хирургического лечения определяется тяжестью атаки, протяженностью поражения толстой кишки, наличием внекишечных проявлений, длительностью анамнеза, эффективностью и безопасностью ранее проводившейся терапии, а также риском развития осложнений ЯК [53, 54].
Целью терапии является достижение и поддержание бесстероидной ремиссии (прекращение приема ГКС в течение 12 недель после начала терапии) [55], профилактика осложнений ЯК, предупреждение операции, а при прогрессировании процесса, и/или развитии опасных для жизни осложнений – своевременное назначение хирургического лечения. Поскольку полное излечение пациентов ЯК достигается только путем удаления толстой кишки (колпроктэктомии), при достижении ремиссии неоперированный пациент должен оставаться на постоянной поддерживающей (противорецидивной) терапии.
Следует особо отметить, что ГКС не могут применяться в качестве поддерживающей терапии.
Ниже представлены рекомендации по выбору препаратов для индукции и поддержания ремиссии в зависимости от протяженности поражения и тяжести атаки [20].
1.2 Проктит. Легкая и среднетяжелая атака
- Данной группе пациентов рекомендовано местное лечение [198].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 5)
Комментарий: в данной ситуации целесообразно назначение суппозиториев с #месалазином**(1 г/сут, при необходимости дозу можно увеличить до 2 г/сутки) или ректальной пены #месалазина (1 г 1 раз/сутки, при необходимости дозу можно увеличить до 2 раз/сутки) [20, 56,57,199]. Оценка терапевтического ответа проводится через 2 недели [56] при положительном ответе на лечение в указанных дозах пролонгируется до 6-8 недель.
- Рекомендуется пациентам при неэффективности лечения ректальными формами месалазина** назначение ректальных форм ГКС [20,58,59].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 2).
Комментарий: в данной ситуации целесообразно назначение будесонида в форме ректальной пены 2 мг в сутки, суппозитории с преднизолоном 10 мг (ex tempore) х 2 раза в сутки с оценкой ответа через 2 недели для достижения ремиссии [20,58,59].
- Рекомендуется пациентам при достижении ремиссии поддерживающая терапия –ректальное введение #месалазина** в свечах 1 г х 3 раза в неделю в виде монотерапии для поддержания ремиссии [20,64, 201].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 2).
Комментарий: также может использоваться #месалазин в виде ректальной пены в том же режиме дозирования. Лечение целесообразно продолжать не менее 2 лет [202].
- Рекомендуется пациентам при неэффективности местного лечения подключить пероральные формы месалазина** в терапевтической дозе согласно инструкции по применению препаратов для достижения ремиссии [60].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2).
- Рекомендуется пациентам при отсутствии эффекта от пероральных форм месалазина назначение ГКС для достижения ремиссии. [20,59].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5).
Комментарий: Доза преднизолона** в данной клинической ситуации эквивалентной 0,5-0,75 мг/кг массы тела преднизолона в таблетках в сутки для достижения ремиссии.
- Рекомендуется пациентам в случае рецидива, требующего повторного назначения ГКС, комбинация ГКС с азатиоприном** (АЗА) или #меркаптопурином** (МП) для достижения ремиссии [20,61].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1).
Комментарий: АЗА** назначается по 2,5 мг/кг, а #МП по 1,5 мг/кг [61, 203]. Местная терапия (ректальная пена будесонида 2 мг в сутки, суппозитории с преднизолоном 10 мг (ex tempore) х1-2 раза в сутки) может быть продолжена.
- Рекомендуется пациентам при достижении ремиссии, индуцированной ГКС, поддерживающая терапия АЗА** 2-2,5 мг/кг (или #МП 1,5 мг/кг) не менее 2 лет для поддержания ремиссии [60,61,203].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1)
- Рекомендуется пациентам, у которых обнаружено ДНК цитомегаловируса при молекулярно-биологическом исследовании биоптатов из толстой кишки терапия ганцикловиром** в дозе 5мг/кг 2 раза в сутки в течение 14-21 дня для элиминации возбудителя [20, 62].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
1.3 Проктит. Тяжёлое течение (развивается крайне редко)
- Рекомендуется пациентам при тяжелом язвенном проктите внутривенное ГКС в дозе, эквивалентной преднизолону** 1-2 мг/кг массы тела в сутки в комбинации с местной терапией месалазином** (суппозитории, ректальная пена) или ГКС (ректальная пена будесонида 2 мг в сутки, суппозитории с преднизолоном 10 мг (ex tempore) 10 мг х 2 раза всутки) для достижения ремиссии [20,59].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
- Рекомендуется пациентам в случае первой атаки поддерживающая терапия при достижении ремиссии проводится местными формами препаратов #месалазина** в форме суппозиториев или месалазина в форме ректальной пены) 1 г х 3 раза в неделю в виде монотерапии или в комбинации с пероральным месалазином в дозе 2-2,4 г – не менее 2 лет для поддержания ремиссии [20,57,60,63-66].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1).
- Рекомендуется пациентам при рецидиве, требующем повторного назначения ГКС (системных или топических), одновременно с ГКС назначить АЗА** 2-2,5 мг/кг (или #МП1,5 мг/кг) и затем продолжение поддерживающей терапии иммунодепрессантами (АЗА или #МП) не менее 2 лет для достижения ремиссии [61].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
- Рекомендуется пациентам, у которых обнаружено ДНК цитомегаловируса при молекулярно-биологическом исследовании биоптатов из толстой кишки терапия ганцикловиром** в дозе 5мг/кг 2 раза в сутки в течение 14-21 дня для элиминации возбудителя [20, 62].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
1.4 Левосторонний и тотальный язвенный колит. Легкая атака
- Рекомендуется пациентам при первой атаке или рецидиве назначение месалазина** внутрь в максимальных терапевтических дозах в соответствие с инструкциями по применению в комбинации с месалазином** суспензия ректальная 4 г/сут для достижения ремиссии [20, 64,67-68].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 5).
Комментарий: терапевтический ответ оценивается через 2 недели. При положительном ответе терапия продолжается до 6-8 недель.
- Рекомендуется пациентам при отсутствии эффекта от комбинированной терапии препаратами #аминосалициловой кислоты** (5-АСК) (аминосалициловая кислота и аналогичные препараты) назначение ректальных форм ГКС [68,69].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2)
Комментарий: целесообразно назначение ректальной пены будесонида 2 мг в сутки или суспензии #гидрокортизон 125-250 мг 1 раз в сутки в виде клизм или ректального капельного введения для достижения ремиссии [213-214].
- Рекомендуется пациентам при достижении ремиссии проводить поддерживающую терапию пероральным месалазином** 2-2,4 г/сут. для поддержания ремиссии [70].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1)
Комментарий: дополнительное введение #месалазина** ректально по 2 г х 2 раза в неделю («терапия выходного дня») увеличивает вероятность долгосрочной ремиссии [215].
- Рекомендуется пациентам при отсутствии ответа на терапию пероральными препаратами #АСК** (аминосалициловая кислота и аналогичные препараты) в сочетании с любым местным вариантом лечения назначение топических ГКС (будесонид**, таблетки кишечнорастворимые с пролонгированным высвобождением, покрытые пленочной оболочкой) или системных ГКС (см. раздел 3.1.4) для достижения терапевтического эффекта [71].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 3)
- Рекомендуется пациентам, у которых обнаружено ДНК цитомегаловируса при молекулярно-биологическом исследовании биоптатов из толстой кишки терапия ганцикловиром** в дозе 5мг/кг 2 раза в сутки в течение 14-21 дня для элиминации возбудителя [20, 62].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 4)
1.5 Левосторонний и тотальный язвенный колит. Среднетяжелая атака
- Рекомендуется пациентам при первой атаке или рецидиве назначение перорального месалазина** в максимальной терапевтической дозе в соответствии с инструкциями к препаратам в комбинации с месалазином** в клизмах 4 г/сут для достижения ремиссии [20,65,66,72].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1).
Комментарий: терапевтический ответ оценивается через 2 недели. При улучшении клинической симптоматики и положительной лабораторной динамике терапия продолжается до 6-8 недель.
- Рекомендуется пациентам при достижении ремиссии поддерживающая терапия препарата мимесалазина** 2,0-2,4 г/сут внутрь + месалазин** суспензия ректальная по 4 г х 2 раза в неделю для поддержания ремиссии [64,66,67,73,190].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1).
Комментарий. Допустимо назначение #сульфасалазина** 2 г/сут вместо месалазина** [210].
- Рекомендуется пациентам при неэффективности АСК** и отсутствии системных признаков воспаления назначение топических ГКС (будесонид**, таблетки кишечнорастворимые с пролонгированным высвобождением, покрытые пленочной оболочкой) [191-193]
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2)
Комментарии. Топические ГКС назначают в дозе 9 мг/сут. После 10-недельного приема будесонида, снижение дозы проводится через день в течение 1-2 недель до полной отмены.
- Рекомендуется пациентам при неэффективности АСК** и при наличии системного воспаления рекомендуется назначение системных ГКС для достижения терапевтического эффекта [71,74-76].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1)
Комментарии. Системные ГКС назначают в дозе, эквивалентной преднизолону** 1 мг/кг массы тела. Снижение дозы системных ГКС производится по 5 мг в 5-7 дней до полной отмены.
- Рекомендуется пациентам в случае непереносимости препаратов АСК** или при необходимости повторного назначения ГКС в течение года и менее комбинировать ГКС с АЗА** 2,0-2,5 мг/кг или #МП** 1,5 мг/кг для достижения терапевтического эффекта [61,77].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 2)
- Рекомендуется пациентам при достижении ремиссии продолжение поддерживающей терапии АЗА** 2,0-2,5 мг/кг/сут или #МП** 1,5 мг/кг не менее 2 лет для поддержания ремиссии [61,77].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2)
- Рекомендуется пациентам при отсутствии эффекта от ГКС в течение 2 недель проведение биологической терапии для достижения ремиссии (инфликсимаб**, адалимумаб**, голимумаб**, ведолизумаб**, тофацитиниб** или устекинумаб**), начиная с индукционного курса, в дозах, соответствующих инструкции по применению [78-82].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2)
Комментарий: Все указанные препараты могут применяться как в первой, так и во второй линии терапии [20]
- Рекомендуется пациентам, получающим инфликсимаб**, комбинировать его с АЗА** 2,0-2,5мг/кг для повышения эффективности лечения [61,83,84].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2)
Комментарии. Допустимо применение #МП 1,5 мг/кг [211] вместо АЗА** в связи с тем, что МП является метаболитом АЗА**. Для других биологических лекарственных препаратов эффективность комбинации с иммунодепрессантами не доказана. Совместное применение АЗА** и тофацитиниба противопоказано [85,86].
- Рекомендуется пациентам при эффективности индукционного курса биологическими лекарственными препаратами проводить поддерживающую терапию ими же в соответствии с инструкцией по применению в течение, как минимум, 2 лет для поддержания ремиссии [87-91].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2)
- Рекомендуется пациентам при первичной неэффективности ингибитора фактора некроза опухоли альфа (анти-ФНО) смена терапии на ведолизумаб**, тофацитиниб** или устекинумаб** для достижения ремиссии [91, 92, 194].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
Комментарий: тофацитиниб**, ведолизумаб** и устекинумаб** могут быть назначены в качестве 1-ой и последующих линий терапии в комбинации с ГКС или без них.
- Рекомендуется пациентам при потере ответа на терапию анти-ФНО (рецидив ЯК на фоне ранее достигнутой ремиссии) оптимизация терапии в виде увеличения дозы препарата (10мг/кг инфликсимаба** каждые 8 недель, 100 мг голимумаба** каждые 4 недели, 80 мг адалимумаба каждые 2 недели) или сокращения интервалов между введениями(инфликсимаб** до 4-6 недель, адалимумаб** каждую неделю) или назначение препаратов другого механизма действия: ведолизумаба**, тофацитиниба** или устекинумаба** длядостижения терапевтического эффекта [87-91,194,195].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2)
Комментарий: смена на другой анти-ФНО возможна, но ее эффективность ниже, чем при переходе на препараты других классов (ведолизумаб**, тофацитиниб** или устекинумаб**).
- Рекомендуется пациентам при потере ответа на ведолизумаб** в стандартной дозе 300 мг каждые 8 недель оптимизация терапии в виде сокращения интервалов между введениями до 4 недель или смена на биологический лекарственный препарат другого класса [93].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 4)
- Рекомендуется пациентам при потере ответа на тофацитиниб** в стандартной дозе 10 мг в день оптимизация терапии до 20 мг в день [94].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4).
Комментарий: Учитывая недавнее появление тофацитиниба**, в том числе в России, доказательная база о возможности перехода с тофацитиниба** на биологические лекарственные препараты недостаточна. Смена препаратов возможна и остается на усмотрение лечащего врача.
Длительность биологической терапии определяется лечащим врачом. Также возможна смена на биологический лекарственный препарат другого класса для достижения ремиссии. В большинстве стран лечение проводят в течение многих лет. Ранняя отмена препаратов, как правило, приводит к рецидиву ЯК в короткие сроки. При невозможности пролонгированного использования биологических лекарственных препаратов, поддерживающая терапия проводится только иммунодепрессантами (АЗА**, МП**). В случае непереносимости аналогов пурина — монотерапия биологическими лекарственными препаратами.
- Рекомендуется пациентам при снижении дозы ГКС до эквивалентной 35-45 мг преднизолона**, назначить дополнительно месалазин** per os в максимальной терапевтической дозе в соответствии с инструкциями к препаратам) для поддержания терапевтического эффекта (в том случае, если пациент не получает иммунодепрессантов, в том числе биологической терапии) [67]
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5).
Комментарий: дальнейшее снижение ГКС следует проводить на фоне месалазина** с последующим переходом на поддерживающую терапию месалазином**
per os 2,0-2,4 г в сутки.
- Рекомендуется пациентам при рецидиве, возникшем на фоне поддерживающей терапии аналогами пурина, назначение биологической терапии (инфликсимаб**, адалимумаб**, голимумаб**, ведолизумаб** или устекинумаб**), а также тофацитиниба** (с отменой аналогов пурина согласно инструкции по медицинскому применению) [87-91,194].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2)
Комментарий: Любой из указанных препаратов может назначаться в качестве первой линии терапии
- Рекомендуется пациентам, у которых обнаружено ДНК цитомегаловируса терапия ганцикловиром** в дозе 5мг/кг 2 раза в сутки в течение 14-21 дня для элиминации возбудителя [20, 62].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
1.6 Левосторонний и тотальный язвенный колит. Тяжелая атака
- Рекомендуется пациентам в качестве первой линии терапии внутривенная терапия ГКС для достижения ремиссии [20,96].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1).
Комментарий: применение ГКС целесообразно в дозе, эквивалентной преднизолону** 2 мг/кг массы тела (при высокой массе тела возможно назначение 1,5мг/кг) в течение 7 дней или применение гидрокортизона** в эквивалентной дозе. Эквивалентность доз и длительности действия ГКС приведена в таблице 6. Ответ оценивается в интервале от 3 до 7 дней. Если в течение трех дней состояние стабильно, то терапию продолжают до 7 дней. Если состояние больного в течение трех дней ухудшается ставится вопрос о «терапии спасения» или околэктомии. Если через 7 дней отмечено клиническое улучшение, то терапию ГКС можно продолжить до стабильного улучшения и затем переходить на пероральный прием препаратов и медленно снижать дозу по 5 мг в 5-7 дней.
В случае отсутствия значимого клинического улучшения через 7 дней состояние расценивается как стероидорезистентность.
- Рекомендуется пациентам дополнительно назначить местную терапию клизмами с месалазином** 4 г в сутки или #гидрокортизон 125-250 мг х 1 раз в сутки в виде клизм или ректального капельного введения для достижения ремиссии [68,69, 213-214].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 5)
- Рекомендуется пациентам при наличии метаболических нарушений инфузионная терапия с целью регидратации, коррекции белково-электролитных нарушений [55].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 5)
Комментарий: гипокалиемия и гипомагниемия повышают риск токсической дилатации ободочной кишки.
- Рекомендуется пациентам при уровне гемоглобина ниже 80 г/л для коррекции анемии в виде гемотрансфузии (эритромасса), при уровне гемоглобина от 80 до 100 г/л – терапия препаратами железа парентерально (железа (III) гидроксид сахарозный комплекс**, железа(III) гидроксид декстран, железа (III) гидроксид олигоизомальтозат**, железа карбоксимальтозат**) [97].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
- Рекомендуется у пациентов с дефицитом массы тела (ИМТ менее 18) назначение дополнительного энтерального, в том числе зондового, питания для улучшения трофологического статуса [98].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 2)
Комментарий: полностью парентеральное питание и/или временное ограничение приема пищи внутрь нецелесообразно.
- При развитии признаков системного воспаления у пациентов рекомендуется назначение антибиотиков с целью профилактики септических осложнений:
— 1 линия – #метронидазол** + фторхинолоны (ципрофлоксацин**, офлоксацин**) [100];
— 2 линия — цефалоспорины [99,101,102].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1)
Таблица 6. Сравнительная характеристика ГКС
- Рекомендуется пациентам при клиническом ответе на ГКС через 7 дней перевод на пероральный прием преднизолона** с последующим снижением до полной отмены по 5-10 мг преднизолона** в 5-7 дней для поддержания ремиссии [55].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
Комментарий: Схема перехода с внутривенных ГКС на пероральные формы рассматривается индивидуально лечащим врачом в зависимости от скорости достижения эффекта и выраженности терапевтического ответа. При развитии стероидорезистентности, если нет непосредственной угрозы жизни или тяжелых осложнений, требующих немедленного оперативного вмешательства, активизация консервативного лечения, которая проводится биологическими лекарственными препаратами или циклоспорином. «Терапия спасения» проводится двумя основными препаратами на фоне сохраняющегося лечения ГКС: инфликсимабом** (в дозе 5 мг/кг в рамках индукционного курса на 0, 2 и 6 неделе) или #циклоспорином**В/в (2-4 мг/кг в течение 7 дней [204-206] с мониторированием показателей функции почек и определением концентрации препарата в крови). Клинический результат такой терапии оценивается через 7 дней. Исследования показали, что эффективность обеих схем на 8 день лечения идентична, поэтому в настоящее время в зарубежной практике используется в основном инфликсимаб**, как более безопасный и не требующий трудоемкого и дорогостоящего определения концентрации. При отсутствии эффекта через 7-8 дней рассматриваются варианты хирургического лечения. При невозможности назначения инфликсимаба** допустимо назначение тофацитиниба** с учетом скорости достижения эффекта в соответствии с инструкцией к применению.
- Рекомендуется пациентам при достижении ремиссии на инфликсимабе** продолжить поддерживающую противорецидивную терапию этим же препаратом по стандартной схеме вкомбинации с АЗА** 2 мг/кг (или #МП 1,5 мг/кг) или без него [84,108,109].
Уровень убедительности рекомендации B (уровень достоверности доказательств – 3)
- Рекомендуется пациентам при положительном ответе на в/в #циклоспорин** через 7 дней перейти на пероральный прием препарата в дозе 2 мг/кг веса с дополнительным назначением АЗА** 2 мг/кг (на фоне терапевтической дозы стероидов) с постепенной отменой стероидов в течение 12 недель до момента достижения терапевтической концентрации и начала действия АЗА** для увеличения продолжительности ремиссии у пациента. При достижении ремиссии можно отменять пероральный циклоспорин, оставив пациента на поддерживающей терапии АЗА** не менее 2 лет [61,77,110,111, 205].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 2).
1.7 Сверхтяжелый язвенный колит любой протяженности
В такой форме может протекать как первая атака ЯК, так любое из последующих обострений (характеристику см. в разделе «классификация ЯК»). Пациент должен быть госпитализирован в многопрофильный (специализированный) стационар для консервативного лечения с последующим обязательным наблюдением врачом-гастроэнтерологом и врачом-колопроктологом (врачом-хирургом) для решения вопроса о целесообразности выполнения хирургического вмешательства в течение 24 часов.
- Рекомендуется пациентам при сверхтяжелой атаке ЯК назначение в/в ГКС в дозе, эквивалентной преднизолону** 2 мг/кг массы тела для достижения терапевтического эффекта [95].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
Комментарий: эффективность консервативной терапии при сверхтяжелой атаке ЯК не превышает 50%. При этом производят оценку клинической картины и лабораторных параметров каждые 24 часа, а при необходимости – чаще. При ухудшении клинической картины и лабораторных показателей единственным путем спасения жизни пациента при сверхтяжелой атаке ЯК является колэктомия.
При существенной положительной динамике со стороны клинической картины и лабораторных показателей с достаточной степенью осторожности можно продолжить в/в терапию ГКС до 14 дней. Если в течение 3 дней положительная динамика отсутствует, то это состояние расценивается как стероидорезистентность.
- В случае стероидорезистентности и непосредственной угрозы жизни пациента или развитиятяжелых осложнений, требующих немедленного оперативного вмешательства, данной группе пациентов рекомендуется назначение терапии «второй линии» (в англоязычной литературе «терапии спасения»), которая включает следующие варианты лечения:
— инфликсимаб** 5 мг/кг (введения в рамках индукционного курса на 0, 2 и 6 неделе) [103,104] или
— #циклоспорин** (лучше в/в) 2-4 мг/кг в течение 7 дней с мониторированием показателей функции почек [105,106].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2)
Комментарий: другие биологические лекарственные препараты и тофацитиниб** в качестве «терапии спасения» не используются. Данной группе пациентов при отрицательной динамике или при отсутствии ответа на 7 день терапии инфликсимабом** или циклоспорином**показано хирургическое лечение [107].
- Рекомендуется пациентам при достижении ремиссии на инфликсимабе** продолжить поддерживающую противорецидивную терапию этим же препаратом по стандартной схеме вкомбинации с АЗА** 2 мг/кг (или #МП 1,5 мг/кг) или без него [84,108,109].
Уровень убедительности рекомендации B (уровень достоверности доказательств – 3)
- Рекомендуется пациентам при положительном ответе на в/в #циклоспорин** через 7 дней перейти на пероральный прием препарата в дозе 2 мг/кг веса с дополнительным назначением АЗА** 2 мг/кг (на фоне терапевтической дозы стероидов) с постепенной отменой стероидов в течение 12 недель до момента достижения терапевтической концентрации и начала действия АЗА** для увеличения продолжительности ремиссии у пациента. При достижении ремиссии можно отменять пероральный циклоспорин, оставив пациента на поддерживающей терапии АЗА** не менее 2 лет [61,77,110,111, 205].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 2).
2. Хирургическое лечение
2.1 Показания к хирургическому лечению ЯК: неэффективность или невозможностьпродолжения консервативной терапии.
Показаниями к хирургическому лечению ЯК служат неэффективность консервативной терапии (гормональная резистентность, неэффективность биологической терапии) или невозможность ее продолжения (гормональная зависимость, непереносимость или противопоказания для проведения консервативной терапии), кишечные осложнения ЯК (токсическая дилатация, перфорация кишки, кишечное кровотечение), а также рак толстой кишки или высокий риск его возникновения.
О неэффективности консервативной терапии свидетельствуют (см. раздел 1.5):
- гормональная резистентность;
- гормональная зависимость.
Гормональную зависимость удается эффективно преодолеть при помощи иммунодепрессантов (биологические лекарственные препараты, АЗА**, МП**) в 40-55% случаев [67, 111], а при гормональной резистентности назначение #циклоспорина** или биологической терапии позволяет индуцировать ремиссию в 43-80% случаев [105]. Однако, участи пациентов с высоким риском осложнений и неэффективностью консервативной терапии при развитии гормональной резистентности или зависимости возможно проведение хирургического лечения без попытки применения биологической терапии, АЗА**, МП**.
2.2 Показания к хирургическому лечению ЯК: кишечные осложнения ЯК
- Рекомендуется пациентам с осложнением ЯК в виде кишечного кровотечения; перфорации толстой кишки при выявлении угрожающих симптомов (симптомы раздражения брюшины, свободный газ в брюшной полости и т.д.); токсической дилатации на фоне адекватной интенсивной терапии, экстренная операция в объеме субтотальной колэктомии или тотальной колэктомии (колпроктэктомии – при выраженной активности в прямой кишке) для увеличения продолжительности жизни пациента [113,114, 125].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 4).
Комментарий: токсическая дилатация ободочной кишки (токсический мегаколон), представляет собой не связанное с обструкцией расширение ободочной кишки 6 см и более сявлениями интоксикации. К факторам риска токсической дилатации относятся гипокалиемия, гипомагниемия, подготовка кишки к колоноскопии при помощи осмотических слабительных и прием антидиарейных препаратов. Косвенно о развитии токсической дилатации свидетельствует внезапное сокращение частоты стула на фоне имевшейся диареи, вздутие живота, а также внезапное уменьшение или исчезновение болевого синдрома и нарастание симптомов интоксикации (нарастание тахикардии, снижение АД).
Перфорация толстойкишки является наиболее опасным осложнением ЯК с почти 50% смертностью.
2.3 Показания к хирургическому лечению ЯК: колоректальный рак
У пациентов с длительным анамнезом ЯК существенно повышен риск колоректального рака,что обусловливает необходимость регулярного обследования для выявления дисплазии эпителия толстой кишки. На вероятность развития рака влияют следующие факторы:
а) длительность анамнеза ЯК: риск колоректального рака составляет 2% при 10-летнем, 8% -при 20-летнем и 18% — при 30-летнем анамнезе [126];
б) начало заболевания в детском и подростковом возрасте, хотя этот фактор может лишь отражать длительность анамнеза и не являться независимым предиктором колоректального рака [127];
в) протяженность поражения: риск наиболее повышен у пациентов с тотальным ЯК, в товремя как у пациентов с проктитом риск не отличается от среднего в популяции;
г) наличие первичного склерозирующего холангита [128];
д) семейный анамнез колоректального рака;
е) тяжелые обострения ЯК в анамнезе или непрерывное течение ЯК. Последствием высокой активности ЯК может являться воспалительный полипоз, также являющийся фактором риска развития колоректального рака [129].
Контрольная колоноскопия должна проводиться в условиях хорошей подготовки кишки и, желательно, в период ремиссии, поскольку активное воспаление затрудняет выявление дисплазии.
Для скрининга неопластических изменений слизистой оболочки используются два подхода:
1. Хромоэндоскопия с прицельной биопсией участков, подозрительных на неоплазию.
2. Биопсия слизистой оболочки по 4 фрагмента из каждых 10 см ободочной и прямой кишки (при эндоскопии в белом свете). Такой подход не исключает обязательной биопсии всех подозрительных образований.
Результаты скрининговой биопсии влияют на тактику дальнейшего лечения и наблюдения.
- Рекомендуется пациентам с ЯК при обнаружении дисплазии высокой степени при биопсии в неизмененной слизистой оболочке (т.е. не в приподнятых образованиях), хирургическое лечение в объеме тотальной колэктомии [126, 207].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4).
Комментарий: Возможно выполнение колпроктэктомии с формированием постоянной концевой илеостомы или тотальной колэктомии с формированием резервуара (колпроктэктомия с одномоментным формированием тонкокишечного резервуара подприкрытием петлевой илеостомы).
Наличие дисплазии должно быть подтверждено вторым независимым патоморфологом. Объем хирургического лечения обсуждается совместно спациентом, тем самым учитывается желание пациента в отношении сохранения анальной дефекации или формирования постоянной илеостомы.
- Рекомендуется пациентам с ЯК при обнаружении дисплазии легкой степени в неизмененной слизистой оболочке (не в приподнятых образованиях) принимать решение индивидуально совместно с пациентом: необходимо обсудить два варианта – тотальная колэктомия (колпроктэктомия) с формированием постоянной концевой илеостомы и формированием резервуара (колпроктэктомия с одномоментным формированием тонкокишечного резервуара под прикрытием петлевой илеостомы) для улучшения качества жизни пациента, но приемлемым может быть продолжение регулярного эндоскопического скрининга с сокращением интервала между исследованиями 6-12 месяцев [126, 208, 209].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4).
Комментарий: объем хирургического лечения обсуждается совместно с пациентом, тем самым учитывается желание пациента в отношении сохранения анальной дефекации или формирования постоянной илеостомы. Пациент вправе воздержаться от оперативного лечения, в таком случае предлагается эндоскопический скрининг.
- Рекомендуется пациентам с ремиссией ЯК, при подтверждении наличия аденоматозного полипа (эндоскопически и по результатам патоморфологического исследования), выполнение стандартной полипэктомии для улучшения качества жизни пациента [128].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4).
- Не рекомендуется колэктомия пациентам с ЯК при наличии полипа с дисплазией в участке толстой кишки, пораженной ЯК, если гистологическое строение полипа соответствует аденоме и признаки дисплазии отсутствуют в окружающей неизменной слизистой оболочке или где-либо в кишке, а также в краях удаленного полипа [128].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4).
2.4 Виды хирургических вмешательств
У большинства пациентов ЯК современная консервативная терапия позволяет контролировать течение воспалительного процесса, однако у 10-30% пациентов в связи с неэффективностью медикаментозного лечения приходится прибегать к хирургическому вмешательству, направленному на удаление толстой кишки [114]. До начала 1980-х годов стандартом хирургического лечения являлась колпроктэктомия с концевой илеостомией, несмотря на эпизодическое формирование илеоректального анастомоза. За последние 20 лет новым золотым стандартом стала восстановительно-пластическая операция – тотальная колэктомия сформированием резервуара (колпроктэктомия с илеоанальным резервуарным анастомозом (ИАРА)) [130,131] (Табл.8). При успешном выполнении данная операция обеспечивает возможность контролируемой дефекации через задний проход с удовлетворительным качеством жизни [132]: средняя частота дефекации после формирования ИАРА составляет от 4 до 8 раз всутки [133-135], а суточный объем полуоформленного/жидкого стула составляет около 700 мл в сутки (в сравнении с 200 мл/сутки у здорового человека).
Таблица 8. Методы хирургического лечения ЯК
2.5 Выбор вида хирургического лечения
Проведение реконструктивно-пластической операции с формированием ИАРА, несмотря на очевидную привлекательность для пациента, возможно не во всех случаях, поскольку ряд факторов ухудшают функциональный исход операции и увеличивают риск осложнений, приводя к необходимости удаления резервуара у 3,5-10% пациентов [136-138].
У пациентов с ЯК, несмотря на более высокую частоту сопутствующих заболеваний после 65 лет, само хирургическое вмешательство с формированием тонкокишечного резервуара у лиц старших возрастных групп безопасно и эффективно [139].
Функция анального держания, играющая ключевую роль для нормального функционирования ИАРА, очевидно, ухудшается в старших возрастных группах [140]. Кроме того, у пациентов старше 60 лет чаще развиваются осложнения, в частности резервуарит и стриктуры анастомоза [141,142]. В то же время, какой-либо определенный возрастной порог для отказа от формирования ИАРА не определен.
Формирование тонкокишечного резервуара (ИАРА) на 30-70% [143-147] повышает риск бесплодия у женщин детородного возраста с ЯК.
Риск бесплодия связан со спаечным процессом, вовлекающим маточные трубы. Планируемая беременность и молодой возраст женщины не являются противопоказаниями к формированию ИАРА, однако, пациентка должна быть предупреждена о потенциальном риске бесплодия. В отдельных случаях возможно рассмотреть вопрос о формировании илеоректального анастомоза в качестве промежуточного этапа хирургического лечения (см.ниже).
У всех пациенток с ЯК, при возникновении показаний к операции, использование лапароскопических технологий снижает риск развития бесплодия на 90% [143-147].
У приблизительно 10% пациентов с колитом даже при изучении операционного материала, полученного при колэктомии, не удается провести дифференциальный диагноз между БК и ЯК, в связи с чем им выставляется диагноз неуточненного язвенного колита. Решение оформировании ИАРА в таких случаях принимается индивидуально, при этом пациент должен быть предупрежден о рисках неэффективности реконструктивно-пластической операции и иных осложнениях, связанных с БК.
Пациентам с ЯК при наличии таких сопутствующих заболеваний, как рак прямой кишки и выраженное анальное недержание (2 или 3 степень) формирование тонкокишечного резервуара (ИАРА) нецелесообразно.
- Рекомендуется пациентам с тяжелой атакой ЯК, не ответивших на консервативное лечение; а также пациентам с ЯК, у которых к моменту выставления показаний к операции, была проведена гормональная терапия преднизолоном** в дозе не менее 20 мг в сутки в течение более чем 6 недель- трехэтапное хирургическое лечение (с колэктомией на первом этапе, формированием тонкокишечного резервуара и петлевой илеостомы — на втором, и закрытие петлевой илеостомы — на третьем этапе) для увеличения продолжительности жизни пациентов [149-151].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4).
Комментарий: колэктомия с концевой илеостомией купирует интоксикацию, обусловленную колитом, что позволяет улучшить общее состояние пациента, восстановить метаболизм, а изучение операционного препарата также позволяет уточнить диагноз и исключить БК. Колэктомия является относительно безопасным вмешательством даже у пациентов в критическом состоянии [149-151], при этом, при достаточной квалификации хирурга безопасным является также выполнение минимально инвазивных или лапароскопических операций [152, 153].
Илеоректальный анастомоз [154-156]: формирование илеоректального анастомоза неприводит к излечению пациента и не исключает возможность рецидива воспаления в прямой кишке и развития рака. Данная операция при ЯК может выполняться только в исключительных случаях у женщин, планирующих беременность. Обязательным условием является наличие ремиссии в прямой кишке и согласие пациентки на регулярное обследование прямой кишки с биопсией слизистой оболочки [148,157].
2.6 Особенности хирургического вмешательства при формировании тонкокишечногорезервуара (ИАРА)
Пациентам с ЯК, которым выполнена колэктомия, реконструктивно-пластические операции с формированием тонкокишечного резервуара (ИАРА) выполняются в специализированных стационарах, поскольку частота осложнений и функциональный исход таких операций существенно зависит от квалификации хирурга (в частности, от числа проведенных аналогичных вмешательств) [148].
Длина сохраняемой прямой и/или сигмовидной кишки.
Пациентам с ЯК при выполнении колэктомии по срочным показаниям при язвенном колите, которым в дальнейшем планируется формирование тонкокишечного резервуара (ИАРА), целесообразно сохранить всю прямую кишку и нижние брыжеечные сосуды для улучшения качества жизни пациентов. Прямую кишку целесообразно пересекать на уровне мыса крестца (т.е. на уровне «ректосигмоидного перехода») или дополнительно сохранять дистальный отдел сигмовидной кишки (решение принимается оперирующим хирургом). При сохранении дистального отдела сигмовидной кишки она выводится на переднюю брюшную стенку в виде концевой сигмостомы. Последний вариант является наиболее безопасным, поскольку при этом в брюшной полости не остается культи кишки. При пересечении прямой кишки на уровне мыса в течение нескольких дней рекомендуется дренирование культи через задний проход для профилактики несостоятельности швов в связи с накоплением в культе слизи. В случае сохранения отключённой прямой или прямой и сигмовидной кишки, возможно развитие вторичных воспалительных изменений слизистой оболочки по типу колита отключеннойкишки. Контролируемые испытания лекарственных средств у пациентов после колэктомии не проводились. Эмпирическое лечение заключается в применении местного месалазина [158], преднизолона, промывании отключенной прямой кишки растворами антисептиков.
Наложение анастомоза при формировании ИАРА.
Пациентам с ЯК, которым планируется хирургическое лечение с формированием тонкокишечного резервуара (ИАРА), сохранять слизистую оболочку между зубчатой линией и анастомозом не более 2 см длиной и проводить под прикрытием петлевой илеостомы для улучшения качества жизни пациентов. Сохранение протяженного участка прямой кишки (более 2 см над зубчатой линией) при использовании сшивающего аппарата для формирования ИАРА может быть причиной хронического воспаления в ней с дисфункцией резервуара, а также способствует сохранению риска дисплазии и (очень редко) рака [154]. При невозможности сформировать анастомоз при помощи сшивающего аппарата следует выполнить брюшно-анальную резекцию прямой кишки и наложить ручной илеоанальный анастомоз.
У пациентов ЯК, перенесших хирургическое лечение с формированием тонкокишечного резервуара (ИАРА), несмотря на то, что при использовании сшивающего аппарата сохраняется небольшой фрагмент слизистой оболочки, риск рака невысок и соответствует таковому при формировании ручного анастомоза [154].
Морфологические изменения эпителиальной выстилки резервуара обычно развиваются через 12-18 месяцев после закрытия илеостомы и характеризуются уплощением и сокращением числа ворсинок, приводящими к их атрофии («толстокишечная метаплазия») [159,160], что потенциально связано с риском развития злокачественной трансформации слизистой оболочки резервуара. Кроме того, при наложении аппаратного ИАРА сохраняется небольшой участок слизистой оболочки прямой кишки («манжетка»). Риск развития рака резервуара повышен у пациентов, оперированных по поводу рака или дисплазии на фоне ЯК (и при обнаружении дисплазии в операционном материале), а также у пациентов с первичным склерозирующим холангитом (ПСХ). Научное обоснование частоты контрольных обследований пациентов сИАРА не выполнялось, однако, у пациентов с наличием вышеуказанных факторов риска целесообразно проведение контрольных эндоскопических исследований (резервуароскопии) с биопсией слизистой оболочки не реже одного раза в 2 года.
2.7 Медикаментозная терапия в период хирургического лечения.
Влияние лекарственной терапии на риск хирургических вмешательств.
- Рекомендуется с осторожностью проводить медикаментозную терапию (гормональную, иммунодепрессивную, терапию с использованием моноклональных антител) в период хирургического лечения для профилактики послеоперационных осложнений [161-166].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4).
Комментарий: прием преднизолона** в дозе более 20 мг в течение более чем 6 недель увеличивает частоту хирургических осложнений [161,162]. Предоперационный прием АЗА иМП не ухудшает исход хирургического лечения [163], в то время как введение инфликсимаба** и циклоспорина**# незадолго до операции может увеличивать частоту послеоперационных осложнений [164,165], хотя данные по инфликсимабу** остаются противоречивыми [166].
Резкое прекращение терапии ГКС может вызвать синдром отмены (острую недостаточность коры надпочечников, т.н. Аддисонический криз), что обусловливает необходимость временного продолжения гормональной терапии после операции до полной отмены.
На настоящий момент отсутствует надежная научная база для обоснования какой-либо схемы прекращения гормональной терапии после колэктомии по поводу ЯК. Доза ГКС для дальнейшего перорального приема в период отмены гормональной терапии определяется длительностью предшествовавшей терапии и величиной использованных доз. Согласно рекомендациям Европейского общества по изучению ЯК и БК (ECCO) [20], в случае, если гормональная терапия перед операцией проводилась не более месяца, сразу после операции возможно прекращение приема ГКС.
Если перед операцией пациент более месяца получал ГКС, после хирургического вмешательства целесообразно перейти с вышеописанной высокой парентеральной дозы ГКС на пероральный прием ГКС внутрь в дозе не ниже верхней границы суточной стрессовой продукции кортизола, то есть не ниже 20 мг преднизолона**.
2.8 Резервуарит и другие осложнения хирургического лечения при формировании тонкокишечного резервуара
Резервуарит представляет собой неспецифическое воспаление тонкокишечного резервуара и наиболее частое осложнение ИАРА. Частота его возникновения колеблется в широком диапазоне от 15 до 50% в течение 10 лет после формирования ИАРА в крупных специализированных центрах [167-169]. Такие различия могут быть обусловлены существенно большим риском резервуарита при ЯК, превышающим частоту этого осложнения при формировании ИАРА по поводу других заболеваний (в частности, семейного аденоматоза толстой кишки) [170,171].
Осложнения резервуарита включают абсцессы, свищи, стеноз резервуаро-анального анастомоза и аденокарциному резервуара. Последнее осложнение встречается исключительно редко и почти всегда – при выявленной дисплазии или раке в операционном препарате, полученном при выполнении колэктомии.
Дифференциальный диагноз при подозрении на резервуарит проводится с синдромом раздраженного резервуара (СРР), ишемическими поражениями, БК и другими редкими причинами дисфункции резервуара, такими как коллагенозный, цитомегаловирусный и Clostridioides difficile-ассоциированный резервуарит. Следует учитывать возможность развития неспецифического илеита, вызываемого приемом НПВП и синдрома избыточного бактериального роста.
Основными препаратами, применяемыми для лечения резервуарита, остаются антибиотики,что позволяет классифицировать резервуарит как антибиотикочувствительный, антибиотикозависимый и антибиотикорезистентный.
- Рекомендуется пациентам с резервуаритом первая линия терапии, включающая 14-дневный курс перорального метронидазола** (15-20 мг/кг/сутки) или ципрофлоксацина** (1000 мг/сут) для достижения терапевтического эффекта [172].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5).
Комментарий: нежелательные явления значительно чаще отмечаются при приеме метронидазола. В случаях антибиотико-резистентного резервуарита возможно назначение перорального будесонида (9 мг) в течение 8 недель.
- Рекомендуется пациентам с резервуаритом при отсутствии эффекта или при развитии зависимости от приема указанных препаратов назначение резервных препаратов –#рифаксимина (2000 мг/сут) и тинидазола (1000–1500 мг/сут), в том числе в комбинации с ципрофлоксацином** (1000 мг/сут), ректальных ГКС, ректальных препаратов месалазина**, АЗА** для достижения терапевтического эффекта [172].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5).
Воспаление слизистой оболочки сохраненного участка прямой кишки и синдром раздраженного резервуара.
Другим потенциальным осложнением ИАРА является воспаление слизистой оболочки прямой кишки, сохраняемой при наложении аппаратного анастомоза.
- Рекомендуется пациентам с проктитом после формирования тонкокишечного резервуара, лечение проводить свечами месалазина** 500 мг 2 раза в сутки и/или ректальными ГКС для достижения терапевтического эффекта [58].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
2.9 Дисфункция илеостомы после хирургического лечения ЯК.
Под дисфункцией илеостомы понимается увеличение объема кишечного отделяемого по илеостоме более 1000 мл в сутки. Данное состояние также сопровождается быстро прогрессирующими метаболическими и водно-электролитными нарушениями [174,186].
- Рекомендуется пациентам с дисфункцией илеостомы для лабораторной диагностики Clostridioides difficile – ассоциированной диареи использовать алгоритм, включающий молекулярно-биологическое исследование фекалий на возбудителя диффициального клостридиоза (Clostridium difficile) или иммунохроматографическое экспресс-исследование кала на токсины A и B клостридии (Clostridium difficile) или иммунохроматографическое экспресс-исследование кала на токсины A и B клостридии (Clostridium difficile)[174,175].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5).
Комментарий: помимо обильного жидкого отделяемого по стоме, в клинической картине также отмечается повышение температуры тела до 39 С, метеоризм, редко жалобы на тошноту, рвоту, боли в животе спастического характера. При лабораторных исследованиях: анемия, гипопротеинемия, гипоальбуминемия, гипокалиемия, повышение уровня СРБ, редко увеличение концентрации креатинина.
- Рекомендуется пациентам с лёгкой дисфункцией илеостомы диетотерапия, спазмолитики и препараты, замедляющие пассаж по ЖКТ, для достижения терапевтического эффекта и улучшения качества жизни пациента [174,175,186].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5).
- Рекомендуется пациентам со среднетяжёлой формой дисфункции илеостомы метронидазол** в дозе 500 мг внутрь три раза в день в течение 10 дней. При отсутствии клинического эффекта от метронидазола** через 5-7 дней производят смену препарата на ванкомицин** в дозе 1000 мг в день per os в течение 10 дней для достижения терапевтического эффекта и улучшения качества жизни пациента [174,176,178,186].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5).
Комментарий: если в лабораторных показателях отмечается увеличение уровня лейкоцитов в крови более 15×109/л, креатинина в сыворотке крови выше 115 мкмоль/л, подъём температуры тела выше 38°C и снижении уровня альбумина менее 25 г/л, пациенты должны получать лечение в условиях круглосуточного стационара. Этим пациентам изначально показано назначение ванкомицина** в дозе 1000 мг внутрь в день в течение 10 дней.
- Рекомендуется пациентам с тяжелой формой дисфункции илеостомы изначально наряду с инфузионной терапией назначить ванкомицин** внутрь в дозе 500 мг 4 раза в день в сочетании с метронидазолом** в дозе 500 мг 3 раза в день внутривенно [179,186].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 5).
Комментарий: при невозможности введения препарата через рот ванкомицин** назначается ректально. При этом препарат в дозе 500 мг разводится в 500 мл 0,9% раствора хлорида натрия и вводится в виде клизм четыре раза в день. Ухудшение состояния пациента с возникновением гипотонии, гипертермия выше 38,5 °C, задержка стула, выраженное вздутие живота, изменение сознания, лейкоцитоз свыше 15 × 109 или лейкопении ниже 2 × 109, повышение уровня лактата в сыворотке крови выше 2,2 ммоль/л, развитие синдрома полиорганной недостаточности требует его перевода в отделение интенсивной терапии для дальнейшего лечения.
Медицинская реабилитация
Реабилитация
Специфические меры реабилитации пациентов с ЯК отсутствуют. Меры медицинской реабилитации направлены на профилактику колоректального рака.
Поскольку в ряде случаев терапия ЯК сопряжена с применением иммунодепрессантов, основным способом реабилитации пациентов является профилактика оппортунистических инфекций, описанная в разделе 5 (Профилактика).
У пациентов, которым потребовалось хирургическое лечение язвенного колита, возможна реабилитация в три этапа.
1-й этап – ранняя реабилитация, осуществляется непосредственно после хирургического лечения со 2-х по 14-е сутки. Основной задачей 1 этапа реабилитации является восстановление нормального функционирования желудочно-кишечного тракта после хирургического вмешательства. Именно на этом этапе чаще всего выявляются и должны быть корригированы нарушения мочеиспускания. Важная роль отводится также контролю гомеостаза, мероприятиям, направленным на заживление послеоперационных ран, купированию послеоперационного болевого синдрома, активизации пациента. В данный период проводится контроль общего анализа крови, биохимического анализа крови, коагулограммы крови, общего анализа мочи.
2-й этап реабилитации начинается после 15 суток и продолжается по мере необходимости в последующем. Направлен на окончательное заживление послеоперационных ран с контролем за деятельностью желудочно-кишечного тракта и других систем организма. Данный этап возможно осуществлять как амбулаторно, так и в условиях стационара дневного или круглосуточного пребывания.
3-й этап реабилитации осуществляется в поздний реабилитационный период у пациентов как с постоянной илеостомой, так и перед реконструктивно-восстановительной операцией. Основной задачей на данном этапе является компенсация функции желудочно-кишечного тракта, мероприятия, направленные на выявление и коррекцию функции запирательного аппарата прямой кишки.
Недостаточность анального сфинктера
Реабилитация возможна на 2 и 3 этапах. У ряда пациентов, у которых оперативное вмешательство по поводу ЯК завершилось формированием тонкокишечного резервуара, отмечается снижение функции держания.
Пациентам с ЯК с недостаточностью анального сфинктера перед реконструктивно-восстановительным лечением целесообразно выполнение исследования функций сфинктерного (запирательного) аппарата прямой кишки (сфинктерометрия, профилометрия, исследование проводимости по срамному нерву) с последующей консультаций врача функциональной диагностики для планирования оперативного вмешательства [180].
Пациентам с ЯК при выявлении недостаточности анального сфинктера 2-3 степени, целесообразно провести 10-дневный цикл электростимуляции с использованием биологической обратной связи (БОС-терапия и тибиальная ней ромодуляция) в условиях дневного или круглосуточного стационара для проведения реабилитационного лечения, улучшения качества жизни пациентов [180, 181].
В реабилитации пациентов с недостаточностью анального сфинктера по данным литературы, широкое применение нашел метод лечения биологической обратной связью (БОС), направленный на улучшение сократительной способности мышц наружного сфинктера и тазового дна за счет увеличения как силы, так и длительности произвольного сжатия [180,181]. Данный неинвазивный метод вовлекает в процесс реабилитации собственные ресурсы организма с выработкой правильных навыков на уровне создания новых условно-рефлекторных связей. Так же эффективным является метод тибиальной нейромодуляции. Нейромодуляция — это процесс, при котором электрический ток по одним нервным путям модулирует существовавшую ранее активность в других нервных путях или центрах.Чрескожная электростимуляция заднего большеберцового нерва применяется при функциональных заболеваниях органов малого таза, так как в составе заднего большеберцового нерва проходят волокна из II и III крестцовых сегментов спинного мозга, играющие значительную роль в иннервации прямой кишки, мочевого пузыря и их сфинктеров.Доказано, что мышечные структуры отключенного запирательного аппарата могут реагировать на терапию биологической обратной связью и проведение тибиальной ней ромодуляции, увеличивая как тонус, так и силу волевых сокращений [180,181]. Стимуляцию тибиального нерва проводят с помощью накожного стимулирующего электрода, что позволяет пациенту после курса предварительного обучения продолжить курс лечения самостоятельно в домашних условиях. В таком случае курс лечения с ежедневными сеансами стимуляции может продлеваться до 1-3 месяцев. Контроль эффективности БОС-терапии производится перед началом и по окончании каждого курса процедур путем комплексного физиологического исследования функции запирательного аппарата прямой кишки (сфинктерометрия + физиологическое исследование резервуарной функции низведенной кишки). При улучшении показателей тонуса и сократительной способности анальных сфинктеров, можно ставить вопрос о выполнении реконструктивно-восстановительной операции, направленной на возобновление естественного пассажа по желудочно-кишечному тракту.
Прогноз
Дополнительная информация, влияющая на течение и исход заболевания
Риск тяжелого обострения ЯК в течение жизни составляет 15%, при этом вероятность тяжелой атаки выше у пациентов с тотальным поражением толстой кишки. При проведении адекватной противорецидивной терапии в течение 5 лет обострений удается избежать у половины пациентов, а в течение 10 лет — у 20% пациентов. В течение первого года после постановки диагноза вероятность колэктомии составляет 4-9% (при тяжелой атаке — около 50%), в дальнейшем с каждым годом заболевания риск колэктомии увеличивается на 1%. Факторами риска агрессивного течения ЯК являются прогрессирование поражения от дистального (проктита) к тотальному, первичный склерозирующий холангит, а также детский и подростковый возраст на момент начала заболевания. Планирование беременности необходимо осуществлять в период ремиссии ВЗК, что позволяет улучшать исходы беременности. Применение беременными большинства препаратов для лечения ВЗК сопряжено с низким риском неблагоприятного воздействия на плод, за исключением метотрексата и препаратов 5-АСК, содержащих дибутилфталат. Отмена анти-ФНО или переход на монотерапию возможны лишь у ограниченного числа пациенток с низким риском реактивации ВЗК. Лечение генно-инженерными биологическими лекарственными препаратами, не противопоказанными при беременности (см. инструкцию по применению), может быть продолжено, если польза для матери превышает потенциальные риски для плода.
Уменьшение рисков, связанных с назначением ГКО, достигается строгим соблюдением принципов гормональной терапии. ГКС не могут применяться в качестве поддерживающей терапии.
При назначении гормональной терапии необходимо учитывать следующее:
- постепенное снижение дозы стероидов до полной отмены — строго обязательно;
- суммарная продолжительность гормональной терапии не должна превышать 12 недель;
- обязательным является сопутствующий прием препаратов кальция, витамина D;
- в период лечение необходим регулярный контроль уровня глюкозы в крови.
Пациентам, которым в результате хирургического лечения была сформирована кишечная стома, может потребоваться консультация и наблюдение специалистом по реабилитации стомированных пациентов.
Госпитализация
Организация оказания медицинской помощи
Медицинская помощь, за исключением медицинской помощи в рамках клинической апробации, в соответствии с федеральным законом от 21.11.2011 № 323-ФЗ (ред. от 47 25.05.2019) «Об основах охраны здоровья граждан в Российской Федерации», организуется и оказывается:
1) в соответствии с положением об организации оказания медицинской помощи по видам медицинской помощи, которое утверждается уполномоченным федеральным органом исполнительной власти;
2) в соответствии с порядками оказания помощи по профилям «гастроэнтерология», «колопроктология», обязательным для исполнения на территории Российской Федерации всеми медицинскими организациями;
3) на основе настоящих клинических рекомендаций;
4) с учетом стандартов медицинской помощи, утвержденных уполномоченным федеральным органом исполнительной власти.
Первичная специализированная медико-санитарная помощь больным ЯК оказывается врачом-гастроэнтерологом, врачом-колопроктологом и иными врачами-специалистами в медицинских организациях, имеющих лицензию на оказание соответствующих видов медицинской деятельности.
При подозрении или выявлении язвенного колита у пациента врачи-терапевты, врачи-терапевты участковые, врачи общей практики (семейные врачи), врачи-специалисты, средние медицинские работники в установленном порядке направляют пациента на консультацию в медицинскую организацию, имеющую в своем составе кабинет врача-гастроэнтеролога, врача-колопроктолога, и/или амбулаторный гастроэнтерологический центр (отделение), и/или амбулаторный колопроктологический центр (отделение), и/или центр диагностики и лечения воспалительных заболеваний кишечника (при наличии в субъекте, организуется на функциональной основе) для оказания ему первичной специализированной медико-санитарной помощи. Консультация в указанных структурных подразделениях медицинской организации должна быть проведена не позднее 15 рабочих дней с даты выдачи направления на консультацию, а в случаях тяжелой формы язвенного колита не позднее 3 рабочих дней с даты выдачи направления на консультацию.
Врач-гастроэнтеролог, врач-колопроктолог медицинской организации, имеющей в своем составе кабинет врача-гастроэнтеролога, врача-колопроктолога, амбулаторный гастроэнтерологический центр (отделение), амбулаторный колопроктологический центр (отделение), центр диагностики и лечения воспалительных заболеваний кишечника, организует своевременное квалифицированное обследование и лечение пациента, включая определение степени выраженности воспалительного процесса, протяженности поражения, наличия кишечных и внекишечных проявлений, в том числе взятие биопсийного материала.
При необходимости лечения и углубленного обследования в стационарных условиях, пациентна правляется лечащим врачом в гастроэнтерологическое отделение, колопроктологическое отделение, центр диагностики и лечения воспалительных заболеваний кишечника или иную медицинскую организацию, оказывающую медицинскую помощь в стационарных условиях пациентов по профилю «гастроэнтерология», «колопроктология».
При подозрении и (или) выявлении язвенного колита у пациента в ходе оказания ему скорой медицинской помощи таких пациентов переводят или направляют в медицинские организации, оказывающие медицинскую помощь по профилю «гастроэнтерология», «колопроктология» для определения тактики ведения и необходимости применения дополнительно других методов специализированного лечения, включая проведение таргетной биологической терапии.
Врач-гастроэнтеролог, врач-колопроктолог медицинской организации, имеющей в своем составе кабинет врача-гастроэнтеролога, врача-колопроктолога, амбулаторный гастроэнтерологический центр (отделение), амбулаторный колопроктологический центр (отделение), центр диагностики и лечения воспалительных заболеваний кишечника направляет пациента в медицинские организации, имеющие для оказания медицинской помощи в стационарных условиях в своем составе гастроэнтерологическое отделение и/или колопроктологическое отделение, и/или центр диагностики и лечения воспалительных заболеваний кишечника для уточнения диагноза (в случае невозможности установления диагноза при оказании первичной специализированной медико-санитарной помощи) и оказания специализированной, в том числе высокотехнологичной, медицинской помощи. Срок начала оказания специализированной, за исключением высокотехнологичной, медицинской помощи определяется по решению комиссии по отбору пациентов для госпитализации в зависимости от тяжести язвенного колита, характера течения, распространённости воспалительного процесса, срок не должен превышать 30 календарных дней с даты выдачи направления на госпитализацию.
Специализированная, в том числе высокотехнологичная, медицинская помощь при язвенном колите оказывается врачами-гастроэнтерологами, врачами-колопроктологами в медицинских организациях, имеющих в своем составе гастроэнтерологическое отделение и/или колопроктологическое отделение, и/или центр диагностики и лечения воспалительных заболеваний кишечника, имеющих лицензию, необходимую материально-техническую базу, сертифицированных специалистов, в стационарных условиях и условиях дневного стационара и включает в себя профилактику, диагностику, лечение язвенного колита, требующих использования специальных методов и сложных уникальных медицинских технологий, а также медицинскую реабилитацию.
Показания для госпитализации в круглосуточный или дневной стационар медицинской организации, оказывающей специализированную, в том числе высокотехнологичную медицинскую помощь при язвенном колите определяются врачом-гастроэнтерологом и/или врачом-колопроктологом с проведением при необходимости мультидисциплинарного консилиума.
Показанием для госпитализации в медицинскую организацию в экстренной или неотложной форме является:
1) наличии осложнений язвенного колита, требующих оказания ему специализированной медицинской помощи в экстренной и неотложной форме;
2) наличие осложнений лечения (хирургическое вмешательство, биологическая терапия, гормональная и цитостатическая терапия и т.д.) язвенного колита.
Показанием для госпитализации в медицинскую организацию в плановой форме является:
1) необходимость выполнения сложных интервенционных диагностических медицинских вмешательств, требующих последующего наблюдения в условиях круглосуточного или дневного стационара;
2) наличие показаний к специализированному лечению язвенного колита (хирургическое вмешательство, гормональная и цитостатическая терапия, биологическая и таргетная терапия), требующему наблюдения в условиях круглосуточного или дневного стационара.
Показанием к выписке пациента из медицинской организации является:
1) завершение курса лечения, или одного из этапов оказания специализированной, в том числе высокотехнологичной медицинской помощи, в условиях круглосуточного или дневного стационара при условии отсутствия осложнений лечения, требующих медикаментозной коррекции и/или медицинских вмешательств в стационарных условиях;
2) отказ пациента или его законного представителя от специализированной, в том числе высокотехнологичной медицинской помощи в условиях круглосуточного или дневного стационара, установленной консилиумом медицинской организации, оказывающей лечение язвенного колита при условии отсутствия осложнений основного заболевания и/или лечения, требующих медикаментозной коррекции и/или медицинских вмешательств в стационарных условиях;
3) необходимость перевода пациента в другую медицинскую организацию по соответствующему профилю оказания медицинской помощи. Заключение о целесообразности перевода пациента в профильную медицинскую организацию осуществляется после предварительной консультации по предоставленным медицинским документам и/или предварительного осмотра пациента врачами специалистами медицинской организации, в которую планируется перевод.
Профилактика
Профилактика
Язвенный колит характеризуется хроническим рецидивирующим течением. Диспансерное наблюдение при ЯК проводится пожизненно. Целью диспансерного наблюдения является, в первую очередь, профилактика колоректального рака. У большинства пациентов в стадии клинической ремиссии колоноскопия должна выполняться не реже, чем каждые 3 года. У части пациентов периодичность диспансерного наблюдения с проведением колоноскопии может быть иной. К особенностям наблюдения за пациентами, получающими иммунодепрессанты (АЗА**, МП**, МТ** и/или биологические лекарственные препараты), относится профилактика оппортунистических инфекции. К факторам риска развития оппортунистических инфекций относят: прием преднизолона** 20 мг в сутки и более в течение 2 недель, прием иммунодепрессантов (АЗА**, МП**, МТ** и биологические лекарственные препараты), возраст старше 50 лет, сопутствующие заболевания (хронические заболевания легких, алкоголизм, органические заболевания головного мозга, сахарный диабет).
Пациентам следует разъяснить необходимость постоянного приема лекарственных препаратов, поскольку соблюдение предписаний по терапии существенно (в 2-2,5 раза) снижает частоту обострений, а сама терапия является методом химиопрофилактики колоректального рака.
- Рекомендуется всем пациентам обязательная вакцинопрофилактика в соответствии с Европейским консенсусом по профилактике, диагностике и лечению оппортунистических инфекций при ВЗК для профилактики инфекций. Необходимым минимумом вакцинопрофилактики является [187]:
— Вакцина для профилактики вирусного гепатита В
— Вакцина для профилактики пневмококковых инфекций
— Вакцина для профилактики гриппа [инактивированная]
— Для женщин до 26 лет, при отсутствии вируса на момент скрининга рекомендуется вакцинация от вируса папилломы человека.
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5).
Комментарий. Пациентам в период терапии ГКС необходим мониторинг уровня гликемии (исследование уровня глюкозы в крови) для профилактики побочного действия глюкокортикоидов. Также необходим пациентам в период терапии иммунодепрессантами ежемесячный контроль уровня лейкоцитов (общий анализ крови) и печёночных ферментов (АЛТ, АСТ, билирубин, щелочная фосфатаза, ГГТ) в начале лечения раз в две недели, далее раз в месяц в течение первых 6 месяцев терапии, далее раз в три месяца для профилактики побочных эффектов от терапии.
- Рекомендуется пациентам перед проведением биологической терапии (ГИБП + малые молекулы (тофацитиниб**) и далее каждые 6 месяцев консультация врача-фтизиатра и скрининг на туберкулез (квантифероновый тест, а при невозможности, проведение внутрикожной пробы с туберкулезным аллергеном – проба Манту, диаскин-тест) для диагностики туберкулеза [182].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5).
- Рекомендуется пациентам до назначения иммуносупрессивной терапии, включая ГИБП и на фоне лечения проводить скрининг для диагностики сопутствующих заболеваний в соответствии с профессиональными клиническими рекомендациями:
1. на наличие маркеров вирусных гепатитов (Определение антител к вирусу гепатита C (Hepatitis C virus) в крови; Определение антител к поверхностному антигену (HBsAg) вируса гепатита B (Hepatitis B virus) в крови) [187]
2. на иммунодефицит человека (Определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV 1) в крови; Определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-2 (Human immunodeficiency virus HIV 2) в крови) [187].
3. на сифилис (Определение антител к бледной трепонеме (Treponema pallidum) в нетрепонемных тестах (RPR, РМП) (качественное и полуколичественное исследование) в сыворотке крови) [212].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
Комментарий: Недопустимы перерывы в лечении без медицинских показаний.
- Не рекомендуется всем пациентам смена оригинального препарата на биоаналог или наоборот более одного раза [196].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5).
Комментарий: в настоящее время зарегистрированы биосимиляры (биоаналоги) анти-ФНО, схожие с оригинальными биологическими лекарственными препаратами по эффективности и безопасности, однако их взаимозаменяемость с оригинальными препаратами в настоящее время не доказана. С учетом отсутствия клинических испытаний у пациентов с ВЗК, доказавших безопасность и эффективность чередования или полного переключения с оригинального препарата на биоаналоги и наоборот, подобный терапевтический подход не рекомендован [196].
- Рекомендуется всем пациентам каждые 6 месяцев выполнять исследование уровня кальпротектина в калеи/или ректороманоскопию с целью оценки эффективности проводимой терапии[39,41,42,183-185].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4).
Комментарий: с точки зрения долгосрочного прогноза течения ЯК целесообразно регулярно оценивать наличие эндоскопической ремиссии (заживления слизистой оболочки).
Информация
Источники и литература
-
Клинические рекомендации Российской гастроэнтерологической ассоциации
- 1.
Travis SP, Dinesen L. Remission in trials of ulcerative colitis: what does it mean?
PractGastroenterol.
2010;30:17–20.
2.
D»Haens G, et al. A review of activity indices and efficacy end points for clinical trials of medicaltherapy in adults with ulcerative colitis.
Gastroenterology
. 2007;132:763–86.
3.
Cosnes J, Gower-Rousseau C, Seksik P, Cortot A. Epidemiology and natural history ofinflammatory bowel diseases.
Gastroenterology
. 2011;140:1785–94.
4.
Белоусова Е.А., Абдулганиева Д.И., Алексеева О.П., Алексеенко С.А. и соавт. Социально-демографическая характеристика, особенности течения и варианты лечениявоспалительных заболеваний кишечника в России. Результаты двух многоцентровыхисследований.
Альманах клинической медицины.
2018;46(5):445-463.
https://doi.org/10.18786/2072-0505-2018-46-5-445-463.
5.
Katsanos KH, Vermeire S, Christodoulou DK, Riis L, et al. Dysplasia and cancer in inflammatorybowel disease 10 years after diagnosis: results of a population-based European collaborativefollow-up study.
Digestion
. 2007;75: 113–21.
6.
Silverberg MS, et al. Toward an integrated clinical, molecular and serological classification ofinflammatory bowel disease: report of a working party of the 2005 Montreal World Congress ofGastroenterology.
Can J Gastroenterol
. 2005;19(Suppl A):5–36.
7.
Truelove SC et al. Cortisone in ulcerative colitis; final report on a therapeutic trial.
Br Med J
.1955;2:1041–8.
8.
Seah D, De Cruz P. Review article: the practical management of acute severe ulcerative colitis.
Aliment Pharmacol
Ther
. 2016 Feb;43(4):482-513.
9.
Hindryckx P, Jairath V, D»Haens G. Acute severe ulcerative colitis: from pathophysiology toclinical management.
Nat Rev Gastroenterol Hepatol.
2016 Sep 1.
10.
Chen JH, Andrews JM, Kariyawasam V, Moran N. IBD Sydney Organisation and the AustralianInflammatory Bowel Diseases Consensus Working Group. Review article: acute severe ulcerativecolitis — evidence-based consensus statements.
Aliment Pharmacol
Ther.
2016 Jul;44(2):127-44.
11.
Schroeder KW, Tremaine WJ, Ilstrup DM. Coated oral 5-aminosalicylic acid therapy for mildly tomoderately active ulcerative colitis. A randomized study.
N Engl J Med
. 1987;317:1625–9.
12.
Григорьева Г.А., Мешалкина Н.Ю. О проблеме системных проявлений воспалительныхзаболеваний кишечника.
Фарматека
. 2011; № 15, с. 44-49.
13.
Sands BE. From symptom to diagnosis: clinical distinctions among various forms of intestinalinflammation. Gastroenterology. 2004;126:1518–32.
14.
Perler B, Ungaro R, Baird G, Malette M. et al. Presenting symptoms in inflammatory boweldisease: descriptive analysis of a community-based inceptive cohort.
BMC Gastroenterol
. 2019;19:47.
15.
Fine KD, Schiller LR. AGA technical review on the evaluation and management of chronicdiarrhea. Gastroenterology. 1999;116:1464–86.
16.
Forrest K, Symmons D, Foster P. Systematic review: is ingestion of paracetamol or non-steroidalanti-inflammatory drugs associated with exacerbations of inflammatory bowel disease? AlimentPharmacol Ther. 2004;20:1035–43.
17.
Mahid SS, Minor KS, Soto RE, et al. Smoking and inflammatory bowel disease: a meta-analysis.Mayo Clin Proc. 2006;81:1462–71.
18.
Vermeire S. Review article: genetic susceptibility and application of genetic testing in clinicalmanagement of inflammatory bowel disease. Aliment Pharmacol Ther. 2006;24:2–10.
19.
Carter MJ, Lobo AJ, Travis SP; IBD Section, British Society of Gastroenterology. Guidelines forthe management of inflammatory bowel disease in adults. Gut. 2004;53:V1–16.
20.
Harbord M, Eliakim R, Bettenworth D, Karmiris K, Katsanos K, Kopylov U, Kucharzik T, MolnárT, Raine T, Sebastian S, de Sousa HT, Dignass A, Carbonnel F; European Crohn’s and ColitisOrganisation [ECCO]. Third European Evidence-based Consensus on Diagnosis and Managementof Ulcerative Colitis. Part 2: Current Management. J Crohns Colitis. 2017 Jan 28;11(7):769-84.doi: 10.1093/ecco-jcc/jjx009.
21.
Travis SP, Jewell DP. Ulcerative colitis: clinical presentation and diagnosis. In: Satsangi J,Sutherland LR, editors. Inflammatory Bowel Diseases. London: Churchill Livingstone. 2003:169–81.
22.
Lucendo AJ,
Arias Á,
Roncero Ó,
Hervías D, et al. Anemia at the time of diagnosis ofinflammatory bowel disease: Prevalence and associated factors in adolescent and adult patients.
Sao Paulo Med J.
2014;132(3):140-6.
23.
Irwin JR,
Ferguson E,
Simms LA,
Hanigan K, et al. Detectable Laboratory Abnormality Is Presentup to 12 Months Prior to Diagnosis in Patients with Crohn»s Disease.
Dig Dis Sci
. 2019Feb;64(2):503-517.
24.
Cherfane CE,
Gessel L,
Cirillo D,
Zimmerman MB,
Polyak S. Monocytosis and a LowLymphocyte to Monocyte Ratio Are Effective Biomarkers of Ulcerative Colitis Disease Activity.
Inflamm Bowel Dis.
2015 Aug;21(8):1769-75.
25.
Feng JR,
Qiu X,
Wang F,
Chen PF, et al. Diagnostic Value of Neutrophil-to-Lymphocyte Ratio andPlatelet-to-Lymphocyte Ratio in Crohn»s Disease.
Gastroenterol Res Pract
. 2017;2017:3526460.doi: 10.1155/2017/3526460.
26.
Yoon JY,
Park SJ,
Hong SP,
Kim TI, et al. Correlations of C-reactive protein levels and erythrocytesedimentation rates with endoscopic activity indices in patients with ulcerative colitis.
Dig Dis Sci.
2014 Apr;59(4):829-37.
27.
Yamamoto-Furusho JK,
Sánchez-Osorio M,
Uribe M. Prevalence and factors associated with thepresence of abnormal function liver tests in patients with ulcerative colitis
.
Ann Hepatol.
2010Oct-Dec;9(4):397-401
28.
Archampong EQ,
Harris J,
Clark CG. The absorption and secretion of water and electrolytesacross the healthy and the diseased human colonic mucosa measured in vitro.
Gut
. 1972Nov;13(11):880-6.
29.
Maharshak N,
Arbel Y,
Gal-Oz A,
Rogowski O, et al. Comparative analysis of Bayer wide-rangeC-reactive protein (wr-CRP) and the Dade-Behring high sensitivity C-reactive protein (hs-CRP) inpatients with inflammatory bowel disease.
J Dig Dis.
2008 Aug;9(3):140-3.
30.
Weber P,
Husemann S,
Vielhaber H,
Zimmer KP,
Nowak-Göttl U. Coagulation and fibrinolysis inchildren, adolescents, and young adults with inflammatory bowel disease.
J Pediatr GastroenterolNutr.
1999 Apr;28(4):418-22.
31.
Issa M, Vikayapal A, Gracham MB et al. Impact of Clostridium difficile in inflammatory boweldisease patients.
Clin Gastroenterol Hepatol.
2007; 5: 345-351.
- 1.
Информация
Список сокращений
АЛТ – аланинаминотрансфераза
АСТ – аспартатаминотрансфераза
5-АСК – аминосалициловая кислота**
АЗА – азатиоприн**
Анти-ФНО – ингибиторы фактора некроза опухоли альфа (ФНО-альфа)
БК – болезнь Крона
БОС – биологическая обратная связь
ВЗК – воспалительные заболевания кишечника
гамма-ГТ – гамма-глютамилтранспептидаза
ГИБП – генно-инженерный биологический лекарственный препарат
ГКС – глюкокортикостероиды
ДИ – доверительный интервал
ЖКТ – желудочно-кишечный тракт
ИАРА – илеоанальный резервуарный анастомоз
ИМТ – индекс массы тела
КТ – компьютерная томография
ЛДГ – лактатдегидрогеназа
МП – меркаптопурин**
МРТ – магнитно-резонансная томография
НПВП – нестероидные противовоспалительные препараты
РКИ – рандомизированное контролируемое испытание
СОЭ – скорость оседания эритроцитов
СРБ – С-реактивный белок
ФНО-альфа – фактор некроза опухоли-альфа
ЯК – язвенный колит
UC – ulcerative colitis – язвенный колит
Термины и определения
Язвенный колит (ЯК) – хроническое заболевание толстой кишки, характеризующееся иммунным воспалением ее слизистой оболочки.
Обострение (рецидив, атака) ЯК – появление типичных симптомов заболевания у больных ЯК в стадии клинической ремиссии, спонтанной или медикаментозно поддерживаемой. На практике признаками клинического обострения являются увеличение частоты дефекаций с выделением крови и/или характерные изменения, обнаруживаемые при эндоскопическом исследовании толстой кишки.
Ремиссия ЯК – исчезновение основных клинических симптомов заболевания [1] и заживление слизистой оболочки толстой кишки («глубокая ремиссия») [2].
Ремиссия ЯК, клиническая – отсутствие примеси крови в стуле, отсутствие императивных/ложных позывов при частоте дефекаций не более 3 раз в сутки.
Ремиссия ЯК, эндоскопическая – отсутствие видимых макроскопических признаков воспаления при эндоскопическом исследовании толстой кишки.
Ремиссия ЯК, гистологическая – отсутствие микроскопических признаков воспаления.
Критерии оценки качества медицинской помощи
Приложение А1. Состав рабочей группы
Конфликты интересов у всех перечисленных авторов отсутствуют.
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций:
1. Врачи -гастроэнтерологи
2. Врачи -колопроктологи
3. Врачи -хирурги
4. Врачи -терапевты
5. Врачи общей практики (семейные врачи)
6. Врачи -эндоскописты
В данных клинических рекомендациях все сведения ранжированы по уровню достоверности (доказательности) в зависимости от количества и качества исследований по данной проблеме.
Таблица П1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
Таблица П2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
Таблица П3. Шкала оценки уровней убедительности рекомендаций (УРР) для методов профилактики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
Порядок обновления клинических рекомендаций
Механизм обновления клинических рекомендаций предусматривает систематическую актуализацию – не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утвержденным КР (клинических рекомендации) но не чаще 1 раз в 6 месяцев.
Приложение А3. Связанные документы
Данные клинические рекомендации разработаны с учетом следующих нормативных актов: порядка оказания медицинской помощи населению по профилю «гастроэнтерология»(утвержден приказом Министерства здравоохранения Российской Федерации № 906н от 12ноября 2012 г), порядка оказания медицинской помощи населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля (утвержден приказом Министерства здравоохранения Российской Федерации № 206н от 02 апреля 2010 г)
Приложение Б. Алгоритмы ведения пациента
Рисунок 1. Алгоритм диагностической и лечебной тактики при язвенном колите
Язвенный колит
Приложение В. Информация для пациентов
Язвенный колит (ЯК) – хроническое воспалительное заболевание, характеризующееся повторяющимися острыми обострениями, после которых следуют периоды ремиссии. Многочисленные исследования показывают, что без лечения у пациентов с ЯК существенно повышается риск колоректального рака и смертность. Несвоевременное и недостаточное лечение может привести к прогрессированию заболевания и не только нарастанию симптомов (диареи с кровью, болей в животе), но и к системным проявлениям: снижению массы тела, лихорадке, анемии. Тяжелое обострение язвенного колита представляет угрозу для жизни из-за риска перфорации (прободения) кишки и развития перитонита. Самое главное, что даже при слабо выраженных симптомах или их отсутствии в кишке может сохраняться воспаление. При неполноценном лечении это постоянное воспаление приводит к развитию колоректального рака, который при ЯК протекает особенно агрессивно. Только постоянная противовоспалительная терапия может уменьшить вероятность развития опухоли.
Язвенный колит – достаточно редкое заболевание, человек с этой болезнью должен по возможности наблюдаться у врача, специализирующегося на лечении именно данной патологии, и строго следовать его рекомендациям по длительной, нередко, пожизненной, лекарственной терапии. Ни уровень физической нагрузки, ни прием конкретных продуктов питания, не влияют на риск обострения язвенного колита так, как влияет на него нерегулярный прием лекарств и несвоевременное обращение к специалисту.
Приложение Г.
Название на русском языке: индекс активности язвенного колита (индекс Мейо)
Оригинальное название: Mayo Score / Disease Activity Index (DAI) for Ulcerative Colitis
Источник: Schroeder KW, Tremaine WJ, Ilstrup DM. Coated oral 5-aminosalicylic acid therapy formildly to moderately active ulcerative colitis. A randomized study. N Engl J Med. 1987;317:1625–9[11].
Тип: шкала оценки
Назначение: оценка тяжести атаки ЯК
Содержание (шаблон):
Ключ: тяжесть атаки ЯК устанавливается по сумме баллов: 0–2 — ремиссия (при этом оценка параметров ректального кровотечения и эндоскопического состояния слизистой = 0 баллов); 3–5 — легкая атака ЯК; 6–9 — среднетяжелая атака ЯК; 10–12 — тяжелая атака ЯК.
Парциальный индекс (или неполная шакала Мейо) без данных эндоскопии: 0–1 балл –клиническая ремиссия (при этом параметр «ректальное кровотечение» = 0 баллов; 1–2 балла –легкая атака; 3–5 баллов – среднетяжелая атака; ≥ 6 баллов – тяжелая атака ЯК.
Прикреплённые файлы
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники. Стандарты лечения
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.
Колит (лат. colitis, от греч. kolon (толстый кишечник) и itis (воспаление) — собирательное понятие, включающее большую группу заболеваний с одним общим признаком: воспалением толстого кишечника.
Основные признаки колита: частый жидкий стул с кровью, боль в животе и высокая температура.
Колиты встречаются в практике гастроэнтерологов, инфекционистов, терапевтов, колопроктологов, хирургов и других специалистов.
Этиология колита
Основные формы колитов можно описать только по отдельности, в зависимости от этиологического фактора. Размеры статьи не позволяют коснуться всех видов колита. Рассмотрим только основные из них.
Инфекционный колит — это заболевание кишечника, возникающее из-за активизации условно-патогенных микроорганизмов в кишечнике или попадания новых болезнетворных микробов из внешней среды.[1]
Инфекционный колит имеет очень широкое распространение: нет человека, ни разу не переносившего данное заболевание. Количество заболевших увеличивается в жаркий период, когда создаются благоприятные условия для распространения инфекции. Поэтому чаще болеют люди в регионах с жарким климатом (Африка, Юго-Восточная и Средняя Азия). Заболевание чаще встречается в детском возрасте, особенно у детей, посещающих учебные заведения (детские сады, школы и т. д.). Гастроэнтерологи и проктологи могут встречать в практике больных с данной патологией, но она не является профильной. Лечат заболевание обычно инфекционисты.
Причины инфекционного колита:
- бактерии (шигеллы, эшерихии, сальмонеллы, клостридии, иерсинии, брюшнотифозная палочка, кампилобактерии, протей, стафилококки);
- вирусы (аденовирус, энтеровирус, ротавирус);
- простейшие (амебы, лямблии и др.);
- возбудители туберкулеза и сифилиса;
- грибки (кандида, актиномицеты). Возникновение грибкового колита свидетельствует о снижении иммунитета и часто проявляется у лиц, страдающих СПИДом, получающих химиотерапию, стероидные гормоны;
- дисбактериоз.
Формы инфекционного колита:
- катаральная;
- фиброзная;
- катарально-геморрагическая;
- флегмонозная;
- флегмонозно-гангренозная;
- некротическая.
Воспалительные явления могут иметь стадийный характер, а могут сразу иметь картину запущенного воспаления. Его выраженность напрямую зависит от характера инфекции. Некротическое и флегмонозно-гангренозное воспаление встречается при клостридиальной инфекции. Катарально-геморрагическое — при дизентерии. Катаральное воспаление встречается чаще при вирусных заболеваниях.[2]
Ишемический колит — воспаление стенки толстого кишечника, возникающее из-за нарушения процессов кровобращения. Существует хроническое и острое нарушение кровообращения.[3]
Причиной нарушения кровообращения является полное прекращение или критическое снижение притока крови к толстой кишке, вследствие чего возникает воспаление. При тяжёлом течении может приводить к некрозу стенки кишечника. Причиной закупорки сосудов могут быть тромбы, но чаще всего к сужению просвета сосуда приводят атеросклеротические бляшки. Поэтому болезнь чаще проявляется у лиц пожилого возраста. Около 79% больных ишемическим колитом старше 48 лет.[4] Частота встречаемости не имеет связи с половой принадлежностью и регионом. Впервые открыт в 1966 году. Ишемический колит является профильным заболеванием для колопроктологов, но им также занимаются общие хирурги и гастроэнтерологи.[5]
Причины ишемического колита:
- атеросклероз сосудов;
- закупорка брыжеечных сосудов вследствие эмболии или тромбоэмболии (в результате аллергических реакций, травм, осложнений операций, системного васкулита, ДВС-синдрома);
- снижение давления крови может приводить к нарушению питания стенки кишки.
Закупорка просвета сосуда приводит к ишемии стенки кишки, а как следствие — к некрозу и далее перфорации.[6]
Объём поражения зависит от размера питающей артерии, длительности закупорки. Если закупорка сосуда происходит постепенно (при образовании атеросклеротических бляшек в сосудах), то говорят о хроническом нарушении кровообращения, что в свою очередь приводит к стриктурам.
При критических состояниях и снижении давления крови (например, анафилактический шок, ДВС-синдром и т.д.), происходит централизация кровообращения, при этом резко снижается приток крови к кишечнику, что приводит к ишемии и некрозу.
При атеросклерозе чаще страдает сигмовидная и поперечная ободочная кишка. Воспаление начинается со слизистой оболочки, затем переходит на все слои.[7]
По характеру поражения выделяют:
- транзиторную форму (когда ишемические процессы обратимы);
- стенозирующую (когда формируются стриктуры);
- гангренозную (когда образуются язвы с дальнейшим развитием некроза, поражение носит необратимый характер).[8]
Лучевой колит — образуется в результате ионизирующего воздействия на стенку толстого кишечника.
Симптомы острого и хронического колита: боль в животе, кровь в кале, диарея, высокая температура, слабость, слизь и кровь в стуле, спазмы.
Симптомы язвенного колита: к перечисленным выше признакам добавляются боли в анусе и анемия.
Боли при колите кишечника:
Инфекционный колит
Клиника инфекционного колита напрямую зависит от возбудителя.
Для любого инфекционного колита независимо от этиологии характерно:
- начало заболевания, как правило, имеет острый характер;
- жидкий частый стул с примесью слизи в кале;
- боли локализуются чаще в левом подреберье, но могут также распространяться по всем отделам живота;
- боль имеет периодический, спазматический характер;
- высокая температура;
- чувство слабости, недомогания;
- сухость кожных покровов и слизистых;
- белый налет на корне языка;
- рвота как первый симптом колита кишечника (если в воспалительный процесс вовлечен желудок).
Для первичной оценки этиологии инфекционного колита оценивают характер дефекации, объём и особенности каловых масс.
- при дезентерии стул очень частый, малыми порциями (до 20 раз за день) со слизью и прожилками алой крови (ректальный «плевок»);
- при амебиазе кал имеет вид малинового желе;
- при сальмонеллезе кал напоминает болотную тину, имеет неприятный запах;
- при псевдомембранозном колите (вызыванном клостридиями) частый жидкий стул с запахом гнили.
Ишемический колит
Симптоматика очень вариабельна, характерно быстрое прогрессирование.
- болезненные ощущения в животе;
- кровь и слизь в стуле;
- неустойчивый, частый стул;
- выраженные боли в околопупочной и левой подвздошной области;
- при ректальном осмотре можно заметить кал с кровью, слизью или гноем;
- при хронической форме боли имеют низкую интенсивность, обычно возникают после еды;
- при длительной хронической ишемии появляются стриктуры в толстой кишке, которые в дальнейшем могут быть следствием непроходимости или малигнизации (раковому перерождению).
Лучевой колит
Обычно колит формируется у лиц, перенёсших курс лучевой терапии по поводу новообразований, локализующихся в области малого таза или брюшной полости.[12]
- большую чувствительность к излучению имеет тонкий кишечник, формируется лучевой энтерит, который клинически проявляется нарушением абсорбции в тонком кишечнике;
- повреждению кишечника свойствен избирательный характер, обычно воспаление локализуется в прямой и сигмовидной кишке, при этом клиника сопоставима с клиникой язвенного и ишемического колита. При воздействии больших доз радиации клиника развивается не сразу, проявляется обильным, жидким стулом, при этом нарушается всасывание в толстом кишечнике.[13]
Толстый кишечник очень восприимчив к ионизирующему излучению.[10] Лучевой колит возникает при воздействии малых доз облучения: происходит атрофия слизистой оболочки (сразу после облучения).
- Усиливаются процессы деления клеток, уменьшается длина ворсинок.
- Активизируются воспалительные процессы с нейтрофильной реакцией. Чаще всего эти процессы локализуются в прямой и сигмовидной кишке.
- При воздействии больших доз (более 40 Гр.) воспалительные процессы могут возникать спустя длительное время после облучения (до нескольких лет), в данной ситуации происходит воспаление мелких сосудов кишечника, что приводит к ишемизации кишечника. Развиваются язвы и стриктуры. Могут поражаться все отделы толстого и тонкого кишечника.[11]
По течению:
- острый;
- хронический.
По этиологии:
- язвенный колит кишечника и болезнь Крона (воспалительные заболевания кишечника с неизвестной этиологией);
- инфекционный (этиологический фактор бактериальный, вирусный, грибковый, паразитарный);
- ишемический (развивается вследствие снижения притока крови к толстой кишке);
- спастический (из-за неправильного питания нарушается моторика толстого кишечника и возникают спазмы);
- токсический (при применении нестероидных противовоспалительных препаратов);
- лучевой (при поражении радиацией).
По локализации:
| Вид колита | Локализация |
|---|---|
| проктит | воспаление прямой кишки |
| панколит | тотальное поражение кишечника |
| тифлит | воспаление слепой кишки |
| трансверзит | воспаление поперечной ободочной кишки |
| сигмоидит | воспаление сигмовидной кишки |
| диффузный колит кишечника | охватывает два и более отдела кишечника |
Поражение кишечной стенки подразделяют на три вида:
- катаральный колит кишечника — слабое воспаление, слизистая краснеет, и возникает отёк;
- эрозивный колит кишечника — появляются эрозии;
- атрофический колит кишечника — слизистая атрофируется.
Инфекционный колит:
- Лабораторные методы:
- анализ кала на вирусы, бактерии, паразиты (позволяет точно поставить диагноз);
- серологическое исследование (определяют антитела к вирусам, паразитам);
- анализ крови на стерильность (при подозрении на сепсис);
- общеклинический анализ крови (высокое СОЭ, увеличение количества лимфоцитов при вирусной этиологии).
- Инструментальные методы:
- ректороманоскопия используется как дополнительный метод для дифференциальной диагностики;
- ультразвуковое исследование используется для исключения осложнений.
Ишемический колит:
- Ректороманоскопия дает возможность оценить состояние слизистой оболочки. При осмотре можно отметить наличие точечных кровоизлияний, сглаженность сосудистого рисунка, бледность слизистой. При обнаружении данных признаков показано взятие биопсии.
- Ирригоскопия — самое необходимое исследование. Обнаруживается симптом пальцевых вдавливаний. Признаки дефектов слизистой свидетельствуют о наличии язв, сужения просвета при стриктурах.
- Колоноскопия показана для уточнения распространенности воспаления, также показана биопсия в области измененного участка.
- Ангиография позволяет определить степень сужения сосуда и его локализацию.[9]
Дифференциальная диагностика
- Злокачественные новообразования. Опухоли развиваются достаточно длительное время, в течении многих лет.
- Инфекционный колит. Преобладают симптомы общей интоксикации (слабость, лихорадка и т.д.). Кроме того, имеет место эпидемический анамнез.
- Язвенный колит и болезнь Крона. Для них характерно достаточно медленное прогрессирование. Проявляются обычно в раннем возрасте.
Лучевой колит:
- При сборе анамнеза учитывают наличие факта облучения ионизирующей радиацией.
- Ректороманоскопия и колоноскопия с биопсией позволяют выявить воспаление слизистой оболочки толстого кишечника. При лучевом энтерите воспаление сочетается с атрофией слизистой. Крипты становятся менее глубокими, уменьшается длина ворсинок. При лучевом колите на слизистой обнаруживают язвы, стриктуры.[14]
Дифференциальная диагностика
- Энтерит лучевого генеза следует дифференцировать с болезнями тонкой кишки, при которых страдает функция всасывания (целиакия), при данных заболеваниях происходит атрофия по гиперрегенераторному типу, а при лучевом поражении преобладают гипорегенераторные процессы слизистой.
- Радиационные поражения толстого кишечника дифференцируют с язвенным колитом, болезнью Крона, новообразованиями толстого кишечника.[15]
Инфекционный колит:
- антибактериальные, противогрибковые средства с учетом чувствительности микроорганизмов. Предпочтение отдают таблетированным формам препаратов;
- восполнение потерянной жидкости и минералов: растворами для приема внутрь (Регидрон и др.), внутривенное введение (раствор Рингера, Трисоль и др.);
- прием сорбентов;
- пробиотики и пребиотики;
- ферменты (креон, фестал);
- симптоматическая терапия (противовоспалительные средства, спазмолитики и др.)
Ишемический колит:
- консервативное лечение колита (щадящая диета, препараты, смягчающие стул, лекарства для улучшения кровотока, дезагреганты, витаминные препараты, дезинтоксикационное лечение, восполнение баланса электролитов и жидкости, гемотрансфузии (при показаниях), антибактериальные препараты);
- оперативное лечение колита.
Показаниями для срочного хирургического лечения служат:
- перфорация, толстокишечная непроходимость. В таком случае удаляется участок кишки, с последующей санацией и дренированием брюшной полости.
- плановое оперативное лечение колита кишечника показано больным в случае сужения (стриктуры) толстого кишечника без явлений острой кишечной непроходимости.
Терапия лучевого колита схожа с терапией язвенного колита и болезни Крона:
- лекарства, содержащие 5-аминосалициловую кислоту (месалазин, салофальк);
- антибактериальная терапия.
Может быть полезно вести дневник питания, чтобы отслеживать, что вы едите, а также свои чувства. Если вы обнаружите, что некоторые продукты вызывают обострение ваших симптомов, вы можете попробовать их устранить.
Диетотерапия
Убедительных доказательств того, что неправильное питание приводит к воспалению кишечника, нет. Но оно может усугубить симптомы болезни, особенно при обострении. Поэтому полезно вести дневник питания и отслеживать свои реакции на определённые продукты.
Также рекомендовано:
- есть меньше молочных продуктов — у пациента может быть непереносимость лактозы, т. е. организм не переваривает молочный сахар;
- есть небольшими порциями по 5–6 раз в день;
- пить больше жидкости — предпочтительнее вода; алкоголь и напитки, содержащие кофеин, стимулируют кишечник и могут усилить симптомы болезни [15].
На сегодняшний день хорошо известны причины возникновения инфекционного колита, разработаны современные методики лечения. Поэтому при неосложненном течении и вовремя начатой терапии удается достигнуть полного выздоровления. Менее благоприятный прогноз у лиц с явлениями иммунодефицита и ослабленной иммунной системой (например, у людей пожилого возраста). Прогноз благоприятный.
Основными методами профилактики являются:
- гигиенические мероприятия (тщательное мытье рук);
- использование только свежих продуктов, чистой воды;
- уделение особого внимания термической обработке пищи.
При транзиторной форме ишемического колита прогноз благоприятный. При гангренозной форме — зависит от вовремя поставленного диагноза и проведенного лечения.
Так как ишемический колит является осложнением других болезней, то для его профилактики необходимо:
- своевременное лечение сопутствующих заболеваний;
- сбалансированное питание.
Лучевой колит приводит к постоянным, необратимым изменениям кишечной стенки, поэтому прогноз неблагоприятный.
При радиационном колите могут появляться язвы и стриктуры на слизистой оболочке толстого кишечника, что может привести к кишечной непроходимости. В таком случае необходимо хирургическое лечение, от своевременности которого зависит прогноз. При правильном и вовремя проведенном лечении прогноз благоприятный. Специальных методов профилактики лучевого колита не существует.
Колит
Колит – это воспалительное заболевание толстой кишки, возникшее вследствие инфекционного, ишемического, лекарственного или иного поражения. Колиты протекают с болевым синдромом, расстройством пищеварения (запорами, поносами), метеоризмом, тенезмами. В рамках диагностики производится исследование кала (копрограмма, бакпосев, на гельминтов и простейших), ирригоскопия, колоноскопия с биопсией слизистой толстого кишечника. Лечение назначается с учетом этиологической формы болезни, включает диету, этиотропную (антибактериальную, противогельминтную и другую терапию), прием ферментов и эубиотиков, фитотерапию, физио- и бальнеотерапию.
Общие сведения
Колитами называют заболевания пищеварительной системы, характеризующиеся развитием воспаления в слизистой оболочке стенки толстой кишки. Различают острый и хронический колит. Для острого колита характерны боли в животе, метеоризм, наличие слизи и прожилок крови в кале, тошнота, позывы к акту дефекации. Могут развиться хроническая форма, язвенное поражение кишечника, кровотечения, иногда канцерофобия.
Хронический колит представляет собой патологические изменения в строении слизистой оболочки в результате продолжительного воспалительного процесса и дистрофии пораженных тканей, в связи с которыми возникают нарушения моторной и секреторной функции толстого кишечника. Хронический колит — довольно часто встречающееся заболевание пищеварительного тракта, нередко воспаление толстой кишки сопровождается поражением тонкого кишечника.
Порядка трети больных хроническим колитом отмечают в качестве причины его развития различные кишечные инфекции (чаще всего дизентерию и сальмонеллез). Во многих случаях заболевание развивается на фоне дисбактериоза (к примеру, после продолжительного курса антибиотикотерапии), в связи с неправильным питанием, склонностью к гиподинамии, злоупотреблением алкогольными напитками.
Колит
Причины колита
Причины возникновения патологии могут быть связаны с нарушением режима и характера питания (неправильные пищевые привычки, нерегулярное нерациональное питание, злоупотребление алкоголем, прием некачественной пищи). Колиты могут возникать как осложнение заболеваний желудочно-кишечного тракта (хронического гастрита, панкреатита, гепатита), а также при пищевых отравлениях и заражении кишечными инфекциями.
Прием многих лекарственных средств может оказывать негативное действие на кишечную флору, ятрогенный дисбактериоз может в свою очередь вызывать воспалительные процессы в толстом кишечнике. Кроме того, колитам могут поспособствовать препараты, нарушающие кислотно-щелочной баланс в просвете кишечника. Иногда причинами воспалительных заболеваний кишечника являются врожденные патологии развития и функциональная недостаточность.
Классификация
Колиты подразделяются на инфекционные (колит при шигеллезе, сальмонеллезе, микобактериоз, туберкулезный колит и т.д.), алиментарные (связанные с нарушениями питания), токсические экзогенные (при продолжительных интоксикациях парами ртути, соединениями фосфора, мышьяка и т. д.) и эндогенные (при интоксикации продуктами катаболизма, например, уратами при подагре), лекарственные (развившиеся после применения лекарственных средств: слабительных, аминогликозидов, антибиотиков).
Выделяют также аллергические (аллергическая реакция на пищевые компоненты, лекарственные средства, некоторые бактерии или продукты их метаболизма) и механические (при хронических запорах, злоупотреблении клизмами, ректальными суппозиториями в результате регулярного механического раздражения слизистой) колиты. Зачастую имеет место несколько этиологических факторов, способствующих развитию воспаления в толстом кишечнике, тогда можно говорить о комбинированном колите.
Симптомы колита
Для хронического воспаления характерны такие клинические проявления, как боль в животе, расстройство дефекации, тенезмы. Болевой синдром при колите характеризуется тупой ноющей болью в нижних и боковых частях живота (часто с левой стороны), либо больной не может достаточно четко локализовать источник боли (разлитая боль в животе). После еды обычно боль усиливается и ослабляется после дефекации и отхождения газов. Кроме того, провоцировать усиление боли может ходьба, тряска, очистительная клизма. Также может отмечаться чувство тяжести в животе, вздутие, метеоризм.
Расстройства стула чаще всего протекают в виде запоров, но может отмечаться и чередование запоров и поносов. Для хронических колитов характерен понос с выделением водянистого кала с прожилками слизи (иногда может отмечаться кровь). Могут возникать тенезмы – ложные позывы к дефекации. Иногда позыв к дефекации заканчивается выделением слизи. При остром воспалительном процессе все перечисленные выше симптомы выражены более ярко, диарея преобладает над запорами.
Воспаление толстого кишечника чаще всего развивается в ее терминальных отделах (проктит и проктосигмоидит). Зачастую причиной колита в таких случаях является острая кишечная инфекция (дизентерия) или хронические запоры. Кроме того, проктосигмоидит является нередким результатом злоупотребления очищающими и лечебными клизмами, приема слабительных средств.
При этой форме колита боль локализуется с левой подвздошной области, возникают частые и болезненные тенезмы, особенно по ночам. Стул, как правило, скудный, может быть наподобие овечьего кала, содержать в больших количествах слизь, реже кровь и гной. При пальпации живота отмечают болезненность в области проекции сигмовидной кишки. Иногда пальпируется врожденная аномалия развития – дополнительная петля сигмы.
Диагностика

Анатомические и функциональные особенности толстого кишечника визуализируются его при контрастной ирригоскопии. Колоноскопия позволяет досконально изучить состояние слизистой на всем протяжении толстой кишки. Кроме того, проведение колоноскопии позволяет взять биоптаты слизистой кишечной стенки для дальнейшего гистологического исследования. Для исключения геморроя, анальной трещины, парапроктита и других патологий показан осмотр проктолога с пальцевым исследованием заднего прохода.
Дифференциальная диагностика хронических колитов проводится с дискинезией толстого кишечника. Однако, необходимо помнить, что продолжительно существующее расстройство моторики кишечника может осложниться воспалительным процессом. Довольно часто клиническая картина колита может сопровождать развивающуюся опухоль толстого кишечника. Для исключения злокачественных образований производят биопсию всех подозрительных участков стенки кишечника.
Кроме того, производят дифференциацию колитов и энтеритов. Иногда имеет место воспаление обоих отделов кишечника. Данные для дифференциальной диагностики хронического колита и заболеваний верхних отделов пищеварительного тракта дают эндоскопические исследования (колоноскопия, фиброгастродуоденоскопия), УЗИ органов брюшной полости и функциональные пробы для выявления маркеров воспаления печени и поджелудочной железы.
Осложнения
Колит может привести к перфорации кишечной стенки с развитием перитонита (характерное осложнение тяжело протекающего неспецифического язвенного колита), кишечному кровотечению, которое способствует развитию анемии, непроходимости кишечника в результате формирования спаек, стриктур, рубцов.
Лечение колита
Хронический колит в период обострения целесообразно лечить в стационаре, в отделении проктологии. Колиты инфекционной природы лечат в специализированных инфекционных отделениях. Значительным элементом в лечении хронического колита является соблюдение лечебной диеты. При этом из рациона исключают все продукты, которые могут механически или химически раздражать слизистую оболочку кишечника, пищу употребляют в протертом виде, с частотой не менее 4-5 раз в день. Кроме того, для исключения молочнокислого брожения больным рекомендуют отказаться от молока, с целью снижения газообразования ограничивают капусту, бобовые.
Из хлебобулочных изделий разрешен подсушенный пшеничный несладкий хлеб. Мясо и рыбу нежирных сортов желательно употреблять приготовленными на пару. При стихании выраженной клинической симптоматики диету постепенно расширяют. Для борьбы с запорами рекомендуют включение в рацион вареных овощей, фруктовых пюре (киселя), хлеба с отрубями. Улучшению прохождения кишечных масс способствует растительное масло и достаточное количество употребляемой в сутки жидкости. Употреблять фрукты и овощи в сыром виде в острый период заболевания нежелательно. Также стоит отказаться от охлажденных блюд, молочнокислых продуктов и пищи с высоким содержанием кислоты. Для регуляции секреции жидкости в кишечнике ограничивают употребление поваренной соли.
В случае инфекционной природы колита и для подавления патогенной бактериальной флоры, развившейся в результате дисбактериоза, назначают антибиотикотерапию короткими курсами (препараты ципрофлоксацин, Нифуроксазид, рифаксимин). Назначения лекарственных средств производится только специалистом. Выявления яиц глистов является показанием к назначению противогельминтных средств. Для облегчения болевого синдрома назначают спазмолитические средства (дротаверин, папаверин).
При лечении проктосигмоидита полезна местная терапия: микроклизмы с отварами ромашки, календулы, с танином или протарголом. При проктите назначают ректальные суппозитории с белладонной, анестезином для снятия выраженной болезненности, вяжущие средства (окись цинка, ксероформ). При поносах вяжущие и обволакивающие средства назначаются внутрь (танин+альбумин, нитрат висмута, белая глина, отвар коры дуб, другие отвары и настои сборов, содержащие дубильные компоненты). При запорах показано проведение гидроколонотерапии. Сильные спазмы при колите могут стать показанием для назначения холинолитиков.
Помимо вышеперечисленных средств, при колитах могут назначать энтеросорбенты (для борьбы с метеоризмом), ферментные препараты (при нарушении пищеварения в результате ферментных недостаточностей), эубиотики (для коррекции дисбиоза). Хороший эффект при терапии хронических колитов дает регулярное санаторно-курортное лечение, бальнеотерапия.
Прогноз и профилактика
В комплекс профилактических мер для предотвращения колитов входит сбалансированная рациональная диета, своевременное выявление и лечение заболеваний пищеварительной системы, меры санитарно-гигиенического режима и соблюдение правил техники безопасности на производствах, связанных с опасными химическими ядами.
Профилактика обострений у лиц, страдающих хроническими заболеваниями толстого кишечника, кроме того, включают регулярное диспансерное наблюдение специалиста в области клинической проктологии. Трудоспособность больных с данной патологией ограничена, им стоит избегать избыточных физических нагрузок, психо-эмоциональных стрессов и деятельности, связанной с частыми командировками и способствующей нарушению режима питания. Прогноз при своевременном выявлении и соблюдении врачебных рекомендаций по лечению хронического колита благоприятный.
|
Литература 1. Неспецифические воспалительные заболевания кишечника / Воробьев Г.И., Халиф И.Л. — 2008 2. Болезни органов пищеварения / Громнацкий Н.И. — 2010 3. Внутренние болезни. Система органов пищеварения / Г.Е. Ройтберг, Струтынский А.В. — 2007 4. Диагностика болезней органов пищеварения .Практическое руководство / Окороков А.Н. — 2000 |
Код МКБ-10 K50-K52 A00-A09 |
Резюме. Язвенный колит – хроническое заболевание, характеризующееся наличием воспаления, которое обычно начинается в прямой кишке и распространяется диффузно в проксимальном направлении, вовлекая часть или всю слизистую оболочку толстой кишки. Этиология язвенного колита до сих пор неизвестна, поэтому отсутствуют лекарственные средства, которые могли бы излечить это грозное заболевание. Весь обширный арсенал фармпрепаратов, который предлагается для лечения язвенного колита, направлен на различные, пока еще недостаточно изученные звенья патогенеза заболевания. Появление нового класса лекарственных средств (генно-инженерных биологических препаратов), к сожалению, не решило эту кардинальную проблему. Единственный способ «излечения» язвенного колита в настоящее время – удаление всей толстой кишки с формированием илеоанального резервуарного анастомоза или постоянной илеостомы. Однако хирургическое лечение язвенного колита сопряжено с множеством осложнений, а иногда и летальными исходами. Главные цели терапии заболевания заключаются в индукции и сохранении бесстероидной клинической и эндоскопической ремиссии, уменьшении частоты осложнений, инвалидизации и улучшении качества жизни. Тяжелые формы язвенного колита, требующие госпитализации и интенсивного консервативного лечения, а иногда и хирургического вмешательства, составляют около 15% всех случаев. Большинство легких и среднетяжелых форм язвенного колита могут успешно лечиться амбулаторно с помощью традиционных лекарственных средств, в первую очередь инновационных препаратов месалазина. Грамотная комбинация пероральных и ректальных форм месалазина позволяет в большинстве случаев добиться не только клинической ремиссии, но и достичь современной цели лечения язвенного колита – заживления слизистой оболочки толстой кишки, то есть эндоскопической ремиссии. В статье изложены современные взгляды на лечение легкой и среднетяжелой форм язвенного колита с различной протяженностью поражения толстой кишки, которые отражены в последних отечественных и зарубежных руководствах.
Язвенный колит (ЯК) – хроническое инвалидизирующее воспалительное заболевание кишечника, которое обычно возникает в молодом возрасте и продолжается в течение всей жизни пациента. Несмотря на то, что заболеваемость ЯК в Западной Европе и Северной Америке стабилизировалась, она продолжает расти в новых индустриальных странах [1].
Согласно популяционным когортным исследованиям большинство пациентов с ЯК имеют легкую или среднетяжелую формы ЯК [2]. Наиболее манифестные проявления заболевания отмечаются на момент выставления диагноза, а в дальнейшем периоды обострений чередуются с ремиссиями. У 14-17% пациентов может быть агрессивное течение ЯК [3-9]. Почти 50% больных ЯК за все время заболевания вынуждены госпитализироваться хотя бы один раз, а среди тех, кто был однажды госпитализирован, риск повторной госпитализации в течение 5 лет достигает 50%. Кумулятивный риск колэктомии в течение 5 и 10 лет составляет около 10-15%. Хотя риск ранней колэктомии снизился, частота долговременной колэктомии в течение продолжительного времени остается стабильной [3, 7, 8, 10]. Кроме существенного снижения качества жизни и работоспособности из-за клинических проявлений заболевания ЯК также ассоциируется с повышенным риском развития колоректального рака (КРР) [57].
Доказанными предикторами агрессивного течения ЯК и колэктомии является молодой возраст (менее 40 лет) на момент установления диагноза, тотальное поражение, выраженная эндоскопическая активность (наличие глубоких язв), внекишечные проявления, необходимость в раннем назначении глюкокортикостероидов (ГКС) и повышение уровней воспалительных маркеров [4, 11-14]. Напротив, у пациентов с ограниченной анатомической протяженностью поражения и незначительной эндоскопической активностью риск колэктомии низкий. В целом примерно у двух третей пациентов с ЯК на момент установления диагноза заболевание ограничивается прямой кишкой и левыми отделами ободочной кишки. Приблизительно у одной пятой части пациентов с дистальным ЯК со временем отмечается распространение поражения (обычно в течение 10 лет после установления диагноза). Как правило, это пациенты с неудовлетворительным контролем за течением заболевания [15-17].
Согласно результатам популяционных когортных исследований более 90% больных получали препараты 5-аминосалициловой кислоты (5-АСК) в течение первого года после установления диагноза, а 60-87% пациентов продолжали и далее использовать 5-АСК. Только 50% пациентов получали ГКС, 20% – иммуносупрессоры, а 5-10% – биологическую терапию в период заболевания [3-9]. Хотя основное внимание акцентировалось на пациентах с тяжелой формой ЯК с высоким риском колэктомии, у большинства наблюдались легкие и среднетяжелые формы с низким риском колэктомии. Таких пациентов обычно лечат врачи общей практики и гастроэнтерологи с помощью различных терапевтических стратегий [18].
Успешное ведение пациентов с ЯК основывается на нескольких принципах: тщательной стратификации и мониторинге, выявлении предикторов агрессивного течения и проведении последующей агрессивной терапии у больных с высоким риском колэктомии, оптимальное ведение пациентов с низким риском колэктомии с легкими и среднетяжелыми формами заболевания, чтобы снизить риск прогрессирования и возникновение осложнений [19].
Российские, американские и европейские клинические консенсусы по ведению пациентов с ЯК ставят основными целями терапии индукцию и сохранение бесстероидной клинической и эндоскопической ремиссии, уменьшение частоты осложнений и инвалидизации, улучшение качества жизни [19-23].
Эндоскопическая ремиссия ЯК, или заживление слизистой оболочки толстой кишки, ассоциируется с более низкой частотой рецидивов, снижением потребности в ГКС, существенно меньшей частотой хирургических операций, более низким риском КРР, более высоким качеством жизни [24-28].
Лечение ЯК можно условно разделить на два этапа – индукцию ремиссии и ее сохранение. Терапевтические стратегии обычно зависят от тяжести атаки (легкая, среднетяжелая, тяжелая) и протяженности поражения толстой кишки (проктит, левосторонний колит, тотальный колит). В статье изложены современные взгляды на лечение легких и среднетяжелых форм ЯК с различной протяженностью поражения толстой кишки, содержащиеся в последних отечественных и зарубежных руководствах.
Современные принципы консервативного лечения легкой и среднетяжелой форм язвенного колита
Первой линией индукционной терапии всех форм ЯК с различной протяженностью поражения толстой кишки является 5-АСК [19, 23, 29-31].
Международное непатентованное название 5-АСК – месалазин. Первым лекарственным препаратом для лечения ЯК, который содержал в своем составе молекулу 5-АСК, был сульфасалазин. Молекула 5-АСК в сульфасалазине соединяется азотной связью с молекулой сульфаниламида сульфапиридина. В толстой кишке под влиянием бактерий кишечной микрофлоры азотная связь разрушается, высвобождая активные компоненты – 5-АСК и сульфапиридин. Противовоспалительным действием обладает только 5-АСК, которая:
- подавляет синтез медиаторов воспаления (простагландинов и лейкотриенов) путем ингибирования циклооксигеназы;
- ингибирует функции нейтрофильных гранулоцитов – миграцию, дегрануляцию, фагоцитоз и образование свободных токсичных кислородных радикалов;
- тормозит синтез фактора, активирующего тромбоциты;
- оказывает антиоксидантное действие;
- участвует в активации PPAR-γ-рецепторов, играющих ключевую роль в поддержании целостности слизистой оболочки кишечника;
- оказывает значимое влияние на экспрессию генов, ответственных за инвазивность, метаболизм и стрессоустойчивость бактерий;
- эффективно ингибирует ядерный (нуклеарный) фактор (NF-κB), отвечающий за регуляцию генной активности и синтез провоспалительных цитокинов (ИЛ-1, ИЛ-6, ИЛ-8, ФНО-α).
Кроме того, месалазин стимулирует апоптоз (запрограммированную гибель клеток) клеток КРР, подавляет митоген-активированную протеинкиназу (МАП-киназу) и уменьшает скорость пролиферации слизистой оболочки толстой кишки у пациентов со спорадическими полипами [32-34]. Сульфапиридин же выступает исключительно в качестве носителя, позволяющего доставить 5-АСК в толстую кишку. У значительного числа больных при длительном приеме сульфасалазина встречаются побочные эффекты. Практически все они обусловлены сульфапиридином. Метаболизм сульфапиридина осуществляется в печени посредством реакций ацетилирования, поэтому у пациентов с медленным фенотипом ацетилирования происходит накопление токсических концентраций сульфапиридина даже при использовании терапевтических доз сульфасалазина. Чтобы снизить вероятность развития побочных эффектов, следует применять сульфасалазин в суточной дозе не выше 3,0 г, что, однако, может существенно сказаться на его клинической эффективности, поскольку доза сульфасалазина 2,0 г стехиометрически соответствует всего лишь 0,75 г месалазина [35].
Большим достижением в лечении воспалительных заболеваний кишечника (ВЗК) была разработка нового поколения препаратов, содержащих чистый месалазин. Эти препараты позволяют избежать побочных эффектов, обусловленных сульфапиридином, и создать высокую концентрацию 5-АСК в зоне воспаления [32, 33]. Препараты месалазина первого поколения для перорального приема отличаются различной защитной оболочкой таблетки, которая растворяется при определенном рН внутрикишечной среды. В таблетках Салофалька месалазин заключен в оболочку из специального полимерного материала, которая растворяется при рН > 6, то есть в терминальном отделе тонкой кишки и правых отделах ободочной кишки. В результате в этих отделах кишечника создается наивысшая концентрация активного лекарственного компонента – месалазина. Суточная доза таблеток Салофалька колеблется от 1,5 до 4,0 г в зависимости от выраженности клинической активности ЯК. Суточную дозу обычно делят на 3-4 приема.
Другая технология используется при производстве микрогранул препарата Пентаса®. При приеме как таблеток, так и гранул Пентасы высвобождение 5-АСК начинается в двенадцатиперстной кишке и равномерно продолжается до прямой кишки [36]. При этом согласно инструкции около 30-50% препарата адсорбируется главным образом в тонкой кишке, в связи с чем в толстой кишке активно около 50-60% месалазина. Это требует увеличения дозы Пентасы в 2 раза при локализации воспалительного процесса в толстой кишке: рекомендованная доза, согласно инструкции Пентаса® (гранулы), для лечения обострения ЯК составляет 4 г/сут, для поддержания ремиссии – 2 г/сут.
Выбор конкретного лекарственного препарата (Пентаса® или Салофальк®) определяется в первую очередь локализацией патологического процесса в кишечнике. При поражении проксимальных отделов подвздошной и тощей кишки предпочтение отдается Пентасе, а при поражении терминального отдела подвздошной и толстой кишки препаратом выбора является Салофальк®. Месалазин имеет хороший профиль безопасности. Побочные эффекты при назначении высоких и низких доз месалазина сопоставимы. Для всех пациентов с хроническими заболеваниями, в том числе ВЗК, характерен плохой комплаенс, т. е. несоблюдение рекомендованной схемы приема лекарственных препаратов. Пациенты предпочитают однократный прием всей суточной дозы назначенного препарата, а не дробный прием в течение дня [37].
Для улучшения соблюдения предписанного режима приема Салофалька была разработана новая лекарственная форма препарата – гранулы Салофальк. Эта инновационная двухкомпонентная лекарственная форма сочетает pH-контролируемое высвобождение активной субстанции с длительным непрерывным выделением месалазина из ядра на основе оригинальной полимерной матрицы. Кишечнорастворимая защитная оболочка обеспечивает pH-зависимое высвобождение активной субстанции, начинающееся в терминальном отделе подвздошной кишки и продолжающееся в нижележащих отделах кишечника. Потеря действующего вещества до подвздошной кишки при этом минимальна.
Полимерное матричное ядро обеспечивает длительное непрерывное выделение активной субстанции на всем протяжении толстой кишки, включая прямую кишку. Нерастворимое ядро гранулы, которое выполняет исключительно функцию доставки действующего вещества в толстую кишку, уже без месалазина может выходить со стулом. Это абсолютно нормальное, предусмотренное явление, никоим образом не свидетельствующее о недостаточном высвобождении действующего вещества из гранул, что подтверждается высокой эффективностью гранул Салофалька при ЯК в большом количестве клинических исследований.
Большое количество гранул (в 3 г Салофалька их содержится около 3500) обеспечивает равномерное и эффективное распределение активной субстанции и, благодаря очень большой площади поверхности (3 г гранул соответствуют 100 см2), гарантирует эффект даже при ускоренном пассаже по кишечнику (диарее). Согласно инструкции Салофальк® гранулы может назначаться всего лишь один раз в день. Благодаря малому размеру гранул (около 1 мм), способствующему беспрепятственному пассажу через желудок, их можно принимать вне зависимости от употребления пищи. Благодаря оптимальному профилю высвобождения гранулы Салофалька позволяют достичь многих клинических эффектов лечения при существенно более низких дозах (3,0 и 1,5 г) по сравнению с другими препаратами месалазина.
Так, по данным объединенного анализа четырех проспективных рандомизированных двойных слепых исследований [38] с участием 705 пациентов с активным ЯК, гранулы Салофалька в дозе 3 г/сут однократно (лечение 8 недель) были эффективны у 86% пациентов с проктосигмоидитом в достижении клинической ремиссии, существенно превосходя таблетки. При этом гранулы Салофалька продемонстрировали и более высокую эффективность в отношении заживления слизистой, по сравнению с таблетками. Это дает основания рассматривать Салофальк® гранулы в качестве препарата выбора перорального месалазина при дистальных формах ЯК [38]. Создавая высокую концентрацию 5-АСК в слизистой оболочке (СО), гранулы Салофалька позволяют достичь гистологического заживления СО толстой кишки. По данным исследования Kruis, 2009, при участии 54 клинических центров в 13 странах и 380 пациентов с обострением ЯК, Салофальк® гранулы 3 г/сут в течение 8 недель как при однократном, так и 3-кратном приеме был эффективен почти у 60% пациентов в достижении гистологического заживления СО – гистологической ремиссии + улучшения [37].
В препарате Мезавант® используется многоматричная система доставки месалазина (технология MMX, Cosmo Pharmaceuticals, Италия). За счет кишечнорастворимой оболочки из эудрагита S высвобождение действующего вещества из таблетки ММХ начинается при pH ≥ 7,0 в толстой кишке, а за счет системы замедленного высвобождения ММХ происходит постепенное высвобождение месалазина на всем протяжении толстой кишки. Таблетки месалазина-ММХ, как и гранулы Салофалька, принимаются один раз в сутки. Следует учитывать, что при использовании таблеток месалазина-ММХ, как и других препаратов с оболочкой из эудрагита S (асакол, месакол), высвобождающих месалазин при значениях pH ≥ 7,0, как минимум у 25% пациентов они могут быть малоэффективны. Это связано с тем, что у значительной доли даже здоровых людей (до 25%) рН ни в одном отделе ЖКТ не достигает уровня 7, тогда как уровень pH достигает 6 у 90% людей уже в подвздошной кишке. При ВЗК отмечается дополнительное закисление среды кишечника: время, когда рН превышает 7, значительно сокращается у больных с мягким и умеренным ЯК по сравнению со здоровыми добровольцами (0,3 ± 0,17 против 9,3 ± 5,3 часа). У некоторых пациентов этот период может быть настолько коротким, что его недостаточно для полного растворения оболочки таблетки из эудрагита S. Риск полного нерастворения таблетки Мезаванта существенно выше у пациентов с распространенным колитом, частым стулом (5 и более раз в сутки) и жидкой его консистенцией (5-6 типы по Бристольской шкале), что в результате увеличивает риск рецидива или усиления воспаления при ЯК [39].
Клинический эффект различных препаратов месалазина во многом определяется разным профилем высвобождения активного вещества. Следует отметить, что, хотя все препараты месалазина позволяют достичь ремиссии, время до наступления улучшения может существенно отличаться. Наиболее быстрый эффект при ЯК (по результатам обзора разных исследований) отмечается при использовании гранул Салофалька – прекращение ректального кровотечения и диареи достигается уже на 11-12 день [38, 40]. Эти данные важны с точки зрения оценки терапевтического ответа для решения вопроса о продолжении текущей терапии или назначении системных стероидов.
Введение в клиническую практику инновационных лекарственных форм месалазина на основе полимерных матриц (с возможностью однократного приема суточной дозы), таких как гранулы Салофалька, способствует не только повышению эффективности стандартной терапии ВЗК, но и значительному улучшению приверженности лечению. Последнее обстоятельство имеет немаловажное значение, учитывая длительность терапии (иногда пожизненной) и необходимость профилактики КРР.
Выбор оптимальной суточной дозы месалазина – важный аспект повышения эффективности лечения ЯК.
Для достижения максимального терапевтического эффекта при использовании препаратов месалазина для индукции ремиссии целесообразно сразу назначать эффективную суточную дозу месалазина, а не использовать тактику эскалации дозы – начинать с невысокой дозы, а при отсутствии эффекта ее повышать [19]. Консенсус ECCO (2021) для купирования легкой и среднетяжелой атак ЯК рекомендует использовать месалазин в суточной дозе более 2 г [23]. Личный клинический опыт позволяет рекомендовать прием таблеток Салофальк 4,0 г в сутки, а при использовании микрогранул Салофальк – 3,0 г в сутки.
Использование ректальных форм месалазина показано при всех клинических формах ЯК, вне зависимости от протяженности поражения толстой кишки.
Ректальные формы месалазина могут использоваться как монотерапия при лечении дистальной формы ЯК или в дополнение к пероральным формам месалазина при тотальном поражении толстой кишки.
Для лечения ЯК в России и за рубежом широко используются местные (топические) формы месалазина. В России представлены все лекарственные местные формы Салофалька: свечи, микроклизмы и пена. Свечи, содержащие активную субстанцию месалазина, уже много лет успешно применяются при лечении ЯК. Активная субстанция свечей Салофалька (месалазин) концентрируется главным образом в прямой кишке. Это было доказано сцинтиграфическими исследованиями с мечеными радиоактивным 99mTc свечей Салофалька по 500 мг. Лечебные клизмы Салофалька объемом 30,0 мл и 60,0 мл содержат 2 и 4 г месалазина соответственно. При использовании микроклизм лекарственная суспензия, содержащая месалазин, распространяется ретроградно по нисходящей кишке до левого изгиба ободочной кишки. При ректальном применении суспензии месалазина наблюдается низкая системная абсорбция. В зависимости от времени удержания этот уровень составляет 5-35% от введенной дозы. Пена Салофалька для ректального применения содержит 1 г месалазина в 30 мл пены. Каждый баллончик рассчитан на 14 впрыскиваний (по 1 г месалазина каждое). Салофальк в форме пены (аэрозоля) позволяет проводить эффективную местную терапию при ВЗК за счет длительной адгезии к слизистой, обеспечивая оптимальный контакт действующего вещества с поверхностью СО, что особенно важно у пациентов с диареей и тенезмами. Эффективность пены сопоставима с эффективностью клизм Салофалька, но при этом пациенты отдают предпочтение пене как существенно более удобной в применении лекарственной форме [41].
Ректальная терапия хорошо переносится подавляющим большинством пациентов. В случаях, когда больной все же испытывает проблемы с удержанием ректально введенного месалазина, рекомендуются следующие подходы, позволяющие повысить переносимость препарата [42]:
- полежать на животе в течение 30 минут после введения препарата;
- принять 2 мг лоперамида за час до ректального введения препарата;
- вводить препарат ректально после естественного опорожнения кишки;
- проводить ректальную терапию вечером или на ночь.
Консенсус Европейской организации по изучению болезни Крона и язвенного колита (ECCO – 2021) для купирования атаки дистального ЯК (поражение до 20 см прямой кишки) рекомендует суточную дозу ректального месалазина от 1 г и выше. Для лечения прок-тита обычно достаточно монотерапии суппозиториями с месалазином в течение 6-8 недель. При проктосигмоидите целесообразно использовать пену или микроклизмы с месалазином. Ректальная терапия всегда эффективнее перорального приема месалазина. Наш клинический опыт свидетельствует о наступлении перелома в течении дистального ЯК при переводе пациентов с проктитом и проктосигмоидитом с пероральных препаратов месалазина на лечение его высокими дозами с помощью ректальных форм (суппозитории, пена, микроклизмы).
Алгоритм терапии легкой и среднетяжелой атаки проктита представлен на рис. 1.
Консенсус ECCO (2021) при протяженном поражении толстой кишки рекомендует комбинированную терапию пероральными и ректальными формами препаратов месалазина [23]. В нескольких крупных исследованиях показано преимущество комбинированной терапии против монотерапии месалазином [43-46]. Комбинированная терапия (месалазин ректально + перорально) активного колита существенно повышает успех лечения, обеспечивая эффект почти у 90% пациентов и более чем в 2 раза сокращая время до наступления ремиссии.
Рекомендуется добавление ректальных ГКС без отмены месалазина при недостаточном эффекте от терапии месалазином при проктите и проктосигмоидите.
Ректальные (топические) ГКС имеют преимущество перед системными ГКС за счет большей таргетности (способности воздействовать на зону воспаления в толстой кишке) и существенно меньшего количества побочных эффектов [47-49]. Их целесообразно использовать для усиления терапевтического ответа на ректальное введение месалазина [50].
Алгоритм консервативного лечения легкой и среднетяжелой атаки левостороннего и тотального колита представлен на рис. 2 и 3.
Месалазин рекомендуется как основное лекарственное средство для противорецидивной терапии ЯК. Доза препарата определяется тяжестью предшествующей атаки, характером течения заболевания и ответом на предшествующую терапию.
Консенсус ECCO (2021) для проведения противорецидивного лечения рекомендует использовать пер-оральную суточную дозу месалазина от 2 г и выше [23]. Эффективная поддерживающая доза варьирует в зависимости от конкретной клинической ситуации. Пациентам с более агрессивным течением ЯК иногда в течение длительного времени приходится применять индукционные дозы месалазина (3-4 г/сут). Еще одним аргументом для длительного использования месалазина с целью сохранения ремиссии является химиопрофилактика КРР [51]. В период ремиссии для улучшения комплаентности пациентов предпочтительно использовать препараты месалазина с возможностью однократного приема (гранулы Салофалька и месалазин-ММХ). Доза гранул Салофалька назначается минимальная – 1,5 г в сутки.
Следует отметить, что Салофальк® гранулы (в США зарегистрированы под названием Apriso®) является единственным препаратом месалазина, получившим одобрение для использования дозы всего 1,5 г/сут для поддержания ремиссии ЯК [52]. Это подтверждено решением Управления по санитарному надзору за качеством пищевых продуктов и медикаментов (Food and Drug Administration, FDA) по результатам клинических исследований эффективности, проведенных в США. Следует отметить, что в дозе 1,5 г/сут гранулы Салофалька обеспечивают стойкую клинико-эндоскопическую ремиссию у 8 из 10 пациентов в течение 2,5 лет [53]. При использовании таблеток месалазина-ММХ минимально рекомендуемая доза согласно инструкции и клиническим исследованиям составляет 2,4 г (рандомизированных клинических исследований по использованию более низкой дозы месалазина-ММХ – 1,2 г не проводилось).
При переходе на поддерживающую дозу месалазина необходимо убедиться в наступлении эндоскопической ремиссии, поскольку по современным критериям эффективности терапии, пока не произошло заживление слизистой, – ремиссия не достигнута. Согласно объединенным рекомендациям по ведению пациентов с ВЗК ECCO и ESGAR (Европейское общество абдоминальных радиологов) от 2019 г., положение 2.1.2: «у больных ЯК с клиническим ответом на лекарственную терапию следует убедиться в заживлении СО при помощи эндоскопии или при исследовании фекального кальпротектина приблизительно через 3-6 месяцев после начала лечения» [54].
При переходе с индукционной на поддерживающую дозу месалазина мы также рекомендуем (рис. 4):
- после индукционного курса лечения месалазином или ГКС выполнение ректоромано- или сигмоскопии для констатации эндоскопической ремиссии;
- при отсутствии эндоскопической ремиссии индукционная доза месалазина не снижается;
- повторная ректоскопия выполняется через 8 недель;
- индукционная доза месалазина сохраняется вплоть до достижения эндоскопической ремиссии, после чего доза снижается до поддерживающей [55].
Пациентам с язвенным проктитом и проктосигмоидитом противорецидивное лечение может проводиться только ректальными формами препаратов месалазина. Доза месалазина колеблется от 1 г ежедневно до 1 г трижды в неделю [23].
Во время ремиссии дополнительное назначение ректального месалазина всего лишь 2 раза в неделю по выходным существенно превосходит по эффективности пероральную монотерапию, приводя к снижению частоты рецидивов более чем в 4 раза (с 77% до 18%) [56]. Следует отметить и доступность такого подхода для пациентов. Так, одного баллона ректальной пены при применении в режиме терапии выходного дня (1 г 2 раза в неделю) хватит на 2 месяца.
В большинстве случаев при легкой и среднетяжелой формах ЯК с помощью грамотной комбинации пероральных и ректальных форм препаратов месалазина и ректальных форм ГКС удается добиться клинической и эндоскопической ремиссии и длительно ее поддерживать. У этой категории пациентов, как правило, необходимости в назначении системных ГКС, иммуносупрессоров и генно-инженерных биологических препаратов не возникает.
КОНФЛИКТ ИНТЕРЕСОВ. Автор статьи подтвердил отсутствие конфликта интересов, о котором необходимо сообщить.
CONFLICT OF INTERESTS. Not declared.
Литература/References
- Ng S. C., Shi H. Y., Hamidi N., et al. Worldwide incidence and prevalence of inflammatory bowel disease in the 21st century: a systematic review of population-based studies // Lancet. 2018; 390: 2769-2778. [PubMed: 29050646.]
- Белоусова Е. А., Абдулганиева Д. И., Алексеева О. П., Алексеенко С. А., Барановский А. Ю., Валуйских Е. Ю., Головенко А. О., Головенко О. В., Жигалова Т. Н., Князев О. В., Куляпин А. В., Лахин А. В., Ливзан М. А., Лубянская Т. Г., Николаева Н. Н., Никитина Н. В., Никулина И. В., Осипенко М. Ф., Павленко В. В., Парфенов А. И., Рогачиков Ю. Е., Светлова И. О., Ткачев А. В., Ткаченко Е. И., Халиф И. Л., Чашкова Е. Ю., Щукина О. Б., Язенок Н. С., Яковлев А. А. Социально-демографическая характеристика, особенности течения и варианты лечения воспалительных заболеваний кишечника в России. Результаты двух многоцентровых исследований // Альманах клинической медицины. 2018. № 5. [Belousova E. A., Abdulganieva D. I., Alekseeva O. P., Alekseenko S. A., Baranovsky A. Yu., Valuiskikh E. Yu., Golovenko A. O., Golovenko O. V., Zhigalova T. N., Knyazev O. V., Kulyapin A.V., Lakhin A.V., Livzan M. A., Lubyanskaya T. G., Nikolaeva N. N., Nikitina N. V., Nikulina I. V., Osipenko M. F., Pavlenko V. V., Parfenov A. I., Rogachikov Yu. E., Svetlova I. O., Tkachev A. V., Tkachenko E. I., Khalif I. L., Chashkova E. Yu., Shchukina O. B., Yazenok N. S., Yakovlev A. A. Socio-demographic characteristics, features of the course and treatment options for inflammatory bowel diseases in Russia. Results of two multicenter studies // Almanakh klinicheskoi meditsiny. 2018. № 5.]
- Burisch J., Pedersen N., Cukovic-Cavka S., et al. Initial disease course and treatment in an inflammatory bowel disease inception cohort in Europe: the ECCO-EpiCom cohort // Inflamm Bowel Dis. 2014; 20: 36-46. [PubMed: 24252978].
- Fumery M., Singh S., Dulai P. S., et al. Natural History of Adult Ulcerative Colitis in Population-based Cohorts: A Systematic Review // Clin Gastroenterol Hepatol. 2017.
- Ng S. C., Zeng Z., Niewiadomski O., et al. Early Course of Inflammatory Bowel Disease in a Population-Based Inception Cohort Study From 8 Countries in Asia and Australia // Gastroenterology. 2016; 150: 86-95 e3; quiz e13-4. [PubMed: 26385074.]
- Niewiadomski O., Studd C., Hair C., et al. Prospective population-based cohort of inflammatory bowel disease in the biologics era: Disease course and predictors of severity // J Gastroenterol Hepatol. 2015; 30: 1346-53. [PubMed: 25867770.]
- Samuel S., Ingle S. B., Dhillon S., et al. Cumulative incidence and risk factors for hospitalization and surgery in a population-based cohort of ulcerative colitis. Inflamm Bowel Dis 2013; 19: 1858-66. [PubMed: 23660997]
- Solberg I. C., Lygren I., Jahnsen J., et al. Clinical course during the first 10 years of ulcerative colitis: results from a population-based inception cohort (IBSEN Study) // Scand J Gastroenterol. 2009; 44: 431-440. [PubMed: 19101844].
- Vegh Z., Burisch J., Pedersen N., et al. Incidence and initial disease course of inflammatory bowel diseases in 2011 in Europe and Australia: results of the 2011 ECCO-EpiCom inception cohort // J Crohns Colitis. 2015; 9: 156-163. [PubMed: 25518058].
- Frolkis A. D., Dykeman J., Negron M. E., et al. Risk of surgery for inflammatory bowel diseases has decreased over time: a systematic review and meta-analysis of population-based studies // Gastroenterology 2013; 145: 996-1006. [PubMed: 23896172.]
- Головенко А. О., Халиф И. Л., Головенко О. В., Веселов В. В. Предикторы эффективности инфликсимаба у больных с тяжелой атакой язвенного колита // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2013; 5 (23): 65-73. [Golovenko A. O., Khalif I. L., Golovenko O. V., Veselov V. V. Predictors of infliximab efficacy in patients with severe attacks of ulcerative colitis // Rossiyskiy zhurnal gastroenterologii, gepatologii, koloproktologii. 2013; 5 (23): 65-73.]
- Dassopoulos T., Cohen R. D., Scherl E. J., et al. Ulcerative Colitis Care Pathway // Gastroenterology. 2015; 149: 238-45. [PubMed: 26025078.]
- Dias C. C., Rodrigues P. P., da Costa-Pereira A., et al. Clinical predictors of colectomy in patients with ulcerative colitis: systematic review and meta-analysis of cohort studies // J Crohns Colitis.
- Khan N. H., Almukhtar R. M., Cole E. B., et al. Early corticosteroids requirement after the diagnosis of ulcerative colitis diagnosis can predict a more severe long-term course of the disease – a nationwide study of 1035 patients // Aliment Pharmacol Ther. 2014; 40: 374-381. [PubMed: 24961751.]
- Picco M. F., Krishna M., Cangemi J. R., et al. Oral mesalamine and clinical remission are associated with a decrease in the extent of long-standing ulcerative colitis // Inflamm Bowel Dis. 2006; 12: 537-442. [PubMed: 16804389.]
- Sahami S., Konte K., Buskens C. J., et al. Risk factors for proximal disease extension and colectomy in left-sided ulcerative colitis // United European Gastroenterol J. 2017; 5: 554-562.
- Torres J., Billioud V., Sachar D. B., et al. Ulcerative colitis as a progressive disease: the forgotten evidence // InflammBowel Dis. 2012; 18: 1356-1363. [PubMed: 22162423].
- Gisbert J. P., Gomollon F., Hinojosa J., et al. Adherence of gastroenterologists to European Crohn’s and Colitis Organisation consensus on ulcerative colitis: a real-life survey in Spain // J Crohns Colitis. 2010; 4: 567-574. [PubMed: 21122561.]
- Singh S., Feuerstein J. D., Binion D. G., Tremaine W. J. AGA Technical Review on the Management of Mild-to-Moderate Ulcerative Colitis // Gastroenterology. 2019; 156 (3): 769-808. DOI: 10.1053/j.gastro.2018.12.008. Epub 2018 Dec 18. Erratum in: Gastroenterology. 2019; 157 (3): 903. PMID: 30576642; PMCID: PMC6858923.
- Feuerstein J. D., Isaacs K. L., Schneider Y., Siddique S. M., Falck-Ytter Y., Singh S; AGA Institute Clinical Guidelines Committee. AGA Clinical Practice Guidelines on the Management of Moderate to Severe Ulcerative Colitis // Gastroenterology. 2020; 158 (5): 1450-1461. DOI: 10.1053/j.gastro.2020.01.006. Epub 2020 Jan 13. PMID: 31945371; PMCID: PMC7175923.
- Lamb C. A., Kennedy N. A., Raine T., Hendy P. A., Smith P. J., Limdi J. K., Hayee B., Lomer M. C. E., Parkes G. C., Selinger C., Barrett K. J., Davies R. J., Bennett C., Gittens S., Dunlop M. G., Faiz O., Fraser A., Garrick V., Johnston P. D., Parkes M., Sanderson J., Terry H; IBD guidelines eDelphi consensus group, Gaya D. R., Iqbal T. H., Taylor S. A., Smith M., Brookes M., Hansen R., Hawthorne A. B. British Society of Gastroenterology consensus guidelines on the management of inflammatory bowel disease in adults // Gut. 2019; 68 (Suppl 3): s1-s106. DOI: 10.1136/gutjnl-2019-318484. Epub 2019 Sep 27. Erratum in: Gut. 2021; 70 (4): 1. PMID: 31562236; PMCID: PMC6872448.
- Peyrin-Biroulet L., Sandborn W., Sands B. E., Reinisch W., Bemelman W., Bryant R. V., D’Haens G., Dotan I., Dubinsky M., Feagan B., et al. Selecting Therapeutic Targets in Inflammatory Bowel Disease (STRIDE): Determining Therapeutic Goals for Treat-to-Target // Am. J. Gastroenterol. 2015, 110, 1324-1338. [CrossRef] [PubMed].
- Raine T., Bonovas S., Burisch J., Kucharzik T., Adamina M., Annese V., Bachmann O., Bettenworth D., Chaparro M., Czuber-Dochan W., et al. ECCO Guidelines on Therapeutics in Ulcerative Colitis: Medical Treatment // J. Crohn’s Colitis. 2022; 16: 2-17. [CrossRef] [PubMed].
- Kim K. O. Endoscopic activity in inflammatory bowel disease: clinical significance and application in practice // Clin Endosc. 2022; 55 (4): 480-488. DOI: 10.5946/ce.2022.108. Epub 2022 Jul 28. PMID: 35898147; PMCID: PMC9329646.
- Laharie D., Filippi J., Roblin X., et al. Impact of mucosal healing on long-term outcomes in ulcerative colitis treated with infliximab: A multicenter experience // Aliment Pharmacol Ther. 2013. DOI: 10.1111/apt.12289.
- Leung C. M., Tang W., Kyaw M., et al. Endoscopic and histological mucosal healing in ulcerative colitis in the first year of diagnosis: results from a population-based inception cohort from six countries in Asia // J Crohns Colitis 2017; 11: 1440-1448.
- Theede K., Kiszka-Kanowitz M., Nordgaard-Lassen I., Mertz Nielsen A. The impact of endoscopic inflammation and mucosal healing on health-related quality of life in ulcerative colitis patients // J Crohns Colitis. 2015; 9: 625-632.
- Walsh A., Palmer R., Travis S. Mucosal healing as a target of therapy for colonic inflammatory bowel disease and methods to score disease activity // Gastrointest Endosc Clin N Am. 2014; 24 (3): 367-378. DOI: 10.1016/j.giec.2014.03.005. Epub 2014 May 6. PMID: 24975528.
- Белоусова Е. А., Никитина Н. В., Цодикова О. М. Лечение язвенного колита легкого и среднетяжелого течения // Фарматека. 2013; 2: 42-46. [Belousova Ye. A., Nikitina N. V., Tsodikova O. M. Treatment of mild and moderate ulcerative colitis // Farmateka. 2013; 2: 42-46.]
- Клинические рекомендации – Язвенный колит – 2020 (22.07.2020). Утверждены Минздравом РФ. https://www.cr.minzdrav.gov.ru. [Clinical guidelines – Ulcerative colitis – 2020 (22.07.2020). Approved by the Ministry of Health of the Russian Federation. https://www.cr.minzdrav.gov.ru]
- Халиф И. Л. Лечебная тактика при язвенном колите // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2006; 3 (16): 58-62. [Khalif I. L. Therapeutic tactics in ulcerative colitis // Rossiyskiy zhurnal gastroenterologii, gepatologii, koloproktologii. 2006; 3 (16): 58-62.]
- Harris M. S., Lichtenstein G. R. Review article: delivery and efficacy of topical 5-aminosalicylic acid (mesalazine) therapy in the treatment of ulcerative colitis // Aliment Pharmacol Ther. 2011; 33: 996-1009.
- Ford A. C., Achkar J. P., Khan K. J., et al. Efficacy of 5-aminosalicylates in ulcerative colitis: systematic review and meta-analysis // Am J Gastroenterol. 2011; 106: 601-616.
- Iacucci M., de Silva S., Ghosh S. Mesalazine in inflammatory bowel disease: A trendy topic once again? // Can. J. Gastroenterol. 2010; 24: 127-133. [CrossRef].
- Das K. M., Dubin R. Clinical pharmacokinetics of sulphasalazine // Clin Pharmacokinet. 1976; 1 (6): 406-425.
- Регистр лекарственных средств России. Энциклопедия лекарств. 28-й вып. М.: РЛС-МЕДИА, 2020. 1368 с. [Register of medicines of Russia. Encyclopedia of drugs. 28-y vyp. M.: RLS-MEDIA, 2020. Р. 1368.]
- Kruis W.., Kiudelis G., Racz I. Once daily versus three times daily mesalazine granules in active ulcerative colitis: a double-blind, double-dummy, randomised, noninferiority trial // Gut. 2009; 58 (2): 233-240.
- Leifeld L., Pfutzer R., Morgenstern J., Gibson P. R., Marakhouski Y., Greinwald R., Mueller R., Kruis W. Mesalazine granules are superior to Eudragit-L-coated mesalazine tablets for induction of remission in distal ulcerative colitis – a pooled analysis // Aliment Pharmacol Ther. 2011; 34 (9): 1115-1122.
- Yuichiro O., Kan U., Hirotaka K., Eri M., Moe Y., Yuma A., Toshimune W., Sachie K., Sizuka S., Yoshihiro M., Zensho I., Toshifumi O., Shigeo K., Masayuki S. The insoluble excretion of multi-matrix system mesalazine preparations in patients with ulcerative colitis // BMC Gastroenterol. 2022; 22 (1): 390. DOI: 10.1186/s12876-022-02474-9. PMID: 35982420; PMCID: PMC9389853.
- Gross V., Bunganic I., Belousova E. A., et al. 3g mesalazine granules are superior to 9mg budesonide for achieving remission in active ulcerative colitis: a double-blind, double-dummy, randomised trial // J Crohns Colitis. 2011; 5: 129-138.
- Pokrotnieks J, Marlicz K, Paradowski L, Margus B, Zaborowski P, Greinwald R. Efficacy and tolerability of mesalazine foam enema (Salofalk foam) for distal ulcerative colitis: a double-blind, randomized, placebo-controlled study. Aliment Pharmacol Ther. 2000 Sep;14(9):1191-8. doi: 10.1046/j.1365-2036.2000.00784.x. PMID: 10971236.
- Ректальная терапия воспалительных заболеваний кишечника / П. Фрай, Г. Роглер, А. О. Головенко, С. И. Ситкин. М.: Прима Принт, 2017. 28 с.: ил. ISBN 978-5-9500690-0-0. [Rectal therapy of inflammatory bowel diseases / P. Fray, G. Rogler, A. O. Golovenko, S. I. Sitkin. M.: Prima Print, 2017. 28 s.: il. ISBN 978-5-9500690-0-0.]
- Frühmorgen P., Demling L. On the efficacy of ready-made-up commercially available salicylazosulphapyridine enemas in the treatment of proctitis, proctosigmoiditis and ulcerative colitis involving rectum, sigmoid and descending colon // Hepatogastroenterology. 1980; 27: 473-476.
- Marteau P, Probert C. S., Lindgren S., et al. Combined oral and enema treatment with Pentasa (mesalazine) is superior to oral therapy alone in patients with extensive mild/moderate active ulcerative colitis: A randomised, double blind, placebo controlled study // Gut. 2005. DOI: 10.1136/ gut.2004.060103.
- Safdi M., DeMicco M., Sninsky C., et al. A double-blind comparison of oral versus rectal mesalamine versus combination therapy in the treatment of distal ulcerative colitis // Am J Gastroenterol. 1997. DOI: 10.1016/0016-5085 (95)27940-7.
- Vecchi M., Meucci G., Gionchetti P., et al. Oral versus combination mesalazine therapy in active ulcerative colitis: a double-blind, doubledummy, randomized multicentre study // Aliment Pharmacol Ther. 2001; 15: 251-256.
- Bar-Meir et al. Budesonide foam vs. hydrocortisone acetate foam in the treatment of active ulcerative proctosigmoiditis // Dis Colon Rectum. 2003; 46: 929-936.
- Hanauer S. B., Robinson M., Pruitt R., et al. Budesonide enema for the treatment of active, distal ulcerative colitis and proctitis: A dose-ranging study // Gastroenterology. 1998. DOI: 10.1016/S0016-5085 (98)70131-3.
- Sandborn W. J., Bosworth B., Zakko S., et al. Budesonide foam induces remission in patients with mild to moderate ulcerative proctitis and ulcerative proctosigmoiditis // Gastroenterology. 2015. DOI: 10.1053/j.gastro.2015.01.037.
- Mulder C. J., Fockens P., Meijer J. W., van der Heide H., Wiltink E. H., Tytgat G. N. Beclomethasone dipropionate (3 mg) versus 5-aminosalicylic acid (2 g) versus the combination of both (3 mg/2 g) as retention enemas in active ulcerative proctitis // Eur J Gastroenterol Hepatol. 1996; 8: 549-553.
- Qiu X., Ma J., Wang K., Zhang H. Chemopreventive effects of 5-aminosalicylic acid on inflammatory bowel disease-associated colorectal cancer and dysplasia: A systematic review with meta-analysis // Oncotarget. 2017. DOI: 10.18632/oncotarget.13715.
- Chibbar R., Moss A. C. Mesalamine in the Initial Therapy of Ulcerative Colitis // Gastroenterol Clin North Am. 2020 Dec; 49 (4).
- Lichtenstein G. R., Gordon G. L., Zakko S., Murthy U., Sedghi S., Pruitt R., Barrett A. C., Bortey E., Paterson C., Forbes W. P. Long-Term Benefi t of Mesalamine Granules for Patients Who Achieved Corticosteroid-Induced Ulcerative Colitis Remission // Dig Dis Sci. 2016; 61 (1): 221-229. DOI: 10.1007/s10620-015-3866-7.
- Maaser C., Sturm A., Vavricka S. R., et al. ECCO-ESGAR Guideline for Diagnostic Assessment in IBD Part 1: Initial diagnosis, monitoring of known IBD, detection of complications // J Crohns Colitis. 2019; 13 (2): 144-164. DOI: 10.1093/ecco-jcc/jjy113.
- Головенко О. В., Хомерики С. Г., Иванова Е. В. и др. Воспалительные заболевания кишечника: клинические, эндоскопические, морфологические аспекты диагностики, принципы современной терапии. 2-е издание, доп. и перераб. М.: Прима Принт, 2022. 258 с.: ил. ISBN 978-5-6046641-3-1. [Golovenko O. V., Khomeriki S. G., Ivanova Ye. V. i dr. Inflammatory bowel diseases: clinical, endoscopic, morphological aspects of diagnosis, principles of modern therapy. 2-ye izdaniye, dop. i pererab. M.: Prima Print, 2022. p 258.: il. ISBN 978-5-6046641-3-1.]
- Yokoyama H., Takagi S., Kuriyama S., Takahashi S., Takahashi H., Iwabuchi M., Takahashi S., Kinouchi Y., Hiwatashi N., Tsuji I., Shimosegawa T. Effect of weekend 5-aminosalicylic acid (mesalazine) enema as maintenance therapy for ulcerative colitis: results from a randomized controlled study // Inflamm Bowel Dis. 2007; 13 (9): 1115-1120.
- Mahon SM. Colorectal cancer screening: Using evidence-based guidelines. Nurse Pract. 2017 Oct 18;42(10):18-26. DOI: 10.1097/01.NPR.0000524663.78727.4e. PMID: 28926493.
О. В. Головенко, ORCID: 0000-0002-7439-0983, drgolovenko@yandex.ru
Федеральное государственное бюджетное образовательное учреждение дополнительного профессионального образования Российская медицинская академия непрерывного профессионального образования Министерства здравоохранения Российской Федерации; 125993, Россия, Москва, ул. Баррикадная, 2/1, стр. 1
Сведения об авторе:
Головенко Олег Владимирович, д.м.н., профессор кафедры гастроэнтерологии Федерального государственного бюджетного образовательного учреждения дополнительного профессионального образования Российской медицинской академии непрерывного профессионального образования Министерства здравоохранения Российской Федерации, 125993, Россия, Москва, ул. Баррикадная, д. 2/1, стр. 1; drgolovenko@yandex.ru
Information about the author:
Oleg V. Golovenko, Dr. of Sci. (Med.), Professor of the Department of gastroenterology at the Federal State Budgetary Educational Institution of Additional Professional Education Russian Medical Academy of Continuing Professional Education of the Ministry of Health of the Russian Federation; 2/1, p. 1 Barrikadnaya str., Moscow, 125993, Russia; drgolovenko@yandex.ru
Современные принципы консервативного лечения легкой и среднетяжелой форм язвенного колита/ О. В. Головенко
Для цитирования: Головенко О. В. Современные принципы консервативного лечения легкой и среднетяжелой форм язвенного колита // Лечащий Врач. 2022; 11 (25): 82-89. DOI: 10.51793/OS.2022.25.11.014
Теги: кишечник, хроническое воспаление, осложнения