Дата публикации 18 июля 2023Обновлено 18 июля 2023
Определение болезни. Причины заболевания
Гидраденит (Hidradenitis suppurativa) — это хроническое кожное заболевание, при котором формируются болезненные воспалительные инфильтраты — скопления клеток, в данном случае лейкоцитов, которые проявляются уплотнением тканей. Со временем в инфильтратах скапливается гной. Он прорывается наружу с образованием свищевых ходов, которые потом рубцуются. Болезнь склонна к рецидиву [1]. Для обозначения гнойного гидраденита также используют термины «инверсное» и «апокриновое акне».
Впервые симптомы гидраденита описал французский анатом и хирург Альфред Вельпо в 1839 году [2]. Однако теория о том, что патология связана с потовыми железами появилась позже: её высказал французский хирург Аристид Вернейль в 1854 году. Он же и предложил название болезни: от греческого hydor — вода и aden – железа, а окончание -it указывает на воспаление [3].
В простонародье гидраденит называют сучьем выменем, так как воспалительные очаги похожи на соски собак.
Распространённость гидраденита
Распространённость патологии, по разным данным, составляет от 0,4 до 4 %. В среднем ею болеет около 1 % населения во всём мире, т. е. каждый сотый человек в течение жизни сталкивается с этим заболеванием [4][5]. При этом женщины болеют в 3 раза чаще, чем мужчины [14].
У представителей негроидной расы обострения гидраденита протекают почти в 3 раза тяжелее, чем у людей европеоидной расы [17]. Распространённость заболевания в первой группе также выше: 1,3 % против 0,75 % [18]. Однако это может быть связано не с расой как таковой, а с большим процентом сопутствующих заболеваний (например, ожирением и диабетом), а также более низким уровнем жизни [19].
Первые симптомы обычно появляются в период полового созревания, но наиболее интенсивно болезнь проявляет себя у пациентов 20–40 лет [6].
Причины развития гидраденита
Ранее считалось, что патология появляется из-за нарушений в работе потовых желёз. Однако современные исследования показывают, что чаще гидраденит связан с патологией волосяного фолликула и является частью синдрома фолликулярной окклюзии — группы заболеваний со сходным механизмом развития (закупоркой устья фолликула), куда входят:
- конглобатное акне — «поверхностный» вариант гидраденита, при котором не формируются свищевые ходы, инфильтраты образуются на открытых участках тела [47];
- абсцедирующий и подрывающий перифолликулит головы — воспалительные очаги развиваются на голове [48];
- пилонидальная киста — воспаление канала в окружности межъягодичной складки, копчика или крестца [7].
Помимо синдрома фолликулярной окклюзии, гидраденит может развиваться вместе с другими болезнями:
- PASH синдром — сочетание гангренозной пиодермии, акне и гнойного гидраденита [8];
- PAPASH синдром — сочетание гнойного артрита, гангренозной пиодермии, акне и гнойного гидраденита [9];
- PASS синдром — сочетание гангренозной пиодермии, вульгарного акне, гнойного гидраденита и анкилозирующего спондилита [10].
В отличие от синдрома фолликулярной окклюзии вышеперечисленные болезни развиваются из-за гиперреактивности иммунной системы. Причиной становится не поражение волосяных фолликулов, а попадание в них каких-либо микроорганизмов. Даже незначительное их количество вызывает «неадекватную» реакцию иммунитета. В этом случае гидраденит относят к аутовоспалительным расстройствам [11].
Несмотря на вышеперечисленные причины, дисфункция потовых желёз всё-таки может играть определённую роль в развитии патологии. Например, нехватка определённых антибактериальных веществ в секрете потовых желёз способствует росту микроорганизмов и провоцирует развитие воспаления [12].
Болезнь может иметь наследственный характер: у 1/3 пациентов гидраденитом также болеет кто-то из родственников, при этом болезнь часто рецидивирует, т. е. появляется снова.
В других случаях патология развивается вследствие провоцирующего фактора, например в результате микротравмы волосяных фолликулов при бритье или при ношении тесной одежды [31]. После лечения болезнь, как правило, не возвращается [13].
К другим факторам риска относятся:
- Женский пол — причиной этому может быть разница в гормональном фоне, так как патология часто обостряется перед менструацией и регрессирует с наступлением менопаузы [15][16].
- Курение — это наиболее серьёзный фактор риска, который увеличивает частоту рецидивов и усугубляет тяжесть течения заболевания. 90 % пациентов с гидраденитом — курильщики [21]. Исследователи предполагают, что токсичные вещества (например, никотин, бензапирен и мышьяк) мешают отделяться отмершим клеткам, тем самым закупоривая волосяные фолликулы [22]. Также начинают выделяться провоспалительные медиаторы, меняется состав секрета потовых желёз, после чего лейкоциты мигрируют к волосяному фолликулу [23][24][25][26]. Всё это провоцирует развитие воспаления. Электронные сигареты и вейпы также могут отрицательно влиять на течение заболевания, так как в их парах содержится никотин.
- Избыточная масса тела и ожирение — в среднем индекс массы тела (ИМТ) пациентов с гнойным гидраденитом на 3 единицы больше, чем у здоровых людей [27]. Трение кожи на складках травмирует волосяные фолликулы, а скопление пота приводит к росту бактерий [28].
- Неправильное питание — сладости, жирная пища, молочные продукты и мучные изделия провоцируют обострения гидраденита [29]. Предполагается, что жиры и углеводы стимулируют синтез андрогенов и инсулина, которые меняют состав секрета потовых желёз [30].
- Повышенное потоотделение (гипергидроз) — усугубляет течение заболевания за счёт роста бактерий [32].
- Антиперспиранты — они блокируют потоотделение с помощью закупорки пор [33].
- Механическая эпиляция — она, как и бритьё, травмирует волосяные фолликулы, способствуя развитию болезни [34].
- Определённые профессии — постоянная работа руками или частая ходьба сопровождается трением кожи в подмышечных и паховых областях [35].
Помимо вышеперечисленных факторов гидраденит может быть связан с избытком андрогенных гормонов, заболеваниями щитовидной железы (гипо- и гипертиреозом), синдромом поликистозных яичников, сахарным диабетом 2-го типа, метаболическим синдромом, а также с хроническими воспалительными заболеваниями кишечника и суставов [30][36][37][38][39][40][41].
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы гидраденита
Обострение гидраденита начинается с появления воспалительного инфильтрата размером до 2 см. Уплотнения развиваются глубоко в коже, на стыке дермы и подкожно-жировой клетчатки, где располагаются апокриновые потовые железы, обычно в подмышках и паху. За 12–48 часов до появления инфильтрата может появиться жжение, зуд, прострелы, боль или ощущение тепла. При больших или множественных очагах повышается температура [42].
Затем кожа в области инфильтрата краснеет и отекает, а прощупывание начинает сопровождаться резкой болью. Уплотнение становится горячим на ощупь. На этапе нагноения центральная часть очага размягчается из-за скопления жидкости. Также могут увеличиться близлежащие лимфатические узлы [1].
Если пациент сам вскрывает инфильтрат, образуется свищевой ход, из которого в течение 1–2 месяцев выделяется гной. Когда инфекционный очаг расположен глубоко, гной может сохраняться до нескольких лет. В дальнейшем свищевой ход заживает и формируется щелевидный рубец.
К другим проявлением гидраденита относят открытые комедоны (чёрные угри) — закупоренные волосяные фолликулы. Чёрные точки в данном случае являются ничем иным, как окисленными «пробками» из слущенных клеток в выходном отверстии фолликула.
Помимо подмышек и паха гидраденит может развиться на внутренней поверхности бёдер (ближе к паху), в промежности, на лобке, вокруг анального отверстия, в складке под грудью и в межгрудной складке, в области сосков и ареол, а также в области больших половых губ, на мошонке и крайней плоти.
Патогенез гидраденита
Чтобы лучше понять механизм развития гидраденита, необходимо обратить внимание на строение волосяных фолликулов и потовых желёз.
У волосяного фолликула есть 3 отдела: воронка (выходное отверстие), перешеек и нижний отдел. В перешеек открываются протоки сальных и потовых желёз, а нижний отдел содержит волосяную луковицу [44].
Выделяют 2 основных типа волосяных фолликулов: пушковые и терминальные [45]. К терминальным волосам относят все явно заметные волосы: на волосистой части головы, лице, груди, животе, спине, ногах, руках, в паху и подмышках. К ним также относятся брови и ресницы. Незаметные с первого взгляда пушковые волосы покрывают всю оставшуюся часть тела, кроме ладоней и подошв.
Также существует 2 типа потовых желёз: апокриновые и эккриновые [46]. Если клетка выделяет секрет через специальные каналы на своей поверхности и при этом не разрушается, это эккриновая железа. При разрушении клетки железу называют апокриновой.
Апокриновые железы связаны с волосяными фолликулами. Бóльшая их часть располагается в подмышках и паху, однако определённое количество также находится и в других частях тела. Их секрет достаточно густой и неприятно пахнет из-за ферментации нормальной микрофлоры кожи.
Потовые железы эккринового типа не связаны с волосяными фолликулами и выделяют более жидкий секрет. Они относительно равномерно распределены по всей поверхности тела, однако больше всего их на ладонях и подошвах. Если эти железы работают неправильно, повышается потоотделение.
В норме клетки волосяного фолликула постоянно обновляются: старые клетки засыхают и «выпадают» через выходное отверстие, а на их место приходят новые. Но если отмершие клетки не могут «отпадать» и скапливаются в выходном отверстии фолликула, образуется своеобразная «пробка». С поверхности кожи через микроскопические ходы в неё проникают бактерии и начинают быстро размножаться. Тогда иммунная система запускает инфекционный воспалительный процесс, после чего формируется глубоко расположенный инфильтрат и начинается нагноение.
Мифы о гидрадените
Вокруг патологии образовалось много домыслов, которые не соответствуют действительности:
- «гидраденит — это инфекционное заболевание» — бактериальная инфекция может быть только следствием болезни, истинной причиной её развития является то, что организм «неадекватно» реагирует на бактерии или не может контролировать их рост;
- «гидраденит связан с нечистоплотностью» — нечистоплотность может спровоцировать обострение за счёт увеличения количества бактерий, однако причины патологии кроются в индивидуальных особенностях организма;
- «гидраденит заразный» — бактерии, которые провоцируют обострения гидраденита входят в нормальную микрофлору кожи, т. е. они есть у всех людей, и обычно не вызывают воспаления, поэтому заразиться гидраденитом нельзя.
Классификация и стадии развития гидраденита
В зависимости от выраженности симптомов и количества перенесённых рецидивов выделяют 3 стадии развития заболевания:
- I стадия — появляются единичные изолированные узлы с возможным их нагноением, рубцов и свищевых ходов нет;
- II стадия — наступает после многочисленных обострений и характеризуется наличием множественных рубцов и единичных изолированных свищевых ходов;
- III стадия — образуется большое количество сливных свищевых ходов и рубцов, деформирующих кожу [49].
Также существует разделение на фенотипические группы (по совокупность признаков). Такая классификация учитывает не только степень выраженности симптомов, но также месторасположение очагов и отдельные проявления, которые наблюдаются не во всех случаях гидраденита:
- обычный тип — классический вариант гидраденита;
- гидраденит по типу фрикционного фурункула — классический вариант болезни, при котором периодически появляются очаги в местах повышенного трения, например в нижней части живота, на задней поверхность бёдер и ягодицах;
- гидраденит по типу рубцующего фолликулита — помимо характерных проявлений, наблюдается множество мелких поверхностных воспалительных очагов в зонах повышенного трения с формирование рубцов при заживлении;
- конглобатный гидраденит — характеризуется сочетанием типичных проявлений гидраденита и конглобатного (шаровидного) акне на лице и спине без образования свищевых ходов и нагноения;
- эктопический тип — признаки конглобатного акне сопровождаются выделением гноя;
- синдромальный тип — гидраденит сочетается с другими воспалительными заболеваниями (PASH, PAPASH и PASS синдромы) [50].
Осложнения гидраденита
При неблагоприятном развитии болезни может развиться:
- Келоидные рубцы. Они развиваются в результате неконтролируемого роста рубцовой ткани, которая прорастает в здоровые ткани и вызывает боль, жжение и зуд. Некоторые пациенты склонны к формированию таких рубцов, поэтому их основной проблемой становятся не обострения гидраденита, а образующийся впоследствии келоидный рубец [51]. Они также снижают растяжимость кожи, поэтому если рубец появится на сгибательных и разгибательных поверхностях, он может сковывать движения сустава [52].
- Рак кожи. Долгое и тяжёлое течение гидраденита с многократными рецидивами и длительно незаживающими гнойными свищами могут вызвать рак кожи в области хронического воспаления [53].
- Хронический болевой синдром. Иногда длительная непроходящая боль может быть главной жалобой пациента, требующей специальной тактики лечения [54].
- Амилоидоз. В ходе воспалительного процесса печень выделяет белок — сывороточный амилоидный протеин А. Если воспаление долгое, этот белок накапливается в различных органах и тканях организма, мешая им работать, т. е. амилоидоз развивается при длительном и тяжёлом течении гидраденита [55]. Это состояние может сопровождаться хронической почечной недостаточностью, циррозом печени, аритмией, нарушением работы желудочно-кишечного тракта и т. д.
- Анемия. Ттак как железо помогает бактериям расти, при долгом воспалении организм «консервирует» его запасы. Соответственно, концентрация гемоглобина (белка, переносящего кислород) в крови снижается и развивается анемия. Обычно она носит лёгкую степень тяжести и никак не проявляется, однако в тяжёлых случаях пациент может испытывать общую слабость, сонливость, лёгкую утомляемость, головокружение и эпизоды потери сознания [56].
- Стигматизация и социальная изоляция. Многие считают, что гидраденит это «болезнь нечистоплотных людей», поэтому некоторые пациенты испытывают значительный психологический дискомфорт. Неприятный запах, сопровождающий обострения, и необходимость часто открывать больничные листы приводят к трудностям с трудоустройством. Больным стыдно показать своё тело, например выйти на пляж, пойти в спортзал, душ, бассейн и т. д. В итоге это приводит к социальной изоляции [57].
Также у пациентов с гидраденитом может развиться флегмона подкожно-жировой клетчатки и сепсис, но пока врачи не сообщали о пациентах с такими осложнениями. Чисто теоретически, если инфильтрат расположен слишком глубоко, гной может прорваться в подкожно-жировую клетчатку, в которой ещё нет защитных клеток иммунитета. В таком случае гнойно-воспалительный процесс развивается «по нарастающей», распространяясь по рыхлой клетчатке как по «губке», разрушая здоровые ткани. В ответ на этот процесс иммунитет выделяет огромное количество веществ, стимулирующих воспалительный процесс: они всасываются в кровоток и оказывают системное воздействие, так что «воспаляется» весь организм — начинается сепсис. В тяжёлых случаях сепсис может закончиться летальным исходом. Однако врачи пока не сообщали о пациентах с такими осложнениями.
Диагностика гидраденита
Обычно врач не испытывает трудностей при постановке диагноза, так как болезнь сопровождается характерными болезненными воспалительными инфильтратами кожи в подмышках и паху. Необходимость дообследования определяют индивидуально.
Лабораторная диагностика
Общий клинический анализ крови может выявить повышение уровня лейкоцитов (лейкоцитоз), С-реактивного белка и увеличение скорости оседания эритроцитов (СОЭ). Эти изменения указывают лишь на наличие и степень выраженности воспаления и обычно не влияют на тактику лечения.
Несмотря на вероятную роль гормонов в течении заболевания, анализы обычно не показывают никаких отклонений от нормы, однако в некоторых случаях они всё же есть, поэтому пациентов просят сдать кровь на ФСГ (фолликулостимулирующий гормон), ЛГ (лютеинизирующий гормон), тестостерон, эстроген и прогестерон [30].
Чтобы исключить сопутствующую патологию щитовидной железы, назначают анализ крови на ТТГ (тиреотропный гормон). Если его показатель выходит за пределы нормы, пациент также проверяет концентрацию сТ3 (свободного трийодтиронина) и сТ4 (свободного тироксина).
При подозрении на сахарный диабет и метаболический синдром анализируют липидный профиль: определяют уровень общего холестерина, липопротеинов низкой плотности (ЛПНП), липопротеинов высокой плотности (ЛПВП) и триглицеридов, а также уровень гликированного гемоглобина в крови.
Инструментальная диагностика
Чтобы исключить синдром поликистозных яичников у женщин, врач собирает данные гинекологического анамнеза: количество беременностей, родов, абортов, регулярность менструаций и т. д.). В дополнение к вышеуказанному анализу крови на половые гормоны им проводят УЗИ органов малого таза [58].
Также делают УЗИ мягких тканей, чтобы проверить наличие нагноений. Если гноя нет, есть шанс обойтись консервативными методами лечения, например антибиотикотерапией. Когда же УЗИ показывает признаки нагноения, проводят хирургическое лечение. В ходе операции дополнительно выполняют забор материала для бактериологического исследования (посева), чтобы определить возбудителя и его чувствительность к антибиотикам. Также посев берут при наличии свища.
Если при консервативном лечении свищ долго не заживает и на очаге постоянно появляются изъязвления, целесообразно выполнить биопсию, чтобы исключить рак кожи.
В исключительных случаях назначают МРТ мягких тканей, которая определяет глубину распространения и размещение свищевых ходов [59]. Обычно это исследование выполняют пациентам с длительным тяжёлым гидраденитом. По результатам исследования определяют объём операции.
Дифференциальная диагностика
Кроме гидраденита, похожую клиническую картину могут иметь конглобатное акне, фурункулы, нагноившаяся эпидермальная киста и пилонидальная киста (эпителиальный копчиковый ход).
Лечение гидраденита
Прежде чем начать лечение, врач должен объяснить пациенту, как и почему у него развилась болезнь, подчеркнуть, что гидраденит не является следствием какой-либо инфекции, не заразен и не связан с нечистоплотностью. Это не только прояснит ситуацию, но и поможет настроиться на позитивный лад. Последующая тактика лечения зависит от стадии заболевания.
Лечение гидраденита I стадии
На раннем этапе, когда ещё нет нагноений, применяют местную антибактериальную терапию: 1%-й клиндамициновый гель (Далацин), 2%-ю мазь или крем фузидовой кислоты (Фуцидин) [60][81].
Иногда в очаг поражения вводят топические глюкокортикостероиды (в частности, Триамцинолон). Они в течение 72 часов останавливают воспалительный процесс, но также имеют побочные эффекты: атрофию кожи в области инъекции, гипопигментацию (потерю пигмента) и образование «холодного» абсцесса — скопления гноя без активного воспаления [61].
В случае нагноения единственным методом лечения является хирургический: очаг вскрывают, очищают и выкачивают гной. Операцию проводят амбулаторно под местной инфильтрационной анестезией.
После вскрытия гидраденита берут посев и промывают рану растворами антисептиков. Чтобы края не склеивались и в ней не скапливался гной, устанавливают дренаж — марлевую турунду или резиновую полоску (обычно от перчатки). В течение нескольких следующих дней пациенту промывают рану, меняют дренажи и делают перевязки. Всё это происходит до тех пор, пока рана не очистится полностью. После этого на неё накладывают повязки с антибактериальной мазью и ждут полного заживления.
Лечение гидраденита II стадии
При наличии сразу нескольких воспалительных очагов и единичных свищевых ходов, помимо местного лечения, используют системную антибиотикотерапию. В первую очередь применяют антибиотики тетрациклинового ряда (например, Доксициклин), в более тяжёлых случаях — комбинацию Клиндамицина и Рифампицина. Возможно применение и других антибактериальных препаратов [53][62].
Как и при терапии акне, в лечении гидраденита могут помочь ретиноиды, например Ацитретин (Изотретиноин в этом случае неэффективен) [63]. Эти препараты замедляют разрастание кератоиноцитов и не дают им закупорить волосяной фолликул. Однако у них есть и побочные эффекты: сухость и шелушение кожи, ломкость ногтей, головная боль. Ретиноиды также влияют на развитие плода, поэтому до начала терапии женщинам необходимо выполнить тест на беременность, а также соблюдать двойную контрацепцию (барьерную и любую другую) за месяц, во время и в течение двух лет после курса лечения [64].
Так как обострения гидраденита могут быть связаны с изменениями гормонального фона, женщинам иногда назначают антиандрогенные препараты (Ципротерон, Спиронолактон, Финастерид) и пероральные контрацептивы [66].
В качестве дополнения используют Цинк, который препятствует миграции лейкоцитов, тем самым останавливая воспаление [65]. Также рекомендуют принимать витамины Д и B12 и Омега 3 [67].
Лечение гидраденита III стадии
Если вышеперечисленные методы не принесли результата, пациенту могут назначить препараты, которые подавляют гиперреактивность иммунной системы с помощью разных механизмов: Адалимумаб, Инфликсимаб, Этанерцепт, Устекинумаб или Анакинру [68][69][70][71][72]. Однако они дорого стоят, а также повышают риск развития вторичных инфекций, в частности — туберкулёза.
На этом этапе чаще всего прибегают к хирургическому лечению, в ходе которого удаляют необратимо изменённую кожу и подкожно-жировую клетчатку вместе со всеми свищевыми ходами, т. е. всю зону, в которой расположены апокриновые потовые железы, что исключает возможность рецидивов.
После иссечения поражённых тканей остаётся большая открытая рана. Существует два варианта дальнейшего развития событий: либо рана заживает самостоятельно с помощью так называемого вторичного натяжения, когда рана заполняется рубцовой тканью и затем зарастает, либо её закрывают с помощью пластики местными тканями, кожно-жировым лоскутом или свободным кожным трансплантатом.
Если рана заживает вторичным натяжением, за ней нужно долго ухаживать (примерно несколько месяцев). В дальнейшем из-за плохой растяжимости рубца могут появиться ограничения в движении сустава (дерматогенная контрактура). С другой стороны, при регулярных перевязках снижается риск развития инфекционных осложнений, поэтому такой метод считается надёжным. Чтобы ускорить заживление, рану закрывают свободным кожным трансплантатом.
Местные ткани или кожно-жировой лоскут, которыми прикрывают рану, хирург «выкраивает» из здоровой кожи пациента. Процесс заживления в таком случае составляет 2–3 недели. Этот метод исключает образование грубого рубца, поэтому риск развития дерматогенной контрактуры минимален. Однако существует вероятность нагноения раны. Чтобы этого избежать, пациенту необходимо тщательно подготовиться к операции, а сам гидраденит должен находиться на стадии ремиссии.
Среди минусов хирургического лечения выделяют болевой синдром, риски развития осложнений, необходимость соблюдать охранительный режим и делать регулярные перевязки до полного заживления ран.
Прогноз. Профилактика
Поскольку заболевание связано с индивидуальными особенностями организма, полного излечения достичь сложно. Однако если контролировать патологию, в этом нет необходимости, поэтому основными целями терапии гидраденита является уменьшение частоты и тяжести рецидивов, а также увеличение продолжительности ремиссий.
Большие надежды возлагают на генно-инженерную биологическую терапию (например, на препараты Адалимумаб, Инфликсимаб, Этанерцепт и т. д.). В крайних случаях делают операцию.
Профилактика гидраденита
Очень важно соблюдать меры профилактики развития рецидивов:
- отказаться от курения [73];
- нормализовать массу тела (однако нельзя слишком быстро сбрасывать лишний вес, так как в этом случае появляются избыточные складки кожи) [74];
- делать лазерную эпиляцию — периодические сеансы лазерной эпиляции предположительно подавляют активность клеток волосяных фолликулов [75];
- отказаться от антиперспирантов — использовать дезодаранты, так как они не закупоривают поры [33];
- носить удобную одежду — одежда из «дышащих» тканей с содержанием серебра и хорошей абсорбционной способностью (например, изготовленные по технологии Sanitized) позволяет снизить потоотделение и предотвратить размножение бактерий, также существует специальная одежда для людей с гидраденитом от фирмы HidraWear: футболки и трусы-боксеры с впитывающими прокладками на подмышках и в паху, или можно использовать отдельные впитывающие повязки [76];
- проходить ботулинотерапию — снижает интенсивность потоотделения [77];
- соблюдать средиземноморскую диету — в рацион должны входить фрукты, овощи, орехи, рыба, бобовые, цельнозерновые продукты и курица, лучше воздержаться от кисломолочных продуктов и тех, что содержат дрожжи (пива, кваса, свежей выпечки, кефира и винограда) [36][78][79][80].
Рекомендации:
— Рекомендуется изначальное назначение пероральных тетрациклинов, таких как доксициклин или лимециклин, в течение как минимум 12 недель, с рассмотрением перерывов в лечении для оценки необходимости в продолжении лечения и для снижения риска антимикробной резистентности.
— Пациентам, которые не реагируют на пероральные тетрациклины, рекомендуется комбинированное лечение с применением перорального клиндамицина 300 мг два раза в день и рифампицин 300 мг два раза в день в течение 10 — 12 недель.
— Рассмотрите применение ацитретина 0,3 — 0,5 мг/кг/день у мужчин и нефертильных женщин, которые не реагируют на лечение антибиотиками.
— Рассмотрите применение дапсона у пациентов, которые не реагируют на лечение антибиотиками.
— При неуспешном применении традиционной системной терапии у пациентов с гидраденитом средне-тяжелой степени, рекомендуется применение адалимумаба 40 мг еженедельно.
— Пациентам, которые не реагируют на адалимумаб, рассмотрите инфликсимаб 5 мг/кг каждые 8 недель.
— Рассмотрите применение 1% раствора клиндамицина.
— Для тщательно отобранных индивидуальных участков поражения во время острой фазы рассмотрите инъекции кортикостероидов непосредственно в участки поражения.
— Рассмотрите применение метформина у пациентов с гидраденитом и сочетанным сахарным диабетом, а также у женщин с гидраденитом и с синдромом поликистозных яичников или беременностью.
— Рассмотрите возможность широкого иссечения для минимизации частоты рецидивов.
— Рассмотрите возможность широкого иссечения у пациентов с неуспешным традиционным системным лечением.
— После выполнения широкого иссечения рассмотрите заживление вторичным натяжением (или лоскут на основе перфорантных сосудов торакодорсальной артерии для подмышечных ран).
— Не рекомендуется применение изотретиноина у пациентов с гидраденитом, если только нет сочетанного умеренно-тяжелого поражения акне лица или туловища.
— Не рекомендуется применение адалимумаба 40 мг через неделю у пациентов с гидраденитом средне-тяжелой степени при неуспешном применении традиционной системной терапии.
— Не рекомендуется применение этанерцепта у пациентов с гидраденитом средне-тяжелой степени при неуспешном применении традиционной системной терапии.
— Не рекомендуется применение криотерапии для лечения участков поражения в острой фазе ввиду боли от процедуры.
— Не рекомендуется применение микроволновой абляции у пациентов с гидраденитом.
Гнойный гидраденит: причины появления, симптомы, диагностика и способы лечения.
Определение
Гнойный гидраденит – это воспаление апокриновых потовых желез.
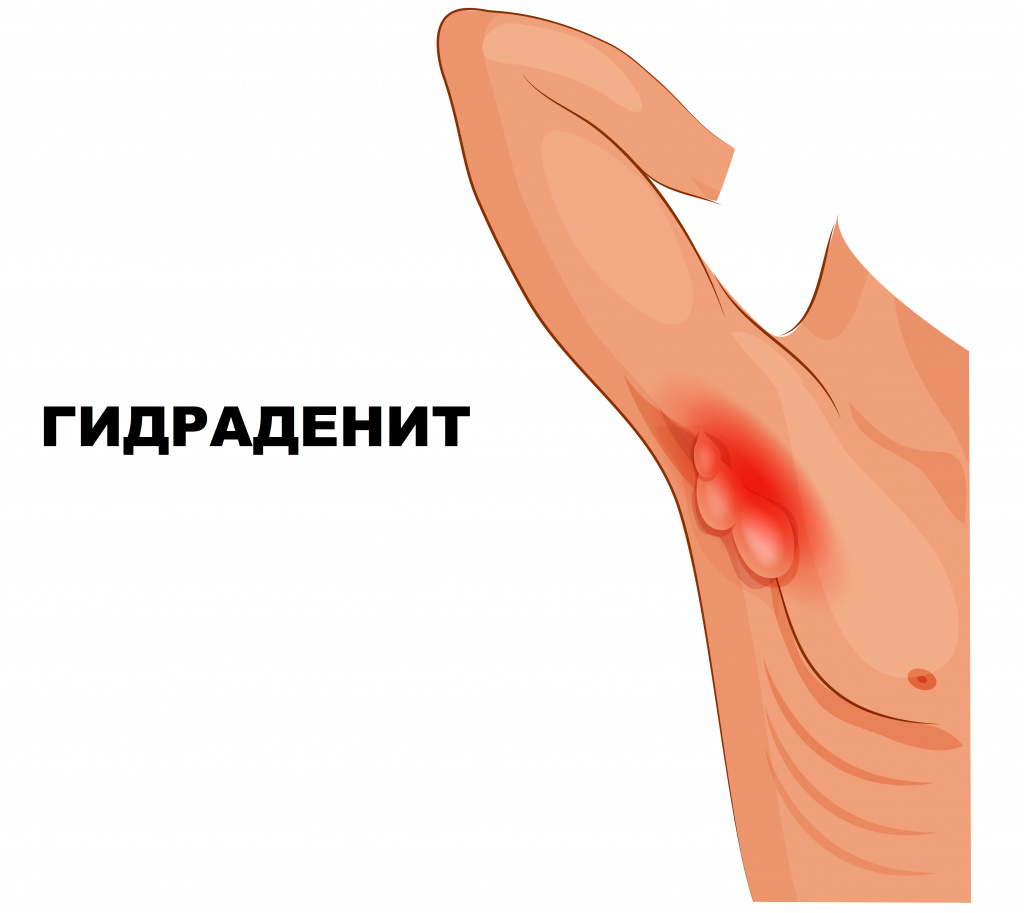
Апокриновые железы не участвуют в терморегуляции, а их секреция тесно связана с половой функцией – манифестирует в период пубертата и угасает с наступлением менопазуы. Этим объясняется тот факт, что заболевание не распространено среди детей и женщин старшего возраста.
Надо заметить, что у женщин апокриновых желез больше, чем у мужчин, в связи с этим гидраденит у них встречается в 4-5 раз чаще.
В общей популяции заболеваемость гнойным гидраденитом составляет примерно 1-4%. Для заболевания характерно хроническое рецидивирующее течение.
Причины возникновения гидраденита
Точный механизм развития гнойного гидраденита до конца не ясен. Большинство исследователей полагают, что в основе заболевания лежит поражение волосяного фолликула – его закупорка с последующим возникновением воспалительного процесса. В результате воспаления стенка фолликула разрывается и его содержимое выходит в дерму, откуда процесс распространяется на апокриновые железы. В дальнейшем происходит инфицирование различными микроорганизмами, как правило, золотистым стафилококком.
Ученые выделяют факторы, которые способствуют развитию гидраденита:
- факторы, снижающие бактерицидную активность кожного сала и пота: загрязнение кожи техническими маслами, горючими жидкостями, нарушение кровоснабжения кожи, переохлаждение или перегрев кожного покрова;
- факторы, повышающие проницаемость кожи: хронические дерматозы, микротравмы (в результате бритья, эпиляции), расчесы, опрелости кожи, гиповитаминозы А и С;
- факторы, снижающие уровень естественной резистентности организма: хронические интоксикации, наличие очагов стафилококковой инфекции в различных органах и тканях, общее переохлаждение и перегревание, нарушения обмена, анемии, переутомление, стресс, гиповитаминозы, эндокринные нарушения (например, сахарный диабет и другие нарушения углеводного обмена);
- факторы, подавляющие нормальную микрофлору кожи и снижающие ее защиту: частое мытье, чрезмерное использование антисептических парфюмерно-косметических средств.
Исследования показали, что чаще болеют хроническим гнойным гидраденитом курильщики, а тяжесть течения заболевания коррелировала с индексом массы тела – чем больше вес человека, тем тяжелее протекает гидраденит.
Классификация гидраденита
Хронический гнойный гидраденит классифицируется по степени тяжести:
- I степень тяжести характеризуется образованием одного или нескольких безболезненных или малоболезненных изолированных узлов и/или абсцессов, которые не склонны к острому прогрессированию и нагноению, фистулообразование («вскрытие» гнойников) и рубцевание отсутствуют.
- II степень тяжести — усиление воспалительного процесса, ограниченного одной локализацией, рецидивирующие узлы и абсцессы не сливаются, вскрываются и образуют свищевые ходы с гнойно-сукровичным отделяемым, некоторые элементы рубцуются.
- III степень тяжести — формируется обширный конгломерат воспалительных инфильтратов, состоящий из сливающихся узлов и абсцессов, усиливается размягчение, образуется множество сообщающихся между собой свищей, которые после заживления рубцуются.
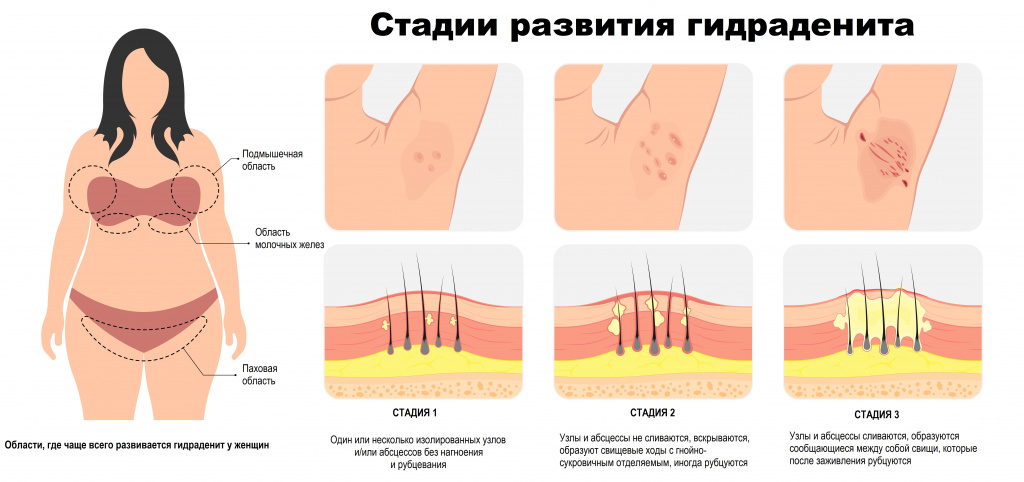
Типичные места локализации гидраденита – подмышечные впадины, где расположено наибольшее количество апокриновых желез, реже – паховая и перианальная области, а также области вокруг сосков и пупка.
В большинстве случаев гидраденит развивается с одной стороны, но иногда процесс может быть двусторонним.
Пациенты отмечают жжение, покалывание, боль или зуд в области поражения, предшествующие развитию заболевания. В глубоких слоях кожи формируются один или несколько плотных узлов диаметром до 3 см. Узлы постепенно увеличиваются, сливаются между собой и спаиваются с окружающими тканями, образуя сплошной болезненный воспалительный инфильтрат багрово-синего оттенка. Через 4-5 дней появляется размягчение (флюктуация), свидетельствующее о наличии гнойного содержимого, узлы вскрываются с появлением отверстия, из которого отделяется гной. После вскрытия гнойника самочувствие пациента, как правило, улучшается. Воспалительный процесс может захватывать несколько потовых желез или мигрировать с одной железы на другую.
После заживления на месте воспаления может остаться рубец.
Диагностика гидраденита
Диагноз «гидраденит» врач может установить на основании характерной клинической картины. Для выявления тяжести процесса и диагностики сопутствующих заболеваний, способных влиять на течение гидраденита, рекомендуют:
- общий (клинический) анализ крови;
Глюкоза (в крови) (Glucose)
A09.05.023 (Номенклатура МЗ РФ, Приказ №804н)
Материал для исследования
Сыворотка или плазма крови. Если нет возможности центрифугировать пробу через 30 мину�…
Креатинин (в крови) (Creatinine)
A09.05.020 (Номенклатура МЗ РФ, Приказ №804н)
Синонимы: Анализ крови на креатинин; Сывороточный креатинин; Креатинин сыворотки, оценка СКФ. Сreat; Сre; Blood Creatinine; Serum Creatinine; …
Билирубин общий (Bilirubin total)
A09.05.021 (Номенклатура МЗ РФ, Приказ №804н)
Синонимы: Общий билирубин крови; Общий билирубин сыворотки.
Totalbilirubin; TBIL.
Краткая характеристика определяемого веществ…
Общий белок (в крови) (Protein total)
A09.05.010 (Номенклатура МЗ РФ, Приказ №804н)
Синонимы: Общий белок сыворотки крови; Общий сывороточный белок.
Total Protein; Serum Тotal Protein; Total Serum Protein; TProt; ТР.
Краткая характ…
Альбумин (в крови) (Albumin)
A09.05.011 (Номенклатура МЗ РФ, Приказ №804н)
Синонимы: Человеческий сывороточный альбумин; ЧСА; Альбумин плазмы;
Human Serum Albumin; ALB.
Краткая характеристик…
К каким врачам обращаться
Поставить диагноз и назначить лечение при гидрадените может
хирург
или дерматолог. При рецидивирующем течении могут потребоваться консультации
терапевта
и
эндокринолога
.
Лечение гидраденита
На первой стадии заболевания обычно ограничиваются местной терапией и используют различные антисептические, а также антибактериальные препараты для наружного применения. При прогрессировании процесса и при хроническом рецидивирующем гидрадените назначается системная антибиотикотерапия. Если процесс сопровождается выраженным болевым синдромом, назначают нестероидные противовоспалительные препараты.
При хроническом гидрадените любой стадии своевременное и широкое хирургическое иссечение гнойных очагов является наиболее эффективным способом лечения, предотвращает рецидивы и осложнения, а также улучшает качество жизни пациента.
Объем и вид хирургического вмешательства определяются хирургом индивидуально для каждого пациента, в зависимости от его возраста, степени тяжести и локализации воспалительного процесса, а также сопутствующих патологий.
Осложнения
Формирование рубцов после перенесенного гидраденита, например, в подмышечной области, может привести к ограничению движения конечности.
Кроме того, образование рубцовой ткани способно нарушить работу лимфодренажной системы и стать причиной возникновения отеков рук, ног или гениталий.
К другим тяжелым осложнением гидраденита относится распространение гнойного процесса с развитием флегмоны или сепсиса.
Профилактика гидраденита
Для профилактики гидраденита необходимо соблюдать санитарно-гигиенические нормы, своевременно проводить антисептическую обработку раневых поверхностей, не допускать появления трещин, микротравм (например, в результате бритья или эпиляции подмышечных областей), натирания кожи предметами одежды.
Снизить риск развития гнойно-воспалительного заболевания кожи может лечение общих заболеваний, которые способствуют развитию гнойничковых поражений (сахарный диабет, болезни ЛОР-органов, пищеварительной системы).
Пациентам с хроническим рецидивирующим гидраденитом рекомендован отказ от курения и снижение избыточной массы тела.
Источники:
- Клинические рекомендации «Пиодермии». Разраб.: Российское общество дерматовенерологов и косметологов. – 2020.
- Бурова С.А., Бородулина К.С. Гнойный гидраденит: вопросы патогенеза, оценочные шкалы, лечение (часть 2) // Клиническая дерматология и венерология. – 2019. – Т. 18. – № 3. – С. 265-269.
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Для корректной оценки результатов ваших анализов в динамике предпочтительно делать исследования в одной и той же лаборатории, так как в разных лабораториях для выполнения одноименных анализов могут применяться разные методы исследования и единицы измерения.
Информация проверена экспертом

Лишова Екатерина Александровна
Высшее медицинское образование, опыт работы — 19 лет
Поделитесь этой статьей сейчас
Рекомендации
-
464
22 Сентября
-
145
07 Сентября
-
129
04 Сентября
Похожие статьи
Инсульт — это клинический синдром, представленный очаговыми и/или общемозговыми нарушениями, развивающийся внезапно вследствие острого нарушения мозгового кровообращения (ОНМК). Клиническая картина инсульта очень разнообразна, симптомы зависят от области поражения.
Кандидоз – инфекционное заболевание, вызываемое дрожжеподобными грибками рода Candida.
Цистит – это воспаление слизистой оболочки мочевого пузыря, встречающееся, по данным медицинской статистики, у 35% лиц в возрасте до 45 лет. Чаще заболевание диагностируется у женщин, чем у мужчин, что объясняется анатомическими особенностями строения мочеполовой системы.
Пародонтит – хроническое воспалительное заболевание тканей, окружающих зуб. Постепенно это приводит к потере зубов у взрослого человека и способствует развитию патологических процессов в организме.
Язвенная болезнь желудка и двенадцатиперстной кишки – хроническое заболевание, характеризуемое образованием язвенных дефектов на слизистой оболочке этих органов и имеющее рецидивирующий характер.
Гнойный гидраденит – это хронический, приводящий к рубцеванию акнеподобный воспалительный процесс, который возникает в области подмышечных ямок, паха, вокруг сосков и ануса. Диагноз ставится при осмотре. Лечение зависит от стадии.
В настоящее время гнойный гидраденит считается хроническим воспалительным состоянием волосяного фолликула и связанных с ним структур. Фолликулярное воспаление и последующая окклюзия приводят к разрыву фолликула и развитию абсцессов, свищевых ходов и рубцов.
Формируются отечные болезненные инфильтраты, напоминающие абсцессы кожи. Эти повреждения часто стерильные. Для хронически протекающего заболевания характерны боль, флуктуация, наличие выделений из очагов поражения и формирование синусовых ходов. В хронических случаях бактериальная инфекция может возникнуть в глубоких нарывах и свищевых ходах. При хроническом поражении кожи подмышечной области сливающиеся воспаленные узелки образуют пальпируемые шнуровидные скопления. Заболевание может приводить к нетрудоспособности из-за боли и неприятного запаха.
-
Клиническая оценка
Диагностика гнойного гидраденита проводится путем обследования. Бактериальные соскобы для исследования должны быть взяты из глубоких гнойников и свищевых ходов у пациентов с хроническим заболеванием, но часто при этом патогенов не обнаруживают. Система определения стадии заболевания по Херли описывает тяжесть заболевания:
-
I стадия: Формирование гнойника, одного или нескольких, без свищевых ходов или рубцов
-
II стадия: Один или несколько, далеко расположенных друг от друга, рецидивирующих гнойников с образованием свищевых ходов или рубцов
-
III стадия: Диффузное или около диффузное разветвление или несколько соединенных между собой свищевых ходов и гнойников по всей зоне поражения
-
I стадия: Клиндамицин местного применения, вводимые внутрь пораженных тканей кортикостероиды и пероральные антибиотики
-
II стадия: более длительные курсы пероральных антибиотиков и иногда дренаж, иссечение или хирургическое вскрывание.
-
III стадия: Инфликсимаб или адалимумаб, часто обширное хирургическое вмешательство, коррекция или пересадка
Цели лечения гнойного гидраденита – предотвращение появления новых поражений, уменьшение воспаления и удаление свищевых ходов.
Для 1-й стадии по Херли типичное лечение включает местное использование раствора клиндамицина 1% 2 раза/день; крем с резорцином 15% наружно 1 раз/день; глюконат цинка перорально (90 мг 1 раз/день); кортикостероиды внутрь поражения (например, от 0,1-0,5 мл раствора триамцинолона ацетонида в концентрации 5-10 мг/мл раз в мес) и короткие курсы пероральных антибиотиков (например, от 7 до 10 дней). Применяют тетрациклин (500 мг 2 раза/день), доксициклин (100–200 мг 1 раз/день), миноциклин (100 мг 1 раз/день) или эритромицин (250–500 мг 4 раза/день) до устранения повреждений. Типичная схема лечения может включать в себя средство для наружного применения (например, подобранного в соответствии с чувствительностью кожи пациента) и пероральный антибиотик; тем не менее, все способы лечения можно использовать как вместе, так и по отдельности. Кожу промывают бензоилпероксидом.
Для II стадии по Херли лечение характеризуется более длительным (например, от 2 до 3 месяцев) курсом тех же пероральных антибиотиков, применяемых для лечения при I стадии болезни; если этого недостаточно, можно добавить клиндамицин в дозировке 300 мг внутрь 2 раза/день и/или рифампицин 600 мг перорально 1 раз/день. Добавление антиандрогенов (например, эстроген перорально или комбинированные пероральные контрацептивы, спиронолактон, ципротерон ацетат [не доступен в США], финастерид или их комбинации) может быть полезным для женщин. Разрез и дренаж могут уменьшить боль абсцесса, но этого недостаточно для контроля заболевания (в отличие от обычных кожных абсцессов). При острых воспалительных поражениях, которые являются не слишком глубокими, предпочтительной является санация раны с помощью панча (т.е., иссечение омертвевших тканей с помощью 5-7 мм панча, с последующим удалением этих тканей, кюретажем или промыванием). Свищевые ходы должны быть иссечены или хирургически вскрыты. Пациенты, у которых глубокие повреждения, должны быть осмотренные пластическим хирургом для рассмотрения хирургического вмешательства и пересадки.
Для III стадии заболевания по Харли медицинская и хирургическая терапии должны быть более агрессивными. Доказательства эффективности в снижении воспаления сильнее в пользу инфликсимаба (5 мг/кг внутривенно в 0-ю, 2-ю и 6-ю недели). В качестве альтернативы, можно применять адалимумаб. Начальная доза составляет 160 мг подкожно в первый день (или разделить дозу на 2 дня подряд), с последующим введением на 15-й день 80 мг подкожно и, начиная с 29 дня, поддерживающая доза по 40 мг подкожно 1 раз в неделю. Использование пероральных ретиноидов (изотретиноин 0,25-0,4 мг/кг 2 раза/день, в течение 4-6 месяцев или ацитретин 0,6 мг/кг 1 раз/день, в течение 9-12 месяцев) было эффективным для некоторых пациентов. Если заболевание сохраняется, то часто требуется масштабное хирургическое вмешательство с пластикой или пересадкой поврежденной области. Аблятивная лазерная коагуляция (CO2 или эрбиевый лазер на иттрий-алюминиевом гранате) является альтернативой хирургическому лечению. Лазерная эпиляция также используется с некоторым успехом.
Рекомендуемые дополнительные меры для всех пациентов с гнойным гидраденитом включают соблюдение надлежащей гигиены кожи, снижения травмирования, обеспечения психологической поддержки и, возможно, избегание диет с высоким гликемическим индексом.
-
Повреждения, как правило, стерильны, за исключением глубоких гнойников и свищевых ходов во время хронического заболевания.
-
Гнойный гидраденит может приводить к нетрудоспособности.
-
Лечить гнойный гидраденит необходимо в соответствии с системой определения стадии заболевания по Херли.
-
Дополнительные меры включают поддержание хорошей гигиены кожи, минимизацию травм, оказание психологической поддержки и, возможно, отказ от высокоуглеводной диеты.
ПРИМЕЧАНИЕ:
Это — Профессиональная версия.
ПОЛЬЗОВАТЕЛИ:
Просмотреть пользовательскую версию

Авторское право © 2023 Merck & Co., Inc., Rahway, NJ, США и ее аффилированные лица. Все права сохранены.

Введение
Гидраденит супаратива / акне инверса (ГС/АИ) — заболевание, известное ранее как синдром фолликулярной окклюзии. Этот термин был введен D.M. Pillsburry, W.B. Shelley и А.М. Kligman в 1956 г. [1]. Нынешнее название применяется с 2006 г., когда оно (после долгого периода путаницы в терминологии) было утверждено на 1-й Международной конференции по ГС/АИ в Дессау (Германия).
По разным данным, распространенность заболевания в мире колеблется от 1% до 4%. Женщины подвержены ГС/АИ в 3 раза чаще, чем мужчины [2, 3].
Долгое время процесс описывался в виде триады: конглобатные акне и инверсные акне, гидраденит и подрывающий фолликулит или перифолликулит головы [4]. И только в 1975 г. был описан четвертый компонент — пилонидальная киста [1]. Все проявления на коже, несмотря на разную локализацию, характеризуются общим патогенезом и сходными гистопатологическими изменениями, в основе которых лежит фолликулярная гиперкератинизация.
Этиология и патогенез ГС/АИ на сегодняшний день до конца не изучены, поэтому современная медицина не способна представить универсальный протокол лечения таких пациентов.
В основе патогенеза заболевания лежит окклюзия волосяных фолликулов, которая в 30–40% случаев обусловлена генетической предрасположенностью к акне [5], гиперкератинизацией и образованием лимфогистиоцитарного воспаления с гранулематозной реакцией. Только в небольшой части случаев (в 4 из 12) наблюдалось воспаление в апокриновых железах, сопровождавшееся воспалением вокруг эккринных желез, волосяных фолликулов и структур, выстланных эпителием. Эти наблюдения свидетельствуют о том, что структуры, выстланные плоским эпителием, вероятно, представляют собой аномальные расширенные волосяные фолликулы, являются более постоянной диагностической особенностью при гнойном гидрадените, чем при воспалении апокриновых желез, которое, по-видимому, является вторичным явлением [6]. Фолликулярная окклюзия приводит к растяжению и разрыву фолликулов с выходом содержимого в окружающую дерму, что способствует миграции нейтрофилов и лимфоцитов в очаг воспаления [7–9], формируя воспалительный инфильтрат с последующим образованием рубцовой ткани [10].
Общепризнанным является тот факт, что бактерии не влияют на развитие заболевания, но вторичная бактериальная инфекция поддерживает воспалительный процесс и способствует рецидивированию [11].
Гистологическая картина при ГС/АИ не имеет специфических критериев. Поэтому в современной дерматологии до сих пор диагноз устанавливается на основании клинической картины заболевания. При патоморфологическом исследовании на ранних стадиях обнаруживают фолликулярную окклюзию с наличием или отсутствием воспаления, фолликулярные кисты, уменьшение объема сальной железы, гиперплазию, нейтрофильные абсцессы [6]. В тяжелых случаях обнаруживают В-клетки и плазматические клетки в псевдофолликулах, абсцессах и пазухах, окруженные хроническим воспалительным инфильтратом, с наличием гистиоцитов и гигантских клеток, а также большое количество грануляционной ткани [12].
Локализации процесса, путаница в терминологии и отсутствие специфических гистологических изменений часто являются причинами неправильной диагностики — дерматологи ориентируются в описании клинической картины только на проявления воспалительного процесса, упуская из виду распространенность высыпаний и формирование абсцессов. Результатом этого являются ошибочные диагнозы: гидраденит или вульгарные акне, что влечет за собой отсутствие терапевтического успеха.
Дебютирует ГС/АИ, как правило, после полового созревания с небольших красных плотных папул или, реже, пустул, которые, постепенно увеличиваясь в размерах, сливаются с окружающими тканями. Постепенно дерматоз трансформируется в хронический воспалительный рецидивирующий процесс с наличием псевдокомедонов, болезненных папул, расположенных в глубоких слоях кожи, с тенденцией к формированию абсцессов, сливающихся в синусы, и с разрешением процесса в рубцы [2–5]. Несомненно, внешне процесс может напоминать вульгарные акне или гидраденит (в зависимости от локализации высыпаний), особенно в самом начале развития, а с учетом возраста пациентов в большинстве случаев такие высыпания определяются как юношеские акне.
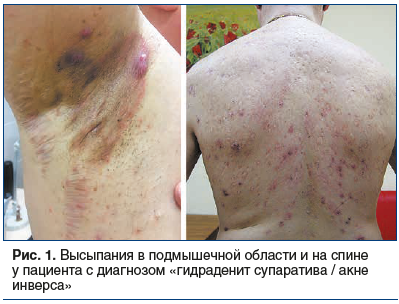
Однако высыпания при ГС/АИ связаны с апокриновыми потовыми железами и кроме лица имеют другие типичные места локализации — это преимущественно подмышечная, паховая и аногенитальная области. Также отмечены случаи ГС/АИ в области живота. У женщин заболевание часто развивается в грудной складке, в области промежности, у мужчин — в анальной зоне [8, 13]. Внимание дерматолога может привлечь также то, что содержимое элементов не эвакуируется, а остается внутридермально в виде округлых подкожных образований [14, 15] (рис. 1, 2).
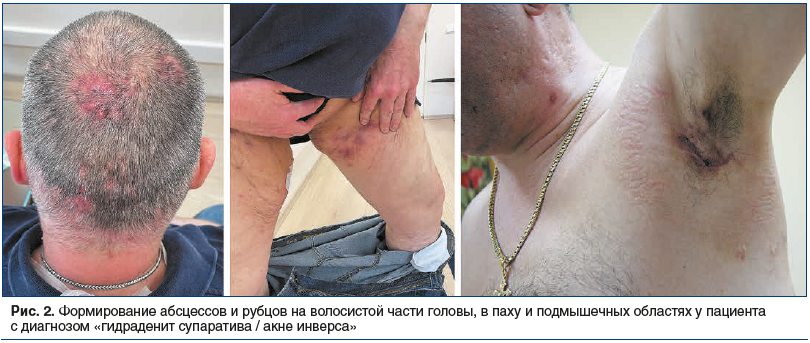
По мере нарастания кожной симптоматики присоединяются общие симптомы. Пациенты жалуются на боль, жжение, обильное потоотделение, слабость, в тяжелых случаях — на невозможность ходить или сидеть, а также на неприятный запах. Такое состояние может продолжаться в течение длительного времени, и, что важно отметить, отсутствует положительная реакция на терапию антибиотиками [5, 16, 17].
Диагностика ГС/АИ
Критерии диагностики заболевания утверждены на 2-м Международном симпозиуме по ГС/АИ (Second International Hidradenitis suppurativa research symposium, 2009). Для постановки диагноза необходимо наличие трех обязательных критериев [18]:
-
Поражения: в начальных стадиях заболевания — глубокие болезненные узлы, абсцессы, дренирующие синусы, рубцы. Вторичные поражения — открытые комедоны по типу «надгробий».
-
Локализация: подмышечная, паховая, анальная области, область промежности, область живота.
-
Хроническое течение с наличием рецидивов.
Проводя дифференциальную диагностику, в первую очередь следует обратить внимание на нетипичные для вульгарных акне места локализации (см. диагностические критерии). Подкрепляет диагноз ГС/АИ отсутствие положительной динамики в ответ на антибиотикотерапию.
При отсутствии высыпаний на лице и дифференциальной диагностике с гидраденитом внимание дерматолога привлечет наличие дренирующих синусов, рубцов, открытых комедонов по типу «надгробий» и локализация не только в подмышечных областях. Немаловажным также является наличие постоянных рецидивов при ГС/АИ.
При дифференциальной диагностике с фурункулом, карбункулом, фолликулярной пиодермией необходимо учитывать характер высыпаний. При ГС/АИ кроме воспалительных элементов, которые, как правило, без хирургического вмешательства самостоятельно не вскрываются, еще присутствуют и макрокомедоны. Дополнительным ориентиром является симметричность высыпаний, характерная для ГС/АИ.
Лечение ГС/АИ
Лечение ГС/АИ требует комплексного подхода, который должен включать немедикаментозные и медикаментозные пути решения проблемы. Необходимо обращать внимание на образ жизни пациента и вредные привычки. Очень большую роль в достижении успеха терапии играют контроль массы тела и отказ от курения.
В.С. Melnik, С.С. Zouboulis опубликовали результаты наблюдения, свидетельствующие о том, что у женщин, страдающих ГС/АИ, отмечается высокая чувствительность к андрогенам [19], поэтому препараты, содержащие андрогены, необходимо исключать из терапии [20]. Внимание пациентов необходимо акцентировать на трех важных фактах. Во-первых, доказано, что на образование фолликулярной окклюзии влияет никотин, вследствие этого у курильщиков заболевание протекает в более тяжелой форме [21]. Во-вторых, ухудшению процесса способствует механическая травматизация высыпаний самими пациентами с последующим более глубоким инфицированием [22]. В-третьих, установлена прямая корреляция между метаболическим синдромом и тяжестью течения ГС/АИ, поэтому всем больным с лишним весом рекомендуется его снижать [21]. Согласно систематическому обзору научной группы альянса ГС/АИ снижение веса (у пациентов с индексом массы тела более 30 кг/м2) с высоким уровнем доказательности способствует уменьшению тяжести заболевания в долгосрочной перспективе [22]. В когортном исследовании, проведенном в Дании, установлено, что возвращение к нормальному весу до полового созревания снижает риск возникновения заболевания до уровня заболеваемости у детей без избыточного веса [22].
Из-за частого сочетания ГС/АИ с болезнью Крона и/или локализации в перианальной области пациента необходимо обследовать у гастроэнтеролога и проктолога [14].
При выборе тактики лечения ГС/АИ практикующим врачам рекомендуется ориентироваться на классификацию этого заболевания, разработанную H.J. Hurley в 1989 г. [9, 19]. Существуют и другие классификации (Sartorius score, the Hidradenitis Suppurativa Severity Index, Physician Global Assessment), но они в основном применяются в клинических научных исследованиях [9].
Согласно классификации Hurley выделяют три стадии заболевания:
I — наличие одного или нескольких изолированных абсцессов без рубцов или пазух.
II — наличие рецидивирующих абсцессов, локализующихся более чем в одной анатомической области. Формирование синусовых ходов.
III — наличие обширных абсцессов с множеством взаимосвязанных пазух, приводящих к формированию рубцов.
Тактика терапии зависит от стадии патологического процесса. При I–II стадии вполне возможно обойтись наружными средствами, в то время как III стадия заболевания рассматривается как показание к биологической терапии [23–25].
Согласно данным современной литературы препаратами первой линии являются антибиотики и стероидные средства на фоне хирургического дренирования гнойных полостей. Согласно рекомендациям European S1 guideline for the treatment of hidradenitis suppurativa/acne inverse, клиндамицин — единственный антибиотик, рекомендуемый для местного применения [9]. У пациентов с I–II стадией ГС/АИ по Херли возможно местное применение клиндамицина 1%, особенно при отсутствии абсцессов [9]. При наличии нескольких поражений и частых обострений может быть рассмотрена терапевтическая группа системных тетрациклинов [26]. Альтернативным вариантом может быть тройной режим приема рифампицина (10 мг/кг 1 р/сут), моксифлоксацина (400 мг 1 р/сут) и метронидазола (500 мг 3 р/сут) в течение 12 нед. с прекращением приема метронидазола через 6 нед. Пациентам со II–III стадией ГС/АИ, у которых имеется несколько активных поражений, следует сразу назначать системный клиндамицин и рифампицин (300 мг 2 р/сут) [27–29]. Антибактериальные препараты оказывают противовоспалительное действие и подавляют рост вторичной бактериальной флоры. Большое значение в терапии имеют высокая дозировка и продолжительная длительность приема препаратов. Схемы лечения системными тетрациклинами и клиндамицином, рекомендуемые при гнойничковых заболеваниях кожи, не дают результата при ГС/АИ, что служит дополнительным дифференциально-диагностическим признаком.
Хорошие результаты наблюдаются при применении в качестве эксфолианта резорцинола 15% 2 р/сут. Его используют как в качестве монотерапии, так и совместно с другими средствами, в зависимости от степени и глубины поражения. Резорцинол обладает кератолитическим, антисептическим действием, а также подавляет зуд [30].
Отдельные авторы предлагают совместное использование метронидазола 400 мг 2 р/сут и клиндамицина 600 мг 3 р/сут внутривенно в течение 2 нед. [31].
Кортикостероидные препараты также являются неотъемлемой частью лечения этого сложного заболевания. Препараты данной группы назначают с целью уменьшения выраженности воспаления. Для системной терапии используется введение триамценолона ацетонида непосредственно в образования [32] или прием внутрь гидрокортизона, дексаметазона, преднизолона. Длительность терапии составляет 7–14 дней [33].
Поскольку имеются наблюдения, подтверждающие взаимосвязь ГС/АИ и повышенной чувствительности к андрогенам [19], оправдано назначение антиандрогенов (ципротерон ацетат, эстрогены, финастерид) [34, 35].
В отношении других препаратов, в частности цитостатиков, имеется меньше публикаций, но в ряде случаев отмечена успешная терапия циклоспорином [36–38].
В современной литературе нет единого взгляда на применение метотрексата в терапии ГС/АИ. В раннем исследовании, проведенном в 2002 г. G.B. Jemec [39], метотрексат использовался в качестве монотерапии на период от 6 нед. до 6 мес., автор отметил ограниченную эффективность препарата при данной патологии. Однако, несмотря на отсутствие эффекта от метотрексата, некоторые исследователи утверждают, что его добавление в низких дозах к терапии биологическими препаратами необходимо с целью предотвращения нейтрализации аутоантител, что предупреждает развитие вторичной резистентности к биологической терапии [9, 40]. Оправдано назначение метотрексата также и при наличии у пациентов с ГС/АИ сопутствующих ревматологических заболеваний [9]. Более поздние исследования, проведенные P. Kozub et al. [41], продемонстрировали, что метотрексат неэффективен ни в качестве монотерапии, ни в сочетании с инфликсимабом. Авторы доказали, что метотрексат не увеличивает клиническую эффективность инфликсимаба [41].
Противоречивость данных об эффективности терапии метотрексатом обсуждается до сих пор. Патогенетически механизм развития заболевания связан с дисфункцией Т-регуляторных клеток и Т-хелперов 17-го типа, что приводит к повышению уровня IL-17А и IL-6, запуская тем самым каскад воспалительных реакций. В данном случае терапевтическое действие метотрексата связано с подавлением Т-хелперов 17-го типа за счет изменения уровней активности и скорости созревания дендритных клеток и Т-лимфоцитов [42]. Однако в литературе нет достаточного количества примеров, когда терапия метотрексатом улучшала течение ГС/АИ [43].
Изотретиноин при данном заболевании может быть неэффективен, поскольку в основе патогенеза заболевания лежит окклюзия волосяных фолликулов с гиперкератинизацией и последующее иммунное воспаление с вовлечением в процесс CD3/CD8 и естественных киллеров (NK-клеток). Была обнаружена отрицательная корреляция между длительностью течения заболевания и процентом NK-клеток, также отмечено увеличение содержания фактора некроза опухоли α и IL-6 [7]. Современные исследования также подтверждают низкую эффективность изотретиноина: около 60% пациентов не реагировали на лечение, а у 13% наблюдались рецидивы [44, 45].
Однако более современный препарат из класса ретиноидов — алитретиноин в дозе 10 мг/сут в течение 2 мес. с последующей поддерживающей дозой 20 мг, согласно данным [46], вызвал стойкую ремиссию у большинства больных. Данное противоречие можно объяснить тем, что алитретиноин (9-цис-агонист ретиноевой и пан-ретиноевой кислот) — новый системный препарат из группы ретиноидов, обладающий противоопухолевой активностью.
Несмотря на многочисленные работы, представленные в мировой литературе, лечение ГС/АИ является очень сложной задачей, ремиссия непродолжительная, составляет менее 1 года или полностью отсутствует, последующие рецидивы приводят к инвалидизации пациента.
Хирургическое вмешательство (либо простое иссечение поврежденных тканей, либо полное местное иссечение с последующей пересадкой кожи) является важной частью ведения таких пациентов и применяется при II–III стадиях заболевания. Важно не только вскрытие воспалительных элементов, но и их дренирование и иссечение дивертикул, как правило, располагающихся глубже основного воспалительного очага [9, 47]. Пациенты с ГС/АИ I–II стадии не нуждаются в хирургических вмешательствах [9].
Встречаются практические рекомендации по применению лазеров при ГС/АИ: carbon dioxide laser [48], NG:Yag laser [49], IPL [50], но наблюдений еще недостаточно, чтобы делать окончательные выводы.
Что касается биологической терапии, то анти-TNFα моноклональные антитела — инфликсимаб и адалимумаб показаны пациентам с III стадией ГС/АИ [9].
Впервые применили адалимумаб у 3 пациентов А.А. Navarini, R.M. Trueb в 2010 г. Все пациенты ранее получали изотретиноин в комбинации с антибиотиком, без эффекта. Применение адалимумаба позволило устранить клинические симптомы и субъективные ощущения. Однако после отмены биологической терапии клинические проявления начали возвращаться, и пациентам назначили повторный курс биологической терапии [51].
В противовес этому исследованию, эффективность адалимумаба доказана в проспективных двойных слепых плацебо-контролируемых исследованиях с участием более 800 больных, что позволило в дальнейшем включить ГС/АИ в перечень показаний для терапии адалимумабом [52, 53].
Адалимумаб следует рассматривать в качестве биологического агента первого выбора при ГС средней/тяжелой степени после неуспешного применения традиционных методов лечения, за которыми следуют инфликсимаб, устекинумаб и анакинра в качестве препаратов второй и третьей линий терапии соответственно [54].
В литературе имеются доказательства эффективности инфликсимаба у 30-летнего пациента с предшествующим неэффективным курсом терапии рифампицином 300 мг/сут, преднизолоном 50 мг/сут и изотретиноином 30 мг/сут. У данного пациента уже после первого введения инфликсимаба наблюдалось значительное уменьшение выраженности воспалительного процесса и снижение болевых ощущений [23]. Положительные результаты также продемонстрированы при лечении другими биологическими препаратами — этанерцептом и устекинумабом [24, 25]. Таким образом, можно сделать выводы, что биологические препараты демонстрируют эффективность у пациентов с ГС/АИ, и поиски оптимальной биологической терапии продолжаются.
Заключение
Гидраденит супаратива / акне инверса до сих пор является загадкой дерматологии. Несмотря на многочисленные исследования в этой области, остаются неясными многие вопросы. Среди них — важный вопрос тактики терапии пациентов с уже сформированной резистентностью к антибиотикам и противопоказаниями к адалимумабу или другим биологическим методам лечения.
Появляются новые теории, которые принципиально меняют концепцию патогенеза, о котором шла речь выше. Два исследования продемонстрировали наличие биопленки в очагах, в основном при тяжелых формах, что объясняет постоянные рецидивы в предыдущих рубцах. Эти данные свидетельствуют о патогенной роли изолированной флоры, вводя новую концепцию болезни — «хозяин — микробиом». Вместо аутовоспалительного процесса с неясным механизмом ГС/АИ можно рассматривать как аутоинфекционный из-за кожной иммунной дисрегуляции. Эта дисрегуляция позволяет аномальной бактериальной инфекции пролиферировать на фоне неадекватной гипервоспалительной реакции вместо эвакуации бактерий из дермы [51].
Эта теория может открыть возможности для разработки новых методов лечения ГС/АИ. Остается еще много вопросов, на которые нужно ответить. В частности, способствует ли ранний микробный сдвиг окклюзии фолликулов? Может ли потеря «микробного щита» быть частично восстановлена посредством иммуномодуляции или трансплантации микробиоты, как это исследовалось при воспалительных заболеваниях кишечника? Экспериментальные исследования в этом направлении уже ведутся, что позволит в скором времени получить более определенные ответы.


![Гидраденит в разных частях тела [83] Гидраденит в разных частях тела [83]](https://probolezny.ru/media/bolezny/gidradenit/gidradenit-v-raznyh-chastyah-tela-83_s.jpeg)


![Стадии гидраденита [82] Стадии гидраденита [82]](https://probolezny.ru/media/bolezny/gidradenit/stadii-gidradenita-82_s.jpeg)

![Дерматогенная контрактура [52] Дерматогенная контрактура [52]](https://probolezny.ru/media/bolezny/gidradenit/dermatogennaya-kontraktura-52_s.jpeg)


