Предложите, как улучшить StudyLib
(Для жалоб на нарушения авторских прав, используйте
другую форму
)
Ваш е-мэйл
Заполните, если хотите получить ответ
Оцените наш проект
1
2
3
4
5
Книга представляет собой практическое руководство по использованию систем капиллярного электрофореза «Капель», первых и единственных серийно выпускаемых в России приборов для реализации различных вариантов современного инструментального метода — капиллярного электрофореза.
Материал книги включает физико-химические основы метода, его аналитические возможности, описание аппаратуры. На примере методик, разработанных специалистами фирмы «Люмэкс», описаны стратегии разработок с указанием методических особенностей и наших практических рекомендаций. Значительное место в руководстве отведено примерам использования метода капиллярного электрофореза в различных областях. Особое внимание уделено вопросам подготовки капилляра и оценке его работоспособности.
Книга написана ведущими специалистами по капиллярному электрофорезу науч но-производственной фирмы «Люмэкс» с привлечением материалов, наработанных пользователями систем капиллярного электрофореза «Капель» в нашей стране и за рубежом.
Книга предназначена, в первую очередь, для инженеров-химиков и лаборантов аналитических лабораторий, только приступающих к изучению или уже использующих в своей ежедневной практике приборы серии «Капель» и разработанные для них методики. Она может быть полезна также исследователям и специалистам, областью интересов которых являются методы разделения и их применение для анализа объектов окружающей среды, пищевых продуктов, лекарственных препаратов, биопроб и т. д.; а также тем, кто занят поиском новых областей использования метода капиллярного электрофореза.
АНАЛИЗ ВОДНЫХ ОБЪЕКТОВ ОКРУЖАЮЩЕЙ СРЕДЫ МЕТОДОМ КАПИЛЛЯРНОГО ЭЛЕКТРОФОРЕЗА
- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Ябловская П.Е.
1
1 ФГАОУ ВПО «Научно-исследовательский институт прикладной экологии Севера Северо-Восточного федерального университета им. М.К. Аммосова»
В статье приведены результаты внедрения методик М03-08-2011 иПНД Ф16.1:2:2.3:2.2.69-10 (ГК «ЛЮМЭКС») по определению водорастворимых форм катионов ианионов впочвах игрунтах. Метод капиллярного электрофореза на сегодняшний день позволяет эффективно, быстро иотносительно недорого решать задачи экологического мониторинга почв сопределением расширенного катионно-анионного состава почвенных вытяжек.
почва
грунт
водная вытяжка
катионы
анионы
капиллярный электрофорез
титриметрия
1.Комарова Н.В., Каменцев Я.С. Практическое руководство по использованию систем капиллярного электрофореза «КАПЕЛЬ».– СПб: ООО «Веда», 2006.– 212 с.
2.Полякова Е.В., Шуваева О.В., Полянская Е.М.// Аналитика иконтроль– 2005(9).– С.70-73.
3.Золотов Ю.А., Дорохова Е.Н., Фадеева В.И. и.др. Основы аналитической химии. В2 кн. Кн. 2.Методы химического анализа/ Под ред. Ю.А.Золотова. 2-е изд. – М.: Высшая школа, 2002.– C. 494.
Актуальным внастоящее время является анализ сложных объектов окружающей среды: смесей органических веществ, втом числе биологического происхождения. Традиционными методами анализа ионного состава растворов являются титриметрия, фотометрия, ионная хроматография. Внастоящее время для анализа объектов окружающей среды широкое применение получил новый экспрессный, простой инадежный метод– капиллярный электрофорез (далее КЭ). По сравнению сметодами ионной хроматографии, потенциометрии или титрования, метод капиллярного электрофореза показал свою высокую эффективность при определении ионного состава питьевых, природных источных вод. В2011 г. ГК «ЛЮМЭКС» (г. Санкт-Петербург) впрактику химического анализа введено определение ионного состава водных вытяжек почв игрунтов, пока еще не получившее широкого применения впочвенно-геохимических иагрохимических исследованиях.
Целью работы является внедрение методики определения водорастворимых форм катионов ианионов впочвах игрунтах, исравнение полученных результатов водных вытяжек почв двумя методами: титриметрии иКЭ.
Материалы иметоды исследования
В2012 году влаборатории физико-химических методов анализа НИИПЭС СВФУ им. М.К. Аммосова (аттестат аккредитации № РОСС RU.0001.517741) были проведены методические работы по внедрению методики М03-08-2011 «Определение массовой доли водорастворимых форм катионов аммония, калия, натрия, магния, кальция впочвах, грунтах ( втом числе тепличных), глинах, торфе, осадках сточных вод, активном иле идонных отложениях» иПНД Ф16.1:2:2.3:2.2.69-10 «Определение массовой доли водорастворимых форм неорганических иорганических анионов впочвах, грунтах ( втом числе тепличных), глинах, торфе, осадках сточных вод, активном иле идонных отложениях».Всего было проанализировано 22 пробы почв со сложным вещественным составом:
10 образцов свысоким содержанием органического вещества,
12 проб сразличным содержанием карбонатов.
Все пробы проанализированы втрех кратной повторности методом капиллярного электрофореза на «Капель–105М ЛЮМЭКС» итрадиционными вагрохимии методами: ГОСТ 26424-85 «Метод определения ионов карбоната ибикарбоната вводной вытяжке», ГОСТ 26425-85 « Методы определения иона хлорида вводной вытяжке», ГОСТ 26426-85 «Методы определения иона сульфата вводной вытяжке», ГОСТ 26427-85 «Метод определения натрия икалия вводной вытяжке», ГОСТ 26428-85 « Методы определения кальция имагния вводной вытяжке».
Для контроля правильности двумя выше названными методами проанализирован стандартный образец (СО) состава засоленной почвы САЗП-98 ОСО № 39804 (ГНУ Всероссийский Научно-Исследовательский Институт Агрохимии имени Д.Н. Прянишникова.) СО предназначен для контроля погрешностей методик выполнения измерений, применяемых при определении состава почв, для контроля метрологических характеристик при проведении средств измерений.
Результаты исследования иих обсуждение
Капиллярный электрофорез– это новый высокоэффективный метод разделения ианализа компонентов сложных смесей. Воснове капиллярного электрофореза лежат электрокинетические явления– электромиграция ионов идругих заряженных частиц иэлектроосмос. При анализе методом КЭ пробу небольшого объема вводят вкварцевый капилляр, заполненный электролитом. Ккапилляру прикладывают напряжение от 10 до 30 кВ. Под действием электрического поля компоненты пробы начинают двигаться сразной скоростью, зависящей от их структуры, заряда имолекулярной массы, и, соответственно вразное время достигают детектора. Полученный изаписанный сигнал представляет собой последовательность пиков по которым, как ив хроматограмме, можно идентифицировать иколичественно определить конкретное соединение (рисунок).

|
Буфер |
10мМ хроматный буфер 30мМ диэтаноламин 3 мМ ЦТАОН |
|
Проба |
Суглинистая почва (5 г.) Экстрагент- дистиллированная вода (25 мл) |
|
Капилляр |
L эфф/ Lобщ = 50/60 см, ID= 75 мкм |
|
Ввод пробы |
30 мбар*5 с |
|
Напряжение |
— 25 кВ |
|
Детектирование |
374 нм, косвенное |
|
Температура |
+20º С |
Найдено впробе, мг/кг: хлорид-2,6 сульфат-3,9 оксалат-0,012 нитрат-5,5 формиат-1,2 фосфат-34.
Электрофореграмма водной вытяжки
Водная методика определения анионов была адаптирована для анализа почв, глин, торфа, грунтов, осадков сточных вод, донных отложений, активного ила. Сучетом состава данных типов проб, оптимизированы условия разделения, что позволило ввести список определяемых компонентов не только неорганические анионы (хлориды, сульфаты, нитраты, фториды, фосфаты), но иостатки органических кислот (оксалаты, формиаты, ацетаты).
Для перевода анионов из почвы враствор предложена водная вытяжка втечение 30 минут при соотношении навески пробы иводы 1:5.При определении анионов вводных вытяжках почв (в том числе водных объектах) вфоновый электролит вводят непрозрачное вУФ-области вещество (оксид хрома) для косвенного фотометрического детектирования. Диапазон измеряемых значений массовой доли анионов икатионов составляет 1-20000 мг/кг (млн).
Методом капиллярного электрофореза определили тринадцать показателей, из них:
–основные катионы: Ca2+, Mg2+, Na+ ,K+ иNH4+;
–неорганические анионы: Сl- , SO2-4, NO3-, PO43-,F- ;
–органические анионы: C2O42-, HCO2-, СН3СОО- .
Титриметрическим методом последовательно определили всего восемь показателей– это четыре основных катиона ианионы: Ca2+, Mg2+, Na+ +K+ , Cl-, SO42-, CO32, HCO3- .
Сопоставимость результатов методом капиллярного электрофореза ититриметрии представлена втабл. 1 и2 на примере пяти образцов. Из определенных катионов ианионов корректное сравнение можно провести только по кальцию, магнию, сульфатам ихлоридам. Содержания натрия икалия сравнению не подлежат т.к. при титриметрии результаты получают расчетным путем сопределением суммы Na++K+.
Таблица 1
Пример сравнения результатов определения катионов разными методами анализа, г/кг
|
№ лаб. |
№ полевой |
Капиллярный электрофорез |
Титриметрия |
||||||
|
Са2+ |
Mg2+ |
Na+ |
К+ |
NH4+ |
Са2+ |
Mg2+ |
Na++К+ |
||
|
312 |
Р-1-Л-12,А0А1 |
125,0 |
23,0 |
31,5 |
19,0 |
6,5 |
100,0 |
25,6 |
97,3 |
|
313 |
Р-1-Л-12, В |
125,0 |
28,0 |
15,0 |
7,5 |
2,0 |
100,0 |
25,6 |
107,5 |
|
314 |
Р-2-Л 12,А0А1 |
192,5 |
41,0 |
13,5 |
12,5 |
5,5 |
150,0 |
30,5 |
319,0 |
|
315 |
Р-2-Л-12,В |
115,0 |
17,5 |
18,0 |
3,4 |
2,5 |
83,3 |
30,5 |
186,0 |
|
316 |
Р-3-Л-12, А0А16(7)-11(14) |
480,0 |
130,0 |
15,0 |
36,5 |
– |
166,6 |
40,6 |
310,0 |
Таблица 2
Пример сравнения результатов определения анионов разными методами анализа, г/кг
|
№ лаб. |
Номер полевой |
Капиллярный электрофорез |
Титриметрия |
||||||||||
|
Сl- |
SO2-4 |
NO3- |
PO3- |
F- |
C2O42- |
НСО2- |
СН3СОО- |
Сl- |
SO2-4 |
СО32- |
НСО3- |
||
|
312 |
Р-1-Л-12,А0А1 |
30,5 |
28,0 |
– |
2,60* |
1,0 |
0,1* |
– |
– |
88,7 |
104,0 |
120,0 |
– |
|
313 |
Р-1-Л-12, В |
7,5 |
1,0 |
– |
28,5 |
0,2 |
– |
– |
– |
94,6 |
48,0* |
150,0 |
– |
|
314 |
Р-2-Л 12,А0А1 |
2,0 |
3,0 |
– |
55 |
– |
– |
– |
– |
94,6 |
96,0 |
210,0 |
– |
|
315 |
Р-2-Л-12,В |
12,5 |
6,5 |
300 |
10,5 |
– |
– |
– |
94,6 |
48,0 |
135,0 |
– |
|
|
316 |
Р-3-Л-12,А0А16(7)-11(14) |
150 |
46 |
435 |
140 |
2,9 |
4,5 |
– |
– |
289,9 |
96,0 |
450,0 |
– |
При анализе двух методов установили, что методом КЭ лучше определять катионы магния икальция, так как диапазон измерений охватывает широкий интервал определяемых компонентов. Например, диапазон измерения кальция при капиллярном электрофорезе от 2 до 20000мг/кг, адиапазон измерений кальция титриметрическим методом, от 234,0 до 390,0мг/кг. Такая же картина наблюдается ипри анализе анионов: диапазон измерения хлорида исульфата КЭ охватывает более широкий интервал, чем при анализе титриметрическим методом.
Из полученных данных видно, что во всех двадцати двух пробах наблюдается наибольшее содержание нитрат-ионов, наименьшее– фторид. Оксалат-ион наблюдается десяти пробах, формиат-ион впяти иацетат-ион только водной пробе.
Титриметрическим методом определены карбонат, бикарбонат, сульфат ихлорид анионы. Наибольшая концентрация наблюдается по карбонат-иону, абикарбонат содержится только водной пробе.
Таким образом, врезультате сравнительного анализа видно, что методом КЭ кроме кальция, магния, натрия, калия определяется еще икатион аммония. Следовательно, спектр определяемых показателей при КЭ шире, чем при титриметрии. При этом при минимальном статистическом обсчете результаты анализа на содержание Ca2+ иMg2+ практически сопоставимы.
В результате определения анионов разными методами анализа выявлено, что метод КЭ по сравнению ститрованием показывает низкие средние минимальные значения.
Для определения контроля правильности выполненного анализа проанализировано стандартный образец САЗП-98 ОСО № 39804 двумя методами КЭ ититриметрии. Втабл. 3 приведены результаты химического анализа стандартного образца. Входе анализа видно, что результаты определения сопоставимы.
Таблица 3
Результаты химического анализа стандартного образца ОСО № 39804
|
Дата |
Показатель |
Капиллярный электрофорез |
Титриметрия |
|
|
мг/кг |
ммоль/100 г |
ммоль/100 г |
||
|
24.08.2012 |
Бикарбонаты |
– |
– |
0,75 |
|
хлориды |
14,9 |
0,21 |
0,20 |
|
|
сульфаты |
1500,0 |
15,6 |
12,2 |
|
|
23.08.2012 |
Калий |
2,34 |
0,03 |
– |
|
натрий |
487,6 |
10,6 |
10,4 |
|
|
кальций |
69,7 |
1,74 |
1,75 |
|
|
магний |
19,6 |
0,81 |
1,00 |
В ходе реализации методики определения водорастворимых форм катионов ианионов впочвах игрунтах (М 03-08-2011 иПНД Ф16.1:2:2.3:2.2.69-10) были проведены процедуры оперативного контроля правильности результатов. Втабл. 4 представлены результаты оперативного контроля КЭ. Втабл. 5 представлены результаты оперативного контроля титриметрическим методом
Таблица 4
Оперативный контроль правильности для капиллярного электрофореза
|
Показатель |
Х1 |
Х2 |
∆ |
│Х1–Х2│ |
Хср⋅0,01⋅∆ |
Если условие │Х1-Х2│≤Хср⋅0,01⋅∆ |
|
калий |
0,036 |
0,03 |
22 |
0,006 |
0,007 |
Приемлем |
|
натрий |
12,2 |
10,6 |
15 |
1,6 |
1,7 |
Приемлем |
|
кальций |
1,56 |
1,74 |
25 |
0,18 |
0,41 |
Приемлем |
|
магний |
0,9 |
0,81 |
20 |
0,09 |
0,17 |
Приемлем |
|
хлорид |
0,20 |
0,21 |
25 |
0,01 |
0,05 |
Приемлем |
|
сульфат |
13,9 |
15,6 |
18 |
1,7 |
2,7 |
Приемлем |
Х1 – аттестованное значение стандартного образца, ммоль/100 г.;
Х2 – оперативное значение, ммоль/100 г;
∆ – точность.
Таблица 5
Оперативный контроль правильности для титриметрического анализа
|
Показатель |
Х1 |
Х2 |
∆ |
│Х1–Х2│ |
Хср⋅0,01⋅∆ |
Если условие │Х1-Х2│≤Хср⋅0,01⋅∆ |
|
натрий |
12,2 |
10,4 |
1,8 |
1,8 |
1,8 |
Приемлем |
|
кальций |
1,56 |
1,75 |
0,19 |
0,19 |
0,22 |
Приемлем |
|
магний |
0,9 |
1,00 |
0,1 |
0,1 |
0,2 |
Приемлем |
|
хлориды |
0,20 |
0,20 |
0,0 |
0,0 |
0,05 |
Приемлем |
|
сульфаты |
13,9 |
12,2 |
1,7 |
1,7 |
2,4 |
Приемлем |
|
бикарбонаты |
0,75 |
0,66 |
0,09 |
0,09 |
0,21 |
Приемлем |
Х1– аттестованное значение стандартного образца, ммоль/100 г;
Х2– оперативное значение, ммоль/100 г;
∆– точность.
С помощью оперативного контроля доказано, что результаты определения методов капиллярного электрофореза ититриметрии приемлемы.
Выводы. Явным преимуществом метода КЭ является возможность одновременного определения всех ионов входе одного анализа, что недоступно фотометрическим ититриметрическим методам. Разрешающая способность КЭ превосходит известные хроматографические методы.
Малый расход реактивов (микролитры), низкая стоимость кварцевого капилляра (в сравнении хроматографическими колонками) инесложная пробоподготовка (фильтрование идегазирование) делают стоимость анализа значительно ниже по сравнению со многими другими методами.
Таким образом, метод капиллярного электрофореза представляет собой универсальный метод, позволяющий эффективно, быстро иотносительно недорого решать задачи экологического мониторинга.
Библиографическая ссылка
Ябловская П.Е. АНАЛИЗ ВОДНЫХ ОБЪЕКТОВ ОКРУЖАЮЩЕЙ СРЕДЫ МЕТОДОМ КАПИЛЛЯРНОГО ЭЛЕКТРОФОРЕЗА // Международный журнал прикладных и фундаментальных исследований. – 2013. – № 8-2.
– С. 200-203;
URL: https://applied-research.ru/ru/article/view?id=3811 (дата обращения: 24.09.2023).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)

|
198 |
Система капиллярного электрофореза «Капель» |
9.2. Подготовка буферных и анализируемых растворов
В капиллярном электрофорезе фактором, ограничивающим нижнюю границу интервала определяемых концентраций, является чистота анализируемых растворов. Мелкие взвешенные частицы, а также микропузырьки, увеличивают амплитуду шума базовой линии, затрудняя распознавание пиков определяемых компонентов. Взвешенные частицы, оседая в капилляре, могут забивать капилляр. Мельчайшие пузырьки воздуха могут образовываться при перемешивании растворов, особенно в присутствии поверхностно-активных веществ. Кроме того, в процессе электрофореза протекающий через капилляр электрический ток нагревает раствор, что приводит к уменьшению растворимости газов в растворе. Выделяющиеся пузыри могут прервать электрическую цепь. По этим причинам основными требованиями при подготовке растворов являются тщательная фильтрация всех используемых в анализе и промывке капилляра растворов и обязательное их дегазирование.
Фильтрование необходимо проводить так, чтобы в раствор не попадали частицы фильтрующего материала. По этой причине следует отказаться от применения бумажных фильтров. В комплект прибора «Капель» входят специальный держатель и набор полимерных фильтров типа «Владипор» с диаметром пор 0,2 мкм. Растворы следует фильтровать небольшими порциями, достаточными для работы в течение дня, отбрасывая первые капли в слив.
Дегазирование растворов лучше всего проводить вакуумированием, помещая отфильтрованные растворы в вакуум-эксикатор на 10 мин. Вакуумирование можно заменить центрифугированием приготовленных растворов в пробирках типа Эппендорф непосредственно перед анализом. Если не указано иначе центрифугирование проводят при скорости вращения 5–6 тысяч об/мин в течение 2–3 минут.
9.3. Возможные трудности при работе с системами капиллярного электрофореза «Капель» и программами сбора данных, причины и способы устранения
В таблице 13 описаны ситуации, мешающие нормальной работе системы капиллярного электрофореза «Капель», приведены причины их возникновения и предложены способы восстановления рабочего состояния.
Таблица 13. Неполадки в работе, причины их вызывающие и способы устранения.
прибор не включается, индикатор «сеть» не светится
|
Причина |
Способ устранения |
на прибор не поступает напря-
проверьте, хорошо ли подсоединен шнур питания к прибору
жение питания
проверьте наличие напряжения в розетке замените шнур питания
|
Глава 9. Общие рекомендации по работе с системами капиллярного электрофореза |
199 |
капилляр не промывается (не появляется капля на выходе капилляра при промывке)
|
Причина |
Способ устранения |
|
|
в капилляре и в пробирке на |
поставьте на вход капилляра пробирку с дистиллирован- |
|
|
входе капилляра находится |
||
|
ной водой и заполните жидкостью капилляр |
||
|
воздух |
||
|
плохое уплотнение стакан- |
опустите и поднимите снова стаканчик с пробиркой на |
|
|
чика на входе капилляра или |
входе капилляра; на ручке подъемного механизма должно |
|
|
кассеты с капилляром во вход- |
чувствоваться небольшое усилие; проверьте, правильно |
|
|
ном узле; при этом показания |
ли отрезана крышка пробирки; подведите под вход ка- |
|
|
давления либо всегда близки |
пилляра другой стаканчик, попробуйте с ним промыть |
|
|
к нулю, либо быстро уменьша- |
капилляр |
|
|
ются |
подтяните левый винт крепления кассеты |
|
|
откройте крышку кассетного отделения, отверните два |
||
|
винта крепления кассеты, аккуратно выньте кассету с |
||
|
капилляром; один из концов капилляра при помощи поли- |
||
|
этиленового капилляра соедините с иглой шприца запол- |
||
|
ненного дистиллированной водой; попробуйте промыть |
||
|
засорился капилляр |
капилляр |
|
|
если капилляр не промывается при помощи шприца, опус- |
||
|
тите оба конца капилляра в емкость с горячей водой не ме- |
||
|
нее чем на 15 мин.; снова попробуйте промыть капилляр |
||
|
при помощи шприца |
||
|
если капилляр не промывается, его следует заменить |
||
|
нет пиков на электрофореграмме |
||
|
Причина |
Способ устранения |
|
|
засорился капилляр (нет капли |
||
|
на выходном конце капилляра |
промойте капилляр, в крайнем случае, замените его |
|
|
в режиме «Промывка») |
||
|
мал объем пробы, конец ка- |
||
|
пилляра не достает до пробы в |
увеличьте объем пробы в пробирке Эппендорф |
|
|
пробирке и она не вводится в |
||
|
капилляр |
||
|
не соблюдены условия анализа |
проверьте условия анализа (качественный и количествен- |
|
|
ный состав буфера, напряжение (ток), параметры ввода |
||
|
по МВИ |
||
|
пробы, геометрию капилляра, температуру, длину волны) |
||
|
вещество пробы не поглощает |
||
|
или слишком слабо поглощает |
измените методику измерений |
|
|
ультрафиолетовое излучение на |
||
|
длине волны детектирования |
||
большой дрейф и шум базовой линии
|
Причина |
Способ устранения |
грязный буфер
замените буфер, профильтруйте его через мембранный фильтр и отцентрифугируйте
грязный капилляр
промойте капилляр 0,5 М раствором NaOH, дистиллированной водой, буфером

|
200 |
Система капиллярного электрофореза «Капель» |
|
|
слишком большое напряжение, |
||
|
буфер в капилляре сильно нагре- |
уменьшите напряжение или измените концентрацию буфера |
|
|
вается с выделением мелких пу- |
||
|
зырьков растворенного в нем газа |
||
|
прибор не успел прогреться |
подождите 30 мин. |
|
|
не горит лампа (при этом сиг- |
выключите и снова включите прибор. Если за 10 мин. |
|
|
налы по опорному и фото кана- |
||
|
лампа не зажглась, ее следует заменить |
||
|
лам порядка 0,000… В) |
||
|
не включается высокое напряжение |
||
|
Причина |
Способ устранения |
|
|
неправильное положение вход- |
поднимите обе пробирки в рабочее положение |
|
|
ной или выходной пробирок |
||
|
не до конца вставлен сменный |
вставьте сменный блок высокого напряжения до упора, |
|
|
блок высокого напряжения |
плотнее завинтите фиксирующие винты |
|
высокое напряжение подано и индицируется на дисплее прибора или на мониторе ПК, но ток равен нулю
|
Причина |
Способ устранения |
|
пузырек воздуха в капилляре |
дегазируйте буфер; установите условия анализа согласно |
|
(недостаточно дегазирован бу- |
МВИ или снизьте концентрацию, температуру |
|
фер, в ходе анализа использова- |
и напряжение в ходе анализа |
|
ны слишком высокие значения |
обязательно удалите из капилляра буфер с пузырьками |
|
напряжения и температуры при |
воздуха, промыв капилляр новой порцией подготовленного |
|
высокой концентрации буфера) |
буфера |
|
колебания температуры системы охлаждения в пределах нескольких градусов |
|
|
Причина |
Способ устранения |
|
нет (или мало) воды в системе |
выключите прибор, долейте воду и снова запустите систе- |
|
охлаждения |
му охлаждения |
|
при вынимании кассеты из кассетного отсека из нее вытекает жидкость |
|
|
Причина |
Способ устранения |
|
не снята лавсановая трубка с за- |
перед выниманием кассеты обязательно снимите трубку |
|
глушки в верхней части кассеты |
с заглушки и дайте стечь теплоносителю |
при запуске анализа ПО не переходит в режим «Ожидание», а выдает окно «О программе „МультиХром для Windows“»
|
Причина |
Способ устранения |
|
отсутствие или неисправность |
вставьте ключ в LPTили USB-порт системного блока |
|
электронного ключа HASP |
компьютера |
|
в данный момент производи- |
|
|
лась печать на принтер, под- |
не производите печать на принтер, подключенный |
|
ключенный через электрон- |
через электронный ключ HASP, когда идет анализ |
|
ный ключ HASP |
|
|
Глава 9. Общие рекомендации по работе с системами капиллярного электрофореза |
201 |
после запуска анализа на приборе ПО «МультиХром» остается в режиме «Ожидание» и не переходит в режим «Измерение»
|
Причина |
Способ устранения |
|
проверьте соединение между разъемом RS-232 прибора и |
|
|
нет связи прибор–компьютер |
COM-портом компьютера; проверьте исправность соедини- |
|
тельного кабеля, разъема RS-232 и COM-порта |
|
|
неправильно настроен про- |
|
|
токол обмена прибора или |
|
|
интерфейс COM-порта, к кото- |
проверьте протокол обмена прибора (должен стоять |
|
рому подключено и настроено |
«1-МультиХром») и интерфейс COM-порта, на который на- |
|
ПО «МультиХром» (при этом в |
строено ПО «МультиХром» (должен стоять «Capel») |
|
строке состояния появляется |
|
|
«Ошибка синхронизации») |
|
|
неправильно настроен сбор |
для метода, в котором записываются электрофореграммы, |
|
данных метода |
выставьте правильный COM-порт |
при построении градуировочной зависимости на электрофореграмме показаны концентрации, не соответствующие указанным в таблице концентраций
|
Причина |
Способ устранения |
в «Отчете» указан метод расчета отличный от «Заказного» (одной из причин этого может
в меню «Опции отчета» установите «Метод расчета —
быть удаление всех строк «Таблицы компонентов»)
Заказной»
Приложение А
Хорошая лабораторная практика при использовании систем капиллярного электрофореза
Берегите от пыли электроды и оптику.
Храните электроды и капилляры в воде между рабочими днями и в выходные (в буферах — в зависимости от их состава).
Используйте один капилляр на одну методику для повышения воспроизводимости результатов измерений.
Подберите оптимальный режим кондиционирования и промывки капилляра
до, между и по окончании анализа.
Для ускорения процесса кондиционирования капилляра используйте промывку буфером под напряжением, однако никогда не делайте это с растворами сильных электролитов!
Во избежание загрязнения после ввода пробы конец капилляра, соприкасавшийся с пробой, следует окунуть в промежуточный раствор с буфером, а уже затем в буфер для анализа. Составы обоих буферов одинаковы!
Фильтруйте и дегазируйте растворы буфера и пробы перед анализом.
По окончании работы освободите прибор от всех пробирок, кроме водных, в которые погружены концы капилляра.
Консервируйте систему КЭ при длительных перерывах в работе (>3 недель).
Используйте пробирки и наконечники однократно. В крайнем случае, отделяйте и тщательно мойте то, что соприкасалось с концентрированными или загрязненными образцами.
Время от времени контролируйте важные параметры анализа:
—величину тока, особенно при смене партии буфера,
—давление (герметичность системы ввода),
—параметры детектора,
—уровень жидкости в системе охлаждения капилляра (стабильность температуры).
Приложение Б
Тестирование систем капиллярного электрофореза «Капель»: проверка работоспособности прибора,
контроль качества подготовки капилляра
Тестирование систем КЭ «Капель» проводится в целях оперативной проверки работоспособности систем, а также для контроля качества подготовки капилляра к работе.
В состав тест-раствора входят три определяемых компонента, порядок миграции которых соответствует порядку перечисления: метка ЭОП — бензиловый спирт, N-фенилантраниловая кислота (N-ФАК) в виде натриевой или литиевой соли, бензойная кислота также в виде соли. Электропроводность и рН раствора определяются наличием буры в концентрации 0,001 М.
Б1. Приготовление запасных и рабочих растворов
Запасный раствор бензилового спирта концентрации 0,4 % (об.).
В мерной колбе вместимостью 100 мл смешивают 400 мкл перегнанного бензилового спирта с 10 мл ацетонитрила. В отдельном сосуде смешивают 30 мл ацетонитрила и 60 мл воды. Полученным раствором заполняют мерную колбу до метки, и тщательно перемешивают.
Запасный раствор N-фенилантраниловой кислоты массовой концентрации 1 мг/мл.
В мерную колбу вместимостью 100 мл последовательно помещают 100 мг N-фе- нилантраниловой кислоты (ч. д. а.) и 50 мг безводного карбоната натрия. Растворяют кислоту, добавляя небольшими порциями горячую дистиллированную воду до полного растворения. Раствор охлаждают, разбавляют водой до метки и перемешивают.
Запасный раствор бензойной кислоты массовой концентрации 1 мг/мл.
В мерную колбу вместимостью 100 мл последовательно помещают 100 мг бензойной кислоты (ч. или ч. д. а.) и 50 мг безводного карбоната натрия. Растворяют кислоту, добавляя небольшими порциями горячую дистиллированную воду до полного растворения. Раствор охлаждают, разбавляют водой до метки и перемешивают.
Запасный раствор буры молярной концентрации 0,05 М.
Раствор готовят из стандарт-титра, предназначенного для кислотно-основных титрований, согласно инструкции. При отсутствии стандарт-титра раствор можно приготовить из х. ч. препарата десятиводного кристаллогидрата натрия тетраборнокислого, растворив в мерной колбе вместимостью 1 л навеску массой 19,071 г. в свежепрокипяченной и охлажденной без доступа воздуха дистиллированной воде.
Примечание. Запасные растворы хранят в полиэтиленовой таре, защищая от воздействия углекислого газа. Срок хранения раствора буры — 2 месяца, всех остальных растворов — не ограничен.
|
204 |
Фирма аналитического приборостроения «Люмэкс» |
Рабочий раствор буры молярной концентрации 0,01 М
В мерную колбу вместимостью 50 мл помещают 10 мл запасного раствора буры, разбавляют до метки дистиллированной водой и тщательно перемешивают. Этот же раствор можно приготовить непосредственно из рН-стандарта буры (рН 9,18 при 25 °С).
Тест-раствор
В мерную колбу вместимостью 100 мл последовательно помещают по 10 мл запасных растворов бензилового спирта и бензойной кислоты, 10 мл рабочего раствора буры и 5 мл запасного раствора N-фенилантраниловой кислоты. Смесь разбавляют до метки водой и перемешивают.
Б2. Условия тестирования
Для определения работоспособности системы капиллярного электрофореза «Капель» или правильности подготовки капилляра к работе проводят анализ тест-рас- твора в следующих условиях:
система КЭ «Капель» с положительной полярностью высокого напряжения;
капилляр: кварцевый, внутренний диамер 75 (50) мкм, эффективная/общая длина 50/60 (65/75) см;
ведущий электролит — 0,01 М раствор буры, рН 9,18;
ввод пробы — гидродинамический, 30 мбарх5 сек;
длина волны — 254 нм — для всех модификаций (для прибора «Капель 105 (М)» на выбор — 220 или 254 нм);
температура — комнатная (для приборов, имеющих жидкостную систему охлаждения капилляра, +20 °С);
анализ — напряжение +20 кВ, время анализа 10–15 минут.
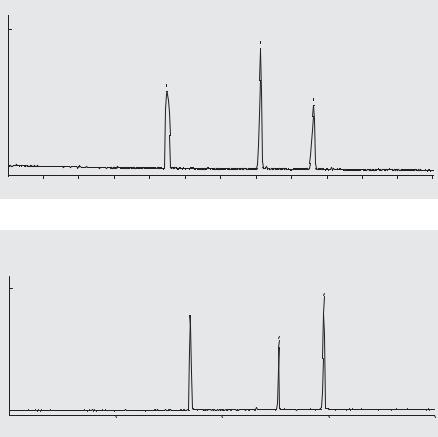
На электрофореграмме (рис. Б1) должны регистрироваться три пика:
Пик 1 — сравнительно широкий, гауссовой формы пик метки ЭОП, время выхода ~4,5 мин.;
Пики 2 и 3 — пики фенилантранилат- и бензоат-анионов с временами выхода ~7 и ~8,5 минут соответственно.
Примечание. Приведенные времена миграции пиков относятся к стандартному капилляру, используемому в системах «Капель» (внутр. диаметр 75 мкм, эффективная длина 50 см, полная длина 60 см). Для кассеты, предназначенной для аминокислотного анализа, в которой применяется капилляр внутренним диаметром 50 мкм и общей длиной 75 см, вид электрофореграммы и времена миграции показаны на рис. Б2.
Время миграции зоны ЭОП служит чувствительным индикатором кондиционного состояния капилляра. При загрязнении внутренней поверхности, особенно катионными и неионогенными поверхностно-активными веществами, время миграции зоны ЭОП увеличивается. Так как направление миграции анионов противоположно направлению ЭОП, то увеличение времени миграции зоны ЭОП приводит к непропорционально большому увеличению времени миграции анионов, что и является указанием на плохую подготовку капилляра.
При необходимости из электрофореграммы можно получить дополнительную информацию о качестве разделения и определения. Так, коэффициент разделения фенилантраниловой и бензойной кислот является мерой разделяющей способности капилляра. Анализ порций тест-раствора, разбавленных 0,001 М раствором буры в 10, 20 и 50 раз позволяет ориентировочно оценить уровень шумов и предел обнаружения бензойной кислоты, а также параметры сходимости измерений, т. е. оценить общее состояние прибора.
|
8 mAU |
ФАК |
|
N- |
|
|
ЭОП |
бензойная |
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
мин |
Рис. Б1. Электрофореграмма тест-раствора для стандартного капилляра.
|
ЭОП |
ФАК |
бензойная |
|
20,7 mAU |
||
|
N- |
Рис. Б2. Электрофореграмма тест-раствора для капилляра со спецгеометрией.
Примечание. Иногда требуется достаточно быстро проверить работоспособность системы капиллярного электрофореза, например, проверить наличие отклика прибора на раствор определяемого компонента при данной длине волны. Для этих целей удобно воспользоваться режимом «Промывка». Сначала капилляр промывают рабо-
|
206 |
Фирма аналитического приборостроения «Люмэкс» |
чим буфером или дистиллированной водой (здесь и далее — без напряжения). Затем на входном конце капилляра устанавливают пробирку с раствором анализируемого вещества и, включив регистрацию сигнала с помощью ПО «МультиХром» или аналогичного программного продукта, начинают промывать капилляр этим раствором не менее 60 сек.
Если при выбранной длине волны раствор анализируемого вещества имеют достаточную оптическую плотность, сигнал будет записан в виде ступени. В первые 15–17 сек. (для стандартной геометрии капилляра: внутренний диаметр 75 мкм, общая длина 60 см) фотометр регистрирует прохождение через окно детектора прозрачного растворителя — буфера или воды, которыми предварительно был заполнен капилляр. Затем в зону детектирования начинает поступать сильно поглощающий раствор. Оптическая плотность возрастает и к 22–25 секунде достигает предельного постоянного значения.
При невозможности сбора данных на компьютер сигналы регистрируют визуально с дисплея «Капели»: уровень нулевого сигнала (А0) считывают до начала подъёма ступени, а предельное значение (Апр) — после, записывая стабилизированное показание. Разность (Апр– А0) есть высота ступени, т. е. оптическая плотность тестового раствора, или фактическая мера чувствительности фотометра.
Наличие ступени однозначно говорит о том, что прибор «видит» анализируемое вещество, т. е. данный компонент можно зарегистрировать при выбранной длине волны, подобрав и при необходимости оптимизировав условия разделения и детектирования.
Приложение В
Ручная промывка капилляра с помощью медицинского шприца
Изложенная в этом приложении схема промывки капилляра может помочь в случае, когда капилляр засорился по вине плохо очищенного буфера или пробы. Кассету с капилляром предварительно необходимо вынуть из прибора. Обратите внимание, что в приборах с жидкостным охлаждением капилляре следует предварительно слить воду из системы охлаждения.
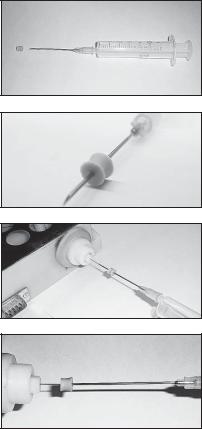
Нам понадобятся следующие материалы:
одноразовый медицинский пластиковый инсулиновый шприц вместимостью 1 мл с иглой (можно использовать шприцы большего объема, например 2 и 5 мл),
кусочек эластичной резины или силикона (обычно можно найти в комплекте ЗИП к прибору «Капель»),
дистиллированная вода (лучше подогретая до 50–60 °С).
Сначала набираем в шприц дистиллированную воду и надеваем на иглу силиконовую прокладку.
После этого аккуратно вставляем выходной конец капилляра в иглу шприца на глубину 20–30 мм.
Далее сдвигаем силиконовую прокладку так, чтобы она герметизировала соединение капилляра и иглы шприца.

|
208 |
Фирма аналитического приборостроения «Люмэкс» |
После этого следует достаточно сильно надавить на поршень пластикового шприца до появления капли на входном конце капилляра. При этом на соединительном участке возможно образование капли и даже брызг, поэтому работать с кассетой лучше на отдельном пустом столе, покрытом листом фильтровальной бумаги, вдали от прибора.
Наш опыт показывает, что чаще всего такого рода загрязнение возникает на входном участке капилляра, поэтому промывка проводится со стороны выхода. Тем не менее, допускается дополнительная промывка и в обратном направлении.
Если вышеописанная процедура не помогает, капилляр можно обрезать. Для этого необходимо при помощи скальпеля, керамического резачка для вскрытия ампул или хозяйственного ножа с острым лезвием нанести однократный надрез на полимерное покрытие капилляра со стороны входа (1–2 мм от конца капилляра), поместить в место надреза каплю дистиллированной воды, после чего при помощи пинцета осторожно отломить надрезанный кончик и проверить капилляр, промыв водой из шприца, наблюдая за появлением капли.
Важно!
Следите за тем, чтобы надрезанный конец капилляра имел срез строго под углом 90°. В противном случае, пики компонентов могут приобрести форму с «хвостами», а также может снизиться воспроизводимость ввода.
Помните, что Вы надрезаете участок капилляра, участвующий в разделении до зоны детектирования. В случае уменьшения эффективной длины капилляра на 2–3 мм, никаких заметных изменений в параметрах миграции, величине тока и т. д. наблюдаться не будет. Если же Вам придется значительно (более 1 см) укоротить капилляр с входного участка, то мы рекомендуем в случае качественной и количественной обработки результатов заложить обновленные данные (время миграции и площадь пика) в градуировочные таблицы.
Если после среза входного конца капилляра и промывки водой из шприца на выходном участке не появилась капля, то следует отрезать 1 мм выходной части капилляра, после чего во время промывки водой ожидать каплю на входе в капилляр.

Авторы: Н. В. Комарова, Я. С. Каменцев
Практическое руководство по использованию систем капиллярного электрофореза «КАПЕЛЬ»
В авторской редакции
Над книгой работали: В. М. Дружихина, Е.В. Родионенко, Е. К. Невоя
Сдано в набор 02.07.2008 г. Подписано в печать 07.07.2008 г. Бумага мелованная. Гарнитура Таймс. Печать офсетная.
Усл. печ. л. 15,5. Тираж 2000 экз. (доп. тираж); . Заказ № 8116.
ООО «Веда», Санкт-Петербург, ул. Итальянская, д. 29, оф. 5
Отпечатано в типографии ООО «Группа М», Санкт-Петербург, ул. Профессора Попова, д. 4а
