Неонатальный сепсис является инвазивной инфекцией, как правило, бактериальной, развивающейся в неонатальном периоде. Симптомы сепсиса многообразны, неспецифичны и включают снижение спонтанной активности, плохое сосание при кормлении, апноэ, брадикардию, колебания температуры тела, расстройство дыхания, рвоту, диарею, вздутие живота, повышенную нервную возбудимость, судороги и желтуху. Диагноз ставят на основании клинических данных и результатов культуральных тестов. Лечение начинают с комбинации ампициллина с гентамицином или цефотаксимом, переходя в дальнейшем на препараты более чувствительные к выявленному возбудителю.
Неонатальный сепсис выявляют с частотой 0,5–8,0 на 1000 новорожденных. Наиболее высокие показатели встречаются у:
-
детей с низкой массой тела (НМТ) при рождении
-
Меньшинство
-
Мужчины
Начало неонатального сепсиса может быть
-
Ранним (≤ 3 дней после рождения)
-
Поздним (после 3 дней)
Сепсис новорожденных с ранним началом, как правило, вызывают микроорганизмы, приобретенные во время родов. Большинство детей имеют симптомы в течение 6 часов после рождения.
В развитии сепсиса с ранним началом в большинстве случаев играют роль стрептококки группы В Стрептококковые инфекции Стрептококки – грамположительные аэробные организмы, вызывающие множество заболеваний, включая фарингит, пневмонию, инфекции ран и кожи, сепсис и эндокардит. Симптомы изменяются в зависимости… Прочитайте дополнительные сведения 
Причиной большинства других случаев являются грамотрицательные кишечные бактерии (например, виды Klebsiella Инфекции, вызываемые Klebsiella, Enterobacter, и Serratia Грамотрицательные бактерии Klebsiella, Enterobacter и Serratia – тесно связанная нормальная флора кишечника, которая редко вызывает заболевание у здоровых хозяев. Диагноз… Прочитайте дополнительные сведения ) и определенные грамположительные микроорганизмы (Listeria monocytogenes Листериоз Листериоз может вызывать различные формы инфекции у человека, такие как бактериемия, менингит, энцефалит, дерматит, окулогляндулярный синдром, внутриматочные и неонатальные инфекции или, редко… Прочитайте дополнительные сведения , энтерококки Энтерококковые инфекции Энтерококки являются грамположительными факультативными аэробными организмами. Enterococcus faecalis и E. faecium вызывают различные инфекции, включая эндокардит, инфекцию мочевых… Прочитайте дополнительные сведения [например, Enterococcus faecalis, E. faecium], стрептококки группы D Стрептококковые инфекции Стрептококки – грамположительные аэробные организмы, вызывающие множество заболеваний, включая фарингит, пневмонию, инфекции ран и кожи, сепсис и эндокардит. Симптомы изменяются в зависимости… Прочитайте дополнительные сведения 




При сепсисе новорожденных с поздним началом возбудитель обычно попадает из окружающей среды (Внутрибольничные инфекции у новорожденных Внутрибольничные инфекции у новорожденных Некоторые инфекции являются приобретенными после помещения в палату новорожденных, а не передаются от матери внутриутробно или время родов. Для некоторых инфекций (например, стрептококки группы… Прочитайте дополнительные сведения ). Стафилококки Стафилококковые инфекции Стафилококки – грамположительные аэробные микроорганизмы. Staphylococcus aureus наиболее патогенный; как правило, он вызывает инфекции кожи, может вызывать пневмонию, эндокардит и остеомиелит… Прочитайте дополнительные сведения 
Хотя всеобщий скрининг и интранатальная антибиотикопрофилактика инфекций, вызванных стрептококками группы B, значительно снизили частоту раннего начала заболеваний, вызванных этим организмом, частота сепсиса с поздним началом осталась неизменной.
Некоторые вирусные инфекции (например, диссеминированная ВПГ-инфекция Неонатальная инфекция вирусом простого герпеса (ВПГ) Неонатальная инфекция, вызванная ВПГ, обычно передается ребенку во время родов. Типичным признаком является везикулезная сыпь, которая может сопровождаться или прогрессировать до диссеминированной… Прочитайте дополнительные сведения 
Некоторые перинатальные и акушерские факторы, связанные с матерью, увеличивают риск, особенно раннего неонатального сепсиса, в следующих случаях:
-
Колонизация стафилококками группы В
Гематогенная и трансплацентарная диссеминация материнской инфекции происходит при передаче некоторых вирусов (например, краснухи Врожденная краснуха Врожденная краснуха является вирусной инфекцией, передаваемой от матери ребенку во время беременности. Признаками этого заболевания являются множественные врожденные аномалии, которые могут… Прочитайте дополнительные сведения , цитомегаловируса Врожденная и перинатальная цитомегаловирусная (ЦМВ) Цитомегаловирусная инфекция может быть приобретена пренатально или перинатально и является наиболее распространенной врожденной вирусной инфекцией. Признаками при рождении, если они присутствуют… Прочитайте дополнительные сведения 



Хотя интенсивность колонизации у матери напрямую связана с риском развития инвазивного заболевания у новорожденных, многие матери с низкой плотностью колонизации рожают детей с высокой плотностью колонизации. Околоплодные воды, контаминированные меконием или сыровидной смазкой, способствуют росту стрептококков группы B и E. coli. Таким образом, некоторые микроорганизмы свода влагалища способны быстро размножаться после преждевременного разрыва плодных оболочек. Организмы обычно достигают кровотока плода в результате аспирации или проглатывания контаминированной амниотической жидкости, что приводит к бактериемии.
Восходящий путь передачи инфекции помогает объяснить такие явления, как высокая частота преждевременного разрыва околоплодных оболочек при неонатальных инфекциях, значение воспаления придатков (амнионит чаще ассоциируется с неонатальным сепсисом, чем центральные плацентиты), повышенный риск развития инфекций у близнеца, расположенного ближе к родовым путям, а также бактериологические характеристики неонатального сепсиса с ранним началом, отражающие состав флоры свода влагалища матери.
Наиболее важным фактором риска при позднем сепсисе являются:
Другие факторы риска включают в себя:
-
Длительное применение внутрисосудистых катетеров
-
Ассоциированные заболевания (могут быть маркерами только при использовании инвазивных процедур)
-
Воздействие антибиотиков (которое отбирает устойчивые штаммы бактерий)
-
Длительная госпитализация
-
контаминированное оборудование, или внутривенно либо энтерально вводимые растворы
Грамположительные микроорганизмы (например, коагулазонегативные стафилококки и Staphylococcus aureus) могут попасть из окружающей среды или с кожи пациента. Грамотрицательные кишечные бактерии, как правило, попадают из эндогенной флоры пациента, которая, возможно, была изменена предшествующей антибактериальной терапией или заселена резистентными микроорганизмами, попавшими с рук персонала (основной способ распространения) или контаминированного оборудования. Таким образом, ситуации, повышающие экспозицию этим бактериям (например, скученность населения, нехватка младшего медицинского персонала, неадекватная обработка рук), повышают распространенность внутрибольничных инфекций.
Факторы риска развития сепсиса, вызванного видами Candida, включают длительное (> 10 дней) использование центральных внутривенных катетеров, перекармливание, использование антибиотиков предыдущего поколения (особенно цефалоспоринов 3-го поколения) или патологию органов брюшной полости.
Начальные очаги инфекции могут находиться в мочевыводящих путях, придаточных пазухах носа, среднем ухе, легких или в пищеварительном тракте и в дальнейшем могут диссеминировать в менингеальные оболочки, почки, кости, суставы, брюшину и кожу.
Симптомы и признаки неонатального сепсиса
Ранние признаки сепсиса новорожденных часто являются неспецифическими и не различаются для разных микроорганизмов (включая вирусы). Особенно частые ранние признаки включают:
-
Сниженную спонтанную активность
-
Плохое сосание
-
Анорексию
-
Апноэ
-
Брадикардию
-
Колебания температуры тела (гипотермия или гипертермия)
Температура повышается только у 10–15% новорожденных, но если она сохраняется (например, > 1 часа), это обычно указывает на инфекцию. Другие симптомы и признаки включают дыхательную недостаточность, неврологические симптомы (например, судороги, повышенную нервную возбудимость), желтуху (особенно возникающую в течение первых 24 часов жизни при отсутствии несовместимости по группам крови систем Rh или АВО и с более высокой, чем ожидалось, концентрацией прямого билирубина), рвоту, диарею и вздутие живота.
При наличии специфических признаков пораженного органа можно заподозрить возбудителя инфекции или причину (этиологию) их возникновения.
-
Большинство новорожденных с ранним началом инфицированности стрептококками группы B (и многие с L. monocytogenes) имеют дыхательную недостаточность, которую трудно отличить от респираторного дистресс-синдрома.
-
Периумбиликальная эритема, выделения или кровотечения без геморрагического диатеза предполагают наличие омфалита.
-
Кома, судороги, опистотонус или выбухающий родничок могут свидетельствовать о наличии менингита, энцефалита или абсцесса мозга.
-
Сниженные спонтанные движения конечностей и отек, повышение температуры, покраснение или болезненность суставов указывают на остеомиелит или гнойный артрит.
-
Необъяснимое вздутие живота может указывать на перитонит или некротический энтероколит (особенно в сочетании с кровавой диареей и наличием лейкоцитов в фекалиях).
-
Кожные везикулы, язвы во рту и гепатоспленомегалия (в частности, с диссеминированным внутрисосудистым свертыванием [ДВС]) могут указывать на диссеминированную ВПГ-инфекцию.
Инфекция, вызванная стрептококками группы B (СГВ), с ранним началом может проявляться в виде скоротечной пневмонии. Часто выявляют акушерские осложнения (особенно у недоношенных детей, при преждевременном разрыве плодных оболочек или хориоамнионите). У > 50% новорожденных инфицированность стрептококками группы B проявляется в течение 6 ч после рождения. 45% новорожденных имеют оценку по шкале APGAR < 5 баллов. Могут присутствовать признаки менингита, но с меньшей частотой. При инфекции с поздним началом (от 3 дней до 12 недель), вызванной стрептококками группы B, часто развивается менингит. Инфекции с поздним началом, вызванные стрептококками группы B, как правило, не связаны с перинатальными факторами риска или очевидной колонизацией шейки матки матери и могут быть приобретены после родов.
-
Высокая степень подозрения наличия заболевания
-
Кровь, цереброспинальная жидкость (ЦСЖ), а иногда и посев мочи
Ранняя диагностика неонатального сепсиса имеет важное значение и требует знания факторов риска (особенно у новорожденных с низкой массой тела при рождении), а также сильного сомнения при любых отклонениях от нормы у новорожденного в первые недели жизни.
Общее количество лейкоцитов и лейкоцитарная формула у новорожденных являются недостаточными предикторами сепсиса с ранним началом. Однако повышенное отношение незрелых форм ко всем полиморфноядерным лейкоцитам > 0,16 чувствительно, и значения ниже указанного числа имеют высокую отрицательную прогностическую ценность. Тем не менее, специфичность низка; до 50% доношенных новорожденных имеют повышенное соотношение. Значения, полученные через 6 часов жизни, более вероятно будут отличаться от нормы и клинически полезны, чем значения, полученные сразу после родов.
Число тромбоцитов может снижаться за несколько часов или дней до появления клинических проявлений сепсиса, но чаще всего остается повышенным до возникновения клинических симптомов или в течение нескольких дней после их появления. Это иногда сопровождается другими симптомами диссеминированного внутрисосудистого свертывания (ДВС) (например, усиленная деградация продуктов фибрина, снижение уровня фибриногена, повышенное международное нормализованное отношение [МНО]). Учитывая сроки этих изменений, количество тромбоцитов обычно не полезно в оценке новорожденного на возможность развития сепсиса.
Из-за большого числа циркулирующих бактерий микроорганизмы иногда можно обнаружить прямо или косвенно связанными с полиморфноядерными лейкоцитами, применяя окрашивание по Граму, метиленовым синим или акридиновым оранжевым лейкоцитарной пленки.
Независимо от результатов общего анализа крови (ОАК) или спинномозговой пункции, у всех новорожденных с подозрением на сепсис (например, выглядящих больными, а также с лихорадкой или гипотермией) следует немедленно начинать применять антибактериальную терапию после получения результатов бактериологического посева (например, крови и спинномозговой жидкости [по возможности]).
Сосуды пуповины часто контаминируются микроорганизмами в месте пуповинного остатка, особенно через несколько часов, поэтому посев крови из пупочного венозного катетера малоинформативен. Таким образом, кровь для культурального исследования должны быть получена путем венепункции, предпочтительно с 2 периферийных участков. Хотя оптимальная подготовка кожи для выполнения получения культуры крови у новорожденных не определена, врачи могут применить йод-содержащие жидкости и дать месту высохнуть. Кроме того, кровь, полученная вскоре после размещения пупочного артериального катетера, может быть также использована для культурального исследования, если это необходимо.
Посев крови следует проводить как на аэробных, так и на анаэробных средах. Тем не менее, минимальное количество крови, необходимое для флакона для культурального исследования крови составляет 1,0 мл; если получено < 2 мл, ее следует разместить в отдельный аэробный флакон для культурального исследования крови. При подозрении на катетер-ассоциированный сепсис образец для посева должен быть получен как через катетер, так и из периферической вены. В > 90% случаев при положительном результате культурального метода рост выявляют в течение 48 часов. Недостаточно данных для того, чтобы рекомендовать посев капиллярной крови.
Виды Candida выращивают в культурах крови и на пластинах кровяного агара, но если есть подозрение на другие грибы, нужно использовать культуральную среду для грибов. Другие виды грибов, кроме Candida, могут давать положительный результат культурального метода только через 4–5 дней, и результат теста может быть отрицательным даже при явно диссеминированном заболевании. Подтверждение колонизации (во рту, в стуле или на коже) может быть полезно, пока не получены результаты посева. Новорожденным с кандидемией следует провести ЛП для выявления кандидозного менингита. Проводят непрямую офтальмоскопию с расширением зрачков для выявления кандидозного поражения сетчатки. УЗИ почек проводят для выявления почечной мицетомы.
Анализ мочи необходим только для оценки сепсиса с поздним началом. Моча должна быть получена путем катетеризации или надлобковой пункции. Хотя только культуральный метод является диагностическим, выявление ≥5 лейкоцитов в поле зрения или любых микроорганизмов в свежей порции мочи, окрашенной по Граму, предположительно доказывает инфекцию мочевыводящих путей. Отсутствие пиурии не исключает такую инфекцию.
Многочисленные анализы часто имеют отклонения при сепсисе, они были оценены как возможные ранние маркеры. В целом, однако, чувствительность их имеет тенденцию к снижению на поздних стадиях заболевания, а специфичность является субоптимальной. Наличие биомаркеров не считается нужным для определения начала приема антибиотиков при неонатальном сепсисе, из-за их низкой положительной прогностической ценности. Они могут играть вспомогательную роль в определении, приемлемого момента для прекращения антибиотикотерапии, если культура остается отрицательной при подозрении на сепсис с ранним началом.
Белки острой фазы воспаления — это белки, вырабатываемые печенью под воздействием IL-1 при наличии воспаления. Наиболее изученным из них является количественный С-реактивный белок. Его концентрация ≥ 1 мг/дл (9,52 нмоль/л) (измеренная методом нефелометрии) обычно считается аномальной. Повышение уровней возникает в течение 6–8 часов от начала развития сепсиса и достигают пика на 1-й день. Чувствительность определения С-реактивного белка выше, если оно проводится после 6–8 часов жизни. Два нормальных значения, получены в период между 8 и 24 ч после рождения, а затем через 24 ч имеют отрицательную прогностическую ценность 99,7%.
Прокальцитонин исследуется как маркер реакции острой фазы неонатального сепсиса. Хотя прокальцитонин кажется более чувствительным, чем C-реактивный белок, он менее специфический (1 Справочные материалы по диагностике Неонатальный сепсис является инвазивной инфекцией, как правило, бактериальной, развивающейся в неонатальном периоде. Симптомы сепсиса многообразны, неспецифичны и включают снижение спонтанной… Прочитайте дополнительные сведения ). Комбинация биомаркеров, которая включает прокальцитонин и С-реактивный белок, может оказаться более полезной для определения длительности антибиотикотерапии (2 Справочные материалы по диагностике Неонатальный сепсис является инвазивной инфекцией, как правило, бактериальной, развивающейся в неонатальном периоде. Симптомы сепсиса многообразны, неспецифичны и включают снижение спонтанной… Прочитайте дополнительные сведения ).
-
1. Pontrelli G, De Crescenzo F, Buzzetti R, et al: Accuracy of serum procalcitonin for the diagnosis of sepsis in neonates and children with systemic inflammatory syndrome: A meta-analysis. BMC Infect Dis 17(1):302, 2017. doi: 10.1186/s12879-017-2396-7
-
2. Stocker M, van Herk W, El Helou S, et al: C-reactive protein, procalcitonin, and white blood count to rule out neonatal early-onset sepsis within 36 hours: A secondary analysis of the neonatal procalcitonin intervention study. Clin Infect Dis 73(2):e383–e390, 2021. doi: 10.1093/cid/ciaa876
Недоношенные дети, рожденные с низкой массой тела, имеют летальность в 2–4 раза выше, чем у доношенных новорожденных. Общая смертность при раннем начале сепсиса составляет 3 – 40% (при инфекции, вызванной стрептококками группы B с ранним началом, она составляет 2 – 10%) и при позднем начале сепсиса – 2 – 20% (при стрептококковой типа B инфекции с поздним началом составляет около 2%). Смертность от сепсиса с поздним началом значительно зависит от этиологии инфекции; уровень смертности при инфекциях, вызванных грамотрицательными бактериями или видами Candida составляет 32–36%. В дополнение к смертности, новорожденные с очень низкой массой тела при рождении, у которых развивается бактериальный сепсис или кандидоз, имеют значительно более высокий риск неблагоприятных неврологических следствий.
-
Антибиотикотерапия
-
Поддерживающая терапия
Основные поддерживающие мероприятия, в том числе управление дыханием и гемодинамикой, комбинируют с антибиотикотерапией.
При позднем сепсисе, здоровым новорожденным из окружения, в котором распространен поздний сепсис, также назначают лечение в виде ампициллина в сочетании с гентамицином или ампициллина в сочетании с цефотаксимом. При подозрении на грамотрицательный менингит можно применять ампициллин, цефотаксим и аминогликозиды. При внутрибольничном сепсисе с поздним началом стартовая терапия должна включать ванкомицин (активен в отношении метициллин-резистентного S. aureus; см. таблицу дозирования ванкомицина для новорожденных [Table Vancomycin Dosage for Neonates ]) плюс аминогликозиды. При преобладании в палате новорожденных P. aeruginosa, можно применять цефтазидим, цефепим или пиперациллин/тазобактам в дополнение, или вместо, аминогликозидов в зависимости от местной восприимчивости.
Для новорожденных, ранее получивших полный 7–14-дневный курс аминогликозидов, и нуждающихся в повторном лечении, должен быть рассмотрены другие варианты аминогликозидов или цефалоспоринов 3-го поколения.
При подозрении на коагулазонегативные стафилококки (например, при использовании постоянного катетера > 72 часов) или при их выделении из крови или других в норме стерильных жидкостей, а также если именно эти микроорганизмы считают возбудителями, стартовая терапия сепсиса с поздним началом должна включать ванкомицин. Однако если возбудитель чувствителен к нафциллину, ванкомицин нужно заменить на цефазолин или нафциллин. Удаление предполагаемого источника инфекции (обычно внутрисосудистого катетера) необходимо для лечения инфекции, поскольку коагулазонегативные стафилококки могут быть защищены биопленкой (оболочка, способствующая присоединению микроорганизмов к катетеру).
Так как при посеве крови грибы рода Candida могут расти 2–3 дня, начало эмпирической терапии амфотерицином В деоксихолатом и удаление инфицированного катетера до момента получения положительного результата наличия грибковой инфекции в гемокультуре может спасти жизнь ребенку.
Обменное переливание крови ранее использовали для тяжелобольных (в частности, с гипотензией и метаболическим ацидозом) новорожденных. Их предполагаемые значения состоят в повышении уровня циркулирующих иммуноглобулинов, снижении количества циркулирующего эндотоксина, повышении уровня гемоглобина (с более высоким уровнем 2,3-бисфосфоглицерина) и улучшении перфузии. Тем не менее ни одного контролируемого проспективного исследования не проводилось.
Свежезамороженная плазма может помочь восстановить недостаточность термостабильного и термолабильного опсонина, которая развивается у маловесных новорожденных, но контролируемые исследования об ее использовании недоступны и следует рассматривать риски, связанные с переливанием.
Рекомбинантные колониестимулирующие факторы (гранулоцитарный колониестимулирующий фактор [G-CSF] и колониестимулирующий фактор гранулоцитов-макрофагов [GM-CSF]) повышают количество нейтрофилов и активность у новорожденных с предполагаемым сепсисом, но не считаются полезными у новорожденных с тяжелой нейтропенией; требуется дальнейшее изучение.
Новорожденные, выглядящие здоровыми, могут быть подвержены риску инфицирования стрептококками группы B. Центры по контролю и профилактике заболеваний (ЦКЗ) и Американская академия педиатрии (AAП) в настоящее время рекомендуют лечить этих детей в зависимости от нескольких факторов (1 Справочные материалы по профилактике Неонатальный сепсис является инвазивной инфекцией, как правило, бактериальной, развивающейся в неонатальном периоде. Симптомы сепсиса многообразны, неспецифичны и включают снижение спонтанной… Прочитайте дополнительные сведения , 2 Справочные материалы по профилактике Неонатальный сепсис является инвазивной инфекцией, как правило, бактериальной, развивающейся в неонатальном периоде. Симптомы сепсиса многообразны, неспецифичны и включают снижение спонтанной… Прочитайте дополнительные сведения ), в том числе учитывать:
-
наличие хориоамнионита;
-
гестационный возраст и длительность разрыва околоплодных оболочек
При отсутствии хориоамнионита и показаний для профилактики инфекции, вызываемой стрептококками группы В, тестирование и лечение не показано.
Если с материнской стороны была показана и соответственно проведена профилактика стрептококка группы В (т.е., был введен пенициллин, ампициллин, цефазолин внутривенно в течение ≥ 4 часов), младенцев необходимо наблюдать в больнице в течение 48 часов; тестирование и лечение осуществляется только при развитии симптомов. Отдельные пациенты, рожденные в сроке гестации ≥ 37 недель, имеющие надежных опекунов и свободный доступ к медицинскому контролю могут вернуться домой после 24 часов.
Если соответствующая профилактика стрептококка группы В не была проведена, новорожденные наблюдаются в больнице в течение 48 часов без антибактериальной терапии. Если время после разрыва околоплодных оболочек ≥ 18 часов до рождения или гестационный возраст < 37 недель, то рекомендуется сразу после рождения и/или в первые 6-12 ч жизни провести посев крови, ОАК с лейкоцитарной формулой, и, возможно, определение уровня С-реактивного белка. Руководство по клиническому течению и оценке лабораторных результатов.
Эффективность внутривенного введения иммуноглобулина для повышения иммунной реактивности новорожденного не была доказана для предотвращения или лечения сепсиса.
Все беременные женщины должны пройти скрининг на колонизацию стрептококками группы В на поздних сроках беременности с использованием вагинальной и ректальной культур.
Женщинам с положительным тестом на стрептококки группы В следует провести профилактику антибиотиками во время родов, за исключением тех, кому проводят кесарево сечение до начала родов и до разрыва околоплодных оболочек.
Женщины с отрицательным анализом на стрептококки группы Б должны получать антибиотики во время родов, если ранее они родили ребенка с болезнью, вызванной стрептококками группы В.
Женщины с неизвестным статусом по стрептококкам группы В (например, потому что им не проводилось тестирование, или его результаты недоступны) должны получать антибиотики ао время родов при наличиии 1 или более из нижеследующих факторов:
-
< 37 недель гестации
-
Разрыв оболочек в течение ≥ 18 часов
-
Температура ≥ 38° C
-
Возможно, если имелся положительный результат скрининга на стрептококки группы В во время предыдущей беременности
Как правило, применяемые антибиотики включают пенициллин, ампициллин или цефазолин, и их необходимо ввести за ≥ 4 часа до родов. При выборе следует принимать во внимание эндемический вид стрептококков группы В, резистентный к антибиотикотерапии.
-
1. Brady MT, Polin RA: Prevention and management of infants with suspected or proven neonatal sepsis. Pediatrics 132:166-8, 2013. doi: 10.1542/peds.2013-1310
-
2. Polin RA and the Committee on Fetus and Newborn: Management of neonates with suspected or proven early-onset bacterial sepsis. Pediatrics 129:1006-1015, 2012. doi: 10.1542/peds.2012-0541
-
4. Puopolo KM, Lynfield R, Cummings JJ, et al: Management of infants at risk for group B streptococcal disease. Pediatrics 144(2):e20191881, 2019. doi: 10.1542/peds.2019-1881
-
Неонатальный сепсис может быть с ранним началом (≤ 3 дней после рождения) или с поздним началом (после 3 дней).
-
Сепсис с ранним началом, как правило, вызывают возбудители, приобретенные во время родов, а симптомы проявляются в течение 6 часов после рождения.
-
Сепсис с поздним началом обычно приобретается из окружающей среды и чаще развиваеися у недоношенных младенцев, особенно при длительной госпитализации и/или использовании внутривенных катетеров.
-
Ранние признаки часто неспецифичны и едва различимы, а лихорадка присутствует только у 10–15% новорожденных.
-
Следует провести культуральное исследование крови и спинномозговой жидкости, а при сепсисе с поздним началом также провести посев мочи.
-
Лечение сепсиса с ранним началом начинают с комбинации ампициллина с гентамицином и/или цефотаксимом при подозрении на грамотрицательный менингит, переходя как можно скорее на препараты чувствительные к выявленному возбудителю.
-
Провести профилактику заражения стрептококком группы В (СГБ) во время родов женщинам с риском передачи СГБ новорожденному.
Бактериальный сепсис новорожденного
Версия: Клинические протоколы МЗ РК — 2023 (Казахстан)
Категории МКБ:
Бактериальный сепсис новорожденного (P36)
Разделы медицины:
Неонатология, Педиатрия
Общая информация
Краткое описание
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «28» июля 2023 года
Протокол №185
КЛИНИЧЕСКИЙ ПРОТОКОЛ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
БАКТЕРИАЛЬНЫЙ СЕПСИС НОВОРОЖДЕННОГО
Сепсис новорожденного – это патологический процесс, в основе которого лежит реакция организма в виде генерализованного (системного) воспаления на бактериальную инфекцию в сочетании с остро возникшими признаками системной дисфункции и доказательствами микробной диссеминации [1].
ВВОДНАЯ ЧАСТЬ
Коды МКБ-10:
Дата разработки/пересмотра протокола:2014 год (пересмотр 2023 г.).
Пользователи протокола: неонатологи, педиатры, врачи общей практики, врачи скорой и неотложной медицинской помощи, анестезиологи и реаниматологи.
Категория пациентов: новорожденные дети.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+), результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование, или мнение экспертов. |
Облачная МИС «МедЭлемент»
Классификация
Классификация бактериального сепсиса новорожденных [1]:
- Ранний неонатальный сепсис (РНС) ─ инфицирование микроорганизмами, приобретенными во время родов (вертикальная передача) с реализацией процесса в первые 72 часа после рождения.
- Поздний неонатальный сепсис (ПНС) ─ инфицирование микрофлорой окружающей среды (горизонтальная передача) с реализацией процесса позже 72 часов после рождения ‒ внутрибольничная инфекция (ВБИ).
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Основные диагностические мероприятия:
- Оценить факторы риска развития раннего и позднего сепсиса.
- Оценить клинические симптомы раннего и позднего сепсиса (физикальное обследование).
- Провести лабораторные и другие дополнительные исследования.
Оценить факторы риска развития раннего неонатального сепсиса.
Таблица 1. Факторы риска развития раннего неонатального сепсиса [17]:
| Настораживающий фактор риска из группы «Красный флаг*»: |
|
| Другие факторы риска: |
|
Примечание: *Наличие фактора, выделенного как «Красный флаг» свидетельствует о высоком риске реализации раннего неонатального сепсиса.
Таблица 2. Факторы риска развития позднего неонатального сепсиса [17]:
- Недоношенность, маловесный к сроку гестации.
- Искусственная вентиляция легких.
- Хирургические вмешательства.
- Вскармливание искусственными смесями.
- Длительное необоснованное парентеральное питание.
- Длительное использование внутрисосудистых катетеров.
- Несоблюдение правил гигиены рук.
- Частые инвазивные процедуры.
- Отсутствие контакта с матерью.
- Неадекватная антибактериальная терапия.
- Нецентрализованное приготовление препаратов парентерального питания.
- Дефицит изделий медицинского назначения одноразового использования или перебой их поставки.
- Либеральное использование инвазивных процедур.
- Нерациональная антибактериальная терапия.
- Неоптимальное соотношение медсестра/пациент.
Физикальное обследование:
Типичной клинической картины сепсиса не существует. Клинические симптомы неонатального сепсиса часто неспецифичны и поэтому о развитии у новорожденного тяжелой бактериальной инфекции можно подозревать при появлении следующих симптомов (правило трех «П»):
- «плохо дышит»;
- «плохо ест»;
- «плохо выглядит»
с последующим выявлением в динамике клинических признаков, представленных в таблицах 3 и 4, отражающих различную степень выраженности полиорганной недостаточности у новорожденного ребенка.
Таблица 3. Клинические признаки раннего неонатального сепсиса 17]:
| Клинические признаки из группы «Красный флаг»: |
|
| Другие клинические показатели: |
|
Таблица 4. Клинические признаки позднего неонатального сепсиса [17]
|
Категория |
Клинические признаки |
| Поведение |
● Обеспокоенность родителей или медицинского работника по поводу изменения поведения ребенка: — ребенок постоянно спит и, если его разбудить, не бодрствует; — крик слабый, болезненный или непрерывный. |
| Респираторная система |
● Повышенная частота дыханий: 60 дыханий в минуту и более. ● Стонущее дыхание. ● Апноэ. ● Насыщение кислородом менее 90% при дыхании комнатным воздухом или повышенная потребность в кислороде в динамике. |
| Сердечно-сосудистая система |
● Постоянная тахикардия: ЧСС 160 ударов в минуту и более или стойкая брадикардия: ЧСС менее 100 ударов в минуту. ● Симптом белого пятна более 3 секунд. ● Холодные конечности. |
| Кожные покровы |
● Цианоз конечностей, носогубного треугольника, языка. ● Бледно-серый колорит кожных покровов, нередко с геморрагическими высыпаниями, не бледнеющими при надавливании. |
| Другие признаки |
● Температура тела 380С, не связанная с температурой окружающей среды. ● Температура тела менее 360С, не связанная с температурой окружающей среды. ● Вздутие живота. ● Судороги. ● Выбухание большего родничка. ● Изменение поведения при кормлении. |
Лабораторные исследования
Бактериологическое исследование крови (для определения возбудителя) и тест на чувствительность к антибиотикам:
— выполняется до начала антибактериальной терапии;
— строгое соблюдение стерильности забора крови;
— достаточное количество крови (не менее 1 мл);
— забор крови проводится из отдельной вены, избегать забора крови на посев из вены пуповины;
— не брать кровь на посев из катетера, который используется для инфузии или введения медикаментов;
— сразу после рождения (у новорожденных с факторами риска у матери) можно взять кровь из культи пуповины (между двумя зажимами);
— посев крови следует проводить как на аэробных, так и на анаэробных средах;
NB! Если в течение 72 часов нет роста ─ вероятность бактериемии очень мала [1].
Общий анализ крови:
- количество лейкоцитов: <5000/мм3 или >20000 /мм3 (>30000/мм3 в первые 2-3 дня жизни);
- абсолютное количество нейтрофилов (тест более чувствителен, чем общее количество лейкоцитов):
- нейтрофилез в первые 1-2 дня ˃20000,
- на 3-7 день ˃7000 и
- более 7 дня ˃6000
- или нейтропения в первые 1-2 дня ˂5000,
- на 3-7 день ˂2000 и
- более 7 дня ˂1500;
- лейкоцитарный индекс: отношение незрелых форм нейтрофилов к общему количеству (зрелых и незрелых) нейтрофилов >0,2;
- тромбоцитопения <150000/мкл.
- Ускоренное СОЭ;
С-реактивный белок (белок острой фазы воспаления) [3,9]: увеличение СРБ (> 10 мг/л непосредственно после родов, > 20(-40) мг/л плюс клинические симптомы через 24 часа (наиболее высокая положительная и отрицательная предиктивная значимость).
- Если концентрация СРБ в крови не превышает 10 мг/л, отрицательная прогностическая ценность составляет 97‐99.5%, т.е. очень малая вероятность, что новорожденный имеет сепсис.
- Дважды определенный отрицательный уровень СРБ через 8-24 часа после рождения и через 24 часа после первого определения, имеет отрицательную прогностическую ценность в 99,7% случаев.
Прокальцитонин (белок острой фазы воспаления) [9,10] — его концентрация увеличивается уже через 4 часа после инфицирования, достигая максимальных величин через 6‐8 ч. Однако концентрация ПКТ, определяемая в первые часы после рождения, повышается у новорожденных не только в ответ на воспаление, но и при асфиксии, РДС, пневмотораксе, что свидетельствует о ее не специфичности для оценки риска реализации раннего неонатального сепсиса.
NB! У здорового новорожденного концентрация прокальцитонина в сыворотке крови составляет 1.5‐2.5 мкг/л и меняется в зависимости от постнатального возраста ребенка, а также при состояниях неинфекционного генеза (асфиксия и
др.).
Для планирования терапевтической тактики и определения необходимости ее модификации, а также для определения потребности в сопутствующей терапии рекомендовано выполнить по показаниям следующие диагностические исследования:
- Газы крови – метаболический/смешанный ацидоз, повышение уровня лактата;
- Бактериологическое исследование спинномозговой жидкости (при клиническом подозрении на менингит: напряженный родничок, судороги, помутнение сознания), в ликворограмме – плеоцитоз и повышение уровня белка;
- Коагулограмма: коагулопатия потребления; повышенное протромбиновое время и частичное тромбопластиновое время, снижение уровня фибриногена.
- Биохимический анализ крови: повышение АЛТ и АСТ, щелочной фосфатазы, билирубина за счет прямой фракции, мочевины, креатинина, азотемия;
- Повышенный показатель интерлейкина-6 (факультативно, референсные показатели в зависимости от лаборатории);
- Измененный гомеостаз глюкозы (гипогликемия или гипергликемия);
- Общий анализ мочи при подозрении на инфекцию мочевых путей;
- ПЦР на TORCH инфекцию;
- При обильных гнойных выделениях из глаз (могут указывать на серьезную хламидийную или гонококковую инфекцию) ─ мазок на бактериологическое исследование и чувствительность к антибиотикам;
- Мазок на культуру содержимого из локальных очагов инфекции (при их наличии) и чувствительность к антибиотикам.
Инструментальные исследования (при наличии показаний):
● Рентгенография органов грудной клетки – двустороннее снижение прозрачности легочной ткани с рентген прозрачными зонами, образованными воздухом в главных дыхательных путях («воздушные бронхограммы»); возможен плевральный выпот; пневматоцеле (при стафилококковой пневмонии).
● Рентгенография пораженного сустава/пораженной конечности при подозрении на остеомиелит/остеоартрит: утолщение надкостницы, признаки разрушения кости, отек мягких тканей, накопление жидкости.
● Рентгенография органов брюшной полости при некротическом энтероколите зависит от стадии заболевания (смотрите клинический протокол «Некротизирующий энтероколит»).
● Эхокардиография для оценки гемодинамического статуса при септическом шоке и подбора вазопрессорных и инотропных препаратов.
● Нейросонография (при наличии судорог, при признаках нарушения ЦНС).
● УЗИ пораженного сустава (при подозрении на остеомиелит и остеоартрит).
NB:
! Не рекомендуется проводить бактериологическое исследование мазков с кожи при отсутствии клинических признаков локализованной инфекции.
! Следует помнить, что референсные нормы лабораторных показателей зависят от срока гестации и возраста ребенка.
! Если это безопасно (состояние ребенка позволяет), рекомендуется выполнение люмбальной пункции для получения образца спинномозговой жидкости, когда:
— имеется серьезное клиническое подозрение на ранний неонатальный сепсис;
— или имеются клинические симптомы или признаки, указывающие на менингит (приложение №1).
Показания для консультации узких специалистов (при наличии показаний, при трудностях диагностики, оценки тяжести состояний, для выбора оптимальной тактики лечения):
- консультация хирурга при подозрении на НЭК, перитонит и плеврит;
- консультация невролога при подозрении на менингит, ВЖК, родовую травму;
- консультация кардиолога при подозрении на эндокардит;
- консультация травматолога при подозрении на остеомиелит и остеоартрит;
- консультация нефролога при подозрении на ИМП и ОПП.
Диагностический алгоритм: (приложение №3)
Дифференциальный диагноз
Дифференциальный диагноз и обоснование дополнительных исследований:
|
Диагноз |
Обоснование для дифференциальной диагностики | Обследования |
Критерии исключения диагноза сепсис |
| ПЛГН |
Тяжесть и не стабильное состояние ребенка; Не стабильная гемодинамика; Потребность в «жестких» параметрах ИВЛ;
Потребность в высоких концентрациях О2; |
Бакпосев крови; ОАК; СРБ; рентгенография органов грудной клетки; ЭхоКГ; Оценка разницы пре-, постдуктальной сатурации |
Потребность в высоких концентрациях О2, в «жестких» параметрах ИВЛ; ЭхоКГ: высокое давление в легочной артерии, увеличение правых отделов сердца, регургитация на уровне трискупидального клапана и т.д. |
| Заболевания легких (синдром мекониальной аспирации, РДС, диафрагмальная грыжа, пневмоторакс и другие формы легочной гипоплазии. |
Тяжесть и не стабильное состояние ребенка; Не стабильная гемодинамика; Потребность в «жестких» параметрах ИВЛ; Потребность в высоких концентрациях О2; Потребность в высоких концентрациях вазопрессоров и инотропов |
Бакпосев крови; ОАК; СРБ; рентгенография органов грудной клетки; ЭхоКГ; Оценка разницы пре-, постдуктальной сатурации |
РДС: преждевременные роды, отсутствие антенатальной стероидной профилактики, на рентгене снижение объема легких, наличие воздушной бронхограммы, снижение пневмотизации ткани легких; Синдром мекониальной аспирации: В анамнезе запоздалые роды, наличие мекония в околоплодных водах, ребенок при рождении неактивный . На рентгенографии – признаки «снежной бури»; Диафрагмальная грыжа – ладьевидный живот, на рентгене наличие органов брюшной полости в грудной клетке, смещение органов средостения в сторону, признаки выраженной дыхательной недостаточности; Пневмоторакс – на рентгенографии органов грудной клетки- наличие воздуха во внелегочном пространстве. |
| ВПС |
Тяжесть и не стабильное состояние ребенка; Не стабильная гемодинамика; Потребность в «жестких» параметрах ИВЛ; Потребность в высоких концентрациях О2; Потребность в высоких концентрациях вазопрессоров и инотропов |
Измерение предуктальной и постдуктальной сатурации; проведение гипероксического и гипервентиляцион-ного тестов; измерение артериального давления на верхней и нижней конечностях; рентегнография органов грудной клетки; ЭхоКГ с допплеровским картированием |
При коарктации дуги аорты характерна разница артериального давления в верхних и нижних конечностях; ЭхоКГ основной метод дифференциальной диагностики ВПС и сепсиса. |
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ: нет.
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ.
Карта наблюдения пациента, маршрутизация пациента:
- При обнаружении у новорожденного, находящегося в родовспомогательной организации 1-го или 2-го уровней хотя бы 2-х симптомов, указанных в подпункте 2.5, следует организовать его перевод в родовспомогательную организацию 3-го уровня (в отделение интенсивной терапии или патологии новорожденных, по показаниям).
Немедикаментозное лечение.
Поддерживающий уход:
- Оптимальный температурный режим, профилактика гипотермии, привлечение матери к уходу за ребенком, уход методом кенгуру, исключительно грудное вскармливание, при его невозможности — кормление сцеженным материнским грудным молоком любым альтернативным методом (шприц, ложка, чашка, зонд).
- Мониторинг состояния жизненно важных функций новорожденного.
- Строгое соблюдение всех положений инфекционного контроля, мытье рук до и после осмотра новорожденного, обучение матери уходу за ребенком.
Медикаментозное лечение:
Основные принципы антибактериальной терапии ребенка с неонатальным сепсисом [8,16,17,24,25]:
1. Поскольку сепсис может проявляться неспецифическими клиническими признаками и его последствия могут быть фатальными для ребенка, поэтому при наличии одного любого фактора риска или клинического признака из группы «Красный флаг», или двух или более факторов риска или клинических признаков, рекомендуется быстрое начало (в течение 1 часа) эмпирической антибактериальной терапии, не ожидая результатов анализов.
2. При решении вопроса о выборе антибиотиков можно использовать местные данные, адаптированные к местной эпидемиологической ситуации и профилю устойчивости патогенов.
3. При эмпирической антибактериальной терапии назначается комбинация антибиотиков узкого спектра действия, эффективных как против грамотрицательных, так и против грамположительных бактерий.
4. Не следует проводить рутинное лечение антибиотиками детям без факторов риска инфекции, или клинических и лабораторных признаков возможной инфекции.
5. При подозрении на развитие раннего неонатального сепсиса в качестве антибиотикотерапии первого выбора рекомендуется внутривенное введение бензилпенициллина/ампициллина с гентамицином, с последующей корректировкой в соответствии с чувствительностью возбудителя инфекции к антибиотикам.
6. Бензилпенициллин назначается в дозе 25 мг/кг через каждые 12 часов. Если
состояние ребенка оценивается очень тяжелым следует рассмотреть возможность сокращения интервала между дозами через каждые 8 часов.
7. Гентамицин вводится в начальной дозе 5 мг/кг, при этом следует помнить, что:
a. в перечне характеристик препарата рекомендуется дозировка от 4 до 7 мг/кг/день, вводимая в разовой дозе;
b. данные, рассмотренные для руководства, поддерживают начальную дозу 5 мг/кг каждые 36 часов, вводимую однократно;
c. вторая доза гентамицина вводится через 36 часов после первой дозы, однако возможен более короткий интервал, если ребенок выглядит очень больным и посев крови показывает грамотрицательную инфекцию.
d. при принятии решения о последующем режиме дозирования гентамицина необходимо учитывать его концентрацию в крови (при наличии возможности).
8. У детей, получающих антибиотики, рекомендуется ежедневная оценка клинических симптомов и, при необходимости, лабораторных данных, рассматривается возможность изменения режима антибиотикотерапии, принимая во внимание:
a. клиническое состояние ребенка (есть или нет улучшения);
b. результаты исследования биомаркеров;
c. результаты микробиологических исследований;
d. экспертные микробиологические рекомендации, включая данные местного эпиднадзора.
9. У детей, получающих антибиотики по наличию факторов риска или клинических признаков возможного сепсиса, следует:
a. проводить контроль уровня С-реактивного белка через 18–24 часа после начала антибактериальной терапии;
b. рассмотреть возможность проведения люмбальной пункции для получения образца спинномозговой жидкости при условии, что это не было сделано при поступлении и является безопасным, а также если:
— у ребенка при бактериологическом исследовании крови получен положительный результат или
— ребенок не отвечает удовлетворительно на лечение антибиотиками или
— у него имеются клинические симптомы или признаки, указывающие на менингит.
10. При лабораторном подтверждении роста бактерий, следует установить их грамм-принадлежность до определения чувствительности к антибиотикам, так как на это уходит более длительный период времени.
11. При бактериологическом подтверждении сепсиса, вызванного грамотрицательными бактериями, следует бензилпенициллин заменить на антибиотик, чувствительный к выделенному возбудителю сепсиса.
12. Оценка результатов лечения антибиотиками проводится после трех дней
лечения.
13. Если состояние ребенка улучшается и результат бактериологического посева крови отрицательный, следует прекратить лечение ампициллином и гентамицином после 3-5 дней терапии.
14. Если состояние ребенка улучшается при положительном бактериологическом посеве крови, то лечение ампициллином и гентамицином продолжается10 дней.
15. Если после трех дней лечения ампициллином и гентамицином состояние не улучшилось или ухудшилось, то проводится смена антибиотика согласно выявленного возбудителя и результата теста на чувствительность.
16. Для профилактики грибковой инфекции во время лечения антибиотиками поздних неонатальных инфекций назначается перорально нистатин.
17. Если пероральное введение нистатина невозможно, назначается флуконазол внутривенно.
18. Рутинное применение иммуноглобулина для лечения и профилактики сепсиса новорожденных не рекомендуется [13].
19. Следует помнить, что, хотя незначительный конъюнктивит встречается часто и имеет доброкачественный характер, гнойные выделения могут свидетельствовать о серьезной инфекции (например, хламидиоз или гонококковая инфекция).
20. У новорожденных детей с гнойными выделениями из глаз срочно берут мазки на микробиологическое исследование методами, позволяющими выявить хламидии и гонококки.
21. При высокой вероятности гонококковой инфекции начинают лечение системного заболевания антибиотиками, ожидая результатов микробиологического исследования мазка.
22. У детей с клиническими признаками пупочной инфекции (гнойные выделения или покраснение пуповинного остатка/пупочной ранки, отек или повышение температуры кожи) выполнить:
a. забор крови на бакпосев;
b. микроскопию мазка пупочного отделяемого и бакпосев;
c. начать лечение внутривенным введением антибиотиков: флуклоксациллин* и гентамицин.
23. Если результаты микробиологического исследования показывают, что инфекция не вызвана грамотрицательной бактерией, введение гентамицина прекратить.
Продолжительность лечения сепсиса (Приложение №2)
Решения через 36 часов у новорожденных с РНС и через 48 часов у новорожденных с ПНС (далее 36/48 часов) после начала лечения антибиотиками:
- У детей, получающих антибиотики по наличию факторов риска или клинических признаков возможного сепсиса, через 36/48 часов от начала антибактериальной терапии следует рассмотреть возможность прекращения введения антибиотиков, если:
— посев крови отрицательный;
— клиническое состояние ребенка удовлетворительное, клинические признаки возможной инфекции отсутствуют;
— уровни и тенденции концентрации С-реактивного белка, ПКТ не превышают нормальные показатели.
- Следует оценить возможность прекращения эмпирической антибактериальной терапии после 36/48 часов с учетом:
— уровня первоначального риска реализации инфекции;
— динамики клинической картины и состояния новорожденного;
— уровня и динамики СРБ.
Продолжительность лечения неонатального сепсиса без менингита [17] (Приложение №3)
- Детям с положительным посевом крови и детям с отрицательным результатом посева крови, но с наличием факторов риска, свидетельствующих о высоком риске реализации неонатального сепсиса, лечение антибиотиками проводится в течение 7 дней.
- Продолжение лечения антибиотиками более 7 дней может быть рассмотрено, если:
— ребенок еще не полностью выздоровел или
— целесообразность продолжения обусловлена идентификацией возбудителя при бактериологическом исследовании крови (при необходимости следует обратиться за консультацией к специалисту-микробиологу) или
— требуется более длительное лечение из-за наличия сопутствующей патологии, такой как некротизирующий энтероколит, остеомиелит или катетер-ассоциированная инфекция, обусловленная постановкой центрального венозного катетера).
- При продолжении антибиотикотерапии более 7 дней, несмотря на отрицательный результат посева крови, следует проводить клиническое обследование ребенка не реже одного раза каждые 24 часа. При этом необходимо решить, следует ли прекратить прием антибиотиков, принимая во внимание:
— клинический прогресс и текущее состояние ребенка;
— уровни и тенденции С-реактивного белка, ПКТ.
Продолжительность лечения неонатального сепсиса при подозрении или подтвержденном менингите у детей с ранним и поздним началом сепсиса:
1. Если ребенок находится в неонатальном отделении и есть подозрение на менингит, но возбудитель неизвестен (например, из-за неинформативности окраски по Граму спинномозговой жидкости), лечение проводится внутривенным введением амоксициллина и цефотаксима.
2. Если установлено (культуральное исследование спинномозговой жидкости), что менингит вызван грамотрицательной инфекцией, следует отменить амоксициллин и проводить лечение только цефотаксимом.
3. Если установлено, что менингит вызван грамположительными бактериями:
— продолжить лечение внутривенным амоксициллином и цефотаксимом, ожидая результатов посева спинномозговой жидкости и
— обратиться за консультацией к специалисту по микробиологии.
4. Если культура спинномозговой жидкости положительна на стрептококк группы B, следует рассмотреть возможность изменения лечения антибиотиками на:
— бензилпенициллин 50 мг/кг каждые 12 часов, обычно в течение не менее 14 дней и
— гентамицин, с начальной дозой 5 мг/кг каждые 36 часов; последующие дозы и интервалы при необходимости корректируются на основании клинической оценки и концентрации гентамицина в крови;
— курс лечения 5 дней.
5. Если посев крови или цереброспинальной жидкости положителен на листерии, следует рассмотреть возможность прекращения приема цефотаксима и лечить согласно чувствительности к антибиотикам или амоксициллином и гентамицином.
6. Если бакпосев спинномозговой жидкости выявил грамположительные бактерии, но не стрептококков группы В и листерии, следует обратиться за консультацией к специалисту-микробиологу по вопросам лечения.
7. При подборе антибактериальных препаратов необходимо ориентироваться на последнюю редакцию «Neofax» [18].
8. В качестве альтернативной схемы ведения новорожденного с гестационным возрастом ≥34 недели и с риском реализации раннего неонатального сепсиса и контроля правильности его диагностики используется калькулятор Kaiser Permanente [20]. Калькулятор следует использовать только в том случае, если это часть проведения проспективного мониторинга, который должен фиксировать:
— общее количество младенцев с факторами риска развития РНС, зарегистрированное с помощью калькулятора;
— число детей, правильно определенных калькулятором, у которых развилась неонатальная инфекция, подтвержденная бакпосевом крови;
— количество младенцев, неправильно идентифицированных калькулятором, у которых не развивается неонатальная инфекция, подтвержденная бакпосевом крови;
— число младенцев, пропущенных калькулятором, у которых развивается неонатальная инфекция, подтвержденная бакпосевом крови.
— Для использования онлайн калькулятора Kaiser Permanente с целью оценки риска раннего неонатального сепсиса используется классификация, данная в калькуляторе, чтобы принять правильные решения.
Общие принципы организации помощи новорожденному с сепсисом, проводимые по показаниям:
- Обеспечение суточной потребности в жидкости согласно массе тела и возраста ребенка, используя стандартизированные (заводского производства) и индивидуализированные растворы для парентерального питания доношенных [14,15], см. КП «Парентеральное питание»).
- Респираторная поддержка (CPAP, ИВЛ, ВЧ ИВЛ, см соответствующие КП).
- Коррекция электролитных нарушений – электролитов (калия, натрия, хлоридов, кальция; см. КП «Парентеральное питание»).
- Поддержка гемодинамики: допамин, добутамин, эпинефрин, норадреналин, вазопрессин.
- Коррекция нарушений гемостаза: в соответствии с изменениями в коагулограмме.
- Медикаментозное и немедикаментозное обезболивание по показаниям
- Симптоматическая терапия.
NB
! Дополнительное медикаментозное лечение проводится соответственно протоколам лечения развившихся осложнений.
Перечень основных лекарственных средств (имеющих 100% вероятность применения):
|
Лекарственная группа |
Лекарственные средства | Способ применения | Уровень доказательности |
| Антибиотик группы полусинтетических пенициллинов | Ампициллин |
Сепсис 34 недель и меньше: — младше 7 суток 50 мг/кг/доза в/в каждые 12 часов — старше 7 суток 75 мг/кг/доза в/в каждые 12 часов 34 недель и старше: — младше 7 суток 50 мг/кг/доза в/в каждые 8 часов — старше 7 суток 50 мг/кг/доза в/в каждые 8 часов Продолжительность: 10 дней при бактериемии без очага; более длительные сроки могут быть необходимы в тяжелых случаях Менингит: — младше 7 суток 100 мг/кг/доза в/в каждые 12 часов — старше 7 суток 75 мг/кг/доза в/в каждые 6 часов Продолжительность: курс лечения 14 дней при не осложненном менингите; более длительные сроки могут быть необходимы в тяжелых случаях |
А |
| Антибиотик группы биосинтетических пенициллинов | Бензилпенициллин |
Сепсис — младше 7 суток 50 000 Ед/кг/доза в/в каждые 8 часов — старше 7 суток 50 000 Ед/кг/доза в/в каждые 8 часов Продолжительность: 10 дней при бактериемии без очага; более длительные сроки могут быть необходимы тяжелых случаях Менингит: — младше 7 суток 150 000 Ед/кг/доза в/в каждые 8 часов — старше 7 суток 125 000 Ед/кг/доза в/в каждые 6 часов Продолжительность: курс лечения 14 дней при не осложненном менингите; более длительные сроки могут быть необходимы в тяжелых случаях |
А |
| Антибиотик группы аминогликозидов | Гентамицин |
29 недель и меньше: — 0 – 7 суток каждые 48 часов по 5 мг/кг в/в — 8 – 28 суток каждые 36 часов по 4 мг/кг в/в — 28 суток и старше каждые 24 часа по 4 мг/кг 30-34 недель: — младше 7 суток каждые 36 часов по 4,5 мг/кг — старше 7 суток каждые 24 часа по 4 мг/кг 35 недель и старше: — каждые 24 часа по 4 мг/кг Продолжительность антибактериальной терапии при определении чувствительности: — Бактериемия 10 дней — Менингит 14 дней — Септический артрит/остеомиелит 3–4 недели — Эндокардит не менее 4 недель |
А |
| Антибиотик группы аминогликозидов | Амикацин |
29 недель и меньше: — 0 – 7 суток каждые 48 часов по 14 мг/кг в/в — 8 – 28 суток каждые 36 часов по 12 мг/кг в/в — 28 суток и старше каждые 24 часа по 12 мг/кг 30-34 недель: — младше 7 суток каждые 36 часов по 12 мг/кг — старше 7 суток каждые 24 часа по 12 мг/кг 35 недель и старше: — каждые 24 часа по 12 мг/кг |
В |
Перечень дополнительных лекарственных средств (менее 100% вероятности применения).
|
Лекарственная группа |
МНН | Способ применения | Уровень доказательности |
| Антибиотик группы гликопептидов | Ванкомицин |
10-15 мг/кг/доза в/в 29 недель и меньше: — младше 14 суток каждые 18 часов — старше 14 суток каждые 12 часов 30-36 недель: — младше 14 суток каждые 12 часов — старше 14 суток каждые 8 часов 37-44 недель: — младше 7 суток каждые 12 часов — старше 7 суток каждые 8 часов Старше 45 недель: — каждые 6 часов. Продолжительность лечения 10 суток. |
А |
| Антибиотик группы пенициллинов широкого спектра действия с ингибитором бета-лактамаз | Пиперациллин/тазобактам |
100 мг/кг/доза в/в 29 недель и меньше: — младше 28 суток каждые 12 часов — старше 28 суток каждые 8 часов 30-36 недель: — младше 14 суток каждые 12 часов — старше 14 суток каждые 8 часов 37-44 недель: — младше 7 суток каждые 12 часов — старше 7 суток каждые 8 часов Старше 45 недель: — каждые 8 часов. При определении чувствительности терапия продолжается 7-14 суток. Более длительные сроки могут быть необходимы в тяжелых случаях. |
А |
| Антибиотик группы пенициллинов широкого спектра | Пиперациллин |
50 – 100 мг/кг/доза в/в 29 недель и меньше: — младше 28 суток каждые 12 часов — старше 28 суток каждые 8 часов 30-36 недель: — младше 14 суток каждые 12 часов — старше 14 суток каждые 8 часов 37-44 недель: — младше 7 суток каждые 12 часов — старше 7 суток каждые 8 часов Старше 45 недель: — каждые 6 часов. Подбор дозы зависит от тяжести течения заболевания. При определении чувствительности терапия продолжается 7-14 суток. Более длительные сроки могут быть необходимы в тяжелых случаях. |
В |
| Антибиотик группы цефалоспоринов I поколения | Цефазолин |
25 мг/кг/доза в/в 29 недель и меньше: — младше 28 суток каждые 12 часов — старше 28 суток каждые 8 часов 30-36 недель: — младше 14 суток каждые 12 часов — старше 14 суток каждые 8 часов 37-44 недель: — младше 7 суток каждые 12 часов — старше 7 суток каждые 8 часов Старше 45 недель:
— каждые 6 часов. |
В |
| Антибиотик группы цефалоспоринов IV поколения | Цефепим |
Доношенные и недоношенные дети до 28 суток: — 30 мг/кг/доза в/в каждые 12 часов Доношенные и недоношенные дети после 28 суток: — 50 мг/кг/доза в/в каждые 12 часов При менингите и при тяжелых инфекциях вследствие Pseudomonas aeruginosa или Enterobacter spp 50 мг/кг/доза в/в каждые 12 часов При определении чувствительности терапия продолжается 7-14 суток. Более длительные сроки могут быть необходимы в тяжелых случаях. |
В |
| Антибиотик группы цефалоспоринов III поколения | Цефотаксим |
— Вне зависимости от срока гестации, но младше 7 суток 50 мг/кг/доза в/в каждые 12 часов — Меньше 32 недель, но старше 7 суток 50 мг/кг/доза в/в каждые 8 часов — Старше 32 недель, но старше 7 суток 50 мг/кг/доза в/в каждые 6 часов При менингите: — В возрасте от 0 до 7 суток: 100-150 мг/кг/сут в/в разделенная на каждые 8-12 часов. Рассмотрите меньшую дозу и большой интервал у детей с массой тела меньше 2000 г — Старше 8 суток: 150-200 мг/кг/сут в/в разделенная на каждые 6 – 8 часов. Рассмотрите меньшую дозу и большой интервал у детей с массой тела меньше 2000 г. При определении чувствительности терапия продолжается 7-14 суток. Более длительные сроки могут быть необходимы в тяжелых случаях |
В |
| Антибиотик группы цефалоспоринов ІІІ поколения | Цефтазидим |
30 мг/кг/доза в/в 29 недель и меньше: — младше 28 суток каждые 12 часов — старше 28 суток каждые 8 часов 30-36 недель: — младше 14 суток каждые 12 часов — старше 14 суток каждые 8 часов 37-44 недель: — младше 7 суток каждые 12 часов — старше 7 суток каждые 8 часов Старше 45 недель: — каждые 8 часов. При менингите: — В возрасте от 0 до 7 суток: 100-150 мг/кг/сут в/в разделенная на каждые 8-12 часов. Рассмотрите меньшую дозу и большой интервал у детей с массой тела меньше 2000 г — Старше 8 суток: 150 мг/кг/сут в/в разделенная на каждые 8 часов. Рассмотрите меньшую дозу и большой интервал у детей с массой тела меньше 2000 г При определении чувствительности терапия продолжается 7-14 суток. Более длительные сроки могут быть необходимы в тяжелых случаях |
В |
| Антибиотик группы цефалоспоринов ІІІ поколения | Цефтриаксон |
— Сепсис: 50 мг/кг в/в каждые 24 часа — Менингит: 100 мг/кг в/в нагрузочная доза, затем 80 мг/кг в/в каждые 24 часа При определении чувствительности терапия продолжается 7-14 суток. Более длительные сроки могут быть необходимы в тяжелых случаях. |
А |
| Антибиотик группы пенициллинов | Нафцилин* |
Обычная доза 25 мг/кг/доза в/в При менингите 50 мг/кг/доза 29 недель и меньше: — младше 28 суток каждые 12 часов — старше 28 суток каждые 8 часов 30-36 недель: — младше 14 суток каждые 12 часов — старше 14 суток каждые 8 часов 37-44 недель: — младше 7 суток каждые 12 часов — старше 7 суток каждые 8 часов Старше 45 недель: — каждые 6 часов. Продолжительность лечения 10 суток. |
В |
| Антибиотик группы линкозамидов | Клиндамицин |
Обычная доза 5 – 7,5 мг/кг/доза в/в 29 недель и меньше: — младше 28 суток каждые 12 часов — старше 28 суток каждые 8 часов 30-36 недель: — младше 14 суток каждые 12 часов — старше 14 суток каждые 8 часов 37-44 недель: — младше 7 суток каждые 12 часов — старше 7 суток каждые 8 часов Старше 45 недель: — каждые 6 часов. При определении чувствительности продолжительность лечения 2 недели. |
В |
| Антибиотик группы карабапенемов | Меропенем |
При отсутствии бактериальной инфекции со стороны ЦНС: — меньше 32 недель и младше 14 суток – 20 мг/кг в/в каждые 12 часов — меньше 32 недель и старше 14 суток – 20 мг/кг в/в каждые 8 часов — старше 32 недель и младше 14 суток – 20 мг/кг в/в каждые 8 часов. — старше 32 недель и старше 14 суток – 30 мг/кг в/в каждые 8 часов. При менингите: — меньше 32 недель и младше 14 суток – 40 мг/кг в/в каждые 12 часов. — меньше 32 недель и старше 14 суток – 40 мг/кг в/в каждые 8 часов. — старше 32 недель – 40 мг/кг в/в каждые 8 часов. При определении чувствительности терапия продолжается 7-14 суток. Более длительные сроки могут быть необходимы в тяжелых случаях. |
В |
| Могут быть использованы антибактериальные препараты на которые имеются чувствительность в результатах бактериологических исследований при отсутствии противопоказаний с возрастом ребенка и токсичности препарата. |
*В соответствии с правилами применения незарегистрированных ЛС.
Хирургическое вмешательство:
При осложнении НЭК:
наличие клинической и рентгенологической картины перфорации кишечника, отека и гиперемии передней брюшной стенки, «неподвижная» петля кишки на серии рентгенограмм, выраженная тромбоцитопения, метаболический ацидоз – перевод в хирургическое отделение.
При осложнении и развитии пневмоторакса: пункция плевральной полости и постановка активного аспиратора (дренаж по Бюлау).
Дальнейшее ведение.
Первичная профилактика [4,14,15]:
- Профилактика инфекций, связанных с медицинской помощью (ИСМП) путем:
- строгого соблюдения всех положений инфекционного контроля, в частности, обработка рук до и после контакта с больным, при необходимости ― изоляция, использование одноразовых ИМН.
- Профилактическое ведение антибиотиков матерям в родах при наличии показаний.
- Минимальное использование инвазивных манипуляций.
- Уменьшение продолжительности использованния внутрисосудистых катетеров.
- Тщательное соблюдение асептики при подготовке растворов для внутрисосудистого введения.
- Ранний переход на полное энтеральное питание материнским грудным молоком.
- Обучение персонала и проверка его знаний положений инфекционного контроля.
- Обучение матерей обработке рук при уходе за ребенком.
- Привлечение матери к уходу за ребенком с соблюдением правил гигиены.
- Постоянный мониторинг больничных инфекций в отделении.
- Использование стандартизированного препарата для парентерального питания.
- Обеспечение контакта «кожа-к-коже» и метода кенгуру с соблюдением правил гигиены.
Индикаторы эффективности лечения и безопасности методов диагностики и лечения, описанных в протоколе:
- исчезновение симптомов заболевания и нормализация лабораторных показателей;
- отсутствие осложнений;
- проведение 1 курса антибактериальной терапии;
- минимальное пребывание новорожденного в отделении реанимации и интенсивной терапии.
Критерии выписки новорожденного:
- Стабильная температура тела (36,5 – 37,5⁰С), хорошо сосет, прибавляет в весе, признаки заболевания отсутствуют, результаты лабораторных исследований в пределах нормы.
- После выписки ― реабилитация в течение 1 года под наблюдением участкового педиатра, врача общей практики, фельдшера, медицинской сестры с соблюдением протокола «Уход за здоровым новорожденным ребенком».
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ:
Показания для плановой госпитализации: нет.
Показания для экстренной госпитализации:
- гипотермия или гипертермия (≤35,5ОС или >37,5 ОС);
- симптомы нарушения микроциркуляции (бледность кожных покровов с мраморным рисунком, цианотичным оттенком);
- дыхательные расстройства (апноэ, тахипноэ, брадипноэ, стонущее дыхание);
- артериальная гипотония;
- тахикардия/брадикардия;
- беспокойство или сонливость;
- судороги;
- непереносимость энтерального питания;
- желтуха, геморрагическая сыпь, кровоточивость.
Информация
Источники и литература
-
Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2023
- Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2023 — 1) Гельфанд Б.Р. Сепсис: классификация, клинико-диагностическая концепция и лечение: Практическое руководство 4-е изд., доп. и перераб. 2017. Издательство: МИА. 408 с.
2) AWMF-Leitlinie 024-008 Bakterielle Infektionen bei Neugeborenen, 31. 01. 2019, vidit 14.08.2020.
3) Polin RA and the Committee on Fetus and Newborn: Management of neonates with suspected or proven early-onset bacterial sepsis. Pediatrics 129:1006-1015, 2012. doi: 10.1542/peds.2012-0541.
4) Brady MT, Polin RA: Prevention and management of infants with suspected or proven neonatal sepsis. Pediatrics 132:166-8, 2013. doi: 10.1542/peds.2013-1310.
5) Heath Neonatal sepsis: an international perspective Archives of Disease in Childhood and Neonatal Edition. S. Vergnano. 2005; 90: F 220-FF22.
6) Dong Y, Speer CP. Late-onset neonatal sepsis: recent developments. Arch Dis Child Fetal Neonatal Ed 2015; 100: F257-63.
7) Kiser C, Nawab U, McKenna K, Aghai ZH. Role of guidelines on length of therapy in chorioamnionitis and neonatal sepsis. Pediatrics 2014;133:992-8.
Caffrey Osvald E, Prentice P. NICU clinical guideline: antibiotics for the prevention and treatment of early-onset neonatal infection. Arch Dis Child Educ Pract Ed 2014; 99:98-100.
9) Pontrelli G, De Crescenzo F, Buzzetti R, et al: Accuracy of serum procalcitonin for the diagnosis of sepsis in neonates and children with systemic inflammatory syndrome: A meta-analysis. BMC Infect Dis 17(1):302, 2017. doi: 10.1186/s12879-017-2396-7.
10) Stocker M, van Herk W, El Helou S, et al: C-reactive protein, procalcitonin, and white blood count to rule out neonatal early-onset sepsis within 36 hours: A secondary analysis of the neonatal procalcitonin intervention study. Clin Infect Dis 73(2):e383–e390, 2021. doi: 10.1093/cid/ciaa876.
11) Escobar GJ, Puopolo KM, Wi S, et al: Stratification of risk of early-onset sepsis in newborns ≥ 34 weeks’ gestation. Pediatrics 133(1):30–36, 2014. doi: 10.1542/peds. 2013-1689. Clarification and additional information. Pediatrics 134(1):193, 2014.
12) Puopolo KM, Benitz WE, Zaoutis TE. Management of Neonates Born at ≤34 6/7 Weeks’ Gestation With Suspected or Proven Early-Onset Bacterial Sepsis. Pediatrics. 2018;142(6):e20182896.
13) Puopolo KM, Benitz WE, Zaoutis TE. Management of Neonates Born at ≥35 0/7 Weeks’ Gestation With Suspected or Proven Early-Onset Bacterial Sepsis. Pediatrics. 2018;142(6):e20182894.
14) Puopolo KM, Lynfield R, Cummings JJ, et al: Management of infants at risk for group B streptococcal disease. Pediatrics 144(2):e20191881, 2019. doi: 1021542/peds. 2019-1881.
15) Ohlsson A, Lacy JB. Intravenous immunoglobulin for suspected or proven infection in neonates. Cochrane Database Syst Rev. 2020; 29:1(1):CD001239.
16) NICU Guideline. Neonatal parenteral nutrition NICE guideline Published: 26 February 2020 www.nice.org.uk/guidance/ng154.
17) Riskin A et al. The ESPGHAN / ESPEN / ESPR / CSPEN working group on pediatric parenteral nutrition ESPGHAN/ESPEN/ESPR Guidelines on pediatric parenteral nutrition: Standard versus individualized parenteral nutrition, Clinical Nutrition (2018).
18) Neonatal infection: antibiotics for prevention and treatment. NICE guideline Published: 20 April 2021 www.nice.org.uk/guidance/ ng195.
19) Neofax 2020.
20) Онлайн калькулятор раннего сепсиса новорожденных Kaiser Permanente https://neonatalsepsiscalculator.kaiserpermanente.org.
21) Roos R, Genzel- Boroviczény O. Checkliste Neoantologie, Thieme Verlag, 6. Auflage, 2018.
22) Children 2023, 10, 848. https://doi.org/10.3390/children10050848.
23) Recommended Antimicrobial Dosage Schedules for Neonates Meghan Mentink, PharmD, BCPPS; Hailey Steuber, PharmD, BCPPS; Sarah Tierney, PharmD, BCPPS; Jennifer Vejzovic, PharmD, BCPPS Updated June 2020.
24) Rallis, D.; Giapros, V.; Serbis, A.; Kosmeri, C.; Baltogianni, M. Fighting Antimicrobial Resistance in Neonatal Intensive Care Units: Rational Use of Antibiotics in Neonatal Sepsis. Antibiotics 2023, 12, 508. https://doi.org/10.3390/ antibiotics12030508
- Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2023 — 1) Гельфанд Б.Р. Сепсис: классификация, клинико-диагностическая концепция и лечение: Практическое руководство 4-е изд., доп. и перераб. 2017. Издательство: МИА. 408 с.
Информация
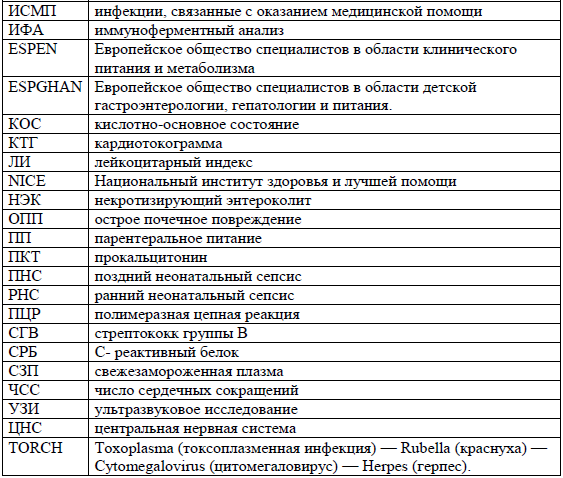
Сокращения, используемые в протоколе:
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ПРОТОКОЛА:
Список разработчиков протокола:
1) Чувакова Тамара Курмангалиевна – доктор медицинских наук, профессор кафедры неонатологии НАО «Медицинский университет Астана».
2) Джаксалыкова Куляш Каликановна – доктор медицинских наук, профессор, заведующая кафедрой неонатологии НАО «Медицинский университет Астана».
3) Карин Бектурган Тынымбаевич – магистр медицинских наук, ассистент кафедры неонатологии, НАО «Медицинский университет Астана».
4) Ахмадьяр Нуржамал Садыр – қызы – доктор медицинских наук, заведующая кафедрой клинической фармакологии НАО «Медицинский университет Астана», врач клинический фармаколог высшей категории.
Указание на отсутствие конфликта интересов: нет.
Рецензенты: Божбанбаева Нишанкуль Сейтбековна — доктор медицинских наук, заведующая кафедрой неонатологии КазНМУ имени Асфендиярова.
Указание условий пересмотра протокола: пересмотр протокола через 5 лет после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Приложение 1
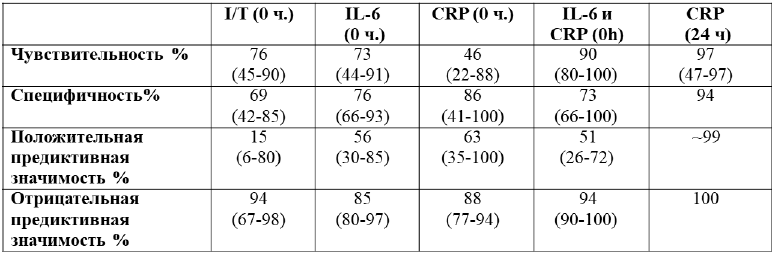
Чувствительность и специфичность, предиктивные показатели С-реактивного белка (CRP), интерлейкина-6 (IL-6), отношение I/T (отношение количества незрелых форм нейтрофилов к общему количеству нейтрофилов) в зависимости от промежутка времени между определением и 1 клиническим подозрением на инфекцию. Данные по руководству AWMF «Бактериальные инфекции новорожденных»
(): Количество часов после первого клинического подозрения
Верхняя граница референсных значений у здоровых новорожденных:
I/T 0,25; IL 6 50/100пг/мл, CRP 10мг/л.
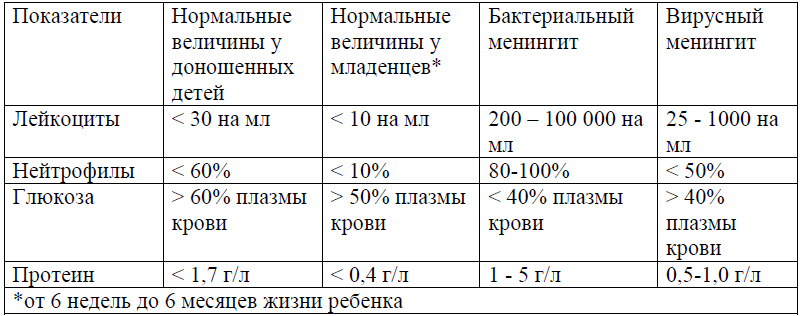
Показатели спинномозговой жидкости у новорожденных [21,22]
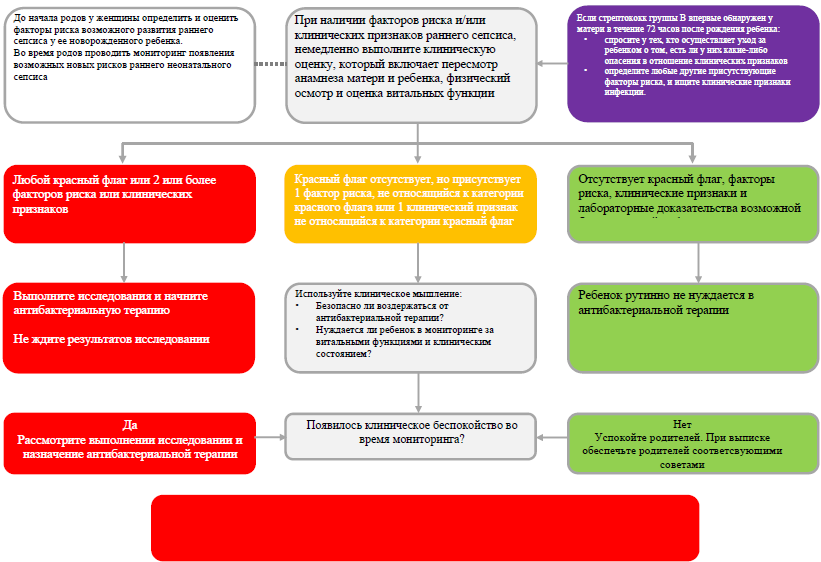
Приложение 3
Определение необходимости назначения антибактериальной терапии в первые 72 часа жизни (NICE 2021)
Приложение 4
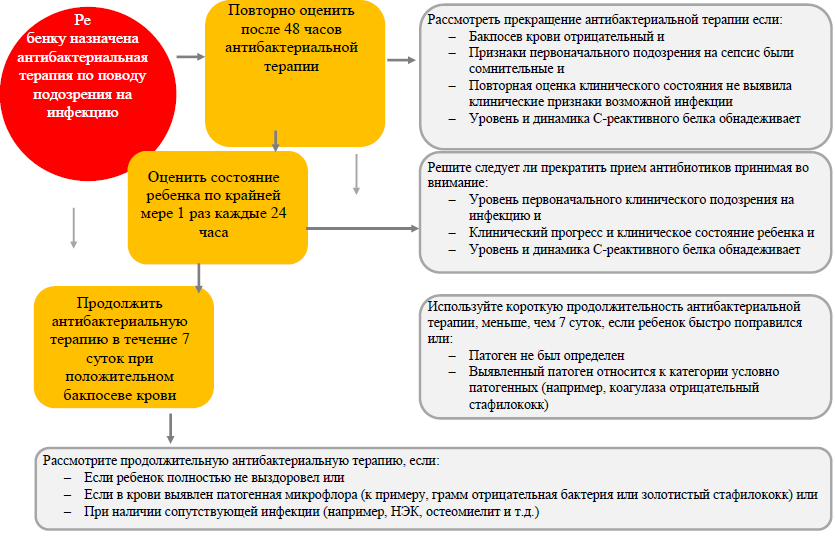
Продолжительность антибактериальной терапии при позднем неонатальном сепсисе без менингита [17]
Прикреплённые файлы
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники. Стандарты лечения
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.
NICE neonatal early onset sepsis guidance: greater consistency, but more investigations, and greater length of stay
Arindam Mukherjee et al.
Arch Dis Child Fetal Neonatal Ed.
2015 May.
Abstract
Background:
In August 2012, new national guidance (National Institute of Health and Care Excellence (NICE) CG149) for management of early onset sepsis (EOS) was introduced in the UK. The guidance outlined a consistent approach for septic screens in newborn infants based on risk factors, and suggested biochemical and clinical parameters to guide management. In particular, it advised a second C-reactive protein level (CRP) 18-24 h into treatment to help determine length of antibiotic course, need for lumbar puncture (LP), and suggested review of blood culture at 36 h.
Objective:
We evaluated impact of this guidance in our neonatal unit.
Methods:
We compared two time periods, before and following the guidance. We evaluated length of stay, second CRP 18-24 h into treatment, percentage of babies having LP and duration of antibiotics.
Results:
Before NICE guidance, 38.1% of screened babies stayed <72 h. This reduced to 18.4% following guidance. Before guidance, 20.9% babies stayed >5 days, which increased to 27.7% following NICE recommendations. Repeat CRP measurements increased from 45% to 97%. In 58% of these babies, repeat CRPs influenced management and hospital stay. An increase in LPs performed from 14% to 23% was noted. There were no positive blood cultures or LP results.
Conclusions:
We envisaged shorter hospital stays with new NICE standards, particularly, with the aim of 36 h blood culture reporting. However, repeat CRP led to further investigations, increased LPs and longer durations of treatment and stay. This, in turn, impacted on workload and cost, and influenced parental experience in the first few days of life.
Keywords:
Infectious Diseases; Neonatology.
Published by the BMJ Publishing Group Limited. For permission to use (where not already granted under a licence) please go to http://group.bmj.com/group/rights-licensing/permissions.
Similar articles
-
Comparison of the management recommendations of the Kaiser Permanente neonatal early-onset sepsis risk calculator (SRC) with NICE guideline CG149 in infants ≥34 weeks’ gestation who developed early-onset sepsis.
Morris R, Jones S, Banerjee S, Collinson A, Hagan H, Walsh H, Thornton G, Barnard I, Warren C, Reid J, Busfield A, Matthes J.
Morris R, et al.
Arch Dis Child Fetal Neonatal Ed. 2020 Nov;105(6):581-586. doi: 10.1136/archdischild-2019-317165. Epub 2020 Mar 13.
Arch Dis Child Fetal Neonatal Ed. 2020.PMID: 32170032
-
C-Reactive Protein (CRP) levels in neonatal meningitis in England: an analysis of national variations in CRP cut-offs for lumbar puncture.
Sturgeon JP, Zanetti B, Lindo D.
Sturgeon JP, et al.
BMC Pediatr. 2018 Dec 3;18(1):380. doi: 10.1186/s12887-018-1354-x.
BMC Pediatr. 2018.PMID: 30509228
Free PMC article. -
[C-reactive protein concentrations during initial (empiric) treatment of neonatal sepsis].
Janković B, Pasić S, Marković M, Veljković D, Milicić M.
Janković B, et al.
Srp Arh Celok Lek. 2001 May-Jun;129 Suppl 1:17-22.
Srp Arh Celok Lek. 2001.PMID: 15637985
Serbian.
-
Duration of empirical antibiotic therapy for infants suspected of early-onset sepsis.
Cotten CM, Smith PB.
Cotten CM, et al.
Curr Opin Pediatr. 2013 Apr;25(2):167-71. doi: 10.1097/MOP.0b013e32835e01f6.
Curr Opin Pediatr. 2013.PMID: 23407181
Free PMC article.Review.
-
Treatment for early-onset neonatal sepsis.
Abdelrhim H, Heaton PA, Routley C, Paul SP.
Abdelrhim H, et al.
Nurs Times. 2014 Apr 2-8;110(14):24-5.
Nurs Times. 2014.PMID: 24772800
Review.
Cited by
-
Comparison of diagnoses of early-onset sepsis associated with use of Sepsis Risk Calculator versus NICE CG149: a prospective, population-wide cohort study in London, UK, 2020-2021.
Piyasena C, Galu S, Yoshida R, Thakkar D, O’Sullivan J, Longley C, Evans K, Sweeney S, Kendall G, Ben-Sasi K, Richards J, Harris C, Jagodzinski J, Demirjian A, Lamagni T, Le Doare K, Heath PT, Battersby C; Neonatal Trainee-Led Research and Improvement Projects (NeoTRIPs) group.
Piyasena C, et al.
BMJ Open. 2023 Jul 27;13(7):e072708. doi: 10.1136/bmjopen-2023-072708.
BMJ Open. 2023.PMID: 37500270
Free PMC article. -
Clinical and laboratory factors associated with neonatal sepsis mortality at a major Vietnamese children’s hospital.
Toan ND, Darton TC, Huong NHT, Nhat LTH, Nguyen TNT, Tuyen HT, Thinh LQ, Mau NK, Tam PTT, Phuong CN, Nhan LNT, Minh NNQ, Xuan NM, Thuong TC, Hung NT, Boinett C, Reece S, Karkey A, Day JN, Baker S.
Toan ND, et al.
PLOS Glob Public Health. 2022 Sep 2;2(9):e0000875. doi: 10.1371/journal.pgph.0000875. eCollection 2022.
PLOS Glob Public Health. 2022.PMID: 36962870
Free PMC article. -
Diagnostic Performance and Patient Outcomes With C-Reactive Protein Use in Early-Onset Sepsis Evaluations.
Dhudasia MB, Benitz WE, Flannery DD, Christ L, Rub D, Remaschi G, Puopolo KM, Mukhopadhyay S.
Dhudasia MB, et al.
J Pediatr. 2023 May;256:98-104.e6. doi: 10.1016/j.jpeds.2022.12.007. Epub 2022 Dec 16.
J Pediatr. 2023.PMID: 36529283
-
Drug utilisation in neonatal units in England and Wales: a national cohort study.
Al-Turkait A, Szatkowski L, Choonara I, Ojha S.
Al-Turkait A, et al.
Eur J Clin Pharmacol. 2022 Apr;78(4):669-677. doi: 10.1007/s00228-021-03267-x. Epub 2022 Jan 13.
Eur J Clin Pharmacol. 2022.PMID: 35028673
Free PMC article. -
Reduction of Duration of Antibiotic Therapy for Suspected Early-Onset Sepsis in Late-Preterm and Term Newborns After Implementation of a Procalcitonin-Guided Algorithm: A Population-Based Study in Central Switzerland.
Zihlmann-Ji J, Braun C, Buettcher M, Hodel M, Lehnick D, Stocker M.
Zihlmann-Ji J, et al.
Front Pediatr. 2021 Jul 22;9:702133. doi: 10.3389/fped.2021.702133. eCollection 2021.
Front Pediatr. 2021.PMID: 34368029
Free PMC article.
MeSH terms
Substances
LinkOut — more resources
-
Full Text Sources
- HighWire
- Ovid Technologies, Inc.
-
Other Literature Sources
- scite Smart Citations
-
Medical
- MedlinePlus Health Information
-
Research Materials
- NCI CPTC Antibody Characterization Program
-
Miscellaneous
- NCI CPTAC Assay Portal
Укажите регион, чтобы мы точнее рассчитали условия доставки
Начните вводить название города, страны, индекс, а мы подскажем
Например:
Москва,
Санкт-Петербург,
Новосибирск,
Екатеринбург,
Нижний Новгород,
Краснодар,
Челябинск,
Кемерово,
Тюмень,
Красноярск,
Казань,
Пермь,
Ростов-на-Дону,
Самара,
Омск
“Сепсис в начале ХХI века. Классификация, клинико-диагностическая концепция и лечение. Патолого-анатомическая диагностика. Практическое руководство”.
Володин Н.Н., Байбарина Е.Н., Самсыгина Г.А., Буслаева Г.Н., Шабалов Н.П., Солдатова И.Г., Румянцев А.Г., Дегтярев Д.Н., Дегтярева М.В.
Синонимы: неонатальный сепсис, бактериальный сепсис новорожденного, генерализованная инфекция бактериальной этиологии.
В последние годы отмечается ухудшение состояния здоровья женщин детородного возраста, и, как следствие, увеличивается рождаемость детей с экстремально низкой массой тела. Все это привело к изменению клинической картины сепсиса, особенно у глубоконедоношенных новорожденных детей, и к переосмыслению понятия «Сепсис новорожденных» с позиций практической неонатологии. С целью упорядочения постановки данного диагноза в клинической практике Рабочая группа экспертов Российской Ассоциации Специалистов Перинатальной Медицины (РАСПМ) в результате проведения многоцентрового анализа историй болезни новорожденных детей за 2000-2003 годы предложила следующее определение неонатального сепсиса:
Неонатальный сепсис – это генерализованное инфекционное заболевание, вызванное условно-патогенной бактериальной микрофлорой, в основе которого лежит дисфункция иммунной системы организма с развитием очага (очагов) гнойного воспаления и/или бактериемии, системной воспалительной реакции (СВР) и полиорганной недостаточности (ПОН) у детей первого месяца жизни.
Код по МКБ – 10:
Р36 Бактериальный сепсис новорожденного, врожденная септицемия.
Р36.0 Сепсис новорожденного, обусловленный стрептококком группы В.
Р36.1 Сепсис новорожденного, обусловленный другими и не уточненными стрептококками.
Р36.2 Сепсис новорожденного, обусловленный золотистым стафилококком.
Р36.3 Сепсис новорожденного, обусловленный другими и не уточненными стафилококками.
Р36.4 Сепсис новорожденного, обусловленный кишечной палочкой.
Р36.5 Сепсис новорожденного, обусловленный анаэробными микроорганизмами.
Р36.8 Сепсис новорожденного, обусловленный другими бактериальными агентами.
Р36.9 Бактериальный сепсис новорожденного не уточненный.
Примеры формулировки диагноза – «Ранний неонатальный сепсис, вызванный стрептококками группы В, септицемия, септический шок», или «Пупочный сепсис стафилококковой этиологии, септикопиемия (гнойный менингит, двухсторонняя мелкоочаговая пневмония, некротизирующий энтероколит 2 ст., омфалит), острая дыхательная недостаточность 3 степени, недостаточность кровообращения 2Б, острая почечная недостаточность, ДВС-синдром».
Эпидемиология В отечественной литературе отсутствуют достоверные сведения о частоте возникновения сепсиса среди новорожденных, что обусловлено отсутствием общепринятых критериев постановки диагноза. По зарубежным данным, частота развития сепсиса среди новорожденных составляет от 0,1 до 0,8%. Среди пациентов отделений реанимации и интенсивной терапии новорожденных (ОРИТН), а также недоношенных новорожденных частота развития сепсиса, в среднем, составляет 14% (от 8,6% среди доношенных детей в ОРИТ до 25% среди недоношенных с гестационным возрастом от 28 до 31 недель).
В структуре неонатальной смертности в Российской Федерации сепсис как причина смерти в течение нескольких десятилетий находится на 4-5 позиции. Показатели летальности от сепсиса также остаются стабильно высокими и составляют 30 – 40 %.
Классификация.
Единой классификации сепсиса новорожденного до настоящего времени у нас в стране не принято.
Выделяют ранний сепсис, при котором клинические симптомы появляются в первые трое суток жизни ребенка, и поздний сепсис новорожденных – сепсис, который манифестирует клинически позднее 4-го дня жизни. Для раннего сепсиса типично внутриутробное, преимущественно интранатальное инфицирование восходящим, контактным или гематогенным путем. Реже инфицирование происходит антенатально. Очевидный первичный очаг инфекции у ребенка, как правило, отсутствует. Источником инфекции является чаще всего микрофлора родовых путей матери. К факторам риска развития раннего неонатального сепсиса относятся недоношенность, внутриутробная гипотрофия и задержка внутриутробного развития, преждевременный разрыв околоплодных оболочек, длительность безводного промежутка более 12 часов, повышение температуры тела и наличие очагов инфекции у матери в родах и раннем послеродовом периоде, хорионамнионит, осложненное течение перинатального периода (перинатальная гипоксия, родовая травма).
Характерно фульминантное развитие клинических симптомов, СВР и ПОН при отсутствии метастатических гнойных очагов.
При позднем сепсисе инфицирование новорожденного происходит, как правило, постнатально. Первичный очаг инфекции обычно присутствует. Сепсис протекает с образованием одного или нескольких метастатических гнойно-воспалительных очагов. Типичное проявление – однотипность возбудителя, выделяемого из очагов воспаления и из крови больного. Источником инфекции может являться как микрофлора матери, так и микрофлора окружающей среды. Факторами риска развития позднего неонатального сепсиса являются недоношенность, гипотрофия, нарушение естественных защитных барьеров кожи и слизистых оболочек при необходимости проведения реанимационных мероприятий, интубации эпидемиологическая гиперергическим, трахеи, обстановка. фульминантным катетеризации Заболевание течением, так вен, может и неблагоприятная характеризоваться медленно как прогрессирующим развитием клинических симптомов, гипореактивным характером.
Сепсис также классифицируют по этиологическому принципу и входным воротам инфекции. Этиологию заболевания определяют по результатам микробиологического исследования крови, ликвора, аспирата из трахеи, мочи, содержимого гнойно- воспалительных очагов у больного ребенка. При отрицательных результатах посевов крови спектр наиболее вероятных возбудителей заболевания следует прогнозировать на основании данных анамнеза, динамики клинического состояния больного на фоне предшествующего курса антибиотиков, эпидемиологической ситуации в отделении, знание которых важно для рационального выбора антибактериальной терапии. При сепсисе целесообразно указывать в клиническом диагнозе этиологию и локализацию входных ворот инфекции, поскольку эта характеристика заболевания имеет определенное эпидемиологическое значение и важна для разработки противоэпидемиологических и профилактических мероприятий. Выделяют пупочный, кожный, отогенный, рино-фарингеальный, урогенный, катетеризационный, пульмоногенный, абдоминальный и другие более редко встречающиеся виды позднего сепсиса новорожденных. Синдромы органной недостаточности определяют тяжесть и нередко исход заболевания, требуют проведения определенной программы терапии, и поэтому их также целесообразно выделять в клиническом диагнозе. Среди них в силу тяжести прогноза особого внимания заслуживает симптомокомплекс септического шока (инфекционно- токсического шока).
Под септическим шоком понимают развитие в условиях сепсиса прогрессирующей артериальной гипотонии, не связанной только с гиповолемией, требующей применения симпатомиметиков.
Этиология.
Спектр наиболее вероятных возбудителей определяется временем инфицирования плода или ребенка (антенатальное, интранатальное или постнатальное) и локализацией входных ворот. Часто встречающийся возбудитель – S. agalacticae, относящийся к стрептококкам группы B, может быть причиной антенатального инфицирования, но чаще инфицирует плод интранатально. E. сoli и реже другие представители кишечной грамотрицательной микрофлоры также могут стать причиной интранального инфицирования плода. Во всех этих случаях клиническая манифестация заболевания отмечается в первые 72 часа жизни ребенка. При позднем сепсисе новорожденных определенную роль играют стрептококки группы B, но значительно большее число случаев заболевания приходится на долю E. сoli, Staph. aureus, Klebsiella pneumoniae, Serratia spp., Pseudomonas spp., Enterobacter spp., коагулазо-негативные стафилококки.
В течение последнего десятилетия частота встречаемости грамположительных и грамотрицательных условно-патогенных микроорганизмов в общей этиологической структуре сепсиса новорожденных стала примерно одинаковой.
В структуре грамотрицательных возбудителей сепсиса возросла роль таких микроорганизмов, как Pseudomonas spp., Кlebsiella spp. и Enterobacter spp. Как правило, эти бактерии выступают в роли возбудителя сепсиса у пациентов ОРИТН, находящихся на искусственной вентиляции легких (ИВЛ) и парентеральном питании (ПП), у хирургических больных. На этиологическую структуру постнатально развившейся болезни существенное влияние оказывает локализация первичного септического очага: в этиологии пупочного сепсиса ведущую роль играют стафилококки и, в меньшей степени, кишечная палочка, а в этиологии кожного сепсиса – стафилококки и ?-гемолитические стрептококки группы А. Прослеживается определенная избирательность спектра возбудителей нозокомиального сепсиса в зависимости от входных ворот инфекции: при катетеризационном сепсисе преобладающую роль играют метициллин-резистентные стафилококки или смешанная микрофлора, обусловленная ассоциацией стафилококков или грам-отрицательной микрофлоры с грибами рода Candida; при абдоминальном госпитальном сепсисе актуальны такие возбудители как энтеробактер, анаэробы.
Патогенез неонатального сепсиса имеет те же закономерности, что и у детей старшего возраста и у взрослых.
Клиническая картина.
Для клинической картины сепсиса независимо от его формы характерна тяжесть общего состояния новорожденного ребенка. Это проявляется выраженными нарушениями терморегуляции (у доношенных, морфофункционально зрелых новорожденных чаще наблюдают лихорадку, у недоношенных, маловесных детей и детей с отягощенным преморбидным фоном более вероятна прогрессирующая гипотермия), нарушением функционального состояния ЦНС (прогрессирующее угнетение или быстро истощаемое беспокойство, подстанывание). Характерны грязновато-бледный или грязновато-серый оттенок кожных покровов, нередко с геморрагиями, участками склеремы, выраженная мраморность кожи, можно наблюдать акроцианоз. В раннем неонатальном периоде может рано появляться и быстро нарастать желтуха. Нередко отмечают развитие общего отечного синдрома. Характерна склонность к спонтанной кровоточивости. Черты лица нередко заострены. Типичны развитие дыхательной недостаточности нередко при отсутствии воспалительных изменений на рентгенограмме, нарушения функции сердца по типу токсической кардиопатии, которая может сопровождаться развитием сердечной недостаточности. Характерно увеличение размеров селезенки и печени, вздутие живота, выраженная венозная сеть на животе, склонность к срыгиваниям, рвоте и анорексии, дисфункция желудочно-кишечного тракта, вплоть до развития пареза кишечника, отсутствие прибавки массы тела.
При раннем сепсисе новорожденных часто отмечается врожденная пневмония, у недоношенных детей одним из частых очагов сепсиса является энтероколит. Развитие менингита более характерно для позднего неонатального сепсиса. Все эти синдромы и симптомы являются отражением различной степени выраженности полиорганной недостаточности у новорожденного (таблица 1).
Первичный септический очаг. После внедрения в клиническую практику современных методов первичной обработки пуповинного остатка и ухода за пупочной ранкой отмечено снижение частоты развития омфалита и пупочного сепсиса, который сейчас встречается менее чем в четверти случаев. На этом фоне значительно возросла частота пульмоногенного (до 20–25%) и абдоминального сепсиса (не менее 20%). Другие локализации первичного очага встречаются значительно реже и не превышают 2–6%. В отдельных случаях входные ворота инфекции установить не удаётся. Это особенно характерно для детей с малым гестационным возрастом.
Септический шок. Септический шок наблюдается, по данным различных авторов, в 10–15% случаев сепсиса новорожденных. В большинстве случаев септический шок развивается при сепсисе, вызванном грамотрицательными микроорганизмами. Кокковая грамположительная микрофлора реже бывает причиной развития шока. Исключение составляют стрептококки группы B и энтерококки: при этой этиологии сепсиса шок развивается практически с такой же частотой, как и при грамотрицательной этиологии болезни. Летальность при развитии септического шока составляет более 40%.
Для клинической картины септического шока у новорожденных детей характерно стремительное, порой катастрофическое, нарастание тяжести состояния, прогрессирующая тенденция к гипотермии, бледность кожи, прогрессирующее угнетение безусловных рефлексов и реакции на раздражители, тахикардия может сменяться брадикардией, характерна усиливающаяся одышка нередко при отсутствии инфильтративных изменений на рентгенограммах легких. Появляется кровоточивость из мест инъекций, иногда появляется петехиальная сыпь или кровоточивость слизистых, пастозность, а затем и отечность всех тканей. Можно наблюдать эксикоз в сочетании с отеком тканей и органов, особенно паренхиматозных.
Самые характерные признаки септического шока – постепенно нарастающая артериальная гипотензия, нечувствительная к введению адреномиметиков, резкое нарушение микроциркуляции (симптом «бледного пятна» более 3 секунд), ДВС-синдром с развитием тромбоцитопении потребления, коагулопатии потребления и депрессии фибринолиза. В таких случаях наряду с кровоточивостью могут стремительно развиваться множественные некрозы, в том числе стенки тонкой кишки, кортикальных отделов почек, миокарда, мозга и других органов.
Шок сопровождается тяжелейшей гормональной дисфункцией, выраженными нарушениями практически всех механизмов регуляции гомеостаза, включая и системный медиаторный ответ организма. Острое течение заболевания развивается при отсутствии септического шока в дебюте болезни или в тех случаях, когда его удалось предотвратить или купировать. Такой вариант течения сепсиса наблюдается в 75 – 85% случаев.
При благоприятном течении процесса длительность заболевания составляет, в среднем, 4 – 6 недель. Период острых проявлений, клиническая картина которого сходна с описанной выше, длится 3-14 дней при современных методах лечения. Затем наступает репарационный период, для которого характерно угасание симптомов токсикоза, постепенное восстановление функций отдельных органов и систем, санация метастатических очагов. Наряду с этим, в клинической картине сохраняются увеличение печени и/или селезенки, бледность кожных покровов, лабильность функций центральной и вегетативной нервной систем, дисбактериоз практически всех локусов тела, контактирующих с внешней средой, отсутствие или недостаточная прибавка массы тела, приводящая к формированию постнатальной гипотрофии.
В этот период легко присоединяется перекрестная инфекция (бактериальная, грибковая или вирусная). Нередки такие источники суперинфекции, как аутофлора ребенка и больничная микрофлора.
Гематологическая картина в острый период сепсиса характеризуется выраженным лейкоцитозом, реже нормальными показателями или лейкопенией, нейтрофильным сдвигом формулы влево до юных форм. Можно наблюдать тромбоцитопению, эозинопению, лимфопению, тенденцию к моноцитозу, анемию. В репарационный период могут быть умеренные эозинофилия и моноцитоз; нейтрофилез в 1/3 случаев сменяется нейтропенией, в 2/3 случаев – нормальными показателями. В периферической крови появляются базофилы и плазматические клетки.
Диагностика.
Диагностика сепсиса складывается из нескольких этапов.
Первый этап – выявление очагов инфекции. Необходимо учитывать такую особенность раннего сепсиса новорожденных, как возможность анте- или интранатального инфицирования плода. На основании анализа данных анамнеза, физикального обследования, соответствующей лабораторной и инструментальной диагностики, динамики патологических симптомов следует исключить или подтвердить развитие у ребенка менингита, пневмонии, энтероколита, пиелонефрита, артрита, остеомиелита, перитонита, кардита, абсцессов и флегмоны мягких тканей и т.д.
Второй этап диагностики – оценка функциональной активности важнейших систем поддержания гомеостаза и диагностика органной недостаточности. В таблице 1 приведены основные клинические, лабораторные и инструментальные характеристики полиорганной недостаточности, которые могут сопровождать сепсис новорожденного и определяют его исход. Мониторирование этих показателей необходимо для проведения адекватной этиотропной и посиндромной терапии.
Третий этап диагностики – оценка системной воспалительной реакции организма новорожденного ребенка. К критериям системной воспалительной реакции у новорожденных детей относят:
1. Аксиллярную температуру >37,5оС или <36,2оС при соблюдении адекватного температурного режима.
2. Изменения в общем анализе крови (таблица 2): Таблица 2. Изменения состава периферической крови, характерные для системной воспалительной реакции у новорожденных детей.
3. Повышение уровня С-реактивного белка (СРБ) в сыворотке крови более 6 мг/л.
4. Повышение уровня прокальцитонина (ПКТ) в сыворотке крови более 2 нг/мл у доношенного ребенка старше 48 часов жизни и старше 96 часов – у недоношенного с очень низкой массой тела при рождении (ОНМТ).
5. Повышение уровня интерлейкина-8 (ИЛ-8) в сыворотке крови более 100 пг/мл. При возможности дополнительной лабораторной диагностики информативными показателями системного воспаления являются увеличение сывороточных уровней других провоспалительных цитокинов (ИЛ-1?, ФНО-?, ИФН-?, Г-КСФ, ИЛ-6), изменения уровней белков острой фазы воспаления, как позитивных реактантов (увеличиваются при наличии системного воспаления; например, гаптоглобин, орозомукоид, С3-компонент комплемента и др.), так и негативных реактантов (уменьшаются при воспалении, например, С4-компонент комплемента, преальбумин).
В первые трое суток жизни наличие хотя бы трех из перечисленных выше признаков является веским основанием для предположения диагноза «сепсис» и немедленного назначения эмпирической антибактериальной терапии, а также проведения всего необходимого объема лечебных мероприятий.
У новорожденных детей старше 4–дневного возраста диагноз «сепсис» следует предполагать при наличии первичного инфекционно-воспалительного очага, нарушении функций двух или более систем организма и хотя бы 3 из перечисленных признаков СВР. Это также является основанием для немедленного начала антибактериальной терапии и комплекса лечебных мероприятий.
Однако, понимая, что диагноз сепсиса до настоящего времени остается клиническим диагнозом, целесообразно в течение 5-7 дней ретроспективно подтвердить его или отвергнуть. Исчезновение признаков системного воспалительного ответа параллельно с санацией очага инфекции и, тем более, отсутствие связи клинических проявлений СВР с инфекцией, свидетельствует против диагноза «сепсис» и требует дальнейшего диагностического поиска.
Обязательным этапом в диагностике сепсиса является микробиологическое исследование, т.е. посев крови, спинномозговой жидкости (по клиническим показаниям), аспирата из трахеи, мочи, отделяемого из гнойных очагов.
Следует строго соблюдать правила забора крови для микробиологического исследования. Необходимо осуществлять забор крови в асептических условиях при пункции интактной периферической вены или первой пункции центральной вены для постановки катетера. Недопустимо проводить забор крови для посева из длительно функционирующего катетера (это целесообразно лишь при изучении эпидемиологической ситуации в отделении). Оптимальный объем крови для посева – 1 мл или более. При технических трудностях и получении меньшего объема крови увеличивается риск получения отрицательных результатов посева крови при наличии низкой концентрации бактерий в кровотоке, особенно на фоне эффективной антибактериальной терапии.
Бактериемия – не абсолютный диагностический признак сепсиса.
Ложноотрицательные результаты посева крови можно получить при заборе материала после начала антибактериальной терапии. Кроме того, ложноотрицательные результаты посева крови могут определяться малым объемом крови при небольшой степени бактериемии и несовершенством лабораторной диагностики на современном этапе, так как целый ряд возбудителей требует особых, специфических питательных сред и не может быть определен при стандартном исследовании. Ложноположительные результаты посева крови также возможны, поскольку бактериемию можно транзиторно наблюдать при любом инфекционном заболевании бактериальной природы.
Наряду с исследованием гемокультуры, этиологическая диагностика сепсиса включает микробиологическое исследование отделяемого из первичного и метастатических очагов. Дифференциальный диагноз. Сепсис следует дифференцировать с врожденными генерализованными формами вирусных инфекций. Дифференциальная диагностика основывается на проведении микробиологического, молекулярно-биологического или вирусологического исследования крови, спинномозговой жидкости, мочи, аспирата из трахеи или слюны методом полимеразной цепной реакции (ПЦР) и/или культуральным методом, серологических исследований уровней специфических IgM и IgG в сыворотке крови, а также их авидности.
Сепсис необходимо дифференцировать с генерализованными микозами, в первую очередь, кандидозом и значительно реже – аспергиллезом. Дифференциальный диагноз основывается на результатах микроскопического и микологического (посев на среду Сабуро) исследований крови, ликвора, отделяемого пиемических очагов.
Наконец, у новорожденных детей сепсис необходимо дифференцировать с наследственной патологией обмена веществ. Так, при наследственных дефектах обмена аминокислот характерны быстрое ухудшение состояния новорожденного после рождения, прогрессирующая одышка, легочно-сердечная недостаточность, угнетение функций ЦНС, гипотермия, лейкопения, тромбоцитопения, анемия. Отличительный признак – стойкий и выраженный метаболический ацидоз, в ряде случаев – появление стойкого запаха. В связи с тяжестью состояния у ребенка можно обнаружить бактериемию, отражающую выраженный дисбиоз и снижение резистентности организма.
Основное в дифференциальной диагностике – биохимические исследования крови, мочи, генетическая диагностика. Галактоземия также может протекать под маской пупочного или позднего неонатального сепсиса. Манифестация данного заболевания характеризуется ухудшением состояния новорожденного ребенка, нарастанием срыгиваний и рвоты, повышением температуры тела, развитием галактозурии, гемолитической желтухи и гемолитической анемии, нарастанием патологической неврологической симптоматики, нарушениями функций печени с повышением уровней трансаминаз, развитием холестаза, гипогликемии, метаболического ацидоза. В отличие от сепсиса воспалительные изменения в общем анализе крови при неосложненных формах галактоземии выражены нерезко, результаты микробиологического и молекулярно-биологического исследования отрицательны.
Диагноз «галактоземия» можно подтвердить при обнаружении высоких уровней галактозы (более 0,2 г/л) в сыворотке крови (тест Гатри), а также изменениями уровней галактокиназы и других ферментов, участвующих в метаболизме галактозы, генетическими исследованиями.
Лечение.
Ребенка с подозрением на сепсис или с установленным диагнозом сепсиса новорожденных необходимо госпитализировать в ОРИТН или отделение патологии новорожденных в зависимости от тяжести состояния (в острой фазе заболевания лечение обязательно проводят в ОРИТН).
Важную роль в профилактике сепсиса играет проведение гигиенических мероприятий (гигиеническая обработка кожи и видимых слизистых, купание) и 13 правильное вскармливание новорожденных. У доношенных детей в отделении патологии новорожденных предпочтение отдают вскармливанию нативным материнским молоком (кормление грудью, кормление нативным молоком из бутылочки, введение его через зонд в зависимости от состояния новорожденного). При отсутствии материнского молока используют адаптированные смеси для вскармливания новорожденных детей, в том числе обогащенные бифидобактериями.
Однако следует помнить, что у детей с транзиторной лактазной недостаточностью и выраженным ацидозом использование кисломолочных смесей нередко приводит к срыгиваниям и диарее. В этом случае целесообразно использование низколактозных и безлактозных адаптированных смесей, в том числе обогащенных пребиотиками. У недоношенных новорожденных при отсутствии грудного молока используют специальные адаптированные смеси для недоношенных новорожденных. При развитии энтероколита и перитонита энтеральное питание отменяют на 7-14 дней, а при последующем возобновлении питания у детей с патологией кишечника и мальабсорбцией рекомендуют использовать смеси, содержащие гидролизат белка и среднецепочечные триглицериды. В период острых проявлений целесообразно пребывание больного ребенка в кувезе при температуре не ниже 300C и влажности не ниже 60%.
Коррекцию жизненно важных функций проводят под контролем следующих параметров:
• оценка кислотно-основного состояния (КОС), pO2, насыщения гемоглобина кислородом;
• уровень Hb, Ht,
• уровни глюкозы, креатинина (мочевины), К, Na, Ca, Mg, по показаниям – билирубина, трансаминаз, общего белка, альбумина и др. показателей,
• оценка АД, ЭКГ.
Лечение сепсиса должно включать медицинские мероприятия, одновременно проводимые в двух направлениях:
1. Этиотропная терапия – воздействие на инфекционный агент (возбудитель заболевания), которое включает наряду с системной антибиотикотерапией местную терапию, направленную на санацию первичного и/или метастатических очагов, коррекцию нарушений биоценоза поверхностей организма ребенка, соприкасающихся с окружающей средой;
2. Патогенетическая терапия, направленная на восстановление изменений гомеостаза, включая нарушения иммунной системы и органные нарушения.
Этиотропная терапия. Антибактериальная терапия – кардинальное и неотложное направление, определяющее этиологическую составляющую лечения сепсиса. Общие принципы выбора антибактериальной терапии в неонатологии следующие:
1. Выбор препаратов в начале терапии (до уточнения этиологии заболевания) осуществляется в зависимости от времени возникновения (ранний, поздний сепсис), условий возникновения (в условиях терапевтического или хирургического отделений, или ОРИТН), локализации первичного септического очага, если он есть.
2. Препаратами выбора при эмпирической терапии должны быть антибиотики или комбинация антибактериальных препаратов с бактерицидным типом действия, обладающих активностью в отношении потенциально возможных возбудителей сепсиса, включая возбудителей – ассоциантов (деэскалационный принцип выбора антибиотикотерапии). При уточнении характера микрофлоры и её чувствительности антибактериальную терапию корригируют путем смены препарата и переходом на препараты более узкого, целенаправленного спектра действия.
3. При выборе антибиотиков предпочтение отдают препаратам, проникающим через гематоэнцефалический барьер и другие биологические барьеры организма, и создающим достаточную терапевтическую концентрацию в спинномозговой жидкости, в веществе мозга и других тканях организма (костная, легочная и т.д.).
4. При выборе препаратов во всех случаях предпочтение отдают антибиотикам с наименьшей токсичностью, при этом обязательно учитывают характер органных нарушений.
5. Предпочтительны препараты с возможностью внутривенного пути введения. Выбор антибиотиков в зависимости от вида сепсиса. При раннем сепсисе новорожденных препаратами выбора считают ампициллин в сочетании с аминогликозидами (гентамицином или амикацином).
При внебольничном пупочном сепсисе антибиотиками первого выбора должны быть комбинация оксациллина аминогликозидами или цефалоспоринов (амикацин).
При кожном сепсисе антибиотиками выбора являются пенициллины (оксациллин и ампициллин) и цефалоспорины 1 и 2-го поколения (цефазолин или цефоруксим), применяемые в комбинации с аминогликозидами (амикацином).
ИВЛ-ассоциированный легочный сепсис у новорожденных чаще обусловлен Ps. aeruginose, Acinetobacter spp., Klebsiella spp. Поэтому антибиотиками выбора считают «защищенные» пенициллины (тикарциллин/клавулановая кислота), уреидопенициллины (пиперациллин) или цефалоспорины 3-го поколения, обладающие активностью в отношении Ps. аeruginosae (цефтазидим) в сочетании с аминогликозидами (амикацином).
Альтернативными антибиотиками имипенем/циластатин – аминогликозидами. При метициллинрезистентных тиенам) в качестве высокой штаммов являются карбапенемы монотерапии вероятности стафилококков или в (меронем, сочетании этиологической целесообразно с роли применение ванкомицина или, при подозрении на его неэффективность, линезолида.
При кишечном сепсисе антибиотиками выбора являются цефалоспорины 3-го поколения, карбоксипенициллины в качестве монотерапии или в сочетании с аминогликозидами (амикацином).
Альтернативные антибиотики при кишечном и урогенном сепсисе – имипенем (тиенам), а при абдоминальном сепсисе – тикарциллин/клавулановая кислота, уреидопенициллины (пиперациллин), метронидазол, линкозамиды, линезолид в качестве монотерапии или в сочетании с аминогликозидами (амикацином).
Катетер-ассоциированный сепсис – одна из форм нозокомиального сепсиса. Основным возбудителем его считают Staph. aureus, причем нередко высеваются метициллинрезистентные штаммы микроорганизма. Поэтому антибиотиками выбора в данном случае являются ванкомицин и линезолид.
Эффективной считают антибактериальную терапию, при проведении которой в течение 48 часов достигают стабилизации состояния больного или даже некоторого улучшения.
Неэффективной считают терапию, при проведении которой в течение 48 часов отмечают нарастание тяжести состояния и органной недостаточности. Это является показанием к переходу на альтернативную антибактериальную терапию, усилению дезинтоксикационной инфузионной терапии, подключению иммунотерапии.
При успешной антибактериальной терапии её длительность составляет в среднем 4 недели, причем за исключением аминогликозидов, длительность курса которых не может превышать 10 дней, курс одного и того же препарата при его явной эффективности может достигать 3 недель.
Основанием для отмены антибактериальных препаратов можно считать санацию первичного и пиемических очагов, отсутствие новых метастатических очагов, купирование признаков острой СВР и полиорганной недостаточности, стойкую прибавку массы тела, нормализацию формулы периферической крови и числа тромбоцитов, отрицательные результаты микробиологического исследования крови, спинномозговой жидкости, аспирата из трахеи, мочи.
Учитывая необходимость длительной и интенсивной антибактериальной терапии и большое значение дисбактериоза в патогенезе инфекционного процесса при сепсисе новорожденных целесообразно проведение антибактериальной терапии сочетать с «терапией сопровождения». К ней относится одновременное назначение пробиотиков (бифидумбактерина, лактобактерина, линекса, примадофилюса, нормофлоринов и др.), а через 7-14 дней после начала антибактериальной терапии подключение антимикотика флуконазола в дозе 6-8 мг/кг массы тела в сутки на 1 введение внутривенно капельно или внутрь, если он не был назначен ранее по результатам микробиологических исследований. Низкая терапевтическая и профилактическая эффективность нистатина не позволяет рекомендовать его для профилактики кандидоза у этой категории больных.
Патогенетическая терапия сепсиса включает следующие основные направления:
• иммунокорригирующую терапию,
• инфузионную терапию,
• восстановление водного и электролитного баланса, коррекцию КОС крови,
• противошоковую терапию,
• восстановление функций основных органов и систем организма.
Основные принципы иммуномодулирующей терапии при неонатальном сепсисе следующие:
1. Иммунотерапия проводится только на фоне адекватной этиотропной и посиндромной базисной терапии.
2. Иммунотерапия – это патогенетическая терапия, один из видов обязательной посиндромной терапии, не зависит от этиологии сепсиса.
3. Иммунотерапия при сепсисе направлена на коррекцию возникающих нарушений гуморального и/или клеточного звеньев иммунитета. Следовательно, ее объем может определяться выявляемыми иммунными нарушениями. Основные методы иммунотерапии при неонатальном сепсисе:
А. Коррекция гуморального иммунитета.
Показаниями к проведению иммунозаместительной терапии являются неонатальный сепсис и септический шок. Патогенетическим обоснованием иммунозаместительной терапии при неонатальном сепсисе являются повышенное потребление собственных иммуноглобулинов плода и новорожденного в ходе опсонизации патогенов и фагоцитоза при сепсисе, а также недостаточный трансплацентарный перенос антител от матери плоду до 36 недели гестации и при фетоплацентарной недостаточности. Иммунозаместительную терапию при неонатальном сепсисе целесообразно проводить препаратом Пентаглобин, обогащенным IgM и IgA. При его отсутствии следует использовать любые поливалентные препараты иммуноглобулинов для внутривенного введения, содержащие преимущественно IgG.
Пентаглобин рекомендуется вводить внутривенно капельно в дозе 5 мл/кг массы тела в сутки со скоростью ? 1,7 мл/кг массы тела в час с помощью инфузионного насоса ежедневно в течение 3-х дней или через день. Доза стандартных препаратов поливалентных иммуноглобулинов для внутривенного введения может составлять 0,5-1 г/кг в сутки.
Уровень доказательности – 1а. Ohlsson A., Lacy J. Intravenous immunoglobulin for suspected or subsequently proven infection in neonates. Review. The Cochrane Database of Systematic Reviews, 2004, Issue 1. Art.No.:CD001239. DOI: 10.1002/14651858.CD001239.pub2.
B. Коррекция клеточного звена иммунитета (по показаниям).
I. Абсолютная лимфопения, выявленная у пациентов в неонатальном периоде, свидетельствует о тяжести инфекционного заболевания независимо от гестационного и постнатального возраста детей, результатов посева крови и природы выявленного возбудителя. При раннем неонатальном сепсисе абсолютная лимфопения развивается статистически значимо чаще, чем абсолютная нейтропения (19% против 3,8% соответственно; р=0,002, двухсторонний точный критерий Фишера (ТКФ). Показатель летальности в группе больных новорожденных с повторяющимися эпизодами лимфопении был статистически значимо выше, чем у детей с однократным эпизодом лимфопении (29,3% против 9,4%, соответственно; р=0,02, ТКФ), что может указывать на непосредственную взаимосвязь между развитием лимфопении как проявлением иммунной недостаточности и смертельным исходом. Обнаружение у ребенка стойкой лимфопении является прогностически неблагоприятным признаком с высоким уровнем информативности: чувствительность (SN) – 77,8%, специфичность (SP) – 73%, диагностический коэффициент (ДК) – 4,6 и относительный риск (RR) – 9,6. Неблагоприятная прогностическая значимость абсолютной лимфопении объясняется количественным дефицитом всех важнейших функциональных субпопуляций лимфоцитов: зрелых Т-лимфоцитов (CD3+), цитотоксических лимфоцитов (CD8+), естественных киллерных клеток производящих интерлейкин-2 (CD16+CD56+), T-лимфоцитов-хелперов фактор лимфоцитов. как роста Это (CD4+), приводит к недостаточности клеточных механизмов врожденного и адаптивного иммунного ответа у новорожденных детей и подчеркивает необходимость применения при регистрации абсолютной лимфопении патогенетически обоснованных способов иммунокоррекции.
При выявлении абсолютной лимфопении (менее 2?109/л) у детей с осложненным течением неонатального периода показано внутривенное капельное введение препарата рекомбинантного интерлейкина-2 (рИЛ-2) человека (Ронколейкин) в дозе 50000-100000 МЕ/кг массы тела в сутки. Перед введением Ронколейкин необходимо развести 0,9%-ным раствором натрия хлорида из расчета 5-10 мл/кг в сутки в зависимости от особенностей водно-электролитного обмена ребенка. Препарат вводится с использованием инфузомата в течение 2-3 часов со скоростью не более 6 мл/час 1 раз в сутки двукратно с интервалом 48-72 часа.
Ронколейкин разрешен к применению в педиатрии и неонатологии в Российской Федерации с февраля 2008 года. Включение Ронколейкина в комплексную терапию тяжелых неонатальных инфекций показано при развитии абсолютной лимфопении. В этих случаях применение Ронколейкина является патогенетически обоснованным и эффективным. Показатель летальности в группе детей, получивших иммунотерапию Ронколейкином, составил 8% (7/85), а в группе сравнения – 20% (12/60) (р=0,047, ТКФ). Среди детей с сепсисом, не имевших показаний к хирургическому лечению, умерли 1 ребенок из 60 получавших Ронколейкин, и 7 из 50 детей группы сравнения (1,7% против 14%, соответственно; р=0,02, ТКФ; отношение шансов (Odds Ratio) = 9,6 (1,1 – 218,9); относительный риск (Relative Risk) = 8,4 (1,1 – 184,3). При проведении иммунокоррекции с использованием препарата рИЛ-2 показатель летальности в подгруппе детей с сепсисом и стойкой лимфопенией и, следовательно, с высоким риском неблагоприятного исхода удалось снизить до 13,2% (против 32,4% в контрольной группе без иммунотерапии, р?2=0,028). О клинической эффективности Ронколейкина свидетельствуют снижение показателя летальности, сокращение длительности санации локализованных очагов инфекции и крови, нормализация показателей гемограммы и иммунного статуса, уменьшение интенсивности системного воспалительного ответа у детей, получавших иммунотерапию Ронколейкином, по сравнению с детьми группы сравнения.
Уровень доказательности – 3b.
1. Ашиткова Н.В., Дегтярева М.В., Володин Н.Н. и соавт. «Диагностическое и прогностическое значение лимфопенических состояний у новорожденных детей с осложненным течением неонатального периода» // «Педиатрия». Журнал имени Г.Н.Сперанского, 2009, No 1, стр. 49- 54.
2. Ашиткова Н.В., Володин Н.Н., Дегтярева М.В., Продеус А.П. и соавт. «Эффективность препарата рекомбинантного интерлейкина-2 человека – Ронколейкина в комплексной терапии неонатального сепсиса и тяжелых неонатальных инфекций» // «Педиатрия». Журнал имени Г.Н.Сперанского, 2009, No 3. II.
При сочетании с вирусной инфекцией или при инфекциях, вызванных внутриклеточными патогенами, а также для усиления цитотоксической активности лимфоцитов и макрофагов при неонатальном сепсисе показано проведение иммунотерапии препаратом рекомбинантного интерферона-?2b человека (Виферон).
Препарат разрешен к применению в неонатологии в Российской Федерации с 1987 года. Патогенетическим обоснованием проведения иммунотерапии препаратами интерферонов (ИФН) являются:
А) Малая клеточная продукция и низкая концентрация ИФН-? и ИФН-? в сыворотке крови новорожденных детей.
Б) Дальнейшее угнетение синтеза эндогенного ИФН при неонатальных бактериальных и вирусных инфекциях и при перинатальной гипоксии.
В) Быстрое развитие абсолютной лимфопении при тяжелых неонатальных инфекциях вследствие гибели неонатальных лимфоцитов путем апоптоза при массивной антигенной нагрузке, снижение количества CD4+ и CD8+ лимфоцитов, снижение цитотоксического потенциала.
Г) Достоверное усиление цитотоксичности неонатальных лимфоцитов и макрофагов под действием экзогенных цитокинов ИФН или ИЛ-2 (Montagna N., 1988).
Особенности интерферонотерапии:
1. Является одним из обязательных видов посиндромной терапии тяжелых инфекций и не зависит от этиологии инфекции.
2. Усиливает противовирусный и антибактериальный иммунитет посредством активации цитотоксичности лимфоцитов и макрофагов и эффективного уничтожения ими клеток, зараженных внутриклеточными возбудителями.
3. Действует через рецепторы к интерферону на клетках, импульсно запускает трансдукцию сигнала внутрь клетки и активацию лимфоцитов.
4. Не требует поддержания постоянной концентрации интерферона в сыворотке крови в течение суток во время проведения курса лечения. Новорожденным детям с сепсисом Виферон назначают по 1 свече (150000 МЕ) 2 раза в день в течение 7-14 дней в прямую кишку.
Показатель летальности в группе детей с внутриутробной инфекцией бактериально- вирусной этиологии, получивших иммунотерапию Вифероном, составил 4,9% (4/81), а в группе детей, получавших только базисную терапию – 18,4% (7/38) (р=0,036, ТКФ); отношение шансов (Odds Ratio) = 0,23 (0,05 – 0,96); относительный риск (Relative Risk) = 0,27 (0,07 – 0,96). Эффективность Виферона определяется снижением показателя летальности, сокращением сроков санации очагов инфекции, нормализации показателей гемограммы и иммунного статуса, у детей, получавших иммунотерапию Вифероном, по сравнению с детьми, получавшими только базисную терапию.
Уровень доказательности – 2b.
1. Долецкий С.Я. Соловьев В.Д. и соавт. Авторское свидетельство No1309984, рег. в 1987 году.
2. Солдатова И.Г., Гетия Е.Г., Володин Н.Н. и соавт. // «Педиатрия». Журнал имени Г.Н.Сперанского, 2007, том 86, No 4.
3. Павлова М.В., Дегтярева М.В., Володин Н.Н. и соавт. // «Педиатрия». Журнал имени Г.Н.Сперанского, 2009, том 87, No 2.
III. При нейтропении и/или гипоэргическом течении сепсиса патогенетически обоснованным является проведение иммунотерапии препаратом Ликопид, разрешенным к применению в педиатрии и неонатологии в Российской Федерации с 1999 года. Ликопид представляет собой глюкозаминил-мурамил-дипептид, минимальный биологически активный фрагмент клеточной стенки большинства бактерий, который действует на клетки моноцитарно-макрофагальной природы через внутриклеточные рецепторы врожденного иммунитета, NOD2 – рецепторы, запуская трансдукцию сигнала внутрь клетки и усиливая в конечном итоге выработку провоспалительных цитокинов. Под действием Ликопида происходит активация функции моноцитов и макрофагов, обуславливающая эффективность фагоцитоза, распознавания и представления антигена, развитие адаптивного иммунного ответа. Ликопид обладает способностью усиливать костномозговое кроветворение, главным образом, гранулоцитопоэз. Ликопид назначают в дозе 0,5 мг (1/2 таблетки) 2 раза в день в течение 7-14 дней. Ликопид растворяют в 3-5 мл теплой кипяченой воды и дают внутрь с ложки, через соску или зонд за 20-30 минут до кормления. Иммунотерапия препаратом Ликопид безопасна, обеспечивает эффективное купирование лабораторных и клинических признаков инфекционного заболевания и системного воспалительного ответа, восстанавливает нормальные показатели гемограммы и иммунного статуса в короткие сроки.
Уровень доказательности – 3b.
1. Таболин В.А., Володин Н.Н., Дегтярева М.В. и соавт., 2000. 2.Кулагина М.Г. и соавт. 2005.
Инфузионная терапия позволяет восполнить дефицит объёма циркулирующей крови, провести коррекцию электролитных расстройств и улучшить гемореологические характеристики циркулирующей крови. В ряде случаев (при невозможности вскармливания) инфузионная терапия становится составляющей парентерального питания новорожденного ребенка.
При расчете объёма инфузионной терапии используют стандартные рекомендации, учитывающие срок гестации новорожденного, его постнатальный возраст, массу тела, наличие обезвоживания или отечного синдрома, лихорадки, рвоты, диареи, объёма энтерального питания.
Противошоковая терапия включает следующие основные направления:
1. Развитие гиповолемического шока требует экстренного возмещения объема циркулирующей крови. С этой целью, в зависимости от конкретной причины гиповолемии и обеспеченности препаратами крови, используются 0,9% водный раствор NaCl, 6% раствор ГЭК, 5% раствор донорского альбумина, свежезамороженная плазма, донорская кровь или эритроцитарная масса. Согласно предварительным статистическим данным, в случае выявления симптомов гиповолемического шока в родильном зале, использование внутривенного медленного введения 10-20 мл/кг 0,9% водного раствора NaCl у недоношенных детей эффективней и безопасней, чем введение аналогичного количества 5% раствора донорского альбумина.
2. В случаях развития кардиогенного шока, необходима постоянная внутривенная инфузия допамина (в дозе от 5 до 20 мкг/мин) и/или добутамина (в дозе от 5 до 15 мкг/кг/мин). Наилучший эффект может быть достигнут при комбинированном введении препаратов в индивидуально подобранных (на основании динамики ЧСС, АД и Диуреза) дозах.
Для эффективного и безопасного применения вышеуказанных препаратов необходимо соблюдать следующие условия
• Вводить через катетер в центральной вене при помощи шприцевого дозатора (перфузора).
• Поддерживать адекватный объем циркулирующей крови.
• Обеспечивать непрерывный контроль за ЧСС, АД, SaO2 и формой зубцов на ЭКГ.
• Постоянно контролировать диурез.
• Регулярно осматривать место введения катетера (утечка препарата может вызвать ишемию подлежащих тканей с их последующей инфильтрацией, что опасно).
• Не допускать резкого увеличения или уменьшения скорости введения введения, тем более перерывов во введении.
• Не смешивать допамин и/или добутамин в одной линии с антибиотиками, мочегонными препаратами, бикарбонатом натрия и препаратами для парентерального питания.
Детям, перенесшим тяжелую асфиксию, необходимо индивидуально подбирать адекватные дозы допамина и добутрекса, ориентируясь на показатели медицинского мониторинга и исходя из знания фармакологических свойств каждого из препаратов. Главным принципом в подборе дозы является постепенное увеличение скорости инфузии на 1-2 мкг/кг/мин до получения необходимого терапевтического эффекта
3. В случаях развития септического шока, помимо вышеперечисленного, в терапии ребенка целесообразно внутривенное введение поливалентных иммуноглобулинов, обогащенных IgM (Пентаглобин) (смотри выше).
4. В случаях рефрактерного к терапии шока показано использование глюкокортикоидных препаратов. Предпочтительным является введение гидрокортизона в разовой дозе 5 мг/кг, у глубоконедоношенных детей стартовой может быть доза гидрокортизона 1-2 мг/кг. При его отсутствии допустимо введение преднизолона в разовой дозе 0,5-1,0 мг/кг, бетаметазона – 0,5-1,0 мг/кг, дексаметазона – 0,5 мг/кг. Коррекция гемостаза включает трансфузии свежезамороженной плазмы в сочетании с назначением гепарина в дозе 50-100 мг на кг массы тела в сутки. Свежезамороженная плазма содержит антитела, белки и, кроме того, содержит факторы свертывания крови, в частности, антитромбин ІІІ, уровень которого существенно падает при развитии сепсиса, что, в свою очередь, обуславливает депрессию фибринолиза и развитие ДВС синдрома.
Восстановительная терапия сепсиса новорожденных.
В восстановительный период необходимы строгое соблюдение гигиенического режима, коррекция биоценоза кишечника, проведение антимикотической терапии (при необходимости), обеспечение грудного вскармливания. В этот же период времени целесообразно проведение нейротрофической и метаболической терапии, направленной на восстановление окислительных внутриклеточных процессов, повышение анаболической направленности обмена веществ. С этой целью показано назначение комплексов витаминов и микроэлементов, незаменимых аминокислот, ферментов, карнитина.
При выраженных нарушениях иммунного гомеостаза, подтвержденных лабораторными исследованиями, показано проведение иммунотерапии. В этот период в зависимости от характера иммунных нарушений могут быть использованы такие препараты, как глюкозаминилмурамилдипептид (Ликопид), рекомбинантный интерферон- ?2b (Виферон). Прогноз Прогноз при сепсисе новорожденных серьезный, летальность при различных видах сепсиса колеблется сейчас от 25 до 55%.
Ключевые слова: новорожденные



 Caffrey Osvald E, Prentice P. NICU clinical guideline: antibiotics for the prevention and treatment of early-onset neonatal infection. Arch Dis Child Educ Pract Ed 2014; 99:98-100.
Caffrey Osvald E, Prentice P. NICU clinical guideline: antibiotics for the prevention and treatment of early-onset neonatal infection. Arch Dis Child Educ Pract Ed 2014; 99:98-100.