Нейронтин® (Neurontin®) инструкция по применению
📜 Инструкция по применению Нейронтин®
💊 Состав препарата Нейронтин®
✅ Применение препарата Нейронтин®
📅 Условия хранения Нейронтин®
⏳ Срок годности Нейронтин®
Описание лекарственного препарата
Нейронтин®
(Neurontin®)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для печатного издания справочника Видаль 2023 года.
Дата обновления: 2023.08.29
Владелец регистрационного удостоверения:
Контакты для обращений:
ВИАТРИС ООО
(Россия)
Код ATX:
N03AX12
(Габапентин)
Лекарственные формы
| Нейронтин® |
Таб., покр. пленочной оболочкой, 600 мг: 20, 50 или 100 шт. рег. №: ЛП-(000961)-(РГ-RU) |
|
|
Таб., покр. пленочной оболочкой, 800 мг: 20, 50 или 100 шт. рег. №: ЛП-(000961)-(РГ-RU) |
Форма выпуска, упаковка и состав
препарата Нейронтин®
Таблетки, покрытые пленочной оболочкой белого цвета, двояковыпуклые, эллиптической формы, с гравировкой «NT» и «16», риской между гравировкой на одной стороне и риской на другой стороне.
Вспомогательные вещества: полоксамер 407 — 80 мг, коповидон — 64.8 мг, крахмал кукурузный — 49.2 мг, магния стеарат — 6 мг; пленочная оболочка: опадрай белый YS-1-18111 — 24 мг, воск травяной (канделила) — 0.6 мг.
10 шт. — блистеры (2) — пачки картонные×.
10 шт. — блистеры (5) — пачки картонные×.
10 шт. — блистеры (10) — пачки картонные×.
Таблетки, покрытые пленочной оболочкой белого цвета, двояковыпуклые, эллиптической формы, с гравировкой «NT» и «26», риской между гравировкой на одной стороне и риской на другой стороне.
Вспомогательные вещества: полоксамер 407 — 106.7 мг, коповидон — 86.4 мг, крахмал кукурузный — 65.6 мг, магния стеарат — 8 мг; пленочная оболочка: опадрай белый YS-1-18111 — 32 мг, воск травяной (канделила) — 0.8 мг.
10 шт. — блистеры (2) — пачки картонные×.
10 шт. — блистеры (5) — пачки картонные×.
10 шт. — блистеры (10) — пачки картонные×.
× пачки картонные с контролем первого вскрытия или без него.
Фармакологическое действие
Габапентин легко проникает в ткань головного мозга и предотвращает развитие судорог в различных животных моделях эпилепсии. Габапентин не обладает сродством к рецепторам ГАМКА (гамма-аминомасляная кислота) и ГАМКВ и не влияет на метаболизм ГАМК. Габапентин не связывается с рецепторами других нейромедиаторов, присутствующих в головном мозге и не влияет на натриевые каналы.
Габапентин обладает высоким сродством и связывается с α-2-δ (альфа-2-дельта) субъединицей потенциалозависимых кальциевых каналов и предполагается, что связь габапентина с α-2-δ субъединицей участвует в механизме противосудорожного эффекта у животных. При скрининге большой группы молекул-мишеней для этого лекарственного препарата показано, что единственной мишенью для него является субъединица α-2-δ.
Результаты, полученные в нескольких доклинических моделях, показывают, что фармакологическая активность габапентина может реализовываться путем связывания с субъединицей α-2-δ посредством подавления высвобождения возбуждающих нейромедиаторов в некоторых участках центральной нервной системы. Такая активность может лежать в основе противосудорожного действия габапентина. Значимость этих механизмов действия габапентина для его противосудорожных эффектов у людей все еще необходимо установить. Эффективность габапентина также показана в нескольких доклинических исследованиях на животных моделях болевого синдрома. Предполагают, что специфическое связывание габапентина с субъединицей α-2-δ приводит к нескольким разным эффектам, которые могут отвечать за обезболивающее действие в животных моделях. Обезболивающее действие габапентина может проявляться на уровне спинного мозга, а также на уровне высших мозговых центров посредством взаимодействий с нисходящими путями, подавляющими передачу болевых импульсов. Значение этих свойств габапентина, выявленных в доклинических исследованиях, неизвестно.
Клиническая эффективность и безопасность
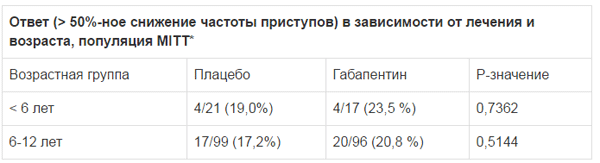
В рамках клинического исследования адъювантной терапии парциальных судорожных приступов у детей в возрасте от 3 до 12 лет было продемонстрировано наличие количественных, но статистически недостоверных различий по частоте снижения количества приступов на более чем 50% в группе габапентина по сравнению с группой плацебо. Дополнительный анализ частоты ответа на терапию в зависимости от возраста (при рассмотрении возраста как непрерывной переменной или при выделении двух возрастных подгрупп: 3–5 лет и 6–12 лет) не выявил статистически достоверного влияния возраста на эффективность терапии.
Результаты данного дополнительного анализа представлены в таблице ниже.
* Модифицированная популяция в зависимости от назначенного лечения (MITT) определялась как совокупность всех пациентов, рандомизированных в группу исследуемой терапии и имевших подлежащие оценке дневники судорожных приступов за период длительностью 28 дней в рамках исходной и двойной слепой фаз исследования.
Фармакокинетика
Всасывание
После приема внутрь Cmax габапентина в плазме крови достигается в течение 2–3 ч. Биодоступность габапентина имеет тенденцию к снижению с увеличением дозы препарата. Абсолютная биодоступность при приеме капсул дозировкой 300 мг составляет приблизительно 60%. Пища, в т.ч. с высоким содержанием жиров, не оказывает клинически значимого влияния на параметры фармакокинетики габапентина.
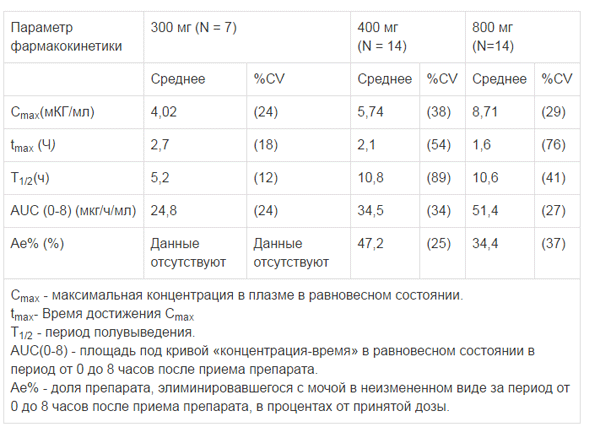
Фармакокинетика габапентина не изменяется при многократном приеме препарата. Несмотря на то, что в рамках клинических исследований концентрация габапентина в плазме крови обычно варьировала в диапазоне 2–20 мкг/мл, это не позволяло прогнозировать ни эффективность, ни безопасность препарата. Параметры фармакокинетики представлены в таблице.
Таблица. Сводные средние (CV, %) параметры фармакокинетики габапентина в равновесном состоянии при многократном приеме с интервалом дозирования длительностью 8 ч
Cmax – максимальная концентрация в плазме крови в равновесном состоянии.
Tmax – время достижения Cmax.
Т1/2 – период полувыведения.
AUC(0-8) – площадь под кривой зависимости концентрации в плазме крови от времени в равновесном состоянии в период от 0 до 8 ч после приема препарата.
Ae% – доля препарата, элиминировавшегося с мочой в неизмененном виде за период от 0 до 8 ч после приема препарата, в процентах от принятой дозы.
Распределение
Габапентин не связывается с белками плазмы крови, и его Vd составляет 57.7 л. У пациентов с эпилепсией концентрация габапентина в спинномозговой жидкости (СМЖ) составляет приблизительно 20% от минимальной равновесной концентрации в плазме крови. Габапентин выделяется с грудным молоком.
Метаболизм
Отсутствуют данные о метаболизме габапентина в организме человека. Габапентин не вызывает индукции неспецифических оксидаз печени, ответственных за метаболизм лекарственных средств.
Выведение
Габапентин выводится в неизмененном виде исключительно путем почечной экскреции. Т1/2 габапентина не зависит от принятой дозы и составляет в среднем от 5 до 7 ч.
Линейность/нелинейность параметров фармакокинетики
Биодоступность габапентина снижается с увеличением принятой дозы, что влечет за собой нелинейность параметров фармакокинетики, которые включают в расчет показатель биодоступности (F), например Ae%, CL/F, Vd/F. Фармакокинетика элиминации (параметры параметров, не включающие F, такие как CLr и T1/2) лучше описывается линейной моделью. Css габапентина в плазме крови являются предсказуемыми на основе данных по кинетике при однократном приеме.
Фармакокинетика у особых групп пациентов
У пожилых лиц и пациентов с нарушением функции почек клиренс габапентина из плазмы крови снижается. Константа элиминации, плазменный клиренс и почечный клиренс габапентина прямо пропорциональны КК.
Габапентин удаляется из плазмы крови при гемодиализе. Пациентам с нарушением функции почек или находящимся на гемодиализе рекомендуется коррекция дозы препарата («Режим дозирования»).
Фармакокинетика габапентина у детей изучалась у 50 здоровых добровольцев в возрасте от 1 месяца до 12 лет. В целом, концентрация габапентина в плазме крови детей старше 5 лет аналогична таковой у взрослых при применении препарата в эквивалентной дозе на основании расчета мг/кг массы тела.
В рамках исследования фармакокинетики у 24 здоровых детей в возрасте от 1 до 48 месяцев параметры экспозиции препарата (AUC) были приблизительно на 30% ниже, Cmax – ниже, а клиренс – выше при расчете на единицу массы тела по сравнению с доступными опубликованными данными по кинетике препарата у детей в возрасте старше 5 лет.
Показания препарата
Нейронтин®
Эпилепсия
- монотерапия парциальных судорог с вторичной генерализацией и без нее у взрослых и детей в возрасте 12 лет и старше (эффективность и безопасность монотерапии у детей в возрасте до 12 лет не установлены);
- как дополнительное средство при лечении парциальных судорог с вторичной генерализацией и без нее у взрослых и детей в возрасте 3 лет и старше (безопасность и эффективность дополнительной терапии габапентином у детей в возрасте менее 3 лет не установлены);
Нейропатическая боль
- лечение нейропатической боли у взрослых в возрасте 18 лет и старше (эффективность и безопасность у пациентов в возрасте до 18 лет не установлены).
Режим дозирования
Препарат принимают внутрь независимо от приема пищи, запивая достаточным количеством жидкости (например, стаканом воды). Допускается деление таблетки пополам.
Дозирование
Для всех показаний схема титрации дозы для начала терапии представлена в таблице №1. Эта схема представлена для взрослых пациентов и подростков в возрасте 12 лет и старше. Схема титрации для детей в возрасте младше 12 лет представлена ниже под отдельным подзаголовком.
Таблица 1. Схема титрации дозы препарата в начале терапии
Прекращение терапии габапентином
Согласно современной клинической практике при необходимости отмены терапии габапентином это следует делать постепенно в течение минимум одной недели вне зависимости от показаний.
Эпилепсия
При эпилепсии обычно требуется длительное лечение. Доза препарата при этом определяется лечащим врачом в зависимости от индивидуальной переносимости и эффективности препарата.
Взрослые и дети в возрасте старше 12 лет
В клинических исследованиях эффективная доза составляла от 900 до 3600 мг/сут. Терапию можно начать по схеме, описанной выше в таблице 1, или с дозы 300 мг 3 раза/сут в 1-й день. В последующем в зависимости от ответа пациента на терапию и переносимости препарата доза может быть повышена на 300 мг/сут каждые 2-3 дня, максимально до 3600 мг/сут. У некоторых пациентов может быть целесообразным более медленное повышение дозы. Минимальное время, за которое можно повысить дозу до 1800 мг/сут составляет 1 неделя, 2400 мг/сут — 2 недели, а для достижения максимальной суточной дозы 3600 мг/сут необходимо не менее 3 недель. В длительных открытых клинических исследованиях была отмечена хорошая переносимость препарата в дозах до 4800 мг/сут. Общая суточная доза должна быть разделена на 3 приема. Максимальный интервал между дозами при трехкратном приеме препарата не должен превышать 12 ч во избежание возобновления судорог.
Дети в возрасте 3-12 лет
Начальная доза препарата варьирует от 10 до 15 мг/кг/сут, которую назначают равными дозами 3 раза/сут и повышают до эффективной приблизительно в течение 3 дней. Эффективная доза габапентина у детей в возрасте 5 лет и старше составляет 25-35 мг/кг/сут равными дозами в 3 приема. Эффективная доза габапентина у детей в возрасте от 3 до 5 лет составляет 40 мг/кг/сут равными дозами в 3 приема. Отмечена хорошая переносимость препарата в дозах до 50 мг/кг/сут при длительном применении. Максимальный интервал между приемом доз препарата не должен превышать 12 ч во избежание возобновления судорог.
Нет необходимости контролировать концентрацию габапентина в плазме. Он может применяться в комбинации с другими противосудорожными препаратами без учета изменения его концентрации в плазме или концентрации других противосудорожных препаратов в сыворотке.
Нейропатическая боль у взрослых
Терапию можно начать по схеме, описанной выше в таблице 1. Альтернативный способ дозирования — начальная доза составляет 900 мг/сут в 3 приема равными дозами. В последующем в зависимости от ответа пациента на терапию и переносимости препарата доза может быть повышена на 300 мг/сут каждые 2-3 дня, максимально до 3600 мг/сут. У некоторых пациентов может быть целесообразным более медленное повышение дозы. Минимальное время, за которое можно повысить дозу до 1800 мг/сут составляет 1 неделя, 2400 мг/сут — 2 недели, а для достижения максимальной суточной дозы 3600 мг/сут необходимо не менее 3 недель.
При лечении периферической нейропатической боли при таких состояниях, как болевая форма диабетической невропатии и постгерпетическая невралгия, эффективность и безопасность применения препарата в течение периода дольше 5 месяцев в клинических исследованиях не изучались. В случае, если пациенту требуется продолжение терапии периферической нейропатической боли дольше 5 месяцев, лечащий врач должен оценить клинический статус пациента и определить необходимость дополнительной терапии.
Рекомендации для всех показаний
У пациентов в тяжелом состоянии, например, в случае пониженной массы тела, после трансплантации органов и т.д., дозу следует повышать медленнее, либо используя меньшие дозы, либо делая большие интервалы перед повышением дозы.
Применение у пожилых пациентов (в возрасте старше 65 лет)
Вследствие возрастного снижения функции почек пожилым пациентам может требоваться коррекция дозы (более подробная информация в таблице 2). Сонливость, периферические отеки и астения у пожилых пациентов могут встречаться чаще.
Применение у пациентов с почечной недостаточностью
Пациентам с нарушенной функцией почек и/или у пациентов, находящихся на гемодиализе рекомендуется снижение дозы габапентина согласно таблице 2:
Таблица 2. Дозирование габапентина у взрослых пациентов в зависимости от функции почек
А Суточную дозу следует назначать в 3 приема; сниженные дозы препарата показаны пациентам с нарушением функции почек (клиренс креатинина <79 мл/мин).
Б Назначают по 300 мг через день.
В У пациентов с КК <15 мл/мин суточную дозу необходимо уменьшить пропорционально КК (например, пациент с КК 7.5 мл/мин должен получить половину дозы, которую получает пациент с КК 15 мл/мин).
Применение у пациентов, находящихся на гемодиализе
Пациентам с анурией, находящимся на гемодиализе, которые ранее не принимали габапентин, препарат рекомендуется назначать в насыщающей дозе 300-400 мг, а затем применять его по 200-300 мг после каждых 4 ч гемодиализа. В дни, когда диализ не проводится, лечение проводить не следует.
Для пациентов со сниженной функцией почек, проходящих диализ, поддерживающая доза габапентина должна подбираться в соответствии с рекомендациями, представленными в таблице 2. В дополнение к поддерживающей терапии рекомендуется прием 200-300 мг габапентина после каждой 4-часовой процедуры диализа.
Побочное действие
Нежелательные реакции, наблюдаемые в клинических исследованиях у пациентов с эпилепсией (при применении габапентина в качестве монотерапии или в комбинации с другими противосудорожными препаратами) или нейропатическими болями, представлены ниже и распределены по системам органов и частоте. Категория частоты определялась следующим образом: очень часто (≥1/10); часто (от ≥1/100 до <1/10); нечасто (от ≥1/1000 до <1/100); редко (от ≥1/10000 до <1/1000); очень редко (<1/10000). Если категория частоты была различной в разных исследованиях, то нежелательной реакции присваивалась более высокая категория.
Нежелательным реакциям, о которых сообщалось в процессе применения препарата после регистрации, присвоена категория частоты «неизвестно» (частоту нельзя рассчитать на основании имеющихся данных).
В каждом разделе по частоте нежелательные реакции представлены в порядке уменьшения серьезности.
Инфекционные и паразитарные заболевания: очень часто — вирусные инфекции; часто — пневмония, инфекция дыхательных путей, инфекция мочевыводящих путей, другие виды инфекции, средний отит.
Со стороны крови и лимфатической системы: часто — лейкопения; неизвестно — тромбоцитопения.
Со стороны иммунной системы: нечасто — аллергические реакции, включая крапивницу; неизвестно — гиперчувствительность, включая системные реакции, такие как лихорадка, высыпания, гепатит, лимфаденопатия, эозинофилия и другие.
Со стороны обмена веществ и питания: часто — анорексия, повышение аппетита.
Психические нарушения: часто — враждебность, спутанность сознания, депрессия, беспокойство, нервозность; нечасто — ухудшение психического состояния; неизвестно — суицидальные мысли, галлюцинации.
Со стороны нервной системы: очень часто — сонливость, головокружение, атаксия; часто — судороги, гиперкинезия, дизартрия, амнезия, тремор, бессонница, головная боль, нарушение чувствительности (например, парестезии, гипестезия), нарушение координации, нистагм, усиление, ослабление или отсутствие рефлексов; нечасто — гипокинезия; редко – потеря сознания; неизвестно — другие нарушения движения (например, хореоатетоз, дискинезия и дистония).
Со стороны органа зрения: часто — нарушение зрения (такие как, амблиопия, диплопия).
Со стороны органа слуха и лабиринтные нарушения: часто – вертиго, неизвестно — шум в ушах.
Со стороны сердечно-сосудистой системы: часто — симптомы вазодилатации или артериальная гипертензия; нечасто — ощущение сердцебиения.
Со стороны дыхательной системы, органов грудной клетки и средостения: часто — одышка, бронхит, фарингит, кашель, ринит.
Со стороны пищеварительной системы: часто — запор, диарея, сухость слизистой оболочки полости рта или глотки, диспепсия, метеоризм, тошнота, рвота, боль в животе, заболевания зубов, гингивит; неизвестно — панкреатит.
Со стороны печени и желчевыводящих путей: неизвестно — гепатит, желтуха.
Со стороны кожи и подкожных покровов: часто — отек лица, пурпура (чаще всего ее описывали как кровоподтеки, возникавшие при физической травме), кожная сыпь, акне, зуд кожи; неизвестно — синдром Стивенса-Джонсона, ангионевротический отек, анафилаксия, многоформная эритема, алопеция, лекарственная кожная сыпь, включая эозинофилию и системные реакции (см. раздел «Особые указания»).
Со стороны костно-мышечной системы: часто — миалгии, артралгия, боль в спине, подергивания мышц; неизвестно — рабдомиолиз, миоклонус.
Со стороны мочевыделительной системы: неизвестно — недержание мочи, острая почечная недостаточность.
Со стороны половых органов и молочной железы: часто — импотенция; неизвестно — увеличение в объеме молочных желез, гинекомастия, половая дисфункция (включая изменения либидо, нарушения эякуляции и аноргазмию).
Общие расстройства и нарушения в месте введения: очень часто — утомляемость, лихорадка; часто — периферические отеки, нарушение походки, астения, боль различной локализации, общее недомогание, гриппоподобный синдром; нечасто — генерализованный отек; неизвестно — синдром отмены (наиболее часто отмечались следующие нежелательные реакции: беспокойство, бессонница, тошнота, боли различной локализации и повышенное потоотделение), боль в груди. Зарегистрированы случаи внезапной необъяснимой смерти, связь которых с лечением габапентином не установлена.
Лабораторные и инструментальные данные: часто — снижение концентрации белых кровяных телец, повышение массы тела; нечасто — повышение активности АЛТ, АСТ и концентрации билирубина в плазме крови, гипергликемия; редко — гипогликемия (преимущественно у пациентов с сахарным диабетом); неизвестно — гипонатриемия, повышение активности КФК.
Травмы, интоксикации и осложнения манипуляций: часто — травмы, переломы, ссадины, связанные с падениями.
Имеются сообщения о развитии острого панкреатита на фоне терапии габапентином. Причинная связь с габапентином остается неясной (см. раздел «Особые указания»).
Имеются сообщения о случаях миопатии с повышением активности креатинкиназы у пациентов с терминальной стадией почечной недостаточности, находящихся на гемодиализе.
Случаи инфекции дыхательных путей, среднего отита, бронхита и судорог были отмечены только в клинических исследованиях. Кроме того, в клинических исследованиях сообщалось о случаях агрессивного поведения и гиперкинезов у детей.
Противопоказания к применению
- повышенная чувствительность к габапентину или вспомогательным компонентам препарата.
С осторожностью следует назначать препарат при почечной недостаточности (см. раздел «Режим дозирования»).
Применение при беременности и кормлении грудью
Беременность
Общий риск, обусловленный эпилепсией и противоэпилептическими препаратами
Риск рождения детей с врожденными аномалиями у матерей, которые проходят лечение противосудорожными препаратами, увеличивается в 2-3 раза. Чаще всего наблюдается расщелина верхней губы и неба, пороки развития сердечно-сосудистой системы и дефекты нервной трубки. При этом прием нескольких противосудорожных препаратов может быть связан с большим риском пороков развития, чем в случае монотерапии. Поэтому, если это возможно, следует применять один из противосудорожных препаратов. Женщинам детородного возраста, а также всем женщинам, у которых возможно наступление беременности, следует проконсультироваться у квалифицированного специалиста. В случае если женщина планирует беременность, следует еще раз оценить необходимость продолжения противосудорожной терапии. При этом противосудорожные препараты не следует отменять резко, т.к. это может вести к возобновлению припадков с тяжелыми последствиями для матери и ребенка. В редких случаях у детей, матери которых страдают эпилепсией, наблюдалась задержка развития. При этом невозможно определить, связана ли задержка развития с генетическими или социальными факторами, болезнью матери или противосудорожной терапией.
Риск, обусловленный габапентином
Габапентин проникает через плацентарный барьер. При применении габапентина сообщалось о врожденных пороках развития и неблагоприятных исходах беременности, однако адекватные контролируемые исследования применения препарата у беременных женщин отсутствуют, и невозможно сделать однозначное заключение о связи габапентина с повышенным риском врожденных аномалий или других неблагоприятных исходах развития при применении его во время беременности вследствие наличия самой эпилепсии и одновременного применения других противоэпилептических лекарственных препаратов в каждом зарегистрированном случае. В экспериментах на животных была показана токсичность препарата в отношении плода. В отношении возможного риска у людей данных нет. Поэтому габапентин следует применять во время беременности только в том случае, если предполагаемая польза для матери оправдывает возможный риск для плода.
Период грудного вскармливания
Габапентин выводится с грудным молоком, влияние его на вскармливаемого ребенка неизвестно, поэтому во время кормления грудью Нейронтин® следует назначать только в том случае, если польза для матери явно перевешивает риск для младенца.
Фертильность
В исследованиях на животных не отмечали влияния габапентина на фертильность.
Применение при нарушениях функции почек
С осторожностью следует назначать препарат при почечной недостаточности.
Применение у детей
Эффективность и безопасность монотерапии парциальных судорог у детей в возрасте до 12 лет не установлены. Безопасность и эффективность дополнительной терапии парциальных судорог габапентином у детей в возрасте менее 3 лет не установлены.
Применение у пожилых пациентов
Вследствие возрастного снижения функции почек пожилым пациентам может требоваться коррекция дозы.
Особые указания
Суицидальные идеи и поведение
Сообщалось о суицидальных мыслях и поведении у пациентов, получавших противоэпилептические средства по нескольким показаниям. Мета-анализ рандомизированных плацебо-контролируемых исследований противоэпилептических средств продемонстрировал небольшое повышение риска появления суицидальных мыслей и поведения. Механизм повышения такого риска неизвестен.
Наблюдались случаи суицидальных мыслей и поведения у пациентов, получавших лечение габапентином в ходе пострегистрационного применения (см. раздел «Побочное действие»).
В случае появления признаков суицидальных мыслей или поведения пациентам (и лицам, осуществляющим уход за пациентами) следует обратиться к врачу.
Пациентов, получающих эти препараты, следует тщательно наблюдать на предмет появления признаков суицидальных мыслей и поведения, а также следует рассмотреть необходимость проведения соответствующего лечения. В случае появления суицидальных мыслей и поведения следует рассмотреть возможность прекращения терапии габапентином.
Острый панкреатит
В случае развития острого панкреатита на фоне приема габапентина, следует оценить возможность отмены препарата.
Судороги (синдром «отмены»)
Хотя синдром «отмены», сопровождающийся развитием судорог, при лечении габапентином не отмечен, резкое прекращение терапии противосудорожными препаратами у пациентов с эпилепсией может провоцировать развитие эпилептического статуса (см. раздел «Режим дозирования»).
Как и при применении других противоэпилептических препаратов, на фоне применения габапентина может отмечаться увеличение частоты судорог или появление другого типа судорог.
Так же как и в случае с другими противоэпилептическими средствами, попытки отменить все сопутствующие противоэпилептические средства, чтобы начать монотерапию габапентином в случае рефрактерности к лечению у пациентов, принимающих несколько противоэпилептических средств, в основном не заканчиваются успехом.
Считается, что габапентин неэффективен при первичных генерализованных припадках, например, абсансах, и даже может усиливать такие припадки у некоторых пациентов. В связи с этим применять габапентин у пациентов со смешанными припадками, включая абсансы, следует с осторожностью.
Пожилые пациенты
Систематические исследования пациентов в возрасте 65 лет и старше, принимающих габапентин, не проводились. В двойном слепом исследовании применения габапентина при нейропатической боли у пациентов в возрасте 65 лет и старше наблюдалась более высокая частота сонливости, периферических отеков и астении по сравнению с пациентами в возрасте младше 65 лет. За исключением этих результатов при клиническом обследовании данной группы пациентов было показано, что профиль нежелательных реакций у них не отличался от остальных.
Дети
Влияние длительной терапии (более 36 недель) габапентином на способность к обучению, интеллект и развитие детей и подростков достаточно не изучено. Следует оценить соотношение возможного риска и пользы при назначении длительной терапии.
Злоупотребление и зависимость
В базе данных пострегистрационных наблюдений имеются сообщения о случаях злоупотребления препаратом и зависимости от него. Как и в случае назначения любого препарата, влияющего на ЦНС, врачам следует тщательно изучать анамнез пациентов на предмет злоупотребления препаратами и наблюдать за ними с целью выявления возможных признаков злоупотребления габапентином (например, стремление необоснованно получить препарат, развитие устойчивости к терапии габапентином, необоснованное повышение дозы препарата).
DRESS-синдром (лекарственная реакция с эозинофилией и системными симптомами)
На фоне приема противоэпилептических препаратов, в т.ч. габапентина, сообщалось о случаях развития тяжелых жизнеугрожающих реакций гиперчувствительности, таких как лекарственная сыпь с сопутствующей эозинофилией и системными симптомами. Необходимо помнить о том, что ранние признаки реакции гиперчувствительности, такие как повышение температуры тела, лимфаденопатия, могут развиваться даже в отсутствии кожной сыпи. В случае появления подобных симптомов, необходимо немедленное обследование пациента. Если не найдено других причин, кроме применения габапентина, применение препарата следует отменить.
Анафилаксия
Прием габапентина может привести к развитию анафилаксии. Следующие симптомы и признаки отмечали в случаях развития анафилаксии на фоне приема габапентина – затруднение дыхания, отек губ, горла и языка, также отмечалось выраженное снижение АД, требующее срочного медицинского вмешательства. Следует предупредить пациентов о том, что при развитии признаков или симптомов развития анафилаксии следует прекратить прием препарата и обратиться за медицинской помощью.
Лабораторные тесты
При совместном применении габапентина и других противосудорожных средств были зарегистрированы ложноположительные результаты при определении белка в моче с помощью тест-полосок Ames N-Multistix SG®. Для определения белка в моче рекомендуется пользоваться более специфичным методом преципитации сульфосалициловой кислотой.
Влияние на ЦНС
Во время лечения габапентином наблюдались случаи головокружения и сонливости, которые могут увеличивать вероятность получения случайной травмы (при падении). В пострегистрационном периоде также сообщалось о случаях спутанности сознания, потери сознания и нарушения умственной деятельности. Поэтому пациентам следует рекомендовать соблюдать осторожность до тех пор, пока им не станут известны возможные эффекты этого лекарственного препарата.
Одновременное применение анальгетиков и других лекарственных препаратов, подавляющих ЦНС
При одновременном применении с опиоидными анальгетиками может отмечаться повышение концентрации габапентина в плазме крови. В связи с этим пациенты, которым требуется проведение одновременной терапии с лекарственными препаратами, подавляющими ЦНС, включая опиоидные анальгетики, нуждаются в тщательном наблюдении на предмет развития признаков угнетения ЦНС, таких как сонливость, седативный эффект и угнетение функции дыхания. Дозы габапентина или одновременно применяемых препаратов, подавляющих ЦНС, включая опиоидные анальгетики, должны быть снижены соответствующим образом (см. раздел «Лекарственное взаимодействие»).
Следует соблюдать осторожность при назначении габапентина одновременно с опиоидами в связи с риском угнетения ЦНС. В популяционном наблюдательном исследовании с использованием контрольной группы у пациентов, принимающих опиоиды, одновременное назначение опиоидов и габапентина было связано с повышенным риском возникновения смертельных исходов, связанных с применением опиоидов, по сравнению с применением только опиоидов (скорректированное отношение шансов [сОШ], 1.49 [95% ДИ, 1.18 до 1.88, p<0.001]).
Совместное применение с антацидами
Габапентин рекомендуется принимать примерно через 2 ч после приема антацида.
Влияние на способность к управлению транспортными средствами и механизмами
Во время приема препарата пациентам не рекомендуется управлять транспортными средствами или пользоваться потенциально опасной техникой до подтверждения отсутствия негативного влияния препарата на выполнение этих функций.
Габапентин влияет на ЦНС и может вызывать головокружение, сонливость, спутанность сознания, потерю сознания или другие симптомы со стороны ЦНС. Даже при незначительной или умеренной выраженности эти нежелательные реакции могут представлять опасность для пациентов, управляющих транспортными средствами или другими механизмами. Особенно велика такая вероятность в начале лечения или после повышения дозы препарата Нейронтин®.
Передозировка
При однократном приеме габапентина в дозе 49 г наблюдались следующие симптомы: головокружение, двоение в глазах, нарушение речи, сонливость, потеря сознания, состояние заторможенности и диарея легкой степени, которые полностью исчезали при проведении симптоматической терапии. Следует учитывать, что после приема габапентина в высоких дозах уменьшается его всасывание в кишечнике.
При передозировке габапентином возможно развитие комы, особенно при одновременном применении других лекарственных препаратов, подавляющих ЦНС.
В рамках экспериментов на мышах и крысах, которым препарат вводился в дозах до 8000 мг/кг, не удалось установить значение летальной дозы габапентина при пероральном введении. Признаки острой токсичности у животных включали атаксию, затруднение дыхания, птоз, гипоактивность или возбуждение.
Лечение: несмотря на то, что габапентин может выводиться при гемодиализе, имеющийся опыт показывает, что обычно подобной необходимости не возникает. Пациентам с тяжелой почечной недостаточностью может быть показан гемодиализ.
Лекарственное взаимодействие
Имеются сообщения о спонтанных случаях, а также по информации из литературных источников возможно угнетение дыхания, симптомы седации и смерть, связанные с приемом габапентина при одновременном назначении с лекарственными препаратами, подавляющими ЦНС, включая опиоидные анальгетики.
В некоторых из этих случаев авторы считали, что одновременное применение габапентина с опиоидами является особой проблемой у ослабленных пациентов, у пожилых пациентов, у пациентов с серьезными сопутствующими респираторными заболеваниями, у пациентов, которым одновременно назначается несколько лекарственных средств, и у пациентов, которые злоупотребляют психоактивными веществами.
В исследовании с участием здоровых добровольцев (N=12) при применении габапентина в дозе 600 мг через 2 ч после приема морфина в виде капсул с пролонгированным высвобождением по 60 мг отмечается увеличение среднего значения AUC габапентина на 44% по сравнению с монотерапией габапентином. В связи с этим пациенты, которым требуется проведение одновременной терапии с опиоидными анальгетиками, должны находиться под тщательным контролем на предмет развития признаков угнетения ЦНС, таких как сонливость, седация и угнетение дыхания, а дозу габапентина и опиоидных анальгетиков следует соответствующим образом снизить.
Взаимодействия между габапентином и фенобарбиталом, фенитоином, вальпроевой кислотой и карбамазепином не отмечено. Фармакокинетика габапентина в равновесном состоянии одинакова у здоровых людей и пациентов, получающих другие противосудорожные средства.
Одновременное применение габапентина с пероральными контрацептивами, содержащими норэтистерон и/или этинилэстрадиол, не сопровождается изменениями фармакокинетики обоих компонентов.
Одновременное применение габапентина с антацидами, содержащими алюминий и магний, сопровождается снижением биодоступности габапентина примерно на 24% (см. раздел «Особые указания»).
Пробенецид не влияет на почечную экскрецию габапентина.
Небольшое снижение (14%) почечной экскреции габапентина при одновременном приеме циметидина, вероятно, не имеет клинического значения.
При одновременном применении напроксена (250 мг) и габапентина (125 мг) отмечалось повышение абсорбции габапентина с 12% до 15%. Габапентин не оказывает влияния на фармакокинетические параметры напроксена. Указанные дозы препаратов меньше минимальных терапевтических. Одновременное применение данных препаратов в больших дозах не изучалось.
Условия хранения препарата Нейронтин®
Препарат следует хранить в недоступном для детей месте, при температуре не выше 25°C.
Срок годности препарата Нейронтин®
Срок годности — 2 года. Не применять после даты истечения срока годности.
Условия реализации
Препарат отпускают по рецепту.
Контакты для обращений
ВИАТРИС ООО
(Россия)

|
|
ООО «Пфайзер» переименовано в ООО «Виатрис». ООО «Виатрис» 125315 Москва, Ленинградский пр-т, д. 72, к. 4 |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Аналоги препарата
Габагамма®
(WOERWAG PHARMA, Германия)
Габапентин
(AUROBINDO PHARMA, Индия)
Габапентин
(ПИК-ФАРМА, Россия)
Габапентин Канон
(КАНОНФАРМА ПРОДАКШН, Россия)
Габапентин-СЗ
(СЕВЕРНАЯ ЗВЕЗДА, Россия)
Катэна®
(BELUPO, Pharmaceuticals & Cosmetics, Хорватия)
Конвалис®
(ЛЕККО, Россия)
Нейронтин®
(VIATRIS SPECIALTY, США)
Тебантин®
(GEDEON RICHTER, Венгрия)
Все аналоги
Нейронтин таблетки — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
П N013567/02-090616
Торговое название:
Нейронтин®
Международное непатентованное название:
Габапентин
Лекарственная форма:
таблетки покрытые пленочной оболочкой
Состав
1 таблетка 600 мг содержит:
Активное вещество: 600,0 мг габапентина.
Вспомогательные вещества: полоксамер 407 80,0 мг, коповидон 64,8 мг, крахмал кукурузный 49,2 мг, магния стеарат 6,0 мг; пленочная оболочка: опадрай белый YS-1-18111 24,0 мг [тальк 17,4 мг, гипролоза 6,6 мг], воск травяной (канделила) 0,6 мг.
1 таблетка 800 мг содержит:
Активное вещество: 800,0 мг габапентина.
Вспомогательные вещества: полоксамер 407 106,7 мг, коповидон 86,4 мг, крахмал
кукурузный 65,6 мг, магния стеарат 8,0 мг; пленочная оболочка: опадрай белый YS-I-18111 32,0 мг [тальк 23,2 мг, гипролоза 8,8 мг], воск травяной (канделила) 0,8 мг.
Описание
Дозировка 600 мг: белые эллиптической формы таблетки, покрытые пленочной оболочкой, с гравировкой «NT» и «16». риской между гравировкой на одной стороне и риской на другой стороне.
Дозировка 800 мг: белые эллиптической формы таблетки, покрытые пленочной оболочкой, с гравировкой «NT» и «26». риской между гравировкой на одной стороне и риской на другой стороне.
Фармакотерапевтическая группа:
противоэпилептическое средство.
КодАТХ: 1М03АХ12.
Фармакологические свойства
Фармакодинамика
Механизм действия
Габапентин легко проникает в ткань головного мозга и предотвращает развитие судорог в различных животных моделях эпилепсии. Габапентин не обладает сродством к рецепторам ГАМКА (гамма-аминомасляная кислота) и ГАМКв и не влияет на метаболизм ГАМК. Габапентин не связывается с рецепторами других нейромедиаторов, присутствующих в головном мозге и не влияет на натриевые каналы.
Габапентин обладает высоким сродством и связывается с α-2-δ(альфа-2- дельта) субъединицей потенциалзависимых кальциевых каналов и предполагается, что связь габапентина с α-2-δ субъединицей участвует в механизме противосудорожного эффекта у животных. При скрининге большой группы молекул-мишеней для этого лекарственного препарата показано, что единственной мишенью для него является субъединица а28. Результаты, полученные в нескольких доклинических моделях, показывают, что фармакологическая активность габапентина может реализовываться путем связывания с субъединицей α-2-δ посредством подавления высвобождения возбуждающих нейромедиаторов в некоторых участках центральной нервной системы. Такая активность может лежать в основе противосудорожного действия габапентина. Значимость этих механизмов действия габапентина для его противосудорожных эффектов у людей все еще необходимо установить. Эффективность габапентина также показана в нескольких доклинических исследованиях на животных моделях болевого синдрома. Предполагают, что специфическое связывание габапентина с субъединицей α-2-δ приводит к нескольким разным эффектам, которые могут отвечать за обезболивающее действие в животных моделях. Обезболивающее действие габапентина может проявляться на уровне спинного мозга, а также на уровне высших мозговых центров посредством взаимодействий с нисходящими путями, подавляющими передачу болевых импульсов. Значение этих свойств габапентина, выявленных в доклинических исследованиях, неизвестно.
Клиническая эффективность и безопасность
В рамках клинического исследования адъювантной терапии парциальных судорожных приступов у детей в возрасте от 3 до 12 лет было продемонстрировано наличие количественных, но статистически недостоверных различий по частоте снижения количества приступов на более чем 50 % в группе габапентина по сравнению с группой плацебо. Дополнительный анализ частоты ответа на терапию в зависимости от возраста (при рассмотрении возраста как непрерывной переменной или при выделении двух возрастных подгрупп: 3-5 лет и 6 — 12 лет) не выявил статистически достоверного влияния возраста на эффективность терапии. Результаты данного дополнительного анализа представлены в таблице ниже.
*Модифицированная популяция «по намерению лечить» (MITT) определялась как совокупность всех пациентов, рандомизированных в группу исследуемой терапии и имевших подлежащие оценке дневники судорожных приступов за период длительностью 28 дней в рамках исходной и двойной слепой фаз исследования.
Фармакокинетика
Всасывание
После приема внутрь максимальная концентрация габапентина в плазме достигается в течение 2-3 часов. Биодоступность габапентина имеет тенденцию к снижению с увеличением дозы препарата. Абсолютная биодоступность при приеме капсул дозировки 300 мг составляет приблизительно 60 %. Пища, в том числе с высоким содержанием жиров, не оказывает клинически значимого влияния на параметры фармакокинетики габапентина. Фармакокинетика габапентина не изменяется при многократном приеме препарата. Несмотря на то, что в рамках клинических исследований концентрация габапентина в плазме обычно варьировала в диапазоне 2-20 мкг/мл, она не позволяла прогнозировать ни эффективность, ни безопасность препарата. Параметры фармакокинетики представлены в таблице.
Таблица.
Сводные средние (CV, %) параметры фармакокинетики габапентина в равновесном состоянии при многократном приеме с интервалом дозирования длительностью восемь часов
Распределение
Габапентин не связывается с белками плазмы, и его объем распределения составляет 57,7 л. У пациентов с эпилепсией концентрация габапентина в спинномозговой жидкости (СМЖ) составляет приблизительно 20 % от минимальной равновесной концентрации в плазме. Габапентин проникает в грудное молоко женщин, кормящих грудью.
Биотрансформация
Отсутствуют данные о метаболизме габапентина в организме человека. Габапентин не вызывает индукции неспецифических оксидаз печени, ответственных за метаболизм лекарственных средств.
Выведение
Габапентин выводится в неизмененном виде исключительно путем почечной экскреции. Период полувыведения габапентина не зависит от принятой дозы и составляет в среднем от 5 до 7 часов.
У пожилых лиц и пациентов с нарушением функции почек клиренс габапентина из плазмы снижается. Константа элиминации, плазменный клиренс и почечный клиренс габапентина прямо пропорциональны клиренсу креатинина.
Габапентин удаляется из плазмы при гемодиализе. Пациентам с нарушением функции почек или находящимся на гемодиализе рекомендуется коррекция дозы препарата (см. раздел «Способ применения и дозы»).
Фармакокинетика габапентина у детей изучалась у 50 здоровых добровольцев в возрасте от 1 месяца до 12 лет. В целом, концентрация габапентина в плазме детей старше 5 лет аналогична таковой у взрослых при применении препарата в эквивалентной дозе на основании расчета мг/кг массы тела.
В рамках исследования фармакокинетики у 24 здоровых детей в возрасте от 1 до 48 месяцев параметры экспозиции препарата (AUC) были приблизительно на 30 % ниже, Сmах— ниже, а клиренс- выше при расчете на единицу массы тела по сравнению с доступными опубликованными данными по кинетике препарата у детей в возрасте старше 5 лет.
Линейность/нелинейность параметров фармакокинетики
Биодоступность габапентина снижается с увеличением принятой дозы, что влечет за собой нелинейность параметров фармакокинетики, которые включают в расчет показатель биодоступности (F), например Ае%, CL/F, Vd/F. Фармакокинетика элиминации (параметры параметров, не включающие F, такие как CLr и Т1/2) лучше описывается линейной моделью.
Равновесные концентрации габапентина в плазме являются предсказуемыми на основе данных по кинетике при однократном приеме.
Показания к применению
Эпилепсия
Монотерапия парциальных судорог с вторичной генерализацией и без нее у взрослых и детей в возрасте 12 лет и старше. Эффективность и безопасность монотерапии у детей в возрасте до 12 лет не установлены.
Как дополнительное средство при лечении парциальных судорог с вторичной генерализацией и без нее у взрослых и детей в возрасте 3 лет и старше. Безопасность и эффективность дополнительной терапии габапентином у детей в возрасте менее 3 лет не установлены.
Нейропатическая боль
Лечение нейропатической боли у взрослых в возрасте 18 лет и старше. Эффективность и безопасность у пациентов в возрасте до 18 лет не установлены.
Противопоказания
Гиперчувствительность к габапентину или вспомогательным компонентам препарата.
Эпилепсия
Применение в качестве монотерапии парциальных судорог с вторичной генерализацией и без нее у детей в возрасте до 12 лет.
Применение в качестве дополнительного средства при лечении парциальных судорог с вторичной генерализацией и без нее у детей в возрасте до 3 лет.
Нейропатическая боль
Для лечения нейропатической боли у детей и подростков в возрасте до 18 лет.
С осторожностью
Почечная недостаточность (см. раздел «Способ применения и дозы»).
Применение при беременности и в период грудного вскармливания
Беременность
Отсутствуют данные о применении препарата у беременных женщин.
Общий риск, связанный с эпилепсией и противоэпилептическими препаратами
Риск рождения детей с врожденными аномалиями у матерей, которые проходят лечение противосудорожными препаратами, увеличивается в 2-3 раза. Чаще всего наблюдается расщелина верхней губы и неба, пороки развития сердечно-сосудистой системы и дефекты нервной трубки. При этом прием нескольких противосудорожных препаратов может быть связан с большим риском пороков развития, чем в случае монотерапии. Поэтому, если это возможно, следует применять один из противосудорожных препаратов. Женщинам детородного возраста, а также всем женщинам, у которых возможно наступление беременности, следует проконсультироваться у квалифицированною специалиста. Если женщина планирует беременность, следует еще раз оценить необходимость продолжения противосудорожной терапии. При этом противосудорожные препараты не следует отменять резко, так как это может вести к возобновлению припадков с тяжелыми последствиями для матери и ребенка. В редких случаях у детей, матери которых страдают эпилепсией, наблюдалась задержка развития. При этом невозможно определить, связана ли задержка развития с генетическими или социальными факторами, болезнью матери или противосудорожной терапией.
Риск, обусловленный габапентином
В экспериментах на животных была показана токсичность препарата в отношении плода. В отношении возможного риска у людей данных нет. Поэтому габапентин следует применять во время беременности только в том случае, если предполагаемая польза для матери оправдывает возможный риск для плода.
Невозможно сделать однозначное заключение о связи габапентина с повышенным риском врожденных аномалий при применении его во время беременности вследствие наличия самой эпилепсии и одновременного применения других противоэпилептических лекарственных препаратов в каждом зарегистрированном случае.
Грудное вскармливание
Габапентин выводится с грудным молоком, влияние его на вскармливаемого ребенка неизвестно, поэтому во время кормления грудью Нейронтин следует назначать только в том случае, если польза для матери явно перевешивает риск для младенца.
Фертильность
В исследованиях на животных не отмечали влияния габапентина на фертильность.
Способ применения и дозы
Дозирование
Для всех показаний схема титрации дозы для начала терапии представлена в таблице №1. Эта схема представлена для взрослых пациентов и подростков в возрасте 12 лет и старше. Схема титрации для детей в возрасте младше 12 лет представлена ниже под отдельным подзаголовком.
Таблица №1 Схема титрации дозы препарата в начале терапии
|
День№1 |
День №2 |
День №3 |
|
300 мг 1 раз в сутки |
по 300 мг 2 раза в сутки |
по 300 мг 3 раза в сутки |
Прекращение терапии габапентином
Согласно современной клинической практике при необходимости отмены терапии габапентином это следует делать постепенно в течение минимум одной недели вне зависимости от показаний.
Эпилепсия
При эпилепсии обычно требуется длительное лечение. Доза препарата при этом определяется лечащим врачом в зависимости от индивидуальной переносимости и эффективности препарата.
Взрослые и дети в возрасте старше 12 лет:
в клинических исследованиях эффективная доза составляла от 900 до 3600 мг/сут. Терапию можно начать по схеме, описанной выше в таблице №1 или с дозы 300 мг 3 раза в сутки в первый день. В последующем в зависимости от ответа пациента на терапию и переносимости препарата доза может быть повышена на 300 мг/сут каждые 2-3 дня, максимально до 3600 мг/сут. У некоторых пациентов может быть целесообразным более медленное повышение дозы. Минимальное время, за которое можно повысить дозу до 1800 мг/сут составляет 1 неделя, 2400 мг/сут — 2 недели, а для достижения максимальной суточной дозы 3600 мг/сут необходимо не менее 3 недель. В дилтельных открытых клинических исследованиях была отмечена хорошая переносимость препарата в дозах до 4800 мг/сут. Общая суточная доза должна быть разделена на три приема. Максимальный интервал между дозами при трехкратном приеме препарата не должен превышать 12 ч во избежание возобновления судорог.
Дети в возрасте 3-12 лет: начальная доза препарата варьирует от 10 до 15 мг/кг/сут, которую назначают равными дозами 3 раза в день и повышают до эффективной приблизительно в течение 3 дней. Эффективная доза габапентина у детей в возрасте 5 лет и старше составляет 25-35 мг/кг/сут равными дозами в 3 приема. Эффективная доза габапентина у детей в возрасте от 3 до 5 лет составляет 40 мг/кг/сут равными дозами в 3 приема. Отмечена хорошая переносимость препарата в дозах до 50 мг/кг/сут при длительном применении. Максимальный интервал между приемом доз препарата не должен превышать 12 часов во избежание возобновления судорог.
Нет необходимости контролировать концентрацию габапентина в плазме. Он может применяться в комбинации с другими противосудорожными препаратами без учета изменения его концентрации в плазме или концентрации других противосудорожных препаратов в сыворотке.
Нейропатическая боль
Взрослые
Терапию можно начать по схеме, описанной выше в таблице №1. Альтернативный способ дозирования — начальная доза составляет 900 мг/сут в три приема равными дозами. В последующем в зависимости от ответа пациента на терапию и переносимости препарата доза может быть повышена на 300 мг/сут каждые 2-3 дня, максимально до 3600 мг/сут. У некоторых пациентов может быть целесообразным более медленное повышение дозы. Минимальное время, за которое можно повысить дозу до 1800 мг/сут составляет 1 неделя, 2400 мг/сут — 2 недели, а для достижения максимальной суточной дозы 3600 мг/сут необходимо не менее 3 недель.
При лечении периферической нейропатической боли, при таких состояниях как болевая форма диабетической нейропатии и постгерпетическая невралгия, эффективность и безопасность применения препарата в течение периода дольше 5 месяцев в клинических исследованиях не изучались. В случае, если пациенту требуется продолжение терапии периферической нейропатической боли дольше 5 месяцев, лечащий врач должен оценить клинический статус пациента и определить необходимость дополнительной терапии.
Рекомендации для всех показаний
У пациентов в тяжелом состоянии, например, в случае пониженной массы тела, после трансплантации органов и т.д., дозу следует повышать медленнее, либо используя меньшие дозы, либо делая большие интервалы перед повышением дозы.
Применение у пожилых пациентов (в возрасте старше 65 лет)
Вследствие возрастного снижения функции почек пожилым пациентам может требоваться коррекция дозы (более подробная информация в таблице №2). Сонливость, периферические отеки и астения у пожилых пациентов могут встречаться чаще.
Применение у пациентов с почечной недостаточностью
Больным с нарушенной функцией почек и/или у пациентов, находящихся на гемодиализе рекомендуется снижение дозы габапентина согласно таблице №2:
Таблица №2. Дозирование габапентина у взрослых пациентов в зависимости от функции почек
|
Клиренс креатинина(мл/мин) |
Суточная доза (мг/сут) A |
|
>80 |
900-3600 |
|
50-79 |
600-1800 |
|
30-49 |
300-900 |
|
15-29 |
150Б-600 |
|
<15в |
150Б-300 |
Суточную дозу следует назначать в три приема; сниженные дозы препарата показаны пациентам с нарушением функции почек (клиренс креатинина < 79 мл/мин) Назначают по 300 мг через день.
У пациентов с клиренсом креатинина <15 мл/мин суточную дозу необходимо уменьшить пропорционально клиренсу креатинина (например, пациент с клиренсом креатинина 7,5 мл/мин должен получать половину дозы, которую получает пациент с клиренсом креатинина 15 мл/мин).
Применение у пациентов, находящихся на гемодиализе
Пациентам с анурией, находящимся на гемодиализе, которые ранее не принимали габапентин, препарат рекомендуется назначать в насыщающей дозе 300-400 мг, а затем применять его по 200-300 мг после каждых 4 ч гемодиализа. В дни, когда диализ не проводится, лечение проводить не следует.
Для пациентов со сниженной функцией почек, проходящих диализ, поддерживающая доза габапентина должна подбираться в соответствии с рекомендациями, представленными в Таблице №2. В дополнение к поддерживающей терапии рекомендуется прием 200-300 мг габапентина после каждой 4-часовой процедуры диализа.
Способ введения
Нейронтин» назначают внутрь.
Габапентин можно принимать вне зависимости от приема пищи, запивая достаточным количеством жидкости (например, стаканом воды). Допускается деление таблетки пополам.
Побочное действие
Нежелательные реакции, наблюдаемые в клинических исследованиях у пациентов с эпилепсией (при применении габапентина в качестве монотерапии или в комбинации с другими противосудорожными препаратами) или невропатическими болями, представлены ниже и распределены по системам органов и частоте. Категория частоты определялась следующим образом: очень часто (>1/10); часто (от > 1/100 до < 1/10); нечасто (от > 1/1000 до <1/100); редко (от >1/10000 до <1/1000); очень редко (<1/10000). Если категория частоты была различной в разных исследованиях, то нежелательной реакции присваивалась более высокая категория.
Нежелательным реакциям, о которых сообщалось в процессе применения препарата после регистрации, присвоена категория частоты «неизвестно» (частоту нельзя рассчитать на основании имеющихся данных).
В каждом разделе по частоте нежелательные реакции представлены в порядке уменьшения серьезности.
Инфекционные и паразитарные заболевания: очень часто — вирусные инфекции; часто —пневмония, инфекция дыхательных путей, инфекция мочевыводящих путей, другие виды инфекции, средний отит.
Нарушения со стороны крови и лимфатической системы: часто — лейкопения; неизвестно — тромбоцитопения.
Нарушения со стороны иммунной системы: нечасто — аллергические реакции, включая крапивницу; неизвестно — гиперчувствительность, включая системные реакции, такие как лихорадка, высыпания, гепатит, лимфаденопатия, эозинофилия и другие.
Нарушения со стороны обмена веществ и питания: часто — анорексия, повышение аппетита.
Психические нарушения: часто — враждебность, спутанность сознания, депрессия, беспокойство, нервозность; нечасто — ухудшение психического состояния; неизвестно —галлюцинации.
Нарушения со стороны нервной системы: очень часто — сонливость, головокружение, атаксия; часто — судороги, гиперкинезия, дизартрия, амнезия, тремор, бессонница, головная боль, нарушение чувствительности (например, парестезии, гипестезия), нарушение координации, нистагм, усиление, ослабление или отсутствие рефлексов; нечасто — гипокинезия; редко — потеря сознания; неизвестно — другие нарушения движения (например, хореоатетоз, дискинезия и дистопия).
Нарушения со стороны органа зрения: часто — нарушение зрения (такие как, амблиопия, диплопия).
Нарушения со стороны органа слуха и лабиринтные нарушения: часто — вертиго, неизвестно — шум в ушах.
Нарушения со стороны сердца: нечасто — ощущение сердцебиения.
Нарушения со стороны сосудов: часто — симптомы вазодилатации или артериальная гипертензия.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения:
часто — одышка, бронхит, фарингит, кашель, ринит.
Нарушения со стороны желудочно-кишечного тракта: часто — запор, диарея, сухость слизистой оболочки полости рта или глотки, диспепсия, метеоризм, тошнота, рвота, боль в животе, заболевания зубов, гингивит; неизвестно — панкреатит.
Нарушения со стороны печени и желчевыводящих путей: неизвестно — гепатит, желтуха.
Нарушения со стороны кожи и подкожных покровов: часто — отек лица, пурпура (чаще всего ее описывали как кровоподтеки, возникавшие при физической травме), кожная сыпь, акне, зуд кожи; неизвестно — синдром Стивенса-Джонсона, ангионевротический отек, анафилаксия, мультиформная эритема, алопеция, лекарственная кожная сыпь, включая эозинофилию и системные реакции (см. раздел «Особые указания»).
Нарушения со стороны скелетно-мышечнои и соединительной ткани: часто — миалгии, артралгия, боль в спине, подергивания мышц; неизвестно — рабдомиолиз, миоклонус.
Нарушения со стороны почек и мочевыводящих путей: неизвестно — недержание мочи, острая почечная недостаточность.
Нарушения со стороны половых органов и молочной железы: часто — импотенция; неизвестно — увеличение в объеме молочных желез, гинекомастия, половая дисфункция (включая изменения либидо, нарушения эякуляции и аноргазмию).
Общие расстройства и нарушения в месте введения: очень часто — утомляемость, лихорадка; часто — периферические отеки, нарушение походки, астения, боль различной локализации, общее недомогание, гриппоподобный синдром; нечасто — генерализованный отек; неизвестно — синдром отмены (наиболее часто отмечались следующие нежелательные реакции: беспокойство, бессонница, тошнота, боли различной локализации и повышенное потоотделение), боль в груди. Зарегистрированы случаи внезапной необъяснимой смерти, связь которых с лечением габапентином не установлена.
Лабораторные и инструментальные данные: часто — снижение концентрации белых кровяных телец, повышение массы тела; нечасто — повышение активности аланинаминотрансферазы, аспартатаминотрансферазы и концентрации билирубина в плазме крови, гипергликемия; редко — гипогликемия (преимущественно у пациентов с сахарным диабетом); неизвестно — гипонатриемия, повышение активности креатинфосфокиназы.
Травмы, интоксикации и осложнения манипуляций: часто — травмы, переломы, ссадины, связанные с падениями.
Имеются сообщения о развитии острого панкреатита на фоне терапии габапентином. Причинная связь с габапентином остается неясной (см. раздел «Особые указания»). Имеются сообщения о случаях миопатии с повышением активности креатинкиназы у пациентов с терминальной стадией почечной недостаточности, находящихся на гемодиализе. Случаи инфекции дыхательных путей, среднего отита, бронхита и судорог были отмечены только в клинических исследованиях. Кроме того, в клинических исследованиях сообщалось о случаях агрессивного поведения и гиперкинезов у детей.
Передозировка
При однократном приеме 49 г габапентина наблюдались следующие симптомы: головокружение, двоение в глазах, нарушение речи, сонливость, потеря сознания, состояние заторможенности и диарея легкой степени, которые полностью исчезали при проведении симптоматической терапии. Следует учитывать, что после приема высоких доз габапентина, уменьшается его всасывание в кишечнике.
При передозировке габапентином возможно развитие комы, особенно при одновременном применении других лекарственных препаратов, подавляющих ЦНС.
Несмотря на то, что габапентин может выводиться при гемодиализе, имеющийся опыт показывает, что обычно подобной необходимости не возникает. Пациентам с тяжелой почечной недостаточностью может быть показан гемодиализ.
В рамках экспериментов на мышах и крысах, которым препарат вводился в дозах до 8000 мг/кг, не удалось установить значение летальной дозы габапентина при пероральном введении. Признаки острой токсичности у животных включали атаксию, затруднение дыхания, птоз, гипоактивность или возбуждение.
Взаимодействие с другими лекарственными средствами
Имеются сообщения о спонтанных случаях, а также по информации из литературных источников возможно угнетение дыхания и/или симптомы седации, связанные с приемом габапентина и опиоидных анальгетиков. В некоторых из этих случаев авторы связывали данные симптомы с одновременным применением габапентина и опиоидов, особенно у пожилых пациентов.
В исследовании с участием здоровых добровольцев (N=12) при применении 600 мг габапентина через 2 часа после приема морфина в виде капсул с пролонгированным высвобождением по 60 мг отмечается увеличение среднего значения AUC габапентина на 44 % по сравнению с монотерапией габапентином. В связи с этим пациенты, которым требуется проведение одновременной терапии с опиоидными анальгетиками, должны находиться под тщательным контролем на предмет развития признаков угнетения центральной нервной системы, таких как сонливость, седация и угнетение дыхания, а дозу габапентина и опиоидных анальгетиков следует соответствующим образом снизить. Взаимодействия между габапентином и фенобарбиталом, фенитоином, вальпроевой кислотой и карбамазепином не отмечено. Фармакокинетика габапентина в равновесном состоянии одинакова у здоровых людей и пациентов, получающих другие противосудорожные средства. Одновременное применение габапентина с пероральными контрацептивами, содержащими норэтистерон и/или этинилэстрадиол, не сопровождается изменениями фармакокинетики обоих компонентов.
Одновременное применение габапентина с антацидами, содержащими алюминий и магний, сопровождается снижением биодоступности габапентина примерно на 24 % (см. раздел «Особые указания»).
Пробенецид не влияет на почечную экскрецию габапентина.
Небольшое снижение (14 %) почечной экскреции габапентина при одновременном приеме циметидина, вероятно, не имеет клинического значения.
При одновременном применении напроксена (250 мг) и габапентина (125 мг) отмечалось повышение абсорбции габапентина с 12 % до 15 %. Габапентин не оказывает влияния на фармакокинетические параметры напроксена. Указанные дозы препаратов меньше минимальных терапевтических. Одновременное применение данных препаратов в больших дозах не изучалось.
Особые указания
Суицидальные идеи и поведение
Имеются сообщения о возникновении суицидальных мыслей или поведения у пациентов, получающих лечение противоэпилептическими препаратами по различным показаниям.
Мета-анализ рандомизированных плацебо-контролируемых исследований противоэпилептических средств также продемонстрировал небольшое повышение риска появления суицидальных мыслей и поведения. Механизм повышения такого риска неизвестен и имеющиеся данные не исключают возможности такого повышения риска для габапентина.
Поэтому пациентов, получающих эти препараты, следует тщательно наблюдать на предмет появления признаков суицидальных мыслей или поведения. У таких пациентов следует рассмотреть необходимость проведения соответствующего лечения. В случае появления признаков суицидальных мыслей или поведения пациентам или их попечителям следует обратиться к врачу.
Острый панкреатит
В случае развития острого панкреатита на фоне приема габапентина, следует оценить возможность отмены препарата.
Судороги (синдром «отмены»)
Хотя синдром «отмены», сопровождающийся развитием судорог, при лечении габапентином не отмечен, резкое прекращение терапии противосудорожными препаратами у пациентов с эпилепсией может провоцировать развитие эпилептического статуса (см. раздел «Способ применения и дозы»).
Как и при применении других противоэпилептических препаратов, на фоне применения габапентина может отмечаться увеличение частоты судорог или появление другого типа судорог.
Так же как и в случае с другими противоэпилептическими средствами, попытки отменить все сопутствующие противоэпилептические средства, чтобы начать монотерапию габапентином в случае рефрактерности к лечению у пациентов, принимающих несколько противоэпилептических средств, в основном не заканчиваются успехом.
Считается, что габапентин неэффективен при первичных генерализованных припадках, например, абсансах, и даже может усиливать такие припадки у некоторых пациентов. В связи с этим применять габапентин у пациентов со смешанными припадками, включая абсансы, следует с осторожностью.
Опиоидные анальгетики
Пациенты, которым требуется проведение одновременной терапии с опиоидными анальгетиками, должны находиться под тщательным контролем на предмет развития признаков угнетения центральной нервной системы, таких как сонливость, седация и угнетение дыхания.
У пациентов, которые одновременно получают габапентин и морфин может наблюдаться повышение концентрации габапентина. Дозу габапентина и опиоидных анальгетиков следует соответствующим образом снизить (см. раздел «Взаимодействие с другими лекарственными средствами»).
Полжилые пациенты
Систематические исследования пациентов в возрасте 65 лет и старше, принимающих габапентин, не проводились. В двойном слепом исследовании применения габапентина при невропатической боли у пациентов в возрасте 65 лет и старше наблюдалась более высокая частота сонливости, периферических отеков и астении по сравнению с пациентами в возрасте младше 65 лет. За исключением этих результатов при клиническом обследовании данной группы пациентов было показано, что профиль нежелательных реакций у них не отличался от остальных.
Дети
Влияние длительной терапии (более 36 недель) габапентином на способность к обучению, интеллект и развитие детей и подростков достаточно не изучено. Следует оценить соотношение возможного риска и пользы при назначении длительной терапии.
Злоупотребление и зависимость
В базе данных пострегистрационных наблюдений имеются сообщения о случаях злоупотребления препаратом и зависимости от него. Как и в случаях назначения любого препарата, влияющего на ЦНС, врачам следует тщательно изучать анамнез пациентов на предмет злоупотребления препаратами и наблюдать за ними с целью выявления возможных признаков злоупотребления габапентином (например, стремление необоснованно получить препарат, развитие устойчивости к терапии габапентином, необоснованное повышение дозы препарата).
DRESS—синдром (лекарственная реакция с эозинофилиеи и системными симптомами)
На фоне приема противоэпилептических препаратов, в том числе габапентина, сообщалось о случаях развития тяжелых жизнеугрожающих реакций гиперчувствительности, таких как лекарственная сыпь с сопутствующей эозинофилиеи и системными симптомами. Необходимо помнить о том, что ранние признаки реакции гиперчувствительности, такие как повышение температуры тела, лимфаденопатия, могут развиваться даже в отсутствии кожной сыпи. В случае появления подобных симптомов, необходимо немедленное обследование пациента.
Если не найдено других причин, кроме применения габапентина, применение препарата следует отменить.
Анафилаксия
Прием габапентина может привести к развитию анафилаксии. Следующие симптомы и признаки отмечали в случаях развития анафилаксии на фоне приема габапентина — затруднение дыхания, отек губ, горла и языка, также отмечалось выраженное снижение артериального давления, требующее срочного медицинского вмешательства. Следует предупредить пациентов о том, что при развитии признаков или симптомов развития анафилаксии следует прекратить прием препарата и обратиться за медицинской помощью.
Лабораторные тесты
При совместном применении габапентина и других противосудорожных средств были зарегистрированы ложноположительные результаты при определении белка в моче с помощью тест-полосок Ames N-Multistix SG®. Для определения белка в моче рекомендуется пользоваться более специфичным методом преципитации сульфосалициловой кислотой.
Влияние на ЦНС
Во время лечения габапентином наблюдались случаи головокружения и сонливости, которые могут увеличивать вероятность получения случайной травмы (при падении). В пострегистрационном периоде также сообщалось о случаях спутанности сознания, потери сознания и нарушения умственной деятельности. Поэтому пациентам следует рекомендовать соблюдать осторожность до тех пор, пока им не станут известны возможные эффекты этого лекарственного препарата.
При одновременном применении с опиоидными анальгетиками может отмечаться повышение концентрации габапентина в плазме крови. В связи с этим пациент нуждается в тщательном наблюдении на предмет развития признаков угнетения центральной нервной системы (ЦНС), таких как сонливость, седация и угнетение функции дыхания. Дозы габапентина или опиоидных анальгетиков должны быть снижены соответствующим образом (см. раздел «Взаимодействие с другими лекарственными средствами»).
Совместное применение с антаиидами
Габапентин рекомендуется принимать примерно через 2 ч после приема антацида.
Влияние на способность управления транспортными средствами и работать с механизмами
Во время приема препарата пациентам не рекомендуется управлять транспортными средставми или пользоваться потенциально опасной техникой до подтверждения отсутствия негативного влияния препарата на выполнение этих функций.
Габапентин влияет на ЦНС и может вызывать головокружение, сонливость, спутанность сознания, потерю сознания или другие симптомы со стороны ЦНС. Даже при незначительной или умеренной выраженности эти нежелательные реакции могут представлять опасность для пациентов, управляющих транспортными средствами или другими механизмами. Особенно велика такая вероятность в начале лечения или после повышения дозы препарата Нейронтин.
Форма выпуска
Таблетки покрытые пленочной оболочкой, 600 мг и 800 мг.
По 10 таблеток в блистеры (контурная ячейковая упаковка) из ПВХ/ПЭ/ПВДХ/алюминиевой фольги с виниловым покрытием.
По 2, 5 или 10 блистеров с инструкцией по применению в картонную пачку.
Условия хранения
При температуре не выше 25 °С.
Хранить в недоступном для детей месте.
Срок годности
2 года.
Не использовать после даты истечения срока годности.
Условия отпуска
Отпускается по рецепту.
Производитель:
«Пфайзер Фармасьютикалз ЭлЭлСи», Пуэрто-Рико
Адрес: км 1,9, Роуд 698, Вега Байя, Пуэрто-Рико 00693.
Выпускающий контроль качества:
«Пфайзер Мэнюфэкчуринг Дойчленд ГмбХ», Германия
Адрес: Моосвальдаллее 1, 79090 Фрайбург, Германия.
Претензии потребителей направлять по адресу:
ООО «Пфайзер»
123317, Москва, Пресненская наб., д. 10 БЦ «Башня на набережной» (Блок С)
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Нежелательные реакции, наблюдаемые в клинических исследованиях у пациентов с эпилепсией (при применении габапентина в качестве монотерапии или в комбинации с другими противосудорожными препаратами) или невропатическими болями, представлены ниже и распределены по системам органов и частоте. Категория частоты определялась следующим образом: очень часто (≥1/10); часто (от ≥1/100 до <1/10); нечасто (от ≥1/1000 до <1/100); редко (от ≥1/10000 до <1/1000); очень редко (<1/10000). Если категория частоты была различной в разных исследованиях, то нежелательной реакции присваивалась более высокая категория.
Нежелательным реакциям, о которых сообщалось в процессе применения препарата после регистрации, присвоена категория частоты «неизвестно» (частоту нельзя рассчитать на основании имеющихся данных).
В каждом разделе по частоте нежелательные реакции представлены в порядке уменьшения серьезности.
Инфекционные и паразитарные заболевания: очень часто — вирусные инфекции; часто —пневмония, инфекция дыхательных путей, инфекция мочевыводящих путей, другие виды инфекции, средний отит.
Нарушения со стороны крови и лимфатической системы: часто — лейкопения; неизвестно— тромбоцитопения.
Нарушения со стороны иммунной системы: нечасто — аллергические реакции, включая крапивницу; неизвестно — гиперчувствительность, включая системные реакции, такие как лихорадка, высыпания, гепатит, лимфаденопатия, эозинофилия и другие.
Нарушения со стороны обмена веществ и питания: часто — анорексия, повышение аппетита.
Психические нарушения: часто — враждебность, спутанность сознания, депрессия, беспокойство, нервозность; нечасто — ухудшение психического состояния; неизвестно — галлюцинации.
Нарушения со стороны нервной системы: очень часто — сонливость, головокружение, атаксия; часто — судороги, гиперкинезия, дизартрия, амнезия, тремор, бессонница, головная боль, нарушение чувствительности (например, парестезии, гипестезия), нарушение координации, нистагм, усиление, ослабление или отсутствие рефлексов; нечасто — гипокинезия; редко – потеря сознания; неизвестно — другие нарушения движения (например, хореоатетоз, дискинезия и дистония).
Нарушения со стороны органа зрения: часто — нарушение зрения (такие как, амблиопия, диплопия).
Нарушения со стороны органа слуха и лабиринтные нарушения: часто – вертиго, неизвестно — шум в ушах.
Нарушения со стороны сердца: нечасто — ощущение сердцебиения.
Нарушения со стороны сосудов: часто — симптомы вазодилатации или артериальная гипертензия.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения:
часто — одышка, бронхит, фарингит, кашель, ринит.
Нарушения со стороны желудочно-кишечного тракта: часто — запор, диарея, сухость слизистой оболочки полости рта или глотки, диспепсия, метеоризм, тошнота, рвота, боль в животе, заболевания зубов, гингивит; неизвестно — панкреатит.
Нарушения со стороны печени и желчевыводящих путей: неизвестно — гепатит, желтуха. Нарушения со стороны кожи и подкожных покровов: часто — отек лица, пурпура (чаще всего ее описывали как кровоподтеки, возникавшие при физической травме), кожная сыпь, акне, зуд кожи; неизвестно — синдром Стивенса-Джонсона, ангионевротический отек, анафилаксия, мультиформная эритема, алопеция, лекарственная кожная сыпь, включая эозинофилию и системные реакции (см. раздел «Особые указания»).
Нарушения со стороны скелетно-мышечной и соединительной ткани: часто — миалгии, артралгия, боль в спине, подергивания мышц; неизвестно — рабдомиолиз, миоклонус. Нарушения со стороны почек и мочевыводящих путей: неизвестно — недержание мочи, острая почечная недостаточность.
Нарушения со стороны половых органов и молочной железы: часто — импотенция; неизвестно — увеличение в объеме молочных желез, гинекомастия, половая дисфункция (включая изменения либидо, нарушения эякуляции и аноргазмию).
Общие расстройства и нарушения в месте введения: очень часто — утомляемость, лихорадка; часто — периферические отеки, нарушение походки, астения, боль различной локализации, общее недомогание, гриппоподобный синдром; нечасто — генерализованный отек; неизвестно — синдром отмены (наиболее часто отмечались следующие нежелательные реакции: беспокойство, бессонница, тошнота, боли различной локализации и повышенное потоотделение), боль в груди. Зарегистрированы случаи внезапной необъяснимой смерти, связь которых с лечением габапентином не установлена.
Лабораторные и инструментальные данные: часто — снижение концентрации белых кровяных телец, повышение массы тела; нечасто — повышение активности аланинаминотрансферазы, аспартатаминотрансферазы и концентрации билирубина в плазме крови, гипергликемия; редко — гипогликемия (преимущественно у пациентов с сахарным диабетом); неизвестно — гипонатриемия, повышение активности креатинфосфокиназы.
Травмы, интоксикации и осложнения манипуляций: часто — травмы, переломы, ссадины, связанные с падениями.
Имеются сообщения о развитии острого панкреатита на фоне терапии габапентином.
Причинная связь с габапентином остается неясной (см. раздел «Особые указания»).
Имеются сообщения о случаях миопатии с повышением активности креатинкиназы у пациентов с терминальной стадией почечной недостаточности, находящихся на гемодиализе. Случаи инфекции дыхательных путей, среднего отита, бронхита и судорог были отмечены только в клинических исследованиях. Кроме того, в клинических исследованиях сообщалось о случаях агрессивного поведения и гиперкинезов у детей.
Обобщенные научные материалы по действующему веществу препарата Нейронтин® (таблетки, покрытые пленочной оболочкой, 600 мг)
Дата последней актуализации: 12.01.2022
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Владелец РУ
- Условия хранения
- Срок годности
- Источники информации
- Фармакологическая группа
- Характеристика
- Фармакология
- Показания к применению
- Нозологическая классификация (МКБ-10)
- Противопоказания
- Применение при беременности и кормлении грудью
- Побочные действия
- Взаимодействие
- Передозировка
- Способ применения и дозы
- Меры предосторожности
- Заказ в аптеках Москвы
- Аналоги (синонимы) препарата Нейронтин®
Действующее вещество
ATX
Владелец РУ
Гедеке ГмбХ
Условия хранения
При температуре не выше 25 °C.
Хранить в недоступном для детей месте.
Срок годности
таблетки, покрытые пленочной оболочкой 600 мг блистер ПВХ/ПЭ/ПВДХ/алюминиевая фольга, 800 мг блистер ПВХ/ПЭ/ПВДХ/алюминиевая фольга — 2 года.
капсулы 300 мг упаковка контурная ячейковая, 100 мг упаковка контурная ячейковая, 400 мг упаковка контурная ячейковая — 3 года.
Не применять по истечении срока годности, указанного на упаковке.
Источники информации
www.rxlist.com, 2021.
Фармакологическая группа
Характеристика
Кристаллическое твердое вещество от белого до почти белого цвета, легко растворяется в воде и как в основных, так и в кислых водных растворах. Молекулярная масса 171,24 Да.
Фармакология
Механизм действия
Точные механизмы, с помощью которых габапентин оказывает обезболивающее и противоэпилептическое действие, неизвестны. Габапентин имеет структурное сходство с нейромедиатором ГАМК, но не влияет на его связывание, поглощение или разложение. Исследования in vitro показали, что габапентин с высоким сродством связывается с субъединицей α2β потенциалзависимых кальциевых каналов, однако влияние этого связывания на терапевтические эффекты габапентина неизвестно.
Фармакокинетика
Все фармакологические эффекты после применения габапентина обусловлены активностью исходного соединения, габапентин не подвергается значительному метаболизму в организме человека.
Биодоступность
Пероральная биодоступность габапентина не пропорциональна дозе, по мере увеличения дозы биодоступность уменьшается. Биодоступность габапентина составляет примерно 60, 47, 34, 33 и 27% после приема в дозах 900, 1200, 2400, 3600 и 4800 мг/сут в 3 приема соответственно. Пища лишь незначительно влияет на скорость и степень всасывания габапентина (увеличение AUC и Cmax на 14%).
Распределение
Менее 3% габапентина циркулирует в связанном с белками плазмы виде. Кажущийся Vd габапентина после в/в введения в дозе 150 мг составляет (58±6) л (среднее значение ± стандартное отклонение). У пациентов с эпилепсией Cmin, достигаемая между двумя приемами в спинномозговой жидкости, составляла примерно 20% от соответствующей концентрации в плазме крови.
Элиминация
Габапентин выводится из системного кровотока почками в неизмененном виде. Габапентин метаболизируется в организме человека незначительно.
T1/2 габапентина составляет от 5 до 7 ч, не зависит от дозы и не меняется после многократного приема. Константа скорости выведения габапентина, плазменный и почечный клиренс прямо пропорциональны Cl креатинина. У пожилых пациентов и пациентов с нарушением функции почек плазменный клиренс габапентина снижен. Габапентин можно удалить из плазмы путем гемодиализа.
Особые группы пациентов
Возраст. Влияние возраста изучалось у пациентов 20–80 лет. Кажущийся пероральный клиренс (CL/F) габапентина снижался с возрастом примерно с 225 мл/мин у лиц моложе 30 лет до примерно 125 мл/мин у лиц старше 70 лет. Почечный клиренс (CLr) и CLr с поправкой на площадь поверхности тела также снижались с возрастом, однако снижение почечного клиренса габапентина с возрастом в значительной степени можно объяснить снижением функции почек.
Пол. Хотя формальных исследований для сравнения фармакокинетики габапентина у мужчин и женщин не проводилось, по-видимому, фармакокинетические параметры для мужчин и женщин схожи и нет значительных гендерных различий.
Раса. Фармакокинетические различия в зависимости от расы не изучались. Поскольку габапентин в основном выводится почками и нет серьезных расовых различий в Cl креатинина, фармакокинетических различий в зависимости от расы не ожидается.
Дети. Фармакокинетика габапентина изучалась у 48 детей от 1 мес до 12 лет после дозы примерно 10 мг/кг. Cmax в плазме крови была одинаковой для всех возрастных групп и наблюдалась через 2–3 ч после введения дозы. В целом у детей от 1 мес до <5 лет экспозиция (AUC) была примерно на 30% ниже, чем в возрасте 5 лет и старше. Соответственно, пероральный клиренс, нормализованный по массе тела, был выше у детей младшего возраста. CL/F габапентина был прямо пропорционален Cl креатинина. T1/2 габапентина составлял в среднем 4,7 ч и был одинаковым для всех исследуемых возрастных групп.
Был проведен популяционный фармакокинетический анализ среди 253 педиатрических пациентов от 1 мес до 13 лет. Пациенты получали габапентин в дозе от 10 до 65 мг/кг/сут 3 раза в день. CL/F был прямо пропорционален Cl креатинина, и эта зависимость была аналогичной после однократной дозы и в состоянии равновесия. При нормализации по массе тела у детей младше 5 лет наблюдались более высокие значения перорального клиренса по сравнению с детьми в возрасте 5 лет и старше. Клиренс сильно варьировал у детей младше 1 года. Нормализованные значения CL/F, наблюдаемые у педиатрических пациентов от 5 лет, соответствовали значениям, наблюдаемым у взрослых после однократной дозы. Пероральный Vd, нормализованный по массе тела, был постоянным во всех возрастных группах.
Эти фармакокинетические данные показывают, что эффективная суточная доза у педиатрических пациентов от 3 до 4 лет с эпилепсией должна составлять 40 мг/кг/сут для достижения средних концентраций в плазме, аналогичных тем, которые достигаются у пациентов в возрасте 5 лет и старше, получающих габапентин в дозе 30 мг/кг/сут.
Почечная недостаточность. Пациенты (n=60) с почечной недостаточностью (средний Cl креатинина 13–114 мл/мин) получали однократно 400 мг габапентина перорально. Средний T1/2 габапентина варьировал от примерно 6,5 ч (пациенты с Cl креатинина >60 мл/мин) до 52 ч (Cl креатинина <30 мл/мин), а почечный клиренс — примерно от 90 мл/мин у пациентов с Cl креатинина >60 мл/мин до 10 мл/мин у пациентов с Cl креатинина <30 мл/мин. CL/F снижался примерно со 190 до 20 мл/мин. Педиатрические пациенты с почечной недостаточностью не изучались.
Гемодиализ. В исследовании с участием взрослых пациентов с анурией (n=11) кажущийся T1/2 габапентина в дни без диализа составлял около 132 ч, во время диализа он сокращался до 3,8 ч. Таким образом, гемодиализ оказывает значительное влияние на выведение габапентина у пациентов с анурией.
Печеночная недостаточность. Поскольку габапентин не метаболизируется, исследования у пациентов с нарушением функции печени не проводились.
Канцерогенность, мутагенность, влияние на фертильность
Габапентин вводили перорально мышам и крысам в двухлетних исследованиях канцерогенности. У мышей, получавших дозы до 2000 мг/кг/сут, не выявлено доказательств канцерогенности, связанной с его применением. При дозе 2000 мг/кг экспозиция габапентина в плазме крови (AUC) у мышей была примерно в 2 раза выше, чем у людей при МРДЧ 3600 мг/сут. У крыс увеличение заболеваемости аденомой и карциномой ацинарных клеток поджелудочной железы было обнаружено у самцов крыс, получавших самую высокую дозу (2000 мг/кг), но не при дозах 250 или 1000 мг/кг/сут. При дозе 1000 мг/кг экспозиция габапентина в плазме крови (AUC) у крыс была примерно в 5 раз выше, чем у людей при МРДЧ.
Исследования по изучению механизма индуцированного габапентином канцерогенеза поджелудочной железы у крыс показывают, что габапентин стимулирует синтез ДНК в ацинарных клетках поджелудочной железы крысы in vitro и таким образом может действовать как промотор опухоли за счет усиления митогенной активности. Неизвестно, обладает ли габапентин способностью увеличивать пролиферацию клеток в других типах клеток или у других видов, включая человека.
Габапентин не продемонстрировал мутагенного или генотоксического потенциала в исследованиях in vitro (тест Эймса, тест на генную мутацию в клетках легких китайского хомячка) и in vivo (тест на хромосомную аберрацию, микроядерный тест в клетках костного мозга китайского хомячка, мышей, тест на внеплановый синтез ДНК в гепатоцитах крысы).
У крыс в дозах до 2000 мг/кг не наблюдалось неблагоприятного воздействия на фертильность или репродуктивную функцию. При дозе 2000 мг/кг экспозиция габапентина в плазме (AUC) у крыс была примерно в 8 раз выше, чем у людей при МРДЧ.
Клинические исследования
Постгерпетическая невралгия
Применение габапентина при постгерпетической невралгии оценивали в двух рандомизированных двойных слепых плацебо-контролируемых многоцентровых исследованиях. Популяция включенных в исследование состояла из 563 пациентов с болью в течение более 3 мес после заживления кожной сыпи опоясывающего лишая (таблица 1).
Таблица 1
Контролируемые исследования постгерпетической невралгии: продолжительность, дозы и количество пациентов
| Исследование | Продолжительность исследования | Целевая доза габапентина, мг/сут1 | Число пациентов, получавших габапентин (n=336) | Число пациентов, получавших плацебо (n=227) |
| 1 | 8 нед | 3600 | 113 | 116 |
| 2 | 7 нед | 1800, 2400 | 223 | 111 |
1 Разделена на 3 приема (3 раза в день).
Каждое исследование включало 7- или 8-недельную двойную слепую фазу (3 или 4 нед титрования и 4 нед фиксированной дозы). Пациенты начали лечение с титрования максимальной дозы габапентина 900 мг/сут в течение 3 дней. Затем дозы должны были титроваться с шагом от 600 до 1200 мг/сут с интервалами от 3 до 7 дней до целевой дозы в течение 3–4 нед. Пациенты записывали свои ощущения боли в ежедневный дневник, используя 11-балльную числовую шкалу оценки боли в диапазоне от 0 (отсутствие боли) до 10 (наихудшая из возможных болей). Для рандомизации требовалось не менее 4 баллов по исходному уровню боли. Анализы проводились с использованием популяции, назначенной для лечения (все рандомизированные пациенты, получившие хотя бы одну дозу исследуемого лекарства).
Оба исследования продемонстрировали эффективность по сравнению с плацебо во всех испытанных дозах.
Снижение средней за неделю оценки боли наблюдалось к 1-й нед в обоих исследованиях и сохранялось до конца лечения. Сопоставимые эффекты лечения наблюдались во всех группах активного лечения. Фармакокинетическое и фармакодинамическое моделирование подтвердило эффективность всех доз.
Дополнительная терапия при эпилепсии с парциальными приступами
Эффективность габапентина в качестве дополнительной терапии (в сочетании с другими противоэпилептическими ЛС) была установлена в многоцентровых плацебо-контролируемых двойных слепых клинических исследованиях с параллельными группами с участием взрослых и детей (3 года и старше) с рефрактерными парциальными припадками.
Доказательства эффективности были получены в трех исследованиях, проведенных с участием 705 пациентов (возраст 12 лет и старше), и в одном исследовании, проведенном с участием 247 детей (от 3 до 12 лет). Включенные в исследование пациенты имели в анамнезе не менее 4 парциальных припадков в месяц, несмотря на получение одного или нескольких противоэпилептических ЛС в терапевтических дозах, и наблюдались при установленной для них схеме приема противоэпилептических ЛС в течение 12-недельного исходного периода (6 нед в исследовании с участием детей). Пациентам, у которых продолжались как минимум 2 (или 4 в некоторых исследованиях) приступа в месяц, к существующей терапии в течение 12-недельного периода лечения добавляли габапентин или плацебо. Эффективность оценивали, прежде всего, по доле пациентов с 50% или более снижением частоты приступов от исходного уровня до лечения (частота ответа на лечение) и производного показателя, названного коэффициентом ответа, который определялся как (T − B) / (T + B), где B — исходная частота приступов у пациента, а T — частота приступов у пациента во время лечения. Коэффициент ответа распределяется в диапазоне от −1 до +1. Нулевое значение указывает на отсутствие изменений, в то время как полное устранение приступов дает значение −1, а увеличение числа припадков будет давать положительные значения. Коэффициент ответа −0,33 соответствует снижению частоты приступов на 50%. Приведенные ниже результаты относятся ко всем парциальным припадкам в популяции назначенных для лечения (все пациенты, получившие любые дозы лечения) в каждом исследовании, если не указано иное.
В одном исследовании сравнивали применение габапентина в дозе 1200 мг/сут, разделенной на 3 приема, с плацебо. Частота ответа на лечение составляла 23% (14 из 61) в группе получавших габапентин и 9% (6 из 66) в группе получавших плацебо, разница между группами была статистически значимой. Коэффициент ответа также был лучше в группе получавших габапентин (−0,199), чем в группе плацебо (−0,044), разница также была статистически значимой.
Во втором исследовании сравнивали в основном применение габапентина в дозе 1200 мг/сут, разделенной на 3 приема (n=101), с плацебо (n=98). Дополнительные дозы габапентина (600 мг/сут, n=53 и 1800 мг/сут, n=54) применяли для получения информации о зависимости доза-ответ. Частота ответа на лечение была выше в группе получавших габапентин в дозе 1200 мг/сут (16%), чем в группе получавших плацебо (8%), но разница не была статистически значимой. Частота ответа на дозу 600 мг (17%) также была незначительно выше, чем в группе плацебо, но частота ответа на лечение в группе получавших 1800 мг (26%) была статистически значимо выше, чем в группе получавших плацебо. Коэффициент ответа был лучше в группе получавших габапентин в дозе 1200 мг/сут (−0,103), чем в группе плацебо (−0,022), но эта разница также не была статистически значимой (p=0,224). Лучший ответ был отмечен в группах получавших габапентин в дозе 600 мг/сут (−0,105) и 1800 мг/сут (−0,222), чем в группе получавших 1200 мг/сут, при этом в группе с дозой 1800 мг/сут достигалась статистически значимая разница по сравнению с плацебо.
В третьем исследовании сравнивали применение габапентина в дозе 900 мг/сут, разделенной на 3 приема (n=111), и плацебо (n=109). Дополнительная группа получала дозу 1200 мг/сут (n=52) для получения информации о зависимости доза-ответ. Статистически значимая разница в частоте ответа наблюдалась в группе получавших 900 мг/сут (22%) габапентина по сравнению с группой плацебо (10%). Коэффициент ответа был также статистически значимо выше в группе получавших габапентин в дозе 900 мг/сут (−0,119) по сравнению с группой плацебо (−0,027), так же как и коэффициент ответа в группе получавших габапентин в дозе 1200 мг/сут (−0,184) по сравнению с плацебо.
В каждом исследовании также анализировали действие габапентина на предотвращение вторично генерализованных тонико-клонических судорог. В эти анализы были включены пациенты, которые испытали вторично генерализованный тонико-клонический приступ либо в исходном состоянии, либо в период лечения во всех трех плацебо-контролируемых исследованиях. Было проведено несколько сравнений коэффициента ответа, которые показали статистически значимое преимущество габапентина по сравнению с плацебо и положительные тенденции почти для всех сравнений.
Анализ частоты ответа с использованием объединенных данных всех трех исследований и всех доз (n=162 для габапентина и 89 для плацебо) также показал значительное преимущество габапентина перед плацебо в снижении частоты вторично генерализованных тонико-клонических приступов.
В двух из трех контролируемых исследований использовалось более одной дозы габапентина. В каждом из них результаты не показали постоянно увеличивающейся реакции на дозу. Однако прослеживается очевидная тенденция к повышению эффективности с увеличением дозы.
Хотя формального анализа эффекта в зависимости от пола не проводилось, оценка коэффициента ответа, полученного в клинических исследованиях (398 мужчин, 307 женщин), указывает на отсутствие серьезных гендерных различий. Не выявлено четко прослеживающейся закономерности, указывающей на то, что возраст каким-либо образом влияет на ответ на габапентин. Число пациентов другой расы, кроме европеоидной, было недостаточно, чтобы можно было провести сравнение эффективности среди расовых групп.
В четвертом исследовании с участием детей от 3 до 12 лет сравнивали применение габапентина в дозе 25–35 мг/кг/сут (n=118) и плацебо (n=127). Для всех парциальных припадков в популяции, получавшей лечение, коэффициент ответа был статистически значимо лучше у получавших габапентин (−0,146), чем плацебо (−0,079). В той же популяции частота ответа на лечение габапентином (21%) особо не отличалась от плацебо (18%).
В исследовании с участием детей от 1 мес до 3 лет сравнивали применение 40 мг/кг габапентина (n=38) с плацебо (n=38) у пациентов, которые получали как минимум одно противоэпилептическое ЛС и имели хотя бы один парциальный припадок в течение периода скрининга (в течение 2 нед до этапа включения). Пациенты имели до 48 ч этапа включения и до 72 ч двойного слепого видео-ЭЭГ-мониторинга для записи и подсчета возникновения случаев приступа. Не выявлено статистически значимых различий ни по коэффициенту ответа, ни по частоте ответа.
Показания к применению
Постгерпетическая невралгия у взрослых; парциальные приступы с вторичной генерализацией и без нее у взрослых и детей от 3 лет и старше с эпилепсией (дополнительная терапия).
Противопоказания
Гиперчувствительность.
Применение при беременности и кормлении грудью
Отсутствуют адекватные данные о рисках, связанных с применением габапентина у беременных женщин. В доклинических исследованиях на мышах, крысах и кроликах габапентин был токсичным для развития плода (увеличение скелетных и висцеральных аномалий плода, а также повышение эмбриофетальной токсичности) при введении беременным животным в дозах, аналогичных или более низких, чем используемые в клинических условиях.
В общей популяции населения США оценочный фоновый риск развития серьезных врожденных дефектов и выкидыша при клинически признанных беременностях составляет от 2 до 4 и от 15 до 20% соответственно. Фоновый риск развития серьезных врожденных дефектов и выкидыша для популяции получавших габапентин неизвестен.
Габапентин после перорального приема секретируется с грудным женским молоком. Воздействие на младенца, находящегося на грудном вскармливании, и на продукцию женского молока неизвестно. При принятии решения о кормлении грудью следует учитывать преимущества грудного вскармливания для развития и здоровья ребенка, наряду с клинической потребностью матери в габапентине и любыми потенциальными побочными эффектами габапентина или основного состояния матери для грудного ребенка.
Побочные действия
Дополнительную информацию о перечисленных ниже серьезных побочных реакциях — см. «Меры предосторожности»: лекарственная реакция с эозинофилией и системными симптомами (DRESS-синдром)/полиорганная гиперчувствительность, анафилаксия и ангионевротический отек, сонливость/седативный эффект и головокружение, эпилептический припадок, спровоцированный отменой, эпилептический статус, суицидальное поведение и мысли, нейропсихические побочные реакции (дети от 3 до 12 лет), внезапная и необъяснимая смерть пациентов с эпилепсией.
Опыт клинических исследований
Поскольку клинические исследования проводятся в различных условиях, частота побочных реакций, наблюдаемая в одном исследовании, не может напрямую сравниваться с аналогичной частотой в другом исследовании, и может не отражать частоту, наблюдаемую в клинической практике.
Постгерпетическая невралгия
Наиболее частыми побочными реакциями, связанными с применением габапентина у взрослых, которые не наблюдались с такой же частотой среди пациентов, получавших плацебо, были головокружение, сонливость и периферические отеки. В двух контролируемых исследованиях постгерпетической невралгии 16% пациентов из 336 получавших габапентин, и 9% пациентов из 227 получавших плацебо прекратили лечение из-за побочных реакций. Побочные реакции, которые наиболее часто приводили к отмене габапентина включали головокружение, сонливость и тошноту. В таблице 2 перечислены побочные реакции, которые отмечались по крайней мере у 1% пациентов с постгерпетической невралгией, принимавших габапентин в плацебо-контролируемых исследованиях, и наблюдались чаще, чем в группе плацебо.
Таблица 2
Побочные реакции в объединенных плацебо-контролируемых исследованиях у пациентов с постгерпетической невралгией
| Системно-органный класс и побочная реакция | Габапентин (n=336), % | Плацебо (n=227), % |
| Со стороны организма в целом | ||
| Астения | 6 | 5 |
| Инфекция | 5 | 4 |
| Случайная травма | 3 | 1 |
| Со стороны пищеварительной системы | ||
| Диарея | 6 | 3 |
| Сухость во рту | 5 | 1 |
| Запор | 4 | 2 |
| Тошнота | 4 | 3 |
| Рвота | 3 | 2 |
| Со стороны обмена веществ и питания | ||
| Периферический отек | 8 | 2 |
| Увеличение веса | 2 | 0 |
| Гипергликемия | 1 | 0 |
| Со стороны нервной системы | ||
| Головокружение | 28 | 8 |
| Сонливость | 21 | 5 |
| Атаксия | 3 | 0 |
| Патологическая обстоятельность мышления | 3 | 0 |
| Нарушение походки | 2 | 0 |
| Расстройство координации | 2 | 0 |
| Со стороны дыхательной системы | ||
| Фарингит | 1 | 0 |
| Со стороны органов чувств | ||
| Амблиопия (отмечалась как затуманенность зрения) | 3 | 1 |
| Конъюнктивит | 1 | 0 |
| Диплопия | 1 | 0 |
| Средний отит | 1 | 0 |
Другие побочные реакции, которые отмечались более чем у 1% пациентов, но в равной степени или чаще в группе плацебо, включали боль, тремор, невралгию, боль в спине, диспепсию, одышку и гриппоподобный синдром.
Не наблюдалось клинически значимых различий между мужчинами и женщинами по типу и частоте развития побочных реакций. Не получено достаточно данных о распределении побочных реакций в зависимости от расы.
Эпилепсия с парциальными приступами (дополнительная терапия)
Наиболее частыми побочными реакциями применения габапентина в комбинации с другими противоэпилептическими ЛС у пациентов старше 12 лет, которые не наблюдались с такой же частотой у пациентов, получавших плацебо, были сонливость, головокружение, атаксия, утомляемость и нистагм.
Наиболее частыми побочными реакциями применения габапентина в сочетании с другими противоэпилептическими ЛС у детей от 3 до 12 лет, которые не наблюдались с такой же частотой у пациентов, получавших плацебо, были вирусная инфекция, лихорадка, тошнота и/или рвота, сонливость и проявление враждебности (см. «Меры предосторожности»).
Примерно 7% из 2074 пациентов старше 12 лет и 7% из 449 пациентов от 3 до 12 лет, получавших габапентин в ходе дорегистрационных клинических исследований, прекратили лечение из-за развития побочной реакции. Наиболее часто с отменой лечения у пациентов старше 12 лет связывались сонливость (1,2%), атаксия (0,8%), повышенная утомляемость (0,6%), тошнота и/или рвота (0,6%) и головокружение (0,6%). У детей от 3 до 12 лет наиболее часто отмена лечения ассоциировалась с эмоциональной лабильностью (1,6%), проявлением враждебности (1,3%) и гиперкинезией (1,1%).
В таблице 3 перечислены побочные реакции, которые отмечались как минимум у 1% пациентов старше 12 лет с эпилепсией, получавших габапентин в плацебо-контролируемых исследованиях, и чаще чем при получении плацебо. В этих исследованиях габапентин или плацебо добавляли к текущей противоэпилептической лекарственной терапии.
Таблица 3
Побочные реакции в объединенных плацебо-контролируемых исследованиях с дополнительным введением габапентина у пациентов >12 лет с эпилепсией
| Системно-органный класс и побочная реакция | Габапентин (плюс базовая терапия, n=543), % | Плацебо (плюс базовая терапия, n=378), % |
| Со стороны организма в целом | ||
| Повышенная утомляемость | 11 | 5 |
| Увеличение веса | 3 | 2 |
| Боль в спине | 2 | 1 |
| Периферический отек | 2 | 1 |
| Со стороны ССС | ||
| Вазодилатация | 1 | 0 |
| Со стороны пищеварительной системы | ||
| Диспепсия | 2 | 1 |
| Сухость во рту или горле | 2 | 1 |
| Запор | 2 | 1 |
| Аномалия зубов | 2 | 0 |
| Со стороны нервной системы | ||
| Сонливость | 19 | 9 |
| Головокружение | 17 | 7 |
| Атаксия | 13 | 6 |
| Нистагм | 8 | 4 |
| Тремор | 7 | 3 |
| Дизартрия | 2 | 1 |
| Амнезия | 2 | 0 |
| Депрессия | 2 | 1 |
| Патологическая обстоятельность мышления | 2 | 1 |
| Расстройство координации | 1 | 0 |
| Со стороны дыхательной системы | ||
| Фарингит | 3 | 2 |
| Кашель | 2 | 1 |
| Со стороны кожи и подкожных тканей | ||
| Эрозия кожи | 1 | 0 |
| Со стороны мочеполовой системы | ||
| Импотенция | 2 | 1 |
| Со стороны органов чувств | ||
| Диплопия | 6 | 2 |
| Амблиопия (часто описывается как затуманенность зрения) | 4 | 1 |
Среди побочных реакций, возникающих с частотой как минимум 10% у пациентов, получавших габапентин, сонливость и атаксия показывали положительную зависимость от дозы.
Общая частота и типы наблюдаемых побочных реакций были одинаковыми среди пациентов мужского и женского пола, получавших габапентин. Частота побочных реакций несколько увеличивалась с возрастом у пациентов, получавших габапентин или плацебо. Только 3% пациентов (28 из 921) в плацебо-контролируемых исследованиях были идентифицированы как представители неевропеоидной расы, поэтому недостаточно данных о распределении побочных реакций в зависимости от расы.
В таблице 4 перечислены побочные реакции, отмечавшиеся как минимум у 2% пациентов от 3 до 12 лет с эпилепсией, получавших габапентин в плацебо-контролируемых исследованиях, и чаще чем при применении плацебо.
Таблица 4
Побочные реакции в плацебо-контролируемых исследованиях с дополнительным введением габапентина у детей от 3 до 12 лет с эпилепсией
| Системно-органный класс и побочная реакция | Габапентин (плюс базовая терапия, n=119), % | Плацебо (плюс базовая терапия, n=128), % |
| Со стороны организма в целом | ||
| Вирусная инфекция | 11 | 3 |
| Лихорадка | 10 | 3 |
| Увеличение веса | 3 | 1 |
| Повышенная утомляемость | 3 | 2 |
| Со стороны пищеварительной системы | ||
| Тошнота и/или рвота | 8 | 7 |
| Со стороны нервной системы | ||
| Сонливость | 8 | 5 |
| Проявление враждебности | 8 | 2 |
| Эмоциональная лабильность | 4 | 2 |
| Головокружение | 3 | 2 |
| Гиперкинез | 3 | 1 |
| Со стороны дыхательной системы | ||
| Бронхит | 3 | 1 |
| Респираторная инфекция | 3 | 1 |
Другие побочные реакции, которые отмечались у более чем 2% детей от 3 до 12 лет, но с той же частотой или чаще в группе плацебо, включали фарингит, инфекцию верхних дыхательных путей, головную боль, ринит, судороги, диарею, анорексию, кашель и средний отит.
Опыт пострегистрационного наблюдения
Побочные реакции, наблюдавшиеся в ходе пострегистрационного применения габапентина, приведены ниже. Поскольку сообщения об этих реакциях поступали в добровольном порядке от популяции неопределенного размера, не всегда возможно надежно оценить их частоту или установить причинно-следственную связь с воздействием габапентина.
Со стороны печени и желчевыводящих путей: желтуха.
Отклонения результатов лабораторных исследований: повышенный уровень креатинкиназы, повышенные результаты функциональных проб печени.
Со стороны обмена веществ и питания: гипонатриемия.
Со стороны скелетно-мышечной системы и соединительной ткани: рабдомиолиз.
Со стороны нервной системы: двигательное расстройство.
Нарушения психики: ажитация.
Со стороны репродуктивной системы и молочных желез: увеличение молочных желез, изменение либидо, нарушения эякуляции и аноргазмия.
Со стороны кожи и подкожной ткани: ангионевротический отек (см. «Меры предосторожности»), многоформная эритема, синдром Стивенса-Джонсона.
Сообщалось также о побочных реакциях, сопровождавших резкое прекращение приема габапентина. Наиболее частыми такими реакциями были беспокойство, бессонница, тошнота, боль и повышенное потоотделение.
Взаимодействие
Реклама: ООО «ВЕДАНТА», ИНН 7714886235, erid 4CQwVszH9pUkKJ7jUDd
Реклама: ООО «РЛС-Библиомед» ИНН 7714758963
Реклама: ООО «ВЕДАНТА», ИНН 7714886235, erid 4CQwVszH9pUkKJ7jUDd
Реклама: ООО «РЛС-Библиомед» ИНН 7714758963
Исследования in vitro
Исследования in vitro были проведены для изучения способности габапентина ингибировать основные изоферменты цитохрома P450 (CYP1A2, CYP2A6, CYP2C9, CYP2C19, CYP2D6, CYP2E1 и CYP3A4), которые опосредуют метаболизм ЛС и ксенобиотиков, с использованием микросомальных ферментов печени человека и селективных маркерных субстратов изоформ. Только при максимальной протестированной концентрации (171 мкг/мл, 1 мМ) наблюдалась небольшая степень ингибирования (от 14 до 30%) изоформы CYP2A6. Никакого ингибирования других протестированных изоформ не наблюдалось при концентрациях габапентина до 171 мкг/мл (примерно в 15 раз больше Cmax при дозе 3600 мг/сут).
Данные о ФКВ in vivo получены в исследованиях с участием здоровых взрослых добровольцев и взрослых пациентов с эпилепсией.
Фенитоин
Однократное (400 мг) и многократное (400 мг 3 раза в день) применение габапентина у пациентов с эпилепсией (n=8), которые получали монотерапию фенитоином в течение не менее 2 мес, не оказывало влияния на Cmin фенитоина в плазме крови непосредственно перед приемом очередной дозы, а фенитоин не влиял на фармакокинетику габапентина.
Карбамазепин
Сопутствующее введение габапентина (400 мг 3 раза в день, n=12) не влияло на Cmin карбамазепина и его 10,11-эпоксидного метаболита в плазме крови непосредственно перед приемом очередной дозы. Аналогичным образом фармакокинетика габапентина не изменялась при введении карбамазепина.
Вальпроевая кислота
Средняя Cmin вальпроевой кислоты в сыворотке крови непосредственно перед приемом очередной дозы до и во время сопутствующего применения габапентина (400 мг 3 раза в день, n=17) не изменялась, и вальпроевая кислота не влияла на фармакокинетические параметры габапентина.
Фенобарбитал
Фармакокинетические параметры фенобарбитала или габапентина (300 мг 3 раза в день, n=12) не различались в зависимости от того, применялись ли эти ЛС по отдельности или вместе.
Другие противоэпилептические ЛС
Габапентин не подвергается значительному метаболизму и не влияет на метаболизм обычно одновременно принимаемых противоэпилептических ЛС.
Напроксен
Совместное применение (n=18) напроксена (250 мг) и габапентина (125 мг) увеличивало абсорбцию габапентина на 12–15%. Габапентин не влиял на фармакокинетические параметры напроксена. Эти дозы ниже терапевтических доз обоих ЛС. Степень взаимодействия в пределах рекомендуемых диапазонов доз неизвестна.
Наркотические анальгетики
Гидрокодон. Совместное применение габапентина и гидрокодона снижает воздействие гидрокодона. Возможность изменения воздействия и эффекта гидрокодона следует учитывать в начале или при прекращении приема габапентина у пациента, принимающего гидрокодон.
Совместное применение габапентина (125–500 мг, n=48) снижало Cmax и AUC гидрокодона (10 мг, n=50) дозозависимым образом по сравнению с введением одного гидрокодона. Значения Cmax и AUC были ниже на 3–4% после приема 125 мг габапентина и на 21–22% после приема 500 мг габапентина соответственно. Механизм этого взаимодействия неизвестен. Гидрокодон увеличивает значения AUC габапентина на 14%. Величина взаимодействия при других дозах неизвестна.
Морфин. При одновременном введении габапентина и морфина следует наблюдать за состоянием пациента на предмет развития признаков депрессии ЦНС, таких как сонливость, седативный эффект и угнетение дыхания.
При приеме капсулы морфина с контролируемым высвобождением 60 мг за 2 ч до приема габапентина в дозе 600 мг (n=12), средняя AUC габапентина увеличивалась на 44% по сравнению с применением его без морфина. На значения фармакокинетических параметров морфина прием габапентина через 2 ч после морфина не влиял. Величина взаимодействия при других дозах неизвестна.
Циметидин
При совместном применении циметидина в дозе 300 мг 4 раза в день (n=12) средний CL/F габапентина снизился на 14%, а Cl креатинина на 10%. Таким образом, циметидин, по-видимому, изменяет почечную экскрецию как габапентина, так и креатинина, эндогенного маркера почечной функции. Ожидается, что это небольшое снижение выведения габапентина циметидином имеет клиническое значение. Эффект габапентина на циметидин не оценивался.
Алгелдрат + магния гидроксид
Средняя биодоступность габапентина снижалась примерно на 20% при одновременном приеме антацида, содержащего алгелдрат + магния гидроксид. Рекомендуется принимать габапентин по крайней мере через 2 ч после приема антацида.
Пероральные контрацептивы
Если исходить из значений AUC и T1/2, фармакокинетический профиль комбинации норэтиндрон + этинилэстрадиол после многократного приема был аналогичным как при одновременном применении габапентина (400 мг 3 раза в день, n=13), так и без него. Cmax норэтиндрона была на 13% выше при одновременном назначении с габапентином, ожидается, что это взаимодействие не будет иметь клинического значения.
Пробенецид
Пробенецид — блокатор почечной канальцевой секреции. Фармакокинетические параметры габапентина без пробенецида и с пробенецидом были сопоставимы. Это указывает на то, что габапентин не удаляется путем почечной канальцевой секреции, который блокируется пробенецидом.
Другие ЛС и результаты лабораторных исследований
Поскольку при добавлении габапентина к другим противоэпилептическим ЛС были получены ложноположительные результаты тестов с помощью тест-полоски Ames N-Multistix SG, для определения присутствия белка в моче рекомендуется более специфическая процедура осаждения сульфосалициловой кислотой.
Злоупотребление и лекарственная зависимость
Габапентин не входит в список контролируемых лекарств.
Злоупотребление. Габапентин не проявляет сродства к бензодиазепиновым, опиоидным (мю, дельта или каппа) или каннабиноидным (CB1) клеточным рецепторам. В небольшом количестве пострегистрационных случаев сообщается о неправильном употреблении и злоупотреблении габапентином. Габапентин принимали в дозах, превышающих рекомендованные, по незарегистрированным показаниям. Большинство пациентов, упоминавшихся в этих отчетах, в анамнезе злоупотребляли применением нескольких веществ или принимали габапентин для облегчения симптомов отмены других веществ. При назначении габапентина необходимы тщательная оценка пациента на предмет злоупотребления ЛС в анамнезе и наблюдение за ним на предмет развития признаков и симптомов злоупотребления габапентином (например, развитие толерантности, самостоятельное повышение дозы и поведение, связанное с поиском наркотиков).
Зависимость. Имеются редкие пострегистрационные сообщения о возникновении симптомов абстиненции вскоре после прекращения приема более высоких, чем рекомендуемые, доз габапентина по незарегистрированным показаниям. Такие симптомы включали ажитацию, дезориентацию и спутанность сознания после внезапного прекращения приема габапентина и исчезали после возобновления его приема. У большинства из этих пациентов анамнез включал сведения о злоупотреблении применением нескольких веществ или применении габапентина для облегчения симптомов отмены других веществ. Зависимость и потенциал злоупотребления габапентином в исследованиях с участием людей не оценивались.
Передозировка
Летальная доза не была выявлена у мышей и крыс, получавших перорально габапентин в однократной дозе до 8000 мг/кг. Признаки острой токсичности у животных включали атаксию, затрудненное дыхание, птоз, седативный эффект, гипоактивность или возбуждение.
Сообщалось о случаях острой передозировки габапентина при пероральном приеме в количестве до 49 г. В этих случаях наблюдались диплопия, невнятная речь, сонливость, летаргия и диарея. Все пациенты выздоровели при поддерживающей терапии. Сообщалось о коме, разрешающейся с помощью диализа, у пациентов с ХПН, получавших габапентин.
Габапентин можно удалить с помощью гемодиализа. Хотя гемодиализ не проводился в нескольких зарегистрированных случаях передозировки, он может быть показан в зависимости от клинического состояния пациента или у пациентов со значительным нарушением функции почек.
Способ применения и дозы
Реклама: ООО «РЛС-Патент», ИНН 5044031277, erid=4CQwVszH9pUkpHxmQQo
Перорально, независимо от приема пищи, проглатывая целиком, запивая водой. Дозу подбирают индивидуально, в зависимости от показания, возраста и состояния пациента. Снижение дозы, отмену или замену альтернативным ЛС необходимо делать постепенно в течение как минимум 1 нед.
Меры предосторожности
Лекарственная реакция с эозинофилией и системными симптомами (DRESS-синдром)/полиорганная гиперчувствительность
Лекарственные реакции с эозинофилией и системными симптомами (DRESS-синдром), также известные как полиорганная гиперчувствительность, наблюдались при применении габапентина. Некоторые из этих реакций были фатальными или опасными для жизни. DRESS-синдром обычно, хотя и не исключительно, проявляется лихорадкой, сыпью и/или лимфаденопатией в сочетании с поражениями других систем органов, такими как гепатит, нефрит, гематологические аномалии, миокардит или миозит, иногда напоминающий острую вирусную инфекцию. Часто присутствует эозинофилия. Это расстройство отличается по своему выражению, и в него могут быть вовлечены другие системы органов, не упомянутые выше. Важно отметить, что ранние проявления гиперчувствительности, такие как лихорадка или лимфаденопатия, могут наблюдаться, даже при отсутствии сыпи. Если такие признаки или симптомы присутствуют, пациента следует немедленно обследовать. Габапентин следует отменить, если не удается установить альтернативную этиологию признаков или симптомов.
Анафилаксия и ангионевротический отек
Габапентин может вызвать развитие анафилаксии и ангионевротического отека после первой дозы или в любой момент во время лечения. Признаки и симптомы в зарегистрированных случаях включали затрудненное дыхание, отек губ, горла и языка, а также гипотонию, требующую неотложной помощи. Пациента следует предупредить о необходимости прекратить прием габапентина и немедленно обратиться за медицинской помощью, если у них появятся признаки или симптомы анафилаксии или ангионевротического отека.
Сонливость/седативный эффект и головокружение
Во время контролируемых исследований эпилепсии у пациентов старше 12 лет, получавших габапентин в дозах до 1800 мг/сут, сонливость, головокружение и атаксия регистрировались чаще чем в группах, получавших плацебо, а именно 19% против 9% для сонливости, 17% против 7% для головокружения и 13% против с 6% для атаксии. В этих исследованиях сонливость, атаксия и повышенная утомляемость были частыми побочными реакциями, приводившими к прекращению приема габапентина у пациентов старше 12 лет, при этом 1,2; 0,8 и 0,6% пациентов сответственно прерывали прием из-за этих явлений.
Во время контролируемых исследований у пациентов с постгерпетической невралгией, сонливость и головокружение регистрировались чаще по сравнению с плацебо у пациентов, получавших габапентин в дозах до 3600 мг/сут, а именно 21% против 5% для сонливости и 28% против 8% для головокружения. Головокружение и сонливость были одними из наиболее частых побочных реакций, приведших к отмене габапентина. Пациенты должны тщательно наблюдаться на предмет признаков депрессии ЦНС, таких как сонливость и седативный эффект, при применении совместно с другими ЛС, обладающими седативными свойствами, из-за потенциального синергизма. Кроме того, у пациентов, которым требуется одновременное применение морфина, может наблюдаться повышение концентрации габапентина и потребоваться корректировка дозы (см. «Взаимодействие»).
Парциальный эпилептический припадок, эпилептический статус
Не следует резко отменять применение противоэпилептических ЛС из-за возможности увеличения частоты приступов. В плацебо-контролируемых исследованиях эпилепсии у пациентов старше 12 лет частота развития эпилептического статуса у пациентов, получавших габапентин, составляла 0,6% (3 из 543) по сравнению с 0,5% у пациентов, получавших плацебо (2 из 378). Среди 2074 пациентов старше 12 лет, получавших габапентин во всех исследованиях эпилепсии (контролируемых и неконтролируемых), 31 (1,5%) имели эпилептический статус. Из них 14 пациентов не имели в анамнезе эпилептического статуса ни до лечения, ни во время приема других ЛС. Поскольку адекватные исторические данные недоступны, невозможно установить, связано ли применение габапентина с более высокой или более низкой частотой эпилептического статуса, чем можно было бы ожидать в аналогичной популяции, не получавшей габапентин.
Суицидальное поведение и мышление
Противоэпилептические ЛС, включая габапентин, увеличивают риск возникновения суицидальных мыслей или поведения у пациентов, принимающих эти ЛС по любым показаниям. Пациенты, получающие какие-либо противоэпилептические ЛС по любым показаниям, должны находиться под наблюдением на предмет появления или ухудшения депрессии, суицидальных мыслей или поведения и/или любых необычных изменений настроения или поведения.
Объединенный анализ 199 плацебо-контролируемых клинических исследований (моно- и дополнительная терапия) 11 различных противоэпилептических ЛС показал, что пациенты, рандомизированные для приема одного из этих ЛС, имели примерно вдвое больший риск (скорректированный ОР 1,8, 95% ДИ: 1,2; 2,7) возникновения суицидальных мыслей или поведения по сравнению с пациентами, рандомизированными для получения плацебо. В исследованиях со средней продолжительностью лечения 12 нед оценочная частота случаев возникновения суицидального поведения или настроения у 27863 пациентов, получавших противоэпилептические ЛС, составила 0,43% по сравнению с 0,24% у 16029 пациентов, получавших плацебо, что представляет собой увеличение примерно на один случай на каждые 530 пролеченных пациентов. В исследованиях зарегистрировано четыре случая самоубийства у пациентов, принимавших лекарства, и ни одного у пациентов, получавших плацебо, но этих данных недостаточно, чтобы сделать определенный вывод о влиянии применения ЛС на решение о самоубийстве.
Повышенный риск возникновения суицидальных мыслей или поведения при применении противоэпилептических ЛС наблюдался уже через 1 нед после начала лечения и сохранялся в течение оцениваемой продолжительности лечения. Поскольку продолжительность большинства исследований, включенных в анализ, не превышала 24 нед, нельзя было оценить риск возникновения суицидальных мыслей или поведения после 24 нед. Этот риск в проанализированных данных в целом был одинаковым для всех ЛС. Повышенный риск при применении противоэпилептических ЛС с различными механизмами действия и по ряду показаний позволяет предположить, что данный риск распространяется на все противоэпилептические ЛС, используемые по любому показанию. В проанализированных клинических испытаниях риск существенно не варьировал в зависимости от возраста (5–100 лет).
Относительный риск возникновения суицидальных мыслей или поведения был выше в клинических исследованиях эпилепсии, чем в исследованиях психиатрических или других состояний, но абсолютные различия были одинаковыми для эпилепсии и психиатрических показаний.
При рассмотрении возможности назначения габапентина или любого другого противоэпилептического ЛС необходимо соотносить риск возникновения суицидальных мыслей или поведения с риском от невылеченного заболевания. Эпилепсия и многие другие заболевания, при которых назначаются противоэпилептические ЛС, сами по себе связаны с заболеваемостью и смертностью, а также с повышенным риском возникновения суицидальных мыслей и поведения. Если во время лечения возникают суицидальные мысли и поведение, врач, назначающий лекарство, должен рассмотреть, может ли появление этих симптомов у любого конкретного пациента быть связано с заболеванием, которое лечится. Пациенты, их опекуны и семьи должны быть проинформированы о том, что противоэпилептические ЛС повышают риск возникновения суицидальных мыслей и поведения, и необходимо проявлять бдительность в отношении появления или ухудшения признаков и симптомов депрессии, любых необычных изменений настроения или поведения или суицидальных мыслей, поведения или мыслей о самоповреждении. О вызывающем беспокойство поведении следует немедленно сообщать лечащему врачу.
Нейропсихические побочные реакции (дети от 3 до 12 лет)
Применение габапентина у детей от 3 до 12 лет с эпилепсией связано с возникновением побочных реакций со стороны ЦНС. Наиболее значимыми из них являются эмоциональная лабильность (в основном поведенческие проблемы), проявление враждебности, включая агрессивное поведение, нарушение мышления, включая проблемы с концентрацией внимания и изменение успеваемости в школе, и гиперкинезия (в основном беспокойство и гиперактивность). У пациентов, получавших габапентин, большинство этих реакций были от легкой до умеренной степени по интенсивности.
В контролируемых клинических исследованиях эпилепсии у детей от 3 до 12 лет частота этих побочных реакций у получавших габапентин по сравнению с плацебо составляла: эмоциональная лабильность — 6% против 1,3%, враждебность — 5,2% против 1,3%, гиперкинез — 4,7% против 2,9% и расстройство мышления — 1,7% против 0%. Один случай о проявлении враждебности был оценен как серьезный. Прекращение применения габапентина потребовалось у 1,3% пациентов со случаями эмоциональной лабильности и гиперкинезии и у 0,9% пациентов со случаями проявления враждебности и расстройства мышления. Один пациент, получавший плацебо (0,4%), выбыл из исследования из-за эмоциональной лабильности.
Туморогенность
В исследовании канцерогенности при пероральном применении габапентин увеличивал частоту возникновения опухолей ацинарных клеток поджелудочной железы у крыс. Клиническое значение этого явления неизвестно. Клинический опыт дорегистрационных исследований габапентина не позволяет оценить его способность вызывать опухоли у людей.
В клинических исследованиях по изучению габапентина в качестве средства дополнительной терапии эпилепсии, включавших в себя 2085 пациенто-лет воздействия у пациентов старше 12 лет, развитие новых опухолей было зарегистрировано у 10 пациентов (2 опухоли молочной железы, 3 — мозга, 2 — легких, 1 — надпочечников, 1 — неходжкинская лимфома, 1 — карцинома эндометрия in situ), а ранее существовавшие опухоли прогрессировали у 11 пациентов (9 — головного мозга, 1 — груди, 1 — простаты) в течение срока применения или в период до 2 лет после прекращения приема габапентина. Отсутствие данных о фоновой заболеваемости и рецидивов в аналогичной популяции, не получавшей габапентин, не позволяет оценить влияние применения габапентина на заболеваемость в этой когорте.
Внезапная и необъяснимая смерть пациентов с эпилепсией
В ходе дорегистрационных исследований было зарегистрировано 8 внезапных и необъяснимых случаев смерти в популяции из 2203 пациентов с эпилепсией, получавших (2103 пациенто-лет воздействия) габапентин.
Некоторые из них могут быть связанны с припадками, случившимися при отсутствии наблюдения, например ночью. Это составляет 0,0038 случая смерти на пациенто-год. Хотя этот показатель превышает ожидаемый для здорового населения в зависимости от возраста и пола, он находится в пределах диапазона оценок частоты внезапных необъяснимых смертей у пациентов с эпилепсией, не получающих габапентин (диапазон от 0,0005 для общей популяции пациентов с эпилепсией до 0,003 для популяции участвовавших в клинических исследованиях и до 0,005 для пациентов с рефрактерной эпилепсией).
Особые группы пациентов
Дети. Безопасность и эффективность применения габапентина при лечении постгерпетической невралгии у детей не установлены.
Безопасность и эффективность применения габапентина в качестве дополнительной терапии при лечении парциальных припадков у детей до 3 лет не установлены.
Пожилой возраст. Общее количество пациентов, получавших габапентин в контролируемых клинических исследованиях с участием пациентов с постгерпетической невралгией, составило 336, из которых 102 (30%) были в возрасте от 65 до 74 лет и 168 (50%) — 75 лет и старше. У пациентов в возрасте 75 лет и старше наблюдался больший эффект от лечения по сравнению с более молодыми пациентами, получавшими ту же дозу. Поскольку габапентин почти полностью выводится почками, больший лечебный эффект, наблюдаемый у пациентов ≥75 лет, может быть следствием повышенного воздействия габапентина из-за возрастного снижения функции почек. Нельзя исключать и влияние других факторов. Профиль и частота побочных реакций были одинаковыми во всех возрастных группах, за исключением периферических отеков и атаксии, частота которых с возрастом увеличивалась.
Клинические исследования по применению габапентина при эпилепсии не включали достаточное количество пациентов в возрасте 65 лет и старше, чтобы определить различия в реакции у пожилых и более молодых субъектов. Опыт клинического применения не выявил различий в ответе у пожилых и более молодых пациентов. В целом следует соблюдать осторожность при подоборе дозы для пожилого пациента, обычно начиная с нижнего предела диапазона дозирования, учитывая бóльшую вероятность снижения функции печени, почек или сердца, а также наличия сопутствующего заболевания или применения другой лекарственной терапии.
Нарушение функции почек. Известно, что габапентин в значительной степени выводится почками, и риск развития побочных реакций может быть выше у пациентов с нарушением функции почек. Поскольку у пожилых пациентов более вероятно снижение функции почек, следует соблюдать осторожность при выборе дозы и корректировать ее на основе значений Cl креатинина.
Применение габапентина у детей с почечной недостаточностью не изучалось.
Необходима корректировка дозы у пациентов, находящихся на гемодиализе.
Влияние на способность управлять автотранспортом и работать со сложным оборудованием. Пациентам, принимающим габапентин, не следует водить машину до тех пор, пока они не приобретут достаточный опыт, чтобы оценить, влияет ли его прием на их способность управлять автомобилем. Исследования эффективности вождения, проведенные с пролекарством габапентина, показывают, что габапентин может вызывать значительные нарушения навыков вождения. Лечащие врачи и пациенты должны учитывать, что способность пациентов оценивать свои собственные навыки вождения, а также степень сонливости, вызванной габапентином, может быть недостаточной. Продолжительность нарушения навыков вождения после начала применения габапентина неизвестна. Неизвестно, связано ли нарушение с сонливостью или другими эффектами габапентина. Кроме того, поскольку габапентин вызывает сонливость и головокружение, пациентам следует рекомендовать не работать со сложными механизмами до тех пор, пока они не приобретут достаточный опыт его применения, чтобы оценить, ухудшает ли он их способность выполнять такие задачи.
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
1 таблетка 600 мг содержит:
Активное вещество: 600,0 мг габапентина.
Вспомогательные вещества: полоксамер 407 80,0 мг, коповидон 64,8 мг, крахмал кукурузный 49,2 мг, магния стеарат 6,0 мг; пленочная оболочка: опадрай белый YS-1-18111 24,0 мг [тальк 17,4 мг, гипролоза 6,6 мг], воск травяной (канделила) 0,6 мг.
1 таблетка 800 мг содержит:
Активное вещество: 800,0 мг габапентина.
Вспомогательные вещества: полоксамер 407 106,7 мг, коповидон 86,4 мг, крахмал
кукурузный 65,6 мг, магния стеарат 8,0 мг; пленочнаяоболочка: опадрай белый YS-I-18111 32,0 мг [тальк 23,2 мг, гипролоза 8,8 мг], воск травяной (канделила) 0,8 мг.
Дозировка 600 мг: белые эллиптической формы таблетки, покрытые пленочной оболочкой, с гравировкой «NT» и «16». риской между гравировкой на одной стороне и риской на другой стороне.
Дозировка 800 мг: белые эллиптической формы таблетки, покрытые пленочной оболочкой, с гравировкой «NT» и «26». риской между гравировкой на одной стороне и риской на другой стороне.
противоэпилептическое средство.
КодАТХ
1М03АХ12.
Фармакодинамика
Механизм действия
Габапентин легко проникает в ткань головного мозга и предотвращает развитие судорог в различных животных моделях эпилепсии. Габапентин не обладает сродством к рецепторам ГАМКА (гамма-аминомасляная кислота) и ГАМКв и не влияет на метаболизм ГАМК. Габапентин не связывается с рецепторами других нейромедиаторов, присутствующих в головном мозге и не влияет на натриевые каналы.
Габапентин обладает высоким сродством и связывается с ?-2-?(альфа-2- дельта) субъединицей потенциалзависимых кальциевых каналов и предполагается, что связь габапентина с ?-2-? субъединицей участвует в механизме противосудорожного эффекта у животных. При скрининге большой группы молекул-мишеней для этого лекарственного препарата показано, что единственной мишенью для него является субъединица а28. Результаты, полученные в нескольких доклинических моделях, показывают, что фармакологическая активность габапентина может реализовываться путем связывания с субъединицей ?-2-? посредством подавления высвобождения возбуждающих нейромедиаторов в некоторых участках центральной нервной системы. Такая активность может лежать в основе противосудорожного действия габапентина. Значимость этих механизмов действия габапентина для его противосудорожных эффектов у людей все еще необходимо установить. Эффективность габапентина также показана в нескольких доклинических исследованиях на животных моделях болевого синдрома. Предполагают, что специфическое связывание габапентина с субъединицей ?-2-? приводит к нескольким разным эффектам, которые могут отвечать за обезболивающее действие в животных моделях. Обезболивающее действие габапентина может проявляться на уровне спинного мозга, а также на уровне высших мозговых центров посредством взаимодействий с нисходящими путями, подавляющими передачу болевых импульсов. Значение этих свойств габапентина, выявленных в доклинических исследованиях, неизвестно.
Клиническая эффективность и безопасность
В рамках клинического исследования адъювантной терапии парциальных судорожных приступов у детей в возрасте от 3 до 12 лет было продемонстрировано наличие количественных, но статистически недостоверных различий по частоте снижения количества приступов на более чем 50 % в группе габапентина по сравнению с группой плацебо. Дополнительный анализ частоты ответа на терапию в зависимости от возраста (при рассмотрении возраста как непрерывной переменной или при выделении двух возрастных подгрупп: 3-5 лет и 6 — 12 лет) не выявил статистически достоверного влияния возраста на эффективность терапии. Результаты данного дополнительного анализа представлены в таблице ниже.
*Модифицированная популяция «по намерению лечить» (MITT) определялась как совокупность всех пациентов, рандомизированных в группу исследуемой терапии и имевших подлежащие оценке дневники судорожных приступов за период длительностью 28 дней в рамках исходной и двойной слепой фаз исследования.
Фармакокинетика
Всасывание
После приема внутрь максимальная концентрация габапентина в плазме достигается в течение 2-3 часов. Биодоступность габапентина имеет тенденцию к снижению с увеличением дозы препарата. Абсолютная биодоступность при приеме капсул дозировки 300 мг составляет приблизительно 60 %. Пища, в том числе с высоким содержанием жиров, не оказывает клинически значимого влияния на параметры фармакокинетики габапентина. Фармакокинетика габапентина не изменяется при многократном приеме препарата. Несмотря на то, что в рамках клинических исследований концентрация габапентина в плазме обычно варьировала в диапазоне 2-20 мкг/мл, она не позволяла прогнозировать ни эффективность, ни безопасность препарата. Параметры фармакокинетики представлены в таблице.
Таблица Сводные средние (CV, %) параметры фармакокинетики габапентина в равновесном состоянии при многократном приеме с интервалом дозирования длительностью восемь часов
Распределение
Габапентин не связывается с белками плазмы, и его объем распределения составляет 57,7 л. У пациентов с эпилепсией концентрация габапентина в спинномозговой жидкости (СМЖ) составляет приблизительно 20 % от минимальной равновесной концентрации в плазме. Габапентин проникает в грудное молоко женщин, кормящих грудью.
Биотрансформация
Отсутствуют данные о метаболизме габапентина в организме человека. Габапентин не вызывает индукции неспецифических оксидаз печени, ответственных за метаболизм лекарственных средств.
Выведение
Габапентин выводится в неизмененном виде исключительно путем почечной экскреции. Период полувыведения габапентина не зависит от принятой дозы и составляет в среднем от 5 до 7 часов.
У пожилых лиц и пациентов с нарушением функции почек клиренс габапентина из плазмы снижается. Константа элиминации, плазменный клиренс и почечный клиренс габапентина прямо пропорциональны клиренсу креатинина.
Габапентин удаляется из плазмы при гемодиализе. Пациентам с нарушением функции почек или находящимся на гемодиализе рекомендуется коррекция дозы препарата (см. раздел «Способ применения и дозировка»).
Фармакокинетика габапентина у детей изучалась у 50 здоровых добровольцев в возрасте от 1 месяца до 12 лет. В целом, концентрация габапентина в плазме детей старше 5 лет аналогична таковой у взрослых при применении препарата в эквивалентной дозе на основании расчета мг/кг массы тела.
В рамках исследования фармакокинетики у 24 здоровых детей в возрасте от 1 до 48 месяцев параметры экспозиции препарата (AUC) были приблизительно на 30 % ниже, Сmах- ниже, а клиренс- выше при расчете на единицу массы тела по сравнению с доступными опубликованными данными по кинетике препарата у детей в возрасте старше 5 лет.
Линейность/нелинейность параметров фармакокинетики
Биодоступность габапентина снижается с увеличением принятой дозы, что влечет за собой нелинейность параметров фармакокинетики, которые включают в расчет показатель биодоступности (F), например Ае%, CL/F, Vd/F. Фармакокинетика элиминации (параметры параметров, не включающие F, такие как CLr и Т1/2) лучше описывается линейной моделью.
Равновесные концентрации габапентина в плазме являются предсказуемыми на основе данных по кинетике при однократном приеме.
Эпилепсия
Монотерапия парциальных судорог с вторичной генерализацией и без нее у взрослых и детей в возрасте 12 лет и старше. Эффективность и безопасность монотерапии у детей в возрасте до 12 лет не установлены.
Как дополнительное средство при лечении парциальных судорог с вторичной генерализацией и без нее у взрослых и детей в возрасте 3 лет и старше. Безопасность и эффективность дополнительной терапии габапентином у детей в возрасте менее 3 лет не установлены.
Нейропатическая боль
Лечение нейропатической боли у взрослых в возрасте 18 лет и старше. Эффективность и безопасность у пациентов в возрасте до 18 лет не установлены.
Гиперчувствительность к габапентину или вспомогательным компонентам препарата.
Эпилепсия
Применение в качестве монотерапии парциальных судорог с вторичной генерализацией и без нее у детей в возрасте до 12 лет.
Применение в качестве дополнительного средства при лечении парциальных судорог с вторичной генерализацией и без нее у детей в возрасте до 3 лет.
Нейропатическая боль
Для лечения нейропатической боли у детей и подростков в возрасте до 18 лет.
С осторожностью
Почечная недостаточность (см. раздел «Способ применения и дозировка»).
Применение при беременности и в период грудного вскармливания
Беременность
Отсутствуют данные о применении препарата у беременных женщин.
Общий риск, связанный с эпилепсией и противоэпилептическими препаратами
Риск рождения детей с врожденными аномалиями у матерей, которые проходят лечение противосудорожными препаратами, увеличивается в 2-3 раза. Чаще всего наблюдается расщелина верхней губы и неба, пороки развития сердечно-сосудистой системы и дефекты нервной трубки. При этом прием нескольких противосудорожных препаратов может быть связан с большим риском пороков развития, чем в случае монотерапии. Поэтому, если это
возможно, следует применять один из противосудорожных препаратов. Женщинам детородного возраста, а также всем женщинам, у которых возможно наступление беременности, следует проконсультироваться у квалифицированною специалиста. Если женщина планирует беременность, следует еще раз оценить необходимость продолжения противосудорожной терапии. При этом противосудорожные препараты не следует отменять резко, так как это может вести к возобновлению припадков с тяжелыми последствиями для матери и ребенка. В редких случаях у детей, матери которых страдают эпилепсией, наблюдалась задержка развития. При этом невозможно определить, связана ли задержка развития с генетическими или социальными факторами, болезнью матери или противосудорожной терапией.
Риск, обусловленный габапентином
В экспериментах на животных была показана токсичность препарата в отношении плода. В отношении возможного риска у людей данных нет. Поэтому габапентин следует применять во время беременности только в том случае, если предполагаемая польза для матери оправдывает возможный риск для плода.
Невозможно сделать однозначное заключение о связи габапентина с повышенным риском врожденных аномалий при применении его во время беременности вследствие наличия самой эпилепсии и одновременного применения других противоэпилептических лекарственных препаратов в каждом зарегистрированном случае.
Грудное вскармливание
Габапентин выводится с грудным молоком, влияние его на вскармливаемого ребенка неизвестно, поэтому во время кормления грудью Нейронтин следует назначать только в том случае, если польза для матери явно перевешивает риск для младенца.
Фертильность
В исследованиях на животных не отмечали влияния габапентина на фертильность.
Способ применения и дозировка
Дозирование
Для всех показаний схема титрации дозы для начала терапии представлена в таблице №1. Эта схема представлена для взрослых пациентов и подростков в возрасте 12 лет и старше. Схема титрации для детей в возрасте младше 12 лет представлена ниже под отдельным подзаголовком.
Таблица №1 Схема титрации дозы препарата в начале терапии
|
День№1 |
День №2 |
День №3 |
|
300 мг 1 раз в сутки |
по 300 мг 2 раза в сутки |
по 300 мг 3 раза в сутки |
Прекращение терапии габапентином
Согласно современной клинической практике при необходимости отмены терапии габапентином это следует делать постепенно в течение минимум одной недели вне зависимости от показаний.
Эпилепсия
При эпилепсии обычно требуется длительное лечение. Доза препарата при этом определяется лечащим врачом в зависимости от индивидуальной переносимости и эффективности препарата.
Взрослые и дети в возрасте старше 12 лет:
в клинических исследованиях эффективная доза составляла от 900 до 3600 мг/сут. Терапию можно начать по схеме, описанной выше в таблице №1 или с дозы 300 мг 3 раза в сутки в первый день. В последующем в зависимости от ответа пациента на терапию и переносимости препарата доза может быть повышена на 300 мг/сут каждые 2-3 дня, максимально до 3600 мг/сут. У некоторых пациентов может быть целесообразным более медленное повышение дозы. Минимальное время, за которое можно повысить дозу до 1800 мг/сут составляет 1 неделя, 2400 мг/сут — 2 недели, а для достижения максимальной суточной дозы 3600 мг/сут необходимо не менее 3 недель. В дилтельных открытых клинических исследованиях была отмечена хорошая переносимость препарата в дозах до 4800 мг/сут. Общая суточная доза должна быть разделена на три приема. Максимальный интервал между дозами при трехкратном приеме препарата не должен превышать 12 ч во избежание возобновления судорог.
Дети в возрасте 3-12 лет:начальная доза препарата варьирует от 10 до 15 мг/кг/сут, которую назначают равными дозами 3 раза в день и повышают до эффективной приблизительно в течение 3 дней. Эффективная доза габапентина у детей в возрасте 5 лет и старше составляет 25-35 мг/кг/сут равными дозами в 3 приема. Эффективная доза габапентина у детей в возрасте от 3 до 5 лет составляет 40 мг/кг/сут равными дозами в 3 приема. Отмечена хорошая переносимость препарата в дозах до 50 мг/кг/сут при длительном применении. Максимальный интервал между приемом доз препарата не должен превышать 12 часов во избежание возобновления судорог.
Нет необходимости контролировать концентрацию габапентина в плазме. Он может применяться в комбинации с другими противосудорожными препаратами без учета изменения его концентрации в плазме или концентрации других противосудорожных препаратов в сыворотке.
Нейропатическая боль
Взрослые
Терапию можно начать по схеме, описанной выше в таблице №1. Альтернативный способ дозирования — начальная доза составляет 900 мг/сут в три приема равными дозами. В последующем в зависимости от ответа пациента на терапию и переносимости препарата доза может быть повышена на 300 мг/сут каждые 2-3 дня, максимально до 3600 мг/сут. У некоторых пациентов может быть целесообразным более медленное повышение дозы. Минимальное время, за которое можно повысить дозу до 1800 мг/сут составляет 1 неделя, 2400 мг/сут — 2 недели, а для достижения максимальной суточной дозы 3600 мг/сут необходимо не менее 3 недель.
При лечении периферической нейропатической боли, при таких состояниях как болевая форма диабетической нейропатии и постгерпетическая невралгия, эффективность и безопасность применения препарата в течение периода дольше 5 месяцев в клинических исследованиях не изучались. В случае, если пациенту требуется продолжение терапии периферической нейропатической боли дольше 5 месяцев, лечащий врач должен оценить клинический статус пациента и определить необходимость дополнительной терапии.
Рекомендации для всех показаний
У пациентов в тяжелом состоянии, например, в случае пониженной массы тела, после трансплантации органов и т.д., дозу следует повышать медленнее, либо используя меньшие дозы, либо делая большие интервалы перед повышением дозы.
Применение у пожилых пациентов (в возрасте старше 65 лет)
Вследствие возрастного снижения функции почек пожилым пациентам может требоваться коррекция дозы (более подробная информация в таблице №2). Сонливость, периферические отеки и астения у пожилых пациентов могут встречаться чаще.
Применение у пациентов с почечной недостаточностью
Больным с нарушенной функцией почек и/или у пациентов, находящихся на гемодиализе рекомендуется снижение дозы габапентина согласно таблице №2:
Таблица №2. Дозирование габапентина у взрослых пациентов в зависимости от функции почек
|
Клиренс креатинина(мл/мин) |
Суточная доза (мг/сут) A |
|
>80 |
900-3600 |
|
50-79 |
600-1800 |
|
30-49 |
300-900 |
|
15-29 |
150Б-600 |
|
<15в |
150Б-300 |
Суточную дозу следует назначать в три приема; сниженные дозы препарата показаны пациентам с нарушением функции почек (клиренс креатинина < 79 мл/мин) Назначают по 300 мг через день.
У пациентов с клиренсом креатинина <15 мл/мин суточную дозу необходимо уменьшить пропорционально клиренсу креатинина (например, пациент с клиренсом креатинина 7,5 мл/мин должен получать половину дозы, которую получает пациент с клиренсом креатинина 15 мл/мин).
Применение у пациентов, находящихся на гемодиализе
Пациентам с анурией, находящимся на гемодиализе, которые ранее не принимали габапентин, препарат рекомендуется назначать в насыщающей дозе 300-400 мг, а затем применять его по 200-300 мг после каждых 4 ч гемодиализа. В дни, когда диализ не проводится, лечение проводить не следует.
Для пациентов со сниженной функцией почек, проходящих диализ, поддерживающая доза габапентина должна подбираться в соответствии с рекомендациями, представленными в Таблице №2. В дополнение к поддерживающей терапии рекомендуется прием 200-300 мг габапентина после каждой 4-часовой процедуры диализа.
Способ введения
Нейронтин» назначают внутрь.
Габапентин можно принимать вне зависимости от приема пищи, запивая достаточным количеством жидкости (например, стаканом воды). Допускается деление таблетки пополам.
Нежелательные реакции, наблюдаемые в клинических исследованиях у пациентов с эпилепсией (при применении габапентина в качестве монотерапии или в комбинации с другими противосудорожными препаратами) или невропатическими болями, представлены ниже и распределены по системам органов и частоте. Категория частоты определялась следующим образом: очень часто (>1/10); часто (от > 1/100 до < 1/10); нечасто (от > 1/1000 до <1/100); редко (от >1/10000 до <1/1000); очень редко (<1/10000). Если категория частоты была различной в разных исследованиях, то нежелательной реакции присваивалась более высокая категория.
Нежелательным реакциям, о которых сообщалось в процессе применения препарата после регистрации, присвоена категория частоты «неизвестно» (частоту нельзя рассчитать на основании имеющихся данных).
В каждом разделе по частоте нежелательные реакции представлены в порядке уменьшения серьезности.
Инфекционные и паразитарные заболевания: очень часто — вирусные инфекции; часто —пневмония, инфекция дыхательных путей, инфекция мочевыводящих путей, другие виды инфекции, средний отит.
Нарушения со стороны крови и лимфатической системы: часто — лейкопения; неизвестно — тромбоцитопения.
Нарушения со стороны иммунной системы: нечасто — аллергические реакции, включая крапивницу; неизвестно — гиперчувствительность, включая системные реакции, такие как лихорадка, высыпания, гепатит, лимфаденопатия, эозинофилия и другие.
Нарушения со стороны обмена веществ и питания: часто — анорексия, повышение аппетита.
Психические нарушения: часто — враждебность, спутанность сознания, депрессия, беспокойство, нервозность; нечасто — ухудшение психического состояния; неизвестно —галлюцинации.
Нарушения со стороны нервной системы: очень часто — сонливость, головокружение, атаксия; часто — судороги, гиперкинезия, дизартрия, амнезия, тремор, бессонница, головная боль, нарушение чувствительности (например, парестезии, гипестезия), нарушение координации, нистагм, усиление, ослабление или отсутствие рефлексов; нечасто — гипокинезия; редко — потеря сознания; неизвестно — другие нарушения движения (например, хореоатетоз, дискинезия и дистопия).
Нарушения со стороны органа зрения: часто — нарушение зрения (такие как, амблиопия, диплопия).
Нарушения со стороны органа слуха и лабиринтные нарушения: часто — вертиго, неизвестно — шум в ушах.
Нарушения со стороны сердца: нечасто — ощущение сердцебиения.
Нарушения со стороны сосудов: часто — симптомы вазодилатации или артериальная гипертензия.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения:
часто — одышка, бронхит, фарингит, кашель, ринит.
Нарушения со стороны желудочно-кишечного тракта: часто — запор, диарея, сухость слизистой оболочки полости рта или глотки, диспепсия, метеоризм, тошнота, рвота, боль в животе, заболевания зубов, гингивит; неизвестно — панкреатит.
Нарушения со стороны печени и желчевыводящих путей: неизвестно — гепатит, желтуха.
Нарушения со стороны кожи и подкожных покровов: часто — отек лица, пурпура (чаще всего ее описывали как кровоподтеки, возникавшие при физической травме), кожная сыпь, акне, зуд кожи; неизвестно — синдром Стивенса-Джонсона, ангионевротический отек, анафилаксия, мультиформная эритема, алопеция, лекарственная кожная сыпь, включая эозинофилию и системные реакции (см. раздел «Особые указания»).
Нарушения со стороны скелетно-мышечнои и соединительной ткани: часто — миалгии, артралгия, боль в спине, подергивания мышц; неизвестно — рабдомиолиз, миоклонус.
Нарушения со стороны почек и мочевыводящих путей: неизвестно — недержание мочи, острая почечная недостаточность.
Нарушения со стороны половых органов и молочной железы: часто — импотенция; неизвестно — увеличение в объеме молочных желез, гинекомастия, половая дисфункция (включая изменения либидо, нарушения эякуляции и аноргазмию).
Общие расстройства и нарушения в месте введения: очень часто — утомляемость, лихорадка; часто — периферические отеки, нарушение походки, астения, боль различной локализации, общее недомогание, гриппоподобный синдром; нечасто — генерализованный отек; неизвестно — синдром отмены (наиболее часто отмечались следующие нежелательные реакции: беспокойство, бессонница, тошнота, боли различной локализации и повышенное потоотделение), боль в груди. Зарегистрированы случаи внезапной необъяснимой смерти, связь которых с лечением габапентином не установлена.
Лабораторные и инструментальные данные: часто — снижение концентрации белых кровяных телец, повышение массы тела; нечасто — повышение активности аланинаминотрансферазы, аспартатаминотрансферазы и концентрации билирубина в плазме крови, гипергликемия; редко — гипогликемия (преимущественно у пациентов с сахарным диабетом); неизвестно — гипонатриемия, повышение активности креатинфосфокиназы.
Травмы, интоксикации и осложнения манипуляций: часто — травмы, переломы, ссадины, связанные с падениями.
Имеются сообщения о развитии острого панкреатита на фоне терапии габапентином. Причинная связь с габапентином остается неясной (см. раздел «Особые указания»). Имеются сообщения о случаях миопатии с повышением активности креатинкиназы у пациентов с терминальной стадией почечной недостаточности, находящихся на гемодиализе. Случаи инфекции дыхательных путей, среднего отита, бронхита и судорог были отмечены только в клинических исследованиях. Кроме того, в клинических исследованиях сообщалось о случаях агрессивного поведения и гиперкинезов у детей.
При однократном приеме 49 г габапентина наблюдались следующие симптомы: головокружение, двоение в глазах, нарушение речи, сонливость, потеря сознания, состояние заторможенности и диарея легкой степени, которые полностью исчезали при проведении симптоматической терапии. Следует учитывать, что после приема высоких доз габапентина, уменьшается его всасывание в кишечнике.
При передозировке габапентином возможно развитие комы, особенно при одновременном применении других лекарственных препаратов, подавляющих ЦНС.
Несмотря на то, что габапентин может выводиться при гемодиализе, имеющийся опыт показывает, что обычно подобной необходимости не возникает. Пациентам с тяжелой почечной недостаточностью может быть показан гемодиализ.
В рамках экспериментов на мышах и крысах, которым препарат вводился в дозах до 8000 мг/кг, не удалось установить значение летальной дозы габапентина при пероральном введении. Признаки острой токсичности у животных включали атаксию, затруднение дыхания, птоз, гипоактивность или возбуждение.
Взаимодействие с другими лекарственными средствами
Имеются сообщения о спонтанных случаях, а также по информации из литературных источников возможно угнетение дыхания и/или симптомы седации, связанные с приемом габапентина и опиоидных анальгетиков. В некоторых из этих случаев авторы связывали данные симптомы с одновременным применением габапентина и опиоидов, особенно у пожилых пациентов.
В исследовании с участием здоровых добровольцев (N=12) при применении 600 мг габапентина через 2 часа после приема морфина в виде капсул с пролонгированным высвобождением по 60 мг отмечается увеличение среднего значения AUC габапентина на 44 % по сравнению с монотерапией габапентином. В связи с этим пациенты, которым требуется проведение одновременной терапии с опиоидными анальгетиками, должны находиться под тщательным контролем на предмет развития признаков угнетения центральной нервной системы, таких как сонливость, седация и угнетение дыхания, а дозу габапентина и опиоидных анальгетиков следует соответствующим образом снизить. Взаимодействия между габапентином и фенобарбиталом, фенитоином, вальпроевой кислотой и карбамазепином не отмечено. Фармакокинетика габапентина в равновесном состоянии одинакова у здоровых людей и пациентов, получающих другие противосудорожные средства. Одновременное применение габапентина с пероральными контрацептивами, содержащими норэтистерон и/или этинилэстрадиол, не сопровождается изменениями фармакокинетики обоих компонентов.
Одновременное применение габапентина с антацидами, содержащими алюминий и магний, сопровождается снижением биодоступности габапентина примерно на 24 % (см. раздел «Особые указания»).
Пробенецид не влияет на почечную экскрецию габапентина.
Небольшое снижение (14 %) почечной экскреции габапентина при одновременном приеме циметидина, вероятно, не имеет клинического значения.
При одновременном применении напроксена (250 мг) и габапентина (125 мг) отмечалось повышение абсорбции габапентина с 12 % до 15 %. Габапентин не оказывает влияния на фармакокинетические параметры напроксена. Указанные дозы препаратов меньше минимальных терапевтических. Одновременное применение данных препаратов в больших дозах не изучалось.
Суицидальные идеи и поведение
Имеются сообщения о возникновении суицидальных мыслей или поведения у пациентов, получающих лечение противоэпилептическими препаратами по различным показаниям.
Мета-анализ рандомизированных плацебо-контролируемых исследований противоэпилептических средств также продемонстрировал небольшое повышение риска появления суицидальных мыслей и поведения. Механизм повышения такого риска неизвестен и имеющиеся данные не исключают возможности такого повышения риска для габапентина.
Поэтому пациентов, получающих эти препараты, следует тщательно наблюдать на предмет появления признаков суицидальных мыслей или поведения. У таких пациентов следует рассмотреть необходимость проведения соответствующего лечения. В случае появления признаков суицидальных мыслей или поведения пациентам или их попечителям следует обратиться к врачу.
Острыйпанкреатит
В случае развития острого панкреатита на фоне приема габапентина, следует оценить возможность отмены препарата.
Судороги (синдром «отмены»)
Хотя синдром «отмены», сопровождающийся развитием судорог, при лечении габапентином не отмечен, резкое прекращение терапии противосудорожными препаратами у пациентов с эпилепсией может провоцировать развитие эпилептического статуса (см. раздел «Способ применения и дозировка»).
Как и при применении других противоэпилептических препаратов, на фоне применения габапентина может отмечаться увеличение частоты судорог или появление другого типа судорог.
Так же как и в случае с другими противоэпилептическими средствами, попытки отменить все сопутствующие противоэпилептические средства, чтобы начать монотерапию габапентином в случае рефрактерности к лечению у пациентов, принимающих несколько противоэпилептических средств, в основном не заканчиваются успехом.
Считается, что габапентин неэффективен при первичных генерализованных припадках, например, абсансах, и даже может усиливать такие припадки у некоторых пациентов. В связи с этим применять габапентин у пациентов со смешанными припадками, включая абсансы, следует с осторожностью.
Опиоидные анальгетики
Пациенты, которым требуется проведение одновременной терапии с опиоидными анальгетиками, должны находиться под тщательным контролем на предмет развития признаков угнетения центральной нервной системы, таких как сонливость, седация и угнетение дыхания.
У пациентов, которые одновременно получают габапентин и морфин может наблюдаться повышение концентрации габапентина. Дозу габапентина и опиоидных анальгетиков следует соответствующим образом снизить (см. раздел «Взаимодействие с другими лекарственными средствами»).
Полжилые пациенты
Систематические исследования пациентов в возрасте 65 лет и старше, принимающих габапентин, не проводились. В двойном слепом исследовании применения габапентина при невропатической боли у пациентов в возрасте 65 лет и старше наблюдалась более высокая частота сонливости, периферических отеков и астении по сравнению с пациентами в возрасте младше 65 лет. За исключением этих результатов при клиническом обследовании данной группы пациентов было показано, что профиль нежелательных реакций у них не отличался от остальных.
Дети
Влияние длительной терапии (более 36 недель) габапентином на способность к обучению, интеллект и развитие детей и подростков достаточно не изучено. Следует оценить соотношение возможного риска и пользы при назначении длительной терапии.
Злоупотребление и зависимость
В базе данных пострегистрационных наблюдений имеются сообщения о случаях злоупотребления препаратом и зависимости от него. Как и в случаях назначения любого препарата, влияющего на ЦНС, врачам следует тщательно изучать анамнез пациентов на предмет злоупотребления препаратами и наблюдать за ними с целью выявления возможных признаков злоупотребления габапентином (например, стремление необоснованно получить препарат, развитие устойчивости к терапии габапентином, необоснованное повышение дозы препарата).
DRESS—синдром (лекарственная реакция с эозинофилиеи и системными симптомами)
На фоне приема противоэпилептических препаратов, в том числе габапентина, сообщалось о случаях развития тяжелых жизнеугрожающих реакций гиперчувствительности, таких как лекарственная сыпь с сопутствующей эозинофилиеи и системными симптомами. Необходимо помнить о том, что ранние признаки реакции гиперчувствительности, такие как повышение температуры тела, лимфаденопатия, могут развиваться даже в отсутствии кожной сыпи. В случае появления подобных симптомов, необходимо немедленное обследование пациента.
Если не найдено других причин, кроме применения габапентина, применение препарата следует отменить.
Анафилаксия
Прием габапентина может привести к развитию анафилаксии. Следующие симптомы и признаки отмечали в случаях развития анафилаксии на фоне приема габапентина — затруднение дыхания, отек губ, горла и языка, также отмечалось выраженное снижение артериального давления, требующее срочного медицинского вмешательства. Следует предупредить пациентов о том, что при развитии признаков или симптомов развития анафилаксии следует прекратить прием препарата и обратиться за медицинской помощью.
Лабораторные тесты
При совместном применении габапентина и других противосудорожных средств были зарегистрированы ложноположительные результаты при определении белка в моче с помощью тест-полосок Ames N-Multistix SG®. Для определения белка в моче рекомендуется пользоваться более специфичным методом преципитации сульфосалициловой кислотой.
Влияние на ЦНС
Во время лечения габапентином наблюдались случаи головокружения и сонливости, которые могут увеличивать вероятность получения случайной травмы (при падении). В пострегистрационном периоде также сообщалось о случаях спутанности сознания, потери сознания и нарушения умственной деятельности. Поэтому пациентам следует рекомендовать соблюдать осторожность до тех пор, пока им не станут известны возможные эффекты этого лекарственного препарата.
При одновременном применении с опиоидными анальгетиками может отмечаться повышение концентрации габапентина в плазме крови. В связи с этим пациент нуждается в тщательном наблюдении на предмет развития признаков угнетения центральной нервной системы (ЦНС), таких как сонливость, седация и угнетение функции дыхания. Дозы габапентина или опиоидных анальгетиков должны быть снижены соответствующим образом (см. раздел «Взаимодействие с другими лекарственными средствами»).
Совместное применение с антаиидами
Габапентин рекомендуется принимать примерно через 2 ч после приема антацида.
Влияние на способность управления транспортными средствами и работать с механизмами
Во время приема препарата пациентам не рекомендуется управлять транспортными средставми или пользоваться потенциально опасной техникой до подтверждения отсутствия негативного влияния препарата на выполнение этих функций.
Габапентин влияет на ЦНС и может вызывать головокружение, сонливость, спутанность сознания, потерю сознания или другие симптомы со стороны ЦНС. Даже при незначительной или умеренной выраженности эти нежелательные реакции могут представлять опасность для пациентов, управляющих транспортными средствами или другими механизмами. Особенно велика такая вероятность в начале лечения или после повышения дозы препарата Нейронтин.
Таблетки покрытые пленочной оболочкой, 600 мг и 800 мг.
По 10 таблеток в блистеры (контурная ячейковая упаковка) из ПВХ/ПЭ/ПВДХ/алюминиевой фольги с виниловым покрытием.
По 2, 5 или 10 блистеров с инструкцией по применению в картонную пачку.
При температуре не выше 25 °С.
Хранить в недоступном для детей месте.
2 года.
Не использовать после даты истечения срока годности.
Отпускается по рецепту.
Производитель
«Пфайзер Фармасьютикалз ЭлЭлСи», Пуэрто-Рико
Адрес: км 1,9, Роуд 698, Вега Байя, Пуэрто-Рико 00693.
Выпускающий контроль качества
«Пфайзер Мэнюфэкчуринг Дойчленд ГмбХ», Германия
Адрес: Моосвальдаллее 1, 79090 Фрайбург, Германия.
Претензии потребителей направлять по адресу
ООО «Пфайзер»
123317, Москва, Пресненская наб., д. 10 БЦ «Башня на набережной» (Блок С)