Менопур Мультидоза — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер
ЛП-002518
Торговое наименование препарата
Менопур® Мультидоза
Международное непатентованное наименование
Менотропины
Лекарственная форма
лиофилизат для приготовления раствора для подкожного введения
Состав
1 флакон с лиофилизатом содержит:
действующее вещество: менотропины (человеческий менопаузальный гонадотропин высокоочищенный, чМГ) — 600 ME ФСГ + 600 ME ЛГ или 1200 ME ФСГ + 1200 ME ЛГ; вспомогательные вещества: лактозы моногидрат 21,0 мг, полисорбат-20 0,005 мг, натрия гидрофосфата гептагидрат 0,268 мг, фосфорной кислоты раствор 1 М q.s., натрия гидрофосфата раствор 0,5 М q.s.
1 шприц с растворителем содержит:
метакрезол 3,63 мг, вода для инъекций до 1,1 мл.
Описание
Лиофилизат: белая или почти белая аморфная масса.
Растворитель: бесцветный прозрачный раствор.
Фармакотерапевтическая группа
Гонадотропины и другие стимуляторы овуляции
Код АТХ
G03GA02
Фармакодинамика:
Действующим веществом препарата Менопур® Мультидоза является человеческий менопаузальный гонадотропин (чМГ) высокой степени очистки, получаемый из мочи женщин в период постменопаузы. Препарат содержит фолликулостимулирующий гормон (ФСГ) и лютеинизирующий гормон (ЛГ).
Органами-мишенями для гормонального эффекта чМГ у женщин являются яичники. ЧМГ стимулирует гаметогенез и синтез половых гормонов.
ФСГ является ключевым фактором роста и развития фолликулов на стадии раннего фолликулогенеза. ЛГ играет важную роль в продукции половых гормонов яичниками и вовлечен в физиологические процессы, приводящие к развитию полноценного преовуляторного фолликула. Стимуляция фолликулярного роста под действием ФСГ, в случае полного отсутствия ЛГ, завершается патологическим развитием фолликула, ассоциированным с низкой концентрацией эстрадиола и неспособностью к лютеинизации неовулирующего фолликула в ответ на нормальный овуляторный стимул.
Принимая во внимание действие ЛГ, заключающееся в усилении синтеза половых гормонов, применение препарата Менопур® Мультидоза в циклах ЭКО/ИКСИ связана с более высокой концентрацией эстрадиола в плазме крови, чем при применении препаратов рекомбинантного ФСГ. Данный аспект следует учитывать при контроле ответа на применение препарата по динамике изменения концентрации эстрадиола. Различия в концентрации эстрадиола в протоколах при применении низких доз препарата для индукции овуляции у пациенток с ановуляторным циклом не обнаружены.
Органами-мишенями для гормонального эффекта чМГ у мужчин являются яички. В яичках ФСГ индуцирует созревание клеток Сертоли, что преимущественно оказывает влияние на деление клеток извитых канальцев и развитие сперматозоидов. При этом необходима высокая внутритестикулярная концентрация андрогенов, которая достигается предшествующей терапией хорионическим гонадотропином человека (чХГ).
Фармакокинетика:
Был установлен фармакокинетический профиль ФСГ, входящего в состав препарата Менопур® Мультидоза.
Абсорбция и распределение
Максимальная концентрация (Сmах) ФСГ в плазме крови достигается в течение 7 ч после подкожного (п/к) введения. Объем распределения, определяемый у здоровых женщин- добровольцев со сниженным количеством рецепторов, после введения повторных доз 150 ME в течение 7 дней составляет 8,9 ± 3,5 МЕ/л.
Выведение
Период полувыведения при повторном введении составляет 30 ± 11 ч. Выводится преимущественно почками.
Кривые зависимости концентрации ЛГ от времени указывают на увеличение концентрации ЛГ после введения препарата Менопур® Мультидоза, однако для фармакокинетического анализа полученных данных недостаточно.
Изучение фармакокинетических свойств препарата Менопур® Мультидоза у пациентов с нарушением функции печени или почек не проводилось.
Показания:
У женщин:
— ановуляция (включая синдром поликистозных яичников (СПКЯ) при неэффективности терапии кломифеном);
— контролируемая гиперстимуляция яичников с целью индукции роста множественных фолликулов при проведении следующих вспомогательных репродуктивных технологий (ВРТ): экстракорпоральное оплодотворение с переносом эмбриона (ЭКО/ПЭ), перенос гамет в маточную трубу (ГИФТ) и интрацитоплазматическая инъекция спермы (ИКСИ).
У мужчин:
— стимуляция сперматогенеза при азооспермии или олигоастеноспермии, обусловленными первичным или вторичным гипогонадотропным гипогонадизмом (в сочетании с препаратами хорионического гонадотропина человека (ХГЧ)).
Противопоказания:
— Повышенная чувствительность к компонентам препарата и растворителя;
— опухоли гипофиза и гипоталамуса;
— детский возраст до 18 лет;
— нарушение функции печени или почек.
У женщин:
— рак яичников, матки или молочной железы;
— беременность и период грудного вскармливания;
— вагинальное кровотечение неясной этиологии;
— наличие кист или увеличение размера яичников, не связанных с СПКЯ;
— первичная недостаточность функции яичников;
— аномалии развития половых органов, несовместимые с беременностью;
— миома матки, несовместимая с беременностью.
У мужчин:
— рак предстательной железы;
— опухоль яичек;
— первичная недостаточность функции яичек.
При наличии в анамнезе заболеваний щитовидной железы и надпочечников, гиперпролактинемии, опухолей гипоталамо-гипофизарной области, соответствующее лечение должно быть проведено до начала терапии чМГ.
С осторожностью:
У женщин — наличие факторов риска развития тромбоэмболических осложнений (индивидуальная или семейная предрасположенность, ожирение с индексом массы тела (ИМТ) > 30 кг/м2), тромбофилия); заболевания маточных труб в анамнезе (см. раздел “Особые указания”).
Беременность и лактация:
Применение препарата Менопур® Мультидоза противопоказано при беременности и в период грудного вскармливания.
Способ применения и дозы:
Препарат Менопур® Мультидоза вводится п/к после растворения лиофилизата во входящем в комплект растворителе.
Лечение препаратом Менопур® Мультидоза следует проводить только под контролем врача, имеющего соответствующую специализацию и опыт лечения бесплодия.
Установлено, что яичники неодинаково реагируют на введение гонадотропинов. По этой причине невозможно разработать универсальную схему дозирования. Доза должна подбираться индивидуально в зависимости от реакции яичников. Препарат Менопур® Мультидоза применяют в виде монотерапии или в комбинации с агонистами или антагонистами гонадотропин рилизинг гормона (ГнРГ). Рекомендуемые дозы и продолжительность терапии зависят от применяемой схемы лечения.
У женщин:
Ановуляция (включая СПКЯ)
Целью лечения препаратом Менопур® Мультидоза является развитие одного зрелого фолликула, из которого после введения препаратов хорионического гонадотропина (чХГ) выйдет ооцит.
Лечение обычно начинают в первые 7 дней менструального цикла. Рекомендуемая начальная доза препарата Менопур® Мультидоза составляет 75-150 ME в сутки в течение не менее 7 дней. Дальнейшую схему лечения подбирают после мониторинга ответа яичников на проводимую терапию на основании результатов ультразвукового исследования (УЗИ) в сочетании с определением концентрации эстрадиола в плазме крови. При отсутствии реакции яичников доза увеличивается на 37,5 ME (одно введение) не чаще 1 раза в неделю, каждое последующее повышение не должно превышать 75 ME. Максимальная суточная доза не должна превышать 225 ME. Если терапевтический ответ не достигнут в течение 4 недель, следует прекратить лечение и начать новый цикл с более высоких начальных доз.
При достижении адекватного ответа яичников на следующий день после последней инъекции препарата Менопур® Мультидоза однократно вводят 5000-10000 ME чХГ для индукции овуляции. Пациентке рекомендуется иметь половые контакты в день введения чХГ и на следующий день введения. В качестве альтернативного метода возможно проведение внутриматочной инсеминации. Пациентка должна находиться под постоянным наблюдением в течение не менее 2 недель после введения чХГ. При чрезмерной реакции яичников на введение препарата Менопур® Мультидоза, курс терапии необходимо прекратить и отказаться от введения чХГ. Пациентке рекомендуется использовать барьерные методы контрацепции или воздержание от половых контактов до наступления менструации.
Контролируемая гиперстимуляция яичников с целью индукции роста множественных фолликулов при проведении ВРТ
Согласно протоколу применения агонистов ГнРГ в соответствии с принципом обратной связи лечение препаратом Менопур® Мультидоза следует назначать примерно через 2 недели после начала лечения агонистами ГнРГ. Если схема лечения не предполагает предварительного применения агонистов ГнРГ, введение препарата Менопур® Мультидоза следует начинать на 2 или 3 день менструального цикла совместно с антагонистами ГнРГ. Рекомендуемая начальная суточная доза препарата Менопур® Мультидоза составляет 150-225 ME в течение не менее первых 5 дней лечения. Дальнейшую схему лечения подбирают после мониторинга ответа яичников на проводимую терапию на основании результатов УЗИ в сочетании с определением концентрации эстрадиола в плазме крови. Рекомендуемая повышающая доза не должна превышать 150 ME. Максимальная суточная доза препарата Менопур® Мультидоза не должна превышать 450 ME. Общая продолжительность терапии не должна превышать 20 дней.
При достижении оптимальной реакции яичников после последней инъекции препарата Менопур® Мультидоза назначается одна инъекция чХГ в дозе 10000 ME для индукции окончательного созревания фолликулов и индукции выхода ооцита. Пациентка должна находиться под постоянным наблюдением в течение не менее 2 недель после введения чХГ. При чрезмерной реакции яичников на введение препарата Менопур® Мультидоза курс терапии необходимо прекратить и отказаться от введения чХГ. Пациентке рекомендуется использовать барьерные методы контрацепции или воздержание от половых контактов до наступления менструации.
У мужчин:
У мужчин для стимуляции сперматогенеза при гипогонадотропном гипогонадизме препарат Менопур® Мультидоза рекомендуется применять в дозе от 75 ME до 150 ME 3 раза в неделю вместе с инъекциями чХГ в дозе 1500 ME 3 раза в неделю, если предшествующая терапия препаратами чХГ (введение 1500-5000 ME чХГ 3 раза в неделю) на протяжении 4-6 месяцев привела к нормализации концентрации тестостерона в плазме крови. Лечение по этой схеме следует продолжать не менее 4 месяцев до улучшения сперматогенеза. При отсутствии положительного эффекта в течение этого времени комбинированная терапия может быть продолжена до получения положительного результата терапии. Согласно исследованиям, для улучшения сперматогенеза может понадобиться не менее 18 месяцев лечения.
Применение в особых клинических случаях
Нарушение функции печени или почек
Клинические исследования у пациентов с нарушением функции печени или почек не проводились.
Дети до 18 лет
Показания к применению препарата Менопур® Мультидоза у детей и подростков в возрасте до 18 лет отсутствуют.
Инструкция по приготовлению раствора
Раствор готовят непосредственно перед введением путем растворения лиофилизата в прилагаемом растворителе. Готовый раствор может вводиться многократно, применение возможно в течение не менее 28 дней.
Не допускается смешивание препарата Менопур® Мультидоза с другими лекарственными средствами в одном шприце!
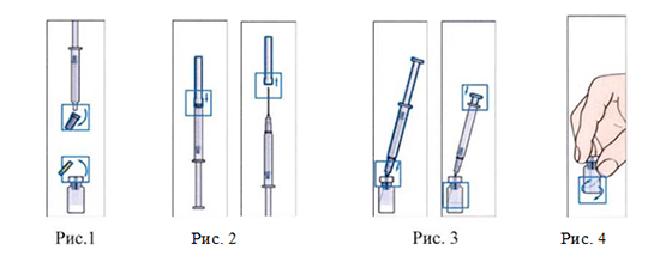
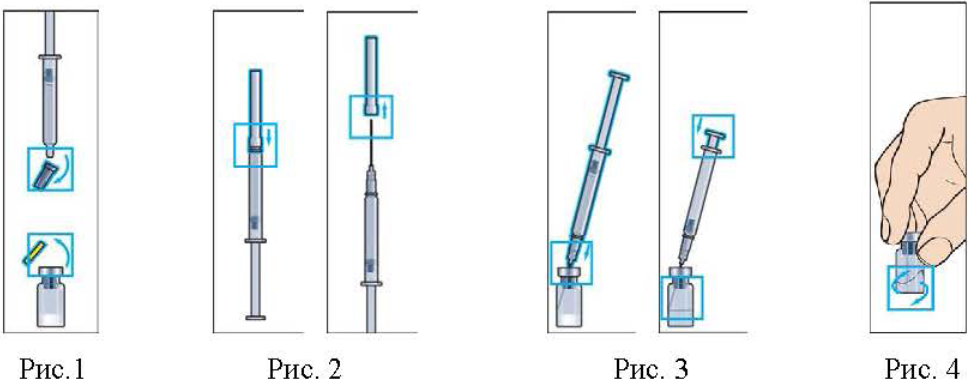
Снимите пластмассовую крышечку с флакона с лиофилизатом. Присоедините иглу для приготовления раствора к шприцу с растворителем и снимите защитный колпачок (Рис.1, 2).
1. Медленно введите растворитель во флакон (Рис. 3).
ФЛАКОН ДЕРЖАТЬ ВЕРТИКАЛЬНО!
2. Круговыми движениями аккуратно перемешайте содержимое флакона до получения прозрачного раствора (Рис. 4). Растворение обычно происходит за 1-2 минуты. Не встряхивать! Не используйте раствор в случае появления нерастворенных частиц или изменения цвета!
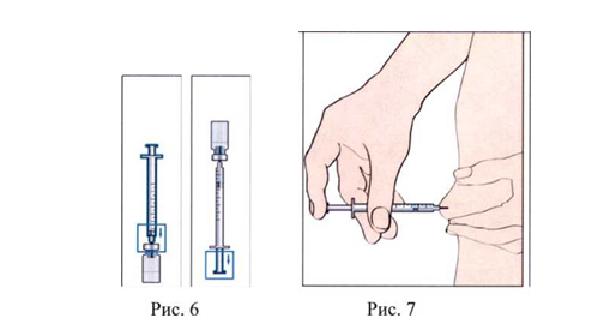
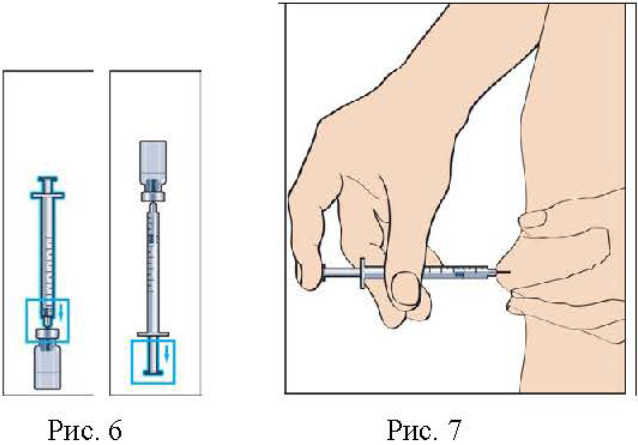
3. Наберите необходимое количество раствора в шприц для инъекции (Рис. 5, 6).
4. Протрите место инъекции спиртовой салфеткой, удалите пузырьки воздуха из шприца и введите препарат, как показано на рис. 7.
Общие указания
Следует избегать встряхивания. В случае помутнения или наличия частиц в растворе его использовать нельзя!
Побочные эффекты:
Частота нежелательных реакций: часто (≥ 1/100 до <1/10), нечасто (≥ 1/1000 до <1/100), редко (≥ 1/10000 до <1/1000), частота неизвестна (в настоящее время данные о распространенности нежелательных реакций отсутствуют, зарегистрированы в период пострегистрационного применения препарата).
Наиболее серьезными и частыми нежелательными реакциями, выявленными при применении препарата Менопур® Мультидоза в клинических исследованиях с частотой до 5%, были синдром гиперстимуляции яичников (СГЯ), боль в животе, головная боль, вздутие живота и боль в месте инъекции. Основные нежелательные реакции, выявленные в клинических исследованиях и в ходе пострегистрационного применения, приведены ниже в таблице.
|
Системноорганный класс |
Часто(≥1/100,<1/10) |
Нечасто(≥1/1000,<1/100) |
Редко(≥1/10000,<1/1000) |
Частота неизвестна |
|
|
Нарушения со стороны иммунной системы |
Реакции гиперчувствительности* |
||||
|
Нарушения со стороны нервной системы |
Головная боль |
Головокружение |
|||
|
Нарушения со стороны органа зрения |
Преходящая слепота, диплопия, мидриаз, скотома, фотопсия, преходящее помутнение стекловидного тела, снижение четкости зрения |
||||
|
Нарушения со стороны сосудов |
Приливы жара |
Венозные и артериальные тромбоэмболии (как правило, при СГЯ) |
|||
|
Нарушения со стороны желудочно-кишечного тракта |
Боль в животе, вздутие живота, тошнота, увеличение живота в объеме |
Рвота, дискомфорт в животе, диарея |
|||
|
Нарушения со стороны кожи и подкожных тканей |
Угревая сыпь, кожные высыпания |
Кожный зуд, крапивница |
|||
|
Нарушения со стороны скелетно-мышечной и соединительной ткани |
Боль в суставах, боль в спине и шее, боль в конечностях |
||||
|
Нарушения со стороны половых органов и молочной железы |
СГЯ**, тазовая боль*** |
Кисты яичников, Нарушения со стороны молочных желез**** |
Перекрут яичника** |
||
|
Общие расстройства и нарушения в месте введения |
Боль в месте инъекции |
Повышенная утомляемость |
Повышение температуры тела, недомогание |
||
|
Лабораторные и инструментальные данные |
Увеличение массы тела |
||||
*Отмечались редкие случаи местных или общих аллергических реакций, в т.ч. случаи анафилактических реакций.
**В клинических исследованиях отмечались связанные с развитием СГЯ нарушения со стороны желудочно-кишечного тракта, такие как вздутие и дискомфорт в животе, тошнота, рвота и диарея. В случаях тяжелого СГЯ в качестве редких осложнений возможно развитие асцита и скопление жидкости в полости таза, экссудативного плеврита, одышки, олигурии, тромбоэмболических осложнений и перекрута яичника.
*** Боль в области придатков матки.
**** Боль и дискомфорт в молочных железах, нагрубание и отечность молочных желез, боль в сосках.
При применении менотропинов у мужчин были отмечены случаи гинекомастии, акне и увеличения массы тела.
Если любые из указанных в инструкции нежелательных реакций усугубляются, или Вы заметили любые другие нежелательные реакции, не указанные в инструкции, сообщите об этом врачу.
Передозировка:
Случаи передозировки при приеме препарата Менопур® Мультидоза неизвестны, однако в таких ситуациях следует ожидать развитие СГЯ.
Подробнее см. раздел “Особые указания”.
Взаимодействие:
Исследование лекарственных взаимодействий препарата Менопур® Мультидоза не проводилось.
Одновременное применение препарата Менопур® Мультидоза с кломифеном может усилить стимуляцию роста фолликулов, несмотря на отсутствие клинических данных о совместном применении этих препаратов. Совместное применение с агонистами ГнРГ может потребовать увеличения дозы препарата Менопур® Мультидоза для достижения оптимальной реакции яичников.
Препарат не следует смешивать в одном шприце с другими лекарственными средствами!
Особые указания:
Менопур® Мультидоза обладает выраженной гонадотропной активностью, в связи с чем при применении препарата могут развиваться нежелательные реакции разной степени тяжести.
Лечение должно проводиться под наблюдением врача, имеющего опыт диагностики и лечения бесплодия!
Применение гонадотропинов требует присутствия квалифицированного медицинского персонала, а также соответствующего оборудования. Перед назначением препарата Менопур® Мультидоза и в процессе лечения следует контролировать состояние яичников (УЗИ и концентрация эстрадиола в плазме крови). Необходимо применять препарат в наиболее низкой эффективной дозе, отвечающей целям лечения.
Первая инъекция препарата должна выполняться под непосредственным наблюдением врача.
Женщины
Перед началом применения препарата Менопур® Мультидоза рекомендуется проведение диагностики причин бесплодия как у женщины, так и у ее партнера, а также установить возможные противопоказания к беременности. Перед началом лечения необходимо провести обследование женщин на наличие гипотиреоза, недостаточности надпочечников, гиперпролактинемии, опухоли гипоталамо-гипофизарной области и при необходимости провести соответствующее лечение.
Проведение контролируемой стимуляции роста фолликулов, вне зависимости от показания к применению у женщин, может привести к увеличению яичников с развитием их гиперстимуляции.
При соблюдении режима дозирования и способа введения препарата в сочетании с мониторингом проводимой терапии, возможно минимизировать риск возникновения вышеуказанных реакций.
Оценка развития фолликула должна проводиться врачом, имеющим соответствующий опыт.
СГЯ
СГЯ — синдром, отличный от неосложненного увеличения яичников, проявления которого зависят от степени тяжести. Он включает в себя значительное увеличение яичников, высокую концентрацию эстрогенов в плазме крови, а также увеличение проницаемости сосудов, что может привести к накоплению жидкости в брюшной, плевральной и, реже, перикардиальной полости.
В тяжелых случаях СГЯ возможны следующие симптомы: боль в животе, вздутие живота, значительное увеличение яичников, увеличение массы тела, одышка, олигурия и симптомы со стороны желудочно-кишечного тракта, включая тошноту, рвоту и диарею. При клиническом обследовании возможно выявление гиповолемии, гемоконцентрации, электролитных нарушений, асцита, гемоперитонеума, экссудативного плеврита, гидроторакса, острого респираторного дистресс-синдрома и тромбоэмболических осложнений.
Чрезмерная реакция яичников на введение гонадотропинов редко приводит к развитию СГЯ, если не вводится чХГ с целью стимуляции овуляции. Поэтому в случае гиперстимуляции яичников не следует вводить чХГ, а пациентку следует предупредить о необходимости воздерживаться от половых контактов или использовать барьерные методы контрацепции не менее 4 дней. СГЯ может быстро прогрессировать (в течение от 24 ч до нескольких дней), становясь серьезным ятрогенным осложнением, поэтому необходимо тщательное наблюдение за пациентками, по крайней мере, в течение не менее 2-х недель после введения чХГ.
Соблюдение рекомендованных доз препарата Менопур® Мультидоза, режима введения и тщательный контроль терапии может свести к минимуму случаи гиперстимуляции яичников и многоплодной беременности. При проведении ВРТ аспирация содержимого всех фолликулов до наступления овуляции может снизить риск развития СГЯ.
СГЯ может быть более тяжелым и затяжным при развитии беременности. Чаще всего СГЯ развивается после прекращения лечения гонадотропинами и достигает максимума тяжести через 7-10 дней после окончания лечения. Обычно СГЯ проходит спонтанно после начала менструации.
При развитии СГЯ тяжелой степени лечение прекращают, пациентку госпитализируют и начинают специфическую терапию.
Развитие СГЯ более характерно для пациенток с СПКЯ.
Многоплодная беременность
При многоплодной беременности отмечается повышенный риск неблагоприятных материнских и перинатальных исходов.
При применении менотропинов многоплодная беременность развивается чаще, чем при естественном зачатии. Отмечается наиболее высокая частота рождения двойни. Для уменьшения риска многоплодной беременности рекомендуется тщательный мониторинг ответа яичников на стимуляцию.
В случае проведения ВРТ вероятность возникновения многоплодной беременности зависит от числа введенных эмбрионов, их качества и возраста пациентки.
Пациентка должна быть предупреждена о потенциальном риске многоплодной беременности до начала лечения бесплодия.
Осложнения беременности
Частота самопроизвольных абортов и преждевременных родов при беременности, наступившей после лечения препаратом Менопур® Мультидоза, выше, чем у здоровой женщины.
Эктопическая беременность
У пациенток с заболеваниями маточных труб в анамнезе, как при естественном зачатии, так и при лечении бесплодия, имеется высокий риск возникновения эктопической беременности. Распространенность внематочной беременности после ЭКО составляет от 2 до 5% по сравнению с 1 до 1,5% в общей популяции.
Новообразования органов репродуктивной системы
Имеются сообщения о новообразованиях яичников и других органов репродуктивной системы, как доброкачественных, так и злокачественных, у женщин, неоднократно получавших препараты для лечения бесплодия. В настоящее время не установлено, увеличивает ли лечение гонадотропинами исходный риск этих опухолей у женщин с бесплодием.
Врожденные пороки развития
Распространенность врожденных пороков развития плода при использовании ВРТ несколько выше, чем при естественном зачатии.
Считается, что это может быть связано с индивидуальными особенностями родителей (возрастом матери, характеристиками спермы) и многоплодной беременностью.
Тромбоэмболические осложнения
Женщины с известными факторами риска развития тромбоэмболических осложнений, таких как индивидуальная или семейная предрасположенность, ожирение (ИМТ > 30 кг/м2) или тромбофилия, могут иметь повышенный риск венозных или артериальных тромбоэмболических осложнений во время или после лечения гонадотропинами. В таких случаях польза их применения должна быть сопоставлена с возможным риском. Следует учитывать, что сама беременность также повышает риск развития тромбоэмболических осложнений.
Мужчины
Применение препарата Менопур® Мультидоза у мужчин с высокой концентрацией ФСГ неэффективно. Для оценки эффективности лечения проводят анализ спермы через 4-6 месяцев после начала лечения.
Влияние на способность управлять транспортными средствами и механизмами:
Исследования влияния менотропинов на способность управлять транспортными средствами и механизмами не проводились. Маловероятно, что препарат Менопур® Мультидоза оказывает отрицательное воздействие на способность управлять транспортными средствами и другими механизмами.
Форма выпуска/дозировка:
Лиофилизат для приготовления раствора для подкожного введения.
Упаковка:
По 600 ME ФСГ + 600 ME ЛГ или 1200 ME ФСГ + 1200 ME ЛГ во флаконы бесцветного стекла типа I, укупоренные бромобутиловой пробкой с алюминиевой обкаткой и крышкой типа «флип-офф».
По 1 мл растворителя в шприцах для одноразового использования бесцветного стекла типа I с резиновым колпачком- наконечником.
600 ME ФСГ + 600 ME ЛГ
1 флакон с лиофилизатом, 1 шприц с растворителем, 1 игла для приготовления раствора в индивидуальной упаковке, 9 шприцев для одноразового использования, градуированных от «0 МЕ» до «600 МЕ» с ценой деления «37,5 МЕ» ФСГ+ЛГ, с иглами в индивидуальных упаковках, с инструкцией по применению в картонную пачку.
1200 ME ФСГ + 1200 ME ЛГ
1 флакон с лиофилизатом, 2 шприца с растворителем, 1 игла для приготовления раствора в индивидуальной упаковке, 18 шприцев для одноразового использования, градуированных от «0 МЕ» до «600 МЕ» с ценой деления «37,5 МЕ» ФСГ+ЛГ, с иглами в индивидуальных упаковках, с инструкцией по применению в картонную пачку.
Условия хранения:
При температуре 2-8 °C. Не замораживать. Хранить в оригинальной упаковке для защиты от света. Приготовленный раствор хранить не более 28 дней при температуре не выше 25 °C.
Хранить в недоступном для детей месте.
Срок годности:
3 года.
Не применять по истечении срока годности, указанного на упаковке.
Условия отпуска
По рецепту
Производитель
Ферринг Интернешнл Сентер СА, Chemin de la Vergognausaz 50, 1162 Saint-Prex, Switzerland, Швейцария
Владелец регистрационного удостоверения/организация, принимающая претензии потребителей:
Ферринг Лечива а.с.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Данное средство обладает выраженной гонадотропной активностью, в связи с чем при его применении могут развиваться побочные явления разной степени тяжести. Лечение необходимо проводить под наблюдением врача, имеющего опыт диагностики и лечения бесплодия.
Применение гонадотропинов требует присутствия квалифицированного медицинского персонала, а также соответствующего оборудования. Перед началом терапии менотропинами и в процессе лечения следует контролировать состояние яичников (УЗИ и концентрация эстрадиола в плазме крови). Необходимо применять средство в наиболее низкой эффективной дозе, отвечающей целям лечения.
Первую инъекцию следует выполнять под непосредственным наблюдением врача.
Перед началом применения менотропинов у женщин рекомендуется проведение диагностики причин бесплодия как у женщины, так и у ее партнера, а также установить возможные противопоказания к беременности. Перед началом лечения необходимо провести обследование женщин на наличие гипотиреоза, недостаточности надпочечников, гиперпролактинемии, опухолей гипоталамуса и гипофиза, при необходимости назначают соответствующее лечение.
Проведение контролируемой стимуляции роста фолликулов, вне зависимости от показания к применению у женщин, может привести к увеличению яичников с развитием их гиперстимуляции.
При соблюдении режима дозирования и способа введения менотропинов в сочетании с мониторингом проводимой терапии, возможно минимизировать риск возникновения вышеуказанных реакций.
Оценку развития фолликула должен проводить врач, имеющий соответствующий опыт.
Синдром гиперстимуляции яичников (СГЯ) — синдром, отличный от неосложненного увеличения яичников, проявления которого зависят от степени тяжести. Он включает в себя значительное увеличение яичников, высокую концентрацию эстрогенов в плазме крови, а также увеличение проницаемости сосудов, что может привести к накоплению жидкости в брюшной, плевральной и, реже, перикардиальной полости.
В тяжелых случаях СГЯ возможны следующие симптомы: боль в животе, вздутие живота, значительное увеличение яичников, увеличение массы тела, одышка, олигурия и желудочно-кишечные симптомы, включая тошноту, рвоту и диарею. При клиническом обследовании возможно выявление гиповолемии, гемоконцентрации, электролитных нарушений, асцита, гемоперитонеума, экссудативного плеврита, гидроторакса, острого респираторного дистресс-синдрома и тромбоэмболических осложнений.
Чрезмерная реакция яичников на введение гонадотропинов редко приводит к развитию СГЯ, если не применяют чХГ с целью стимуляции овуляции. Поэтому в случае гиперстимуляции яичников не следует вводить чХГ, а пациентку следует предупредить о необходимости воздерживаться от половых контактов или использовать барьерные методы контрацепции не менее 4 дней. СГЯ может быстро прогрессировать (в течение от 24 ч до нескольких дней), становясь серьезным медицинским осложнением, поэтому необходимо тщательное наблюдение за пациентками, по крайней мере, в течение не менее 2 недель после введения чХГ.
Соблюдение рекомендованных доз и схем применения и тщательный контроль терапии может свести к минимуму случаи гиперстимуляции яичников и многоплодной беременности. При проведении вспомогательных репродуктивных технологий (ВРТ) аспирация содержимого всех фолликулов до наступления овуляции может снизить риск развития СГЯ.
СГЯ может быть более тяжелым и затяжным при развитии беременности. Чаще всего СГЯ развивается после прекращения лечения гонадотропинами и достигает максимума тяжести через 7-10 дней после окончания лечения. Обычно СГЯ проходит спонтанно после начала менструации.
При развитии СГЯ тяжелой степени лечение прекращают, пациентку госпитализируют и начинают специфическую терапию.
Развитие СГЯ более характерно для пациенток с СПКЯ.
При многоплодной беременности отмечается повышенный риск неблагоприятных материнских и перинатальных исходов.
При применении менотропинов многоплодная беременность развивается чаще, чем при естественном зачатии. Отмечается наиболее высокая частота рождения двойни. Для уменьшения риска многоплодной беременности рекомендуется тщательный мониторинг ответа яичников на стимуляцию.
В случае проведения ВРТ вероятность возникновения многоплодной беременности зависит от числа введенных эмбрионов, их качества и возраста пациентки.
Пациентка должна быть предупреждена о потенциальном риске многоплодной беременности до начала лечения.
Частота самопроизвольных абортов и преждевременных родов при беременности, наступившей после лечения менотропинами, выше, чем у здоровых женщин.
У пациенток с заболеваниями маточных труб в анамнезе, как при естественном зачатии, так и при лечении бесплодия, имеется высокий риск возникновения эктопической беременности.
Имеются сообщения о новообразованиях яичников и других органов репродуктивной системы, как доброкачественных, так и злокачественных, у женщин, которые подверглись нескольким схемам введения менотропинов для лечения бесплодия. Пока не установлено, увеличивает ли лечение гонадотропинами исходный риск этих опухолей у женщин с бесплодием.
Распространенность врожденных пороков развития плода при использовании ВРТ несколько выше, чем при естественном зачатии. Считается, что это может быть связано с индивидуальными особенностями родителей (возрастом матери, характеристиками спермы) и многоплодной беременностью.
Женщины с известными факторами риска развития тромбоэмболических осложнений, таких как индивидуальная или семейная предрасположенность, ожирение (ИМТ > 30 кг/м2) или тромбофилия, могут иметь повышенный риск венозных или артериальных тромбоэмболических осложнений во время или после лечения гонадотропинами. В таких случаях польза их применения должна быть сопоставлена с возможным риском. Следует учитывать, что сама беременность также повышает риск развития тромбоэмболических осложнений.
Применение менотропинов у мужчин с высокой концентрацией ФСГ в крови неэффективно. Для оценки эффективности лечения проводят анализ спермы через 4-6 месяцев после начала лечения.
МНН: Менотропины
Производитель: Ферринг ГмбХ
Анатомо-терапевтическо-химическая классификация: Human menopausal gonadotropin
Номер регистрации в РК:
№ РК-ЛС-5№019140
Информация о регистрации в РК:
17.05.2017 — 17.05.2023
- Скачать инструкцию медикамента
Торговое название
Менопур
Международное непатентованное название
Нет
Лекарственная форма
Порошок лиофилизированный для приготовления раствора для инъекций 600 МЕ, 1200 МЕ в комплекте с растворителем
Состав
Один флакон содержит Менопур 600 МЕ
активное вещество — менотропин высокоочищенный (человеческий менопаузальный гонадотропин высокоочищенный), содержащий 600 МЕ ФСГ (фолликулостимулирующего гормона) и 600 МЕ ЛГ (лютеинизирующего гормона,
Менопур 1200 МЕ
активное вещество — менотропин высокоочищенный (человеческий менопаузальный гонадотропин высокоочищенный), содержащий 1200 МЕ ФСГ (фолликулостимулирующего гормона) и 1200 МЕ ЛГ (лютеинизирующего гормона,
вспомогательные вещества: лактозы моногидрат, натрия гидрофосфат гептагидрат, полисорбат 20, 1 М раствор кислоты фосфорной, 0.5 М раствор натрия гидрофосфата гептагидрата.
растворитель: м-крезол, вода для инъекций.
Описание
Растворитель: Прозрачный бесцветный раствор.
Фармакотерапевтическая группа
Код АТС G03GA02
Фармакологические свойства
Биодоступность менотропина выше после подкожного введения, чем после внутримышечного введения. После внутримышечного введения 300 МЕ ФСГ и 300 МЕ ЛГ полученные значения составляют: AUC0- = 320,1 мМЕ/мл/ч, Cmax = 4,15 мМЕ/мл, tmax= 18 ч; после подкожного введения AUC0- = 385,2 мМЕ/мл х ч, Cmax = 5,62 мМЕ/мл, tmax= 12 ч. Период полувыведения составляет 56 ч после внутримышечного введения и 51 ч после подкожного введения. Менотропин выводится преимущественно почками.
Фармакодинамика
Менопур является препаратом человеческого менопазуального гонадотропина высокой степени очистки. Препарат содержит фолликулостимулирующий (ФСГ) и лютеинизирующий гормоны (ЛГ) в соотношении 1:1, по 600 МЕ или по 1200 МЕ ФСГ и ЛГ, которые вырабатываются гипофизом человека. Действующее вещество получают из мочи женщин в постменопаузальном периоде. Менотропин, обладающий ФСГ и ЛГ активностью, индуцирует рост и созревание фолликулов, а также гонадную секрецию стероидов у женщин, не страдающих первичной недостаточностью яичников. ФСГ запускает фолликулярный рост на стадии раннего фолликулогенеза, а ЛГ участвует в овариальном стероидогенезе и в физиологических процессах, приводящих к развитию предовуляторного фолликула.
Показания к применению
Стимуляция созревания фолликулов при бесплодии.
Монофолликулярная стимуляция
— гипо- или нормогонадотропная аменорея, олигоменорея
— ановуляторные циклы и недостаток лютеиновой фазы у женщин,
которые оказались нечувствительными к лечению кломифеном
Мультифолликулярная стимуляция
— контролируемая суперовуляция яичников с целью индукции
множественного роста фолликулов при проведении вспомогательных
репродуктивных технологий (ВРТ)
Способ применения и дозы
Лечение препаратом Менопур должно проводиться под наблюдением врача.
Препарат вводят подкожно или внутримышечно после растворения в прилагаемом растворителе.
Приготовленный раствор предназначен для многократного применения и может храниться в течение 28 дней.
Режимы дозирования, описанные ниже, аналогичны как для подкожного, так и для внутримышечного введения.
Доза препарата подбирается индивидуально, в зависимости от реакции яичников, и корригируется по результатам ультразвукового исследования яичников и уровня эстрадиола в крови.
Менопур может применяться как отдельно, так и в комбинации с агонистом или антагонистом гонадотропин-рилизинг-гормона (ГнРГ).
Длительность лечения зависит от индивидуальных особенностей пациентки и от применяемого протокола лечения.
Монофолликулярная стимуляция
Применение Менопура следует начинать в течение первых 7 дней менструального цикла. Рекомендуемая начальная доза составляет 75 МЕ в день (или 150 МЕ каждые 2 дня). Дальнейший режим лечения следует подбирать индивидуально, основываясь на результаты клинического наблюдения (включая ультразвуковое исследование яичников и\или контроль уровня эстрадиола). Лечение продолжается пока соответствующие уровни эстрогена (содержание эстрадиола в плазме – 1.1-2.9 нмол/л = 300-800 пг/мл) и соответствующее созревание фолликула (диаметр ≤18 мм) не достигнуты. В случае отсутствия результата лечение может быть отменено либо продолжено в увеличенной дозировке, но делать это не чаще одного раза в течение 7 дней. Рекомендованное одноразовое увеличение дозы составляет 37,5 МЕ, но не более 75 МЕ. Максимальная суточная доза препарата не должна превышать 225 МЕ. Курс лечения длится 7 — 12 дней максимум. Если уровень плазменного эстрогена повышается слишком быстро (более 100% в 2-3 дня), доза Менопура должна быть уменьшена. Если Менопур применяется в комбинации с ФСГ, доза Менопура должна быть уменьшена соответственно.
При достижении оптимального результата ввести разовую дозу хорионического гонадотропного гормона (ХГГ) от 5000 до 10000 МЕ на следующий день после последней введенной дозы Менопура. Пациентке рекомендуется иметь половые контакты в день введения ХГГ и на следующий день. Альтернативным способом является проведение искусственного внутриматочного оплодотворения. Пациентка должна находиться под тщательным наблюдением на протяжении 2-х недель после введения ХГГ.
Если наблюдается чрезмерная реакция на применение Менопура, курс лечения необходимо прекратить и не вводить ХГГ. Пациентка должна использовать барьерный метод контрацепции или отказаться от половых контактов до начала следующих менструальных кровотечений.
Мультифолликулярная стимуляция
Для пациентов, которые прошли курс лечения с применением агониста ГнРГ, лечение Менопуром следует начинать приблизительно через 2 недели после начала лечения агонистом. Рекомендованная суточная доза Менопура составляет 150-225 МЕ на протяжении, минимум, первых 5 дней лечения.
Основываясь на клинических наблюдениях (включая ультразвуковое исследование и\или контроль уровня эстрадиола), последующее дозирование должно быть индивидуальным, но не превышать 150 МЕ, максимальная суточная доза – 450 МЕ. Длительность лечения не должна превышать 20 дней.
При использовании протоколов, не предусматривающих десенсибилизацию с применением агонистов ГнРГ, терапию с применением Менопура следует начинать на 2-3 день менструального цикла. Рекомендованная доза и режим дозирования Менопура такие же, как для протоколов с применением агонистов ГнРГ.
При достижении оптимальной реакции организма вводится разовая доза от 5000 до 10000 МЕ хорионического гонадотропного гормона (ХГГ) для индукции окончательного созревания фолликула и подготовки к выходу ооцита. Овуляция наступает 32-48 часов спустя. Пациентке рекомендуется иметь ежедневные половые контакты со дня введения ХГГ к ожидаемому времени овуляции. Пациентка должны находиться под тщательным наблюдением на протяжение 2 недель после введения ХГГ.
Если наблюдается чрезмерная реакция на применение Менопура, курс лечения необходимо прекратить и отменить введение ХГГ. Пациентка должна использовать барьерный метод контрацепции или отказаться от половых контактов до начала следующих менструальных кровотечений.
Приготовление раствора
Порошок следует разводить только тем растворителем, который находится в упаковке. Присоедините иглу для разведения к предварительно заполненному шприцу с растворителем. Введите весь растворитель во флакон с порошком. Порошок должен быстро раствориться до получения прозрачного раствора. В противном случае осторожно вращайте флакон до получения прозрачного раствора. Следует избегать интенсивного встряхивания. Нельзя использовать непрозрачный раствор или раствор, содержащий видимые частицы.
Шприцы для введения градуированы в единицах от 37,5 до 600 МЕ ФСГ и ЛГ. Отберите назначенную дозу препарата в шприц для введения и сразу введите. 1 мл раствора содержит 600 МЕ ФСГ и ЛГ.
Побочные действия
Часто
— боль, отек и зуд в месте инъекции
— головная боль
— тошнота, рвота, ощущение тяжести и боль в животе
— чувство напряжения в молочных железах
— боль в области таза, увеличение яичников, кисты яичников,
повышенный риск внематочной беременности, многоплодная
беременность
— синдром гиперстимуляции яичников (СГЯ) легкая и средняя степень
— гриппоподобные симптомы, такие как повышение температуры и боль в
суставах
Редко
— венозные и артериальные тромбозы (тромбоз глубоких вен, легочная
эмболия в основном в сочетании с синдромом гиперстимуляции
яичников (СГЯ)
— синдром гиперстимуляции яичников (СГЯ) тяжелая степень
Очень редко
— локализованные или генерализованные аллергические реакции
Противопоказания
— гиперчувствительность к действующему веществу или любому из
вспомогательных веществ
— опухоли гипофиза или гипоталамуса, гиперпролактинемия
— экстрагенитальная эндокринопатия, обусловленная тяжелыми
заболеваниями щитовидной железы и надпочечников
— карцинома яичников, матки или молочных желез
— гинекологические кровотечения неустановленной этиологии
— киста яичников или увеличение яичников, не связанное с синдромом
поликистозных яичников
— беременность и период лактации
— детский и подростковый возраст до 18 лет
— первичная несостоятельность яичников
— аномалии половых органов, несовместимые с беременностью
— фиброзные новообразования матки, несовместимые с беременностью
— бесплодие без нарушения нормального созревания фолликулов (за
исключением пациентов, которые участвуют в программах
вспомогательных репродуктивных технологий (ВРТ))
Лекарственные взаимодействия
Не смешивать с другими лекарственными средствами. Несмотря на отсутствие клинического опыта, предполагается, что одновременное применение Менопура и кломифена цитрата может усиливать реакцию фолликулярного созревания. При совместном применении Менопура с агонистами ГнРГ с целью гипофизарной десенсибилизации могут понадобиться более высокие дозы Менопура для достижения желаемой реакции со стороны яичников.
Менопур может применяться в сочетании с препаратом Бравель (урофоллитропин (ФСГ)). Исследования показали, что совместное введение этих препаратов не влияет на их биодоступность.
Менопур может применяться в сочетании с препаратом Хорагон (человеческий хорионический гонадотропин, чХГ) для лечения женщин с целью индукции овуляции после стимуляции фолликулярного роста.
Особые указания
Менопур должен применяться исключительно под наблюдением специалиста, специализирующегося на лечении бесплодия.
Прежде чем начать лечение, необходимо провести исследование причин бесплодия у обоих партнеров, а также провести медицинское обследование относительно наличия возможных противопоказаний. В частности, пациенток необходимо обследовать на наличие гипотиреоидизма, адренокортикальной недостаточности, гиперпролактинемии, гипофизарной или гипоталамической опухоли, назначить соответствующее лечение, предусмотренное при этих патологических состояниях. Перед началом лечения бесплодия у женщин следует оценить функциональное состояние яичников (ультразвуковая диагностика и уровень эстрадиола в крови). Первая инъекция Менопура должна быть проведена под тщательным контролем врача. У пациенток, которым проводится стимуляция роста фолликулов, может наблюдаться увеличение размера яичников или развиваться синдром гиперстимуляции яичников (СГЯ). Соблюдение рекомендуемого режима дозирования Менопура и тщательный контроль за реакцией яичников помогут минимизировать риск развития этих побочных эффектов.
Синдром гиперстимуляции яичников (СГЯ)
СГСЯ представляет собой клиническое явление, отличающееся от неосложненного увеличения яичников, и может проявиться с возрастанием степени тяжести. Признаки СГСЯ включают: увеличение яичников, высокие сывороточные уровни половых гормонов и увеличение проницаемости сосудов, которое может приводить к накоплению жидкости в перитонеальной, плевральной и, в редких случаях, перикардиальной полостях.
В тяжелых случаях СГСЯ могут наблюдаться следующие симптомы: абдоминальная боль, увеличение живота, чрезмерное увеличение яичников, увеличение массы тела, одышка, олигурия и желудочно-кишечные симптомы, такие как тошнота, рвота и диарея. При клиническом обследовании могут быть выявлены: гиповолемия, сгущение крови, нарушение баланса электролитов, асцит, гемоперитонеум, плевральный выпот, гидроторакс, острая дыхательная недостаточность и тромбоэмболия. Кроме того, может произойти разрыв яичниковых кист.
Чрезмерная овариальная реакция на лечение гонадотропинами редко приводит к развитию СГСЯ до тех пор, пока для инициирования овуляции не вводится чХГ. Следовательно, в случае овариальной гиперстимуляции не следует вводить чХГ. Также нужно посоветовать пациентке воздерживаться от половых контактов или использовать барьерные методы контрацепции на протяжении не менее 4 дней. СГСЯ может очень быстро прогрессировать (от 24 часов до нескольких дней) и приобретать серьезную симптоматику. Следовательно, пациентка должна находиться под медицинским контролем в течение периода лечения и не менее 2 недель после введения чХГ.
Минимизировать риск развития овариальной гиперстимуляции и многоплодной беременности можно, придерживаясь рекомендованного дозирования и режима введения препарата Менопур, а также тщательно контролируя курс лечения. При проведении ВРТ риск развития гиперстимуляции можно снизить путем аспирации всех фолликулов перед овуляцией.
Критерии оценки чрезмерной реакции яичников:
В случае монофолликулярного возбуждения: повышение уровня эстрадиола в плазме более чем на 4000 пмол/л или 1100 пг/мл и/или более чем 3 фолликула диаметром, по крайней мере, 16 мм.
В случае мультифолликулярной стимуляции: повышение уровня эстрадиола в плазме более чем 11нмол/л или 3000 пг/мл и имеется 20 фолликулов диаметром, по крайней мере, 12 мм.
Если уровень эстрадиола превышает 20 нмол/л или 5500 пг/мл и есть, по крайней мере, 40 фолликулов, чХГ не должен быть введен.
СГСЯ может становиться более тяжелым и продолжительным в случае наступления беременности. Наиболее часто СГСЯ развивается после завершения гормонального лечения и достигает максимальной частоты приблизительно через 7-10 дней после окончания лечения. Обычно СГСЯ проходит спонтанно с началом менструаций.
В случае тяжелого СГСЯ лечение гонадотропинами следует прекратить, если оно все еще продолжается, пациентку следует госпитализировать и начать специфическое лечение СГСЯ.
Данный синдром чаще встречается у женщин с синдромом поликистозных яичников.
Многоплодная беременность
У пациенток, у которых проводится индукция овуляции с применением гонадотропинов, частота многоплодных беременностей выше, чем при естественном оплодотворении. Для минимизации риска многоплодия необходимо вести тщательное наблюдение за реакцией яичников пациентки.
У пациенток, которым проводится процедура ВРТ, риск многоплодных беременностей главным образом зависит от количества пересаженных эмбрионов, их качества и возраста пациентки.
Невынашивание
Количество случаев невынашивания беременности выше у женщин, которым проводилась стимуляция созревания фолликулов или при проведении программы ВРТ, чем в случаях естественного зачатия.
Внематочная беременность
У женщин с заболеваниями маточных труб высокий риск развития внематочной беременности не зависимо от того, наступила данная беременность в результате естественного зачатия или лечения бесплодия. Сообщалось, что после проведения ВРТ частота случаев внематочной беременности составляла 2-5 % в сравнении с 1-1,5 % случаев естественного зачатия.
Новообразования репродуктивных органов
У женщин, которые неоднократно получали медикаментозное лечение по поводу бесплодия, наблюдалось развитие как доброкачественных, так и злокачественных новообразований яичников и других органов репродуктивной системы, связь между лечением с применением гонадотропина и склонностью к новообразованиям не выяснена.
Врожденные пороки развития
Распространенность врожденных пороков развития плода у женщин после проведения ВРТ может незначительно превышать количество пороков при естественном зачатии, это может быть результатом индивидуальных особенностей родителей (например, возраст матери, характеристики спермы и т.д.).
Тромбоэмболические нарушения
У женщин с повышенным риском развития тромбоэмболических состояний ввиду наследственной предрасположенности, ожирением (индекс массы тела > 30 кг/м2) или тромбофилией могут развиваться венозные или артериальные тромбоэмболические нарушения как во время, так и после окончания лечения гонадотропином. Следует отметить, что сама по себе беременность также несет повышенный риск тромбоэмболических осложнений.
Особенности влияния на способность управлять транспортным средством или потенциально опасными механизмами
Не влияет.
Передозировка
Симптомы: возможно развитие синдрома гиперстимуляции яичников (СГЯ).
Лечение: При легкой степени СГЯ специфического лечения не требуется. Пациентка должна находиться под тщательным медицинским контролем. При средней степени СГЯ показан клинический мониторинг и симптоматическое лечение, при необходимости внутривенное введение кровозаменителей с высокой гемоконцентрацией. При тяжелой степени СГЯ необходима обязательная госпитализация, поскольку в таких случаях могут развиться состояния, угрожающие жизни, требующие интенсивного медицинского вмешательства.
Форма выпуска и упаковка
Препарат, содержащий 600 МЕ/1200 МЕ фолликулостимулирующего гормона и 600 МЕ /1200 МЕ лютеинизирующего гормона, помещен в бесцветный стеклянный флакон.
По 1 мл растворителя в предварительно заполненном шприце.
1 флакон с препаратом и 1 шприц с растворителем, 1 игла для разведения вложены в пластиковую ячейковую упаковку (запечатанная прозрачной пленкой или с пластиковой крышкой). Отдельно 9 шприцев для введения и 9 спиртовых салфеток вложены в картонную ячейковую упаковку и обвернуты пленкой. 1 пластиковая ячейковая упаковка и 1 картонная ячейковая упаковка вместе с инструкцией по медицинскому применению на государственном и русском языках вложены в картонную коробку (для дозировки 600 МЕ).
1 флакон с препаратом и 2 шприца с растворителем, 1 игла для разведения вложены в пластиковую ячейковую упаковку (запечатанная прозрачной пленкой или с пластиковой крышкой). Отдельно 18 шприцев для введения и 18 спиртовых салфеток вложены в картонную ячейковую упаковку и обвернуты пленкой. 1 пластиковая ячейковая упаковка и 1 картонная ячейковая упаковка вместе с инструкцией по медицинскому применению на государственном и русском языках вложены в картонную коробку (для дозировки 1200 МЕ).
Условия хранения
Хранить при температуре 2 — 8 °С в оригинальной упаковке. Не замораживать.
Разведенный препарат можно хранить в течение 28 дней при температуре не выше 25 °С.
Хранить в недоступном для детей месте!
Срок хранения
3 года
Не использовать по истечении срока годности, указанного на упаковке.
Условия отпуска из аптек
По рецепту
Производитель
«Ферринг ГмбХ», Германия
Витланд 11, Постфаш 2145, Д-24109б Киль
Владелец регистрационного удостоверения «Ферринг Интернешнл Сентер СА», Швейцария
Адрес организации, принимающей на территории Республики Казахстан претензии от потребителей по качеству продукции (товара), ответственной за пострегистрационное наблюдение за безопасностью лекарственного средства
Представительство «Ферринг Фармацевтикалс С.А.» в Республике Казахстан
г. Алматы, 050059
пр. Аль-Фараби, 7
блок 5А, офис 131
Бизнес Центр «Нурлы Тау»
тел./факс : +7(727) 311 5447
| 335769811477977073_ru.doc | 86 кб |
| 365141551477978245_kz.doc | 114.5 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники
Выбор описания
| Лек. форма | Дозировка |
|---|---|
|
лиофилизат для приготовления раствора для подкожного введения |
600 МЕ ФСГ+600 МЕ ЛГ 1200 МЕ ФСГ+1200 МЕ ЛГ |
лиофилизат для приготовления раствора для подкожного введения
600 МЕ ФСГ+600 МЕ ЛГ
1200 МЕ ФСГ+1200 МЕ ЛГ
Описание препарата Менопур® Мультидоза (лиофилизат для приготовления раствора для подкожного введения, 600 МЕ ФСГ+600 МЕ ЛГ) отсутствует в БД РЛС®
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Фармакологическая группа
- Показания по МКБ-10
Действующее вещество
ATX
Фармакологическая группа
Дата обновления: 22.02.2023
Менопур® Мультидоза
Menopur® Multidosa
Регистрационный номер
Торговое наименование
Менопур® Мультидоза
Международное непатентованное наименование
Лекарственная форма
лиофилизат для приготовления раствора для подкожного введения
Состав
1 флакон с лиофилизатом содержит:
активное вещество:
менотропины — 600 МЕ ФСГ + 600 МЕ ЛГ или 1200 МЕ ФСГ + 1200 МЕ ЛГ;
вспомогательные вещества: лактозы моногидрат 21,0 мг, полисорбат-20 0,005 мг, динатрия гидрофосфата гептагидрат 0,268 мг, фосфорной кислоты раствор 1 М q.s., динатрия гидрофосфата раствор 0,5 М q.s.
1 шприц с растворителем содержит: метакрезол 3,63 мг, вода для инъекций до 1,1 мл.
Описание
Лиофилизат: белая или почти белая аморфная масса.
Растворитель: бесцветный прозрачный раствор.
Фармакотерапевтическая группа
Код АТХ
Фармакологические свойства
Фармакодинамика
Действующим веществом препарата Менопур® Мультидоза является человеческий менопаузальный гонадотропин (чМГ) высокой степени очистки, получаемый из мочи женщин в период постменопаузы. Препарат содержит фолликулостимулирующий гормон (ФСГ) и лютеинизирующий гормон (ЛГ).
Органами-мишенями для гормонального эффекта чМГ у женщин являются яичники. ЧМГ ФСГ стимулирует гаметогенез и синтез половых гормонов.
ФСГ является ключевым фактором роста и развития фолликулов на стадии раннего фолликулогенеза. ЛГ играет важную роль в продукции половых гормонов яичниками и вовлечен в физиологические процессы, приводящие к развитию полноценного преовуляторного фолликула. Стимуляция фолликулярного роста под действием ФСГ, в случае полного отсутствия ЛГ, завершается патологическим развитием фолликула, ассоциированным с низкой концентрацией эстрадиола и неспособностью к лютеинизации неовулирующего фолликула в ответ на нормальный овуляторный стимул. Принимая во внимание действие ЛГ, заключающееся в усилении синтеза половых гормонов, применение препарата Менопур® Мультидоза в циклах ЭКО/ИКСИ связана с более высокой концентрацией эстрадиола в плазме крови, чем при применении препаратов рекомбинантного ФСГ. Данный аспект следует учитывать при контроле ответа на применение препарата по динамике изменения концентрации эстрадиола. Различия в концентрации эстрадиола в протоколах при применении низких доз препарата для индукции овуляции у пациенток с ановуляторным циклом не обнаружены.
Органами-мишенями для гормонального эффекта чМГ у мужчин являются яички. В яичках ФСГ индуцирует созревание клеток Сертоли, что преимущественно оказывает влияние на деление клеток извитых канальцев и развитие сперматозоидов. При этом необходима высокая внутритестикулярная концентрация андрогенов, которая достигается предшествующей терапией хорионическим гонадотропином человека (чХГ).
Фармакокинетика
Был установлен фармакокинетический профиль ФСГ, входящего в состав препарата Менопур® Мультидоза.
Абсорбция и распределение
Максимальная концентрация (Cmax) ФСГ в плазме крови достигается в течение 7 ч после подкожного (п/к) введения. Объём распределения, определяемый у здоровых женщин- добровольцев со сниженным количеством рецепторов, после введения повторных доз 150 ME в течение 7 дней составляет 8,9 ± 3,5 МЕ/л.
Выведение
Период полувыведения при повторном введении составляет 30 ± 11 ч. Выводится преимущественно почками.
Кривые зависимости концентрации ЛГ от времени указывают на увеличение концентрации ЛГ после введения препарата Менопур® Мультидоза, однако для фармакокинетического анализа полученных данных недостаточно.
Изучение фармакокинетических свойств препарата Менопур® Мультидоза у пациентов с нарушением функции печени или почек не проводилось.
Показания
У женщин:
- ановуляция (включая синдром поликистозных яичников (СПКЯ) при неэффективности терапии кломифеном);
- контролируемая гиперстимуляция яичников с целью индукции роста множественных фолликулов при проведении следующих вспомогательных репродуктивных технологий (ВРТ): экстракорпоральное оплодотворение с переносом эмбриона (ЭКО/ПЭ), перенос гамет в маточную трубу (ГИФТ) и интрацитоплазматическая инъекция спермы (ИКСИ).
У мужчин:
- стимуляция сперматогенеза при азооспермии или олигоастеноспермии, обусловленными первичным или вторичным гипогонадотропным гипогонадизмом (в сочетании с препаратами хорионического гонадотропина человека (ХГЧ)).
Противопоказания
- Гиперчувствительность к действующему веществу или к любому из вспомогательных веществ препарата и компонентам растворителя;
- опухоли гипофиза и гипоталамуса;
- детский возраст до 18 лет;
- нарушение функции печени или почек.
У женщин:
- рак яичников, матки или молочной железы;
- беременность и период грудного вскармливания;
- вагинальное кровотечение неясной этиологии;
- наличие кист или увеличение размера яичников, не связанных с СПКЯ;
- первичная недостаточность функции яичников;
- аномалии развития половых органов, несовместимые с беременностью;
- миома матки, несовместимая с беременностью.
У мужчин:
- рак предстательной железы;
- опухоль яичек;
- первичная недостаточность функции яичек.
При наличии в анамнезе заболеваний щитовидной железы и надпочечников, гиперпролактинемии, опухолей гипоталамо-гипофизарной области, соответствующее лечение должно быть проведено до начала терапии чМГ.
С осторожностью
У женщин — наличие факторов риска развития тромбоэмболических осложнений (индивидуальная или семейная предрасположенность, ожирение с индексом массы тела (ИМТ) > 0 кг/м2), тромбофилия); заболевания маточных труб в анамнезе (см. раздел “Особые указания”).
Применение при беременности и в период грудного вскармливания
Применение препарата Менопур® Мультидоза противопоказано при беременности и в период грудного вскармливания.
Способ применения и дозы
Препарат Менопур® Мультидоза вводится п/к после растворения лиофилизата во входящем в комплект растворителе.
Лечение препаратом Менопур® Мультидоза следует проводить только под контролем врача, имеющего соответствующую специализацию и опыт лечения бесплодия.
Установлено, что яичники неодинаково реагируют на введение гонадотропинов. По этой причине невозможно разработать универсальную схему дозирования. Доза должна подбираться индивидуально в зависимости от реакции яичников. Препарат Менопур® Мультидоза применяют в виде монотерапии или в комбинации с агонистами или антагонистами гонадотропин рилизинг гормона (ГнРГ). Рекомендуемые дозы и продолжительность терапии зависят от применяемой схемы лечения.
У женщин:
Ановуляция (включая СПКЯ)
Целью лечения препаратом Менопур® Мультидоза является развитие одного зрелого фолликула, из которого после введения препаратов хорионического гонадотропина (чХГ) выйдет ооцит.
Лечение обычно начинают в первые 7 дней менструального цикла. Рекомендуемая начальная доза препарата Менопур® Мультидоза составляет 75—150 ME в сутки в течение не менее 7 дней. Дальнейшую схему лечения подбирают после мониторинга ответа яичников на проводимую терапию на основании результатов ультразвукового исследования (УЗИ) в сочетании с определением концентрации эстрадиола в плазме крови.
При отсутствии реакции яичников доза увеличивается на 37,5 ME (одно введение) не чаще 1 раза в неделю, каждое последующее повышение не должно превышать 75 ME. Максимальная суточная доза не должна превышать 225 ME. Если терапевтический ответ не достигнут в течение 4 недель, следует прекратить лечение и начать новый цикл с более высоких начальных доз.
При достижении адекватного ответа яичников на следующий день после последней инъекции препарата Менопур® Мультидоза однократно вводят 5000–10000 ME чХГ для индукции овуляции. Пациентке рекомендуется иметь половые контакты в день введения чХГ и на следующий день введения. В качестве альтернативного метода возможно проведение внутриматочной инсеминации. Пациентка должна находиться под постоянным наблюдением в течение не менее 2 недель после введения чХГ. При чрезмерной реакции яичников на введение препарата Менопур® Мультидоза, курс терапии необходимо прекратить и отказаться от введения чХГ. Пациентке рекомендуется использовать барьерные методы контрацепции или воздержание от половых контактов до наступления менструации.
Контролируемая гиперстимуляция яичников с целью индукции роста множественных фолликулов при проведении ВРТ
Согласно протоколу применения агонистов ГнРГ в соответствии с принципом обратной связи лечение препаратом Менопур® Мультидоза следует назначать примерно через 2 недели после начала лечения агонистами ГнРГ. Если схема лечения не предполагает предварительного применения агонистов ГнРГ, введение препарата Менопур® Мультидоза следует начинать на 2 или 3 день менструального цикла совместно с антагонистами ГнРГ. Рекомендуемая начальная суточная доза препарата Менопур® Мультидоза составляет ISO- 225 ME в течение не менее первых 5 дней лечения. Дальнейшую схему лечения подбирают после мониторинга ответа яичников на проводимую терапию на основании результатов УЗИ в сочетании с определением концентрации эстрадиола в плазме крови. Рекомендуемая повышающая доза не должна превышать 150 ME. Максимальная суточная доза препарата Менопур® Мультидоза не должна превышать 450 ME. Общая продолжительность терапии не должна превышать 20 дней.
При достижении оптимальной реакции яичников после последней инъекции препарата Менопур® Мультидоза назначается одна инъекция чХГ в дозе 10000 ME для индукции окончательного созревания фолликулов и индукции выхода ооцита. Пациентка должна находиться под постоянным наблюдением в течение не менее 2 недель после введения чХГ. При чрезмерной реакции яичников на введение препарата Менопур® Мультидоза курс терапии необходимо прекратить и отказаться от введения чХГ. Пациентке рекомендуется использовать барьерные методы контрацепции или воздержание от половых контактов до наступления менструации.
У мужчин:
У мужчин для стимуляции сперматогенеза при гипогонадотропном гипогонадизме препарат Менопур® Мультидоза рекомендуется применять в дозе от 75 ME до 150 ME 3 раза в неделю вместе с инъекциями чХГ в дозе 1500 ME 3 раза в неделю, если предшествующая терапия препаратами чХГ (введение 1500–5000 ME чХГ 3 раза в неделю) на протяжении 4-6 месяцев привела к нормализации концентрации тестостерона в плазме крови. Лечение по этой схеме следует продолжать не менее 4 месяцев до улучшения сперматогенеза. При отсутствии положительного эффекта в течение этого времени комбинированная терапия может быть продолжена до получения положительного результата терапии. Согласно исследованиям, для улучшения сперматогенеза может понадобиться не менее 18 месяцев лечения.
Особые группы пациентов
Нарушение функции печени или почек
Клинические исследования у пациентов с нарушением функции печени или почек не проводились.
Дети
Показания к применению препарата Менопур® Мультидоза у детей и подростков в возрасте до 18 лет отсутствуют.
Инструкция по приготовлению раствора
Раствор готовят непосредственно перед введением путём растворения лиофилизата в прилагаемом растворителе. Готовый раствор может вводиться многократно, применение возможно в течение не менее 28 дней.
Не допускается смешивание препарата Менопур® Мультидоза с другими лекарственными средствами в одном шприце!
Снимите пластмассовую крышечку с флакона с лиофилизатом. Присоедините иглу для приготовления раствора к шприцу с растворителем и снимите защитный колпачок (Рис. 1,2).
1. Медленно введите растворитель во флакон (Рис. 3).
ФЛАКОН ДЕРЖАТЬ ВЕРТИКАЛЬНО!
2. Круговыми движениями аккуратно перемешайте содержимое флакона до получения прозрачного раствора (Рис. 4). Растворение обычно происходит за 1–2 минуты. Не встряхивать! Не используйте раствор в случае появления нерастворённых частиц или изменения цвета!
3. Наберите необходимое количество раствора в шприц для инъекции (Рис. 5, 6).
4. Протрите место инъекции спиртовой салфеткой, удалите пузырьки воздуха из шприца и введите препарат, как показано на рис. 7.
Общие указания
Следует избегать встряхивания. В случае помутнения или наличия частиц в растворе его использовать нельзя!
Побочное действие
Частота нежелательных реакций (HP): часто (≥1/100 до <1/10), нечасто (≥1/1 000 до <1/100), редко (≥1/10 000 до <1/1 000), частота неизвестна (в настоящее время данные о распространённости HP отсутствуют, зарегистрированы в период пострегистрационного применения препарата).
Наиболее серьезными и частыми HP, выявленными при применении препарата Менопур® Мультидоза в клинических исследованиях с частотой до 5 %, были синдром гиперстимуляции яичников (СГЯ), боль в животе, головная боль, вздутие живота и боль в месте инъекции. Основные HP, выявленные в клинических исследованиях и в ходе пострегистрационного применения, приведены ниже в таблице.
|
Системно-органный класс |
Часто (≥1/100, <1/10) |
Нечасто (≥1/1000, <1/100) |
Редко (≥1/10000, <1/1000) |
Частота неизвестна |
|
Нарушения со стороны иммунной системы |
Реакции гиперчувствительности* |
|||
|
Нарушения со стороны нервной системы |
Головная боль |
Головокружение |
||
|
Нарушения со стороны органа зрения |
Преходящая слепота, диплопия, мидриаз, скотома, фотопсия, преходящее помутнение стекловидного тела, снижение чёткости зрения |
|||
|
Нарушения со стороны сосудов |
Приливы жара |
Венозные и артериальные тромбоэмболии (как правило, при СГЯ) |
||
|
Нарушения со стороны желудочно-кишечного тракта |
Боль в животе, вздутие живота, тошнота, увеличение живота в объёме |
Рвота, дискомфорт в животе, диарея |
||
|
Нарушения со стороны кожи и подкожных тканей |
Угревая сыпь, кожные высыпания |
Кожный зуд, крапивница |
||
|
Нарушения со стороны скелетно- мышечной и соединительной ткани |
Боль в суставах, боль в спине и шее, боль в конечностях |
|||
|
Нарушения со стороны половых органов и молочной железы |
СГЯ**, тазовая боль*** |
Кисты яичников, нарушения со стороны молочных желёз**** |
Перекрут яичника** |
|
|
Общие расстройства и нарушения в месте введения |
Боль в месте инъекции |
Повышенная утомляемость |
Повышение температуры тела, недомогание |
|
|
Лабораторные и инструменталъные данные |
Увеличение массы тела |
Отмечались редкие случаи местных или общих аллергических реакций, в том числе случаи анафилактических реакций.
** В клинических исследованиях отмечались связанные с развитием СГЯ нарушения со стороны желудочно-кишечного тракта, такие как вздутие и дискомфорт в животе, тошнота, рвота и диарея. В случаях тяжёлого СГЯ в качестве редких осложнений возможно развитие асцита и скопление жидкости в полости таза, экссудативного плеврита, одышки, олигурии, тромбоэмболических осложнений и перекрута яичника.
*** Боль в области придатков матки.
**** Боль и дискомфорт в молочных железах, нагрубание и отёчность молочных желёз, боль в сосках.
При применении менотропинов у мужчин были отмечены случаи гинекомастии, акне и увеличения массы тела.
Если любые из указанных в инструкции HP усугубляются, или Вы заметили любые другие HP, не указанные в инструкции, сообщите об этом врачу.
Передозировка
Случаи передозировки при приёме препарата Менопур® Мультидоза неизвестны, однако в таких ситуациях следует ожидать развитие СГЯ.
Подробнее см. раздел “Особые указания”.
Взаимодействие с другими лекарственными средствами
Исследование лекарственных взаимодействий препарата Менопур® Мультидоза не проводилось.
Одновременное применение менотропинов с кломифеном может усилить стимуляцию роста фолликулов, несмотря на отсутствие клинических данных о совместном применении этих препаратов. Совместное применение с агонистами ГнРГ может потребовать увеличения дозы менотропинов для достижения оптимальной реакции яичников.
Препарат не следует смешивать в одном шприце с другими лекарственными средствами!
Особые указания
Препарат Менопур® Мультидоза обладает выраженной гонадотропной активностью, в связи с чем при применении препарата могут развиваться HP разной степени тяжести. Лечение должно проводиться под наблюдением врача, имеющего опыт диагностики и лечения бесплодия!
Применение гонадотропинов требует присутствия квалифицированного медицинского персонала, а также соответствующего оборудования. Перед назначением препарата Менопур® Мультидоза и в процессе лечения следует контролировать состояние яичников (УЗИ и концентрация эстрадиола в плазме крови). Необходимо применять препарат в наиболее низкой эффективной дозе, отвечающей целям лечения.
Первая инъекция препарата должна выполняться под непосредственным наблюдением врача.
Женщины
Перед началом применения препарата Менопур® Мультидоза рекомендуется проведение диагностики причин бесплодия как у женщины, так и у ее партнера, а также установить возможные противопоказания к беременности. Перед началом лечения необходимо провести обследование женщин на наличие гипотиреоза, недостаточности надпочечников, гиперпролактинемии, опухоли гипоталамо-гипофизарной области и при необходимости провести соответствующее лечение.
Проведение контролируемой стимуляции роста фолликулов, вне зависимости от показания к применению у женщин, может привести к увеличению яичников с развитием их гиперстимуляции.
При соблюдении режима дозирования и способа введения препарата в сочетании с мониторингом проводимой терапии, возможно минимизировать риск возникновения вышеуказанных реакций.
Оценка развития фолликула должна проводиться врачом, имеющим соответствующий опыт.
СГЯ
СГЯ — синдром, отличный от неосложнённого увеличения яичников, проявления которого зависят от степени тяжести. Он включает в себя значительное увеличение яичников, высокую концентрацию эстрогенов в плазме крови, а также увеличение проницаемости сосудов, что может привести к накоплению жидкости в брюшной, плевральной и, реже, перикардиальной полости.
В тяжёлых случаях СГЯ возможны следующие симптомы: боль в животе, вздутие живота, значительное увеличение яичников, увеличение массы тела, одышка, олигурия и симптомы со стороны желудочно-кишечного тракта, включая тошноту, рвоту и диарею. При клиническом обследовании возможно выявление гиповолемии, гемоконцентрации, электролитных нарушений, асцита, гемоперитонеума, экссудативного плеврита, гидроторакса, острого респираторного дистресс-синдрома и тромбоэмболических осложнений.
Чрезмерная реакция яичников на введение гонадотропинов редко приводит к развитию СГЯ, если не вводится чХГ с целью стимуляции овуляции. Поэтому в случае гиперстимуляции яичников не следует вводить чХГ, а пациентку следует предупредить о необходимости воздерживаться от половых контактов или использовать барьерные методы контрацепции не менее 4 дней. СГЯ может быстро прогрессировать (в течение от 24 ч до нескольких дней), становясь серьёзным ятрогенным осложнением, поэтому необходимо тщательное наблюдение за пациентками, по крайней мере, в течение не менее 2-х недель после введения чХГ.
Соблюдение рекомендованных доз препарата Менопур» Мультидоза, режима введения и тщательный контроль терапии может свести к минимуму случаи гиперстимуляции яичников и многоплодной беременности. При проведении ВРТ аспирация содержимого всех фолликулов до наступления овуляции может снизить риск развития СГЯ.
СГЯ может быть более тяжёлым и затяжным при развитии беременности. Чаще всего СГЯ развивается после прекращения лечения гонадотропинами и достигает максимума тяжести через 7–10 дней после окончания лечения. Обычно СГЯ проходит спонтанно после начала менструации.
При развитии СГЯ тяжёлой степени лечение прекращают, пациентку госпитализируют и начинают специфическую терапию.
Развитие СГЯ более характерно для пациенток с СПКЯ.
Многоплодная беременность
При многоплодной беременности отмечается повышенный риск неблагоприятных материнских и перинатальных исходов.
При применении менотропинов многоплодная беременность развивается чаще, чем при естественном зачатии. Отмечается наиболее высокая частота рождения двойни. Для уменьшения риска многоплодной беременности рекомендуется тщательный мониторинг ответа яичников на стимуляцию.
В случае проведения ВРТ вероятность возникновения многоплодной беременности зависит от числа введённых эмбрионов, их качества и возраста пациентки.
Пациентка должна быть предупреждена о потенциальном риске многоплодной беременности до начала лечения бесплодия.
Осложнения беременности
Частота самопроизвольных абортов и преждевременных родов при беременности, наступившей после лечения препаратом Менопур® Мультидоза, выше, чем у здоровой женщины.
Эктопическая беременность
У пациенток с заболеваниями маточных труб в анамнезе, как при естественном зачатии, так и при лечении бесплодия, имеется высокий риск возникновения эктопической беременности. Распространённость внематочной беременности после ЭКО составляет от 2 до 5 % по сравнению с 1 до 1,5 % в общей популяции.
Новообразования органов репродуктивной системы
Имеются сообщения о новообразованиях яичников и других органов репродуктивной системы, как доброкачественных, так и злокачественных, у женщин, неоднократно получавших препараты для лечения бесплодия. В настоящее время не установлено, увеличивает ли лечение гонадотропинами исходный риск этих опухолей у женщин с бесплодием.
Врождённые пороки развития
Распространённость врождённых пороков развития плода при использовании ВРТ несколько выше, чем при естественном зачатии. Считается, что это может быть связано с индивидуальными особенностями родителей (возрастом матери, характеристиками спермы) и многоплодной беременностью.
Тромбоэмболические осложнения
Женщины с известными факторами риска развития тромбоэмболических осложнений, таких как индивидуальная или семейная предрасположенность, ожирение (ИМТ > 0 кг/м2) или тромбофилия, могут иметь повышенный риск венозных или артериальных тромбоэмболических осложнений во время или после лечения гонадотропинами. В таких случаях польза их применения должна быть сопоставлена с возможным риском. Следует учитывать, что сама беременность также повышает риск развития тромбоэмболических осложнений.
Мужчины
Применение препарата Менопур® Мультидоза у мужчин с высокой концентрацией ФСГ неэффективно. Для оценки эффективности лечения проводят анализ спермы через 4–6 месяцев после начала лечения.
Влияние на способность управлять транспортными средствами, механизмами
Исследования влияния менотропинов на способность управлять транспортными средствами и механизмами не проводились. Маловероятно, что препарат Менопур® Мультидоза оказывает отрицательное воздействие на способность управлять транспортными средствами и другими механизмами.
Форма выпуска
Лиофилизат для приготовления раствора для подкожного введения.
По 600 ME ФСГ + 600 ME ЛГ или 1200 ME ФСГ + 1200 ME Л Г во флаконы бесцветного стекла типа I, укупоренные бромобутиловой пробкой с алюминиевой обкаткой и крышкой типа «флип-офф».
По 1 мл растворителя в шприцах для одноразового использования бесцветного стекла типа I с резиновым колпачком-наконечником.
600 ME ФСГ + 600 ME ЛГ
1 флакон с лиофилизатом, 1 шприц с растворителем, 1 игла для приготовления раствора в индивидуальной упаковке, 9 шприцев для одноразового использования, градуированных от «0 МЕ» до «600 МЕ» с ценой деления «37,5 МЕ» ФСГ+ЛГ, с иглами в индивидуальных упаковках, с инструкцией по применению в картонную пачку.
1200 МЕ ФСГ + 1200 МЕ ЛГ
1 флакон с лиофилизатом, 2 шприца с растворителем, 1 игла для приготовления раствора в индивидуальной упаковке, 18 шприцев для одноразового использования, градуированных от «0 МЕ» до «600 МЕ» с ценой деления «37,5 МЕ» ФСГ+ЛГ, с иглами в индивидуальных упаковках, с инструкцией по применению в картонную пачку.
Хранение
При температуре 2–8 °C. Не замораживать. Хранить в оригинальной упаковке для защиты от света. Приготовленный раствор хранить не более 28 дней при температуре не выше 25 °C.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности, указанного на упаковке.
Условия отпуска из аптек
Отпускают по рецепту
Производитель
Ferring, GmbH, Германия
Держатель (владелец) регистрационного удостоверения
Ферринг Лечива а.с.,
К Рубнику 475, 25242 Есенице у Прагу, Чешская Республика.
Производитель
Ферринг ГмбХ,
Витланд 11, 24109 Киль, Германия.
Организация, принимающая претензии от потребителей
ООО «Ферринг Фармасетикалз»
115054 г. Москва, Космодамианская наб. 52 стр.4.
Тел.: (495) 287-03-43, Факс: (495) 287-03-42.