Описание препарата Лирика® (капсулы, 150 мг) основано на официальной инструкции, утверждено компанией-производителем в 2014 году
Дата согласования: 30.06.2014
Особые отметки:
Содержание
- Фотографии упаковок
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Аналоги (синонимы) препарата Лирика®
- Заказ в аптеках Москвы
Фотографии упаковок

30.06.2014
Действующее вещество
ATX
Фармакологическая группа
Нозологическая классификация (МКБ-10)
Список кодов МКБ-10
- F41.1 Генерализованное тревожное расстройство
- G40.0 Локализованная (фокальная) (парциальная) идиопатическая эпилепсия и эпилептические синдромы с судорожными припадками с фокальным началом
- G40.1 Локализованная (фокальная) (парциальная) симптоматическая эпилепсия и эпилептические синдромы с простыми парциальными припадками
- G40.2 Локализованная (фокальная) (парциальная) симптоматическая эпилепсия и эпилептические синдромы с комплексными парциальными судорожными припадками
- G62.9 Полинейропатия неуточненная
- M79.1 Миалгия
- R52.2 Другая постоянная боль
Состав
| Капсулы | 1 капс. |
| активное вещество: | |
| прегабалин | 25 мг |
| 75 мг | |
| 150 мг | |
| 300 мг | |
| вспомогательные вещества: лактозы моногидрат — 35/8,25/16,5/33 мг; крахмал кукурузный — 20/8,375/16,75/33,5 мг; тальк — 20/8,375/16,75/33,5 мг | |
| состав капсулы | |
| корпус: титана диоксид (2,4423/2,4423/2,4423/2,4423%), желатин (для всех дозировок — до 100%) | |
| крышечка: краситель железа оксид красный (для дозировки 75 мг — 1,7361%, для дозировки 300 мг — 0,7361%); титана диоксид (2,4423/0,409/2,4423/0,409%); желатин (для всех дозировок — до 100%) | |
| чернила: шеллак (24–27%); этанол (23–26%); изопропанол (0,5–3%); бутанол (0,5–3%); пропиленгликоль (3–7%); аммиака раствор концентрированный (1–2%); калия гидроксид (0,05–0,1%); вода очищенная (15–18%); краситель железа оксид черный (24–28%) |
Описание лекарственной формы
Капсулы, 25 мг: твердые, желатиновые, размер №4, с крышечкой и корпусом белого цвета. Черными чернилами на корпусе капсулы указаны дозировка и код продукта («PGN 25»), на крышечке — «Pfizer».
Капсулы, 75 мг: твердые, желатиновые, размер №4, с крышечкой от красно-коричневого до темно-красно-коричневого* цвета и корпусом белого цвета. Черными чернилами на корпусе капсулы указаны дозировка и код продукта («PGN 75»), на крышечке — «Pfizer».
Капсулы, 150 мг: твердые, желатиновые, размер №2, с крышечкой белого цвета и корпусом белого цвета. Черными чернилами на корпусе капсулы указаны дозировка и код продукта («PGN 150»), на крышечке — «Pfizer».
Капсулы, 300 мг: твердые, желатиновые, размер №0, с крышечкой от красно-коричневого до темно-красно-коричневого цвета* и корпусом белого цвета. Черными чернилами на корпусе капсулы указаны дозировка и код продукта («PGN 300»), на крышечке — «Pfizer».
Содержимое капсулы — порошок от белого до почти белого цвета.
* В оригинальных сертификатах производителя данные цвета описаны как: «от красно-коричневого до темно-красно-коричневого» — «orange»; «от светло-красно-коричневого до красно-коричневого» —«light orange», что соответствует цвету пантонов сравнения, используемых в Европейском Союзе при проведении данного вида анализа
Фармакологическое действие
Фармакологическое действие
—
противоэпилептическое.
Фармакодинамика
Действующим веществом является прегабалин — аналог ГАМК — (S)-3-(аминометил)-5-метилгексановая кислота.
Механизм действия
Было установлено, что прегабалин связывается с дополнительной субъединицей (α-2-дельта-протеин) потенциалзависимых кальциевых каналов в ЦНС, необратимо замещая (3Н)-габапентин. Предполагается, что такое связывание может способствовать проявлению его анальгетического и противосудорожного эффектов.
Нейропатическая боль
Эффективность прегабалина отмечена у больных с диабетической нейропатией и постгерпетической невралгией.
Установлено, что при приеме прегабалина курсами до 13 нед по 2 раза в сутки и до 8 нед по 3 раза в сутки, в целом риск развития побочных эффектов и эффективность препарата при приемах по 2 или по 3 раза в сутки одинаковы.
При приеме курсом продолжительностью до 13 нед боль уменьшалась в течение 1-й нед, а эффект сохранялся до конца лечения.
Отмечалось уменьшение индекса боли на 50% у 35% больных, получавших прегабалин, и 18% больных, принимавших плацебо. Среди пациентов, не испытывавших сонливости, эффект такого снижения боли отмечался у 33% больных группы прегабалина и 18% больных группы плацебо. У 48% пациентов, принимавших прегабалин, и у 16% пациентов, принимавших плацебо, возникала сонливость.
Фибромиалгия
Выраженное снижение болевой симптоматики, связанной с фибромиалгией, отмечается при применении прегабалина в дозах от 300 до 600 мг/сут. Эффективность доз 450 и 600 мг/сут сравнима, однако переносимость 600 мг/сут обычно хуже.
Также применение прегабалина связано с заметным улучшением функциональной активности пациентов и снижением выраженности нарушений сна. Применение прегабалина в дозе 600 мг/сут приводило к более выраженному улучшению сна по сравнению с дозой 300–450 мг/сут.
Эпилепсия
При приеме препарата в течение 12 нед по 2 или 3 раза в сутки отмеченные риск развития побочных эффектов и эффективность препарата одинаковы. Уменьшение частоты судорог начиналось в течение 1-й нед.
Генерализованное тревожное расстройство
Уменьшение симптоматики генерализованного тревожного расстройства отмечается на 1-й нед лечения. При применении препарата в течение 8 нед у 52% пациентов, получавших прегабалин, и у 38% пациентов, получавших плацебо, отмечалось 50% уменьшение симптоматики по шкале тревожности Гамильтона (HAM-A).
Фармакокинетика
Параметры фармакокинетики прегабалина в равновесном состоянии у здоровых добровольцев, больных эпилепсией, получавших противоэпилептическую терапию, и пациентов, получавших его по поводу хронических болевых синдромов, были аналогичны.
Всасывание. Прегабалин быстро всасывается натощак. Tmax препарата в плазме — 1 ч как при однократном, так и повторном применении. Биодоступность прегабалина при приеме внутрь составляет ≥90% и не зависит от дозы. При повторном применении Css достигается через 24–48 ч. При применении препарата после приема пищи Cmax снижается примерно на 25–30%, а Tmax увеличивается приблизительно до 2,5 ч. Однако прием пищи не оказывает клинически значимое влияние на общее всасывание прегабалина.
Распределение. Vd прегабалина после приема внутрь составляет примерно 0,56 л/кг. Препарат не связывается с белками плазмы.
Метаболизм. Прегабалин практически не подвергается метаболизму. После приема меченного прегабалина примерно 98% радиоактивной метки определяется в моче в неизмененном виде. Доля N-метилированного производного прегабалина, который является основным метаболитом, обнаруживаемым в моче, составляет 0,9% от дозы. Не отмечены признаки рацемизации S-энантиомера прегабалина в R-энантиомер.
Выведение. Прегабалин выводится в основном почками в неизмененном виде.
Средний T1/2 составляет 6,3 ч. Клиренс прегабалина из плазмы и почечный клиренс прямо пропорциональны клиренсу креатинина (см. Нарушение функции почек). У больных с нарушенной функцией почек и пациентов, находящихся на гемодиализе, необходима коррекция дозы (см. «Способ применения и дозы», табл. 1).
Линейность/нелинейность. Фармакокинетика прегабалина в диапазоне рекомендуемых суточных доз носит линейный характер, межиндивидуальная вариабельность низкая (<20%). Фармакокинетику препарата при повторном применении можно предсказать на основании данных приема единичной дозы. Следовательно, необходимости в регулярном мониторировании концентрации прегабалина нет.
Особые группы пациентов
Пол. Не оказывает клинически значимое влияние на концентрацию прегабалина в плазме.
Нарушение функции почек. Клиренс прегабалина прямо пропорционален клиренсу креатинина. Учитывая, что препарат в основном выводится почками, у больных с нарушенной функцией почек рекомендуется снизить дозу прегабалина. Кроме того, прегабалин эффективно удаляется из плазмы при гемодиализе (после 4-часового сеанса гемодиализа концентрации прегабалина в плазме снижаются примерно на 50%), после гемодиализа необходимо назначить дополнительную дозу препарата (см. «Способ применения и дозы», табл. 1).
Нарушение функции печени. Фармакокинетика прегабалина у больных с нарушением функции печени специально не изучалась. Прегабалин практически не подвергается метаболизму и выводится в основном в неизмененном виде с мочой, поэтому нарушение функции печени не должно существенно изменять концентрации препарата в плазме.
Пожилые пациенты (старше 65 лет). Клиренс прегабалина с возрастом имеет тенденцию к снижению, что отражает возрастное снижение клиренса креатинина. Пожилым людям с нарушенной функцией почек может потребоваться снижение дозы препарата (см. «Способ применения и дозы», табл. 1).
Показания
- нейропатическая боль у взрослых;
- эпилепсия (в качестве дополнительной терапии у взрослых с парциальными судорожными приступами, сопровождающимися или не сопровождающимися вторичной генерализацией);
- генерализованное тревожное расстройство у взрослых;
- фибромиалгия у взрослых.
Противопоказания
- повышенная чувствительность к действующему веществу или любому другому компоненту препарата;
- редкие наследственные заболевания, в т.ч. непереносимость галактозы, лактазная недостаточность и нарушение всасывания глюкозы/галактозы;
- детский и подростковый возраст до 17 лет включительно (нет данных по применению).
С осторожностью: почечная недостаточность (см. «Способ применения и дозы»); сердечная недостаточность (см. «Побочные действия»); возможное наличие редких наследственных заболеваний (см. «Особые указания»). В связи с зарегистрированными единичными случаями бесконтрольного применения прегабалина, его необходимо назначать с осторожностью у пациентов с лекарственной зависимостью в анамнезе. Такие пациенты нуждаются в пристальном медицинском наблюдении во время лечения препаратом.
Применение при беременности и кормлении грудью
Адекватных данных о применении прегабалина при беременности нет.
В экспериментальных исследованиях на животных препарат оказывал токсическое действие на репродуктивную функцию. В связи с этим прегабалин можно назначать при беременности только в том случае, если предполагаемая польза для матери явно перевешивает возможный риск для плода.
При лечении прегабалином женщины репродуктивного возраста должны пользоваться адекватными методами контрацепции.
Сведений о выведении прегабалина с грудным молоком у женщин нет, однако замечено, что у крыс он выводится с грудным молоком. В связи с этим во время лечения прегабалином не рекомендуется кормить грудью.
Способ применения и дозы
Реклама: ООО «РЛС-Патент», ИНН 5044031277, erid=4CQwVszH9pUkpHxmQQo
Внутрь, независимо от приема пищи, в суточной дозе от 150 до 600 мг в 2 или 3 приема.
Нейропатическая боль: начальная доза — 150 мг/сут. В зависимости от достигнутого эффекта и переносимости, через 3–7 дней дозу можно увеличить до 300 мг/сут, а при необходимости еще через 7 дней — до максимальной дозы 600 мг/сут.
Эпилепсия: начальная доза — 150 мг/сут. С учетом достигнутого эффекта и переносимости, через 1 нед дозу можно увеличить до 300 мг/сут, а еще через неделю — до максимальной дозы 600 мг/сут.
Фибромиалгия: начальная доза — 150 мг/сут. В зависимости от достигнутого эффекта и переносимости, через 3–7 дней дозу можно увеличить до 300 мг/сут. При отсутствии положительного эффекта дозу увеличивают до 450 мг/сут, а при необходимости еще через 7 дней — до максимальной дозы 600 мг/сут.
Генерализованное тревожное расстройство: начальная доза — 150 мг/сут. В зависимости от достигнутого эффекта и переносимости, через 3–7 дней дозу можно увеличить до 300 мг/сут. При отсутствии положительного эффекта дозу увеличивают до 450 мг/сут, а при необходимости еще через 7 дней — до максимальной дозы 600 мг/сут.
Отмена прегабалина
Если лечение пациентов прегабалином необходимо прекратить, рекомендуется делать это постепенно в течение минимум 1 нед.
Особые группы пациентов
Нарушение функции почек. Пациентам с нарушенной функцией почек дозу подбирают индивидуально, с учетом клиренса креатинина (табл. 1), который рассчитывают по следующей формуле:
У больных, получающих лечение гемодиализом, суточную дозу прегабалина подбирают с учетом функции почек. Непосредственно после каждого 4-часового сеанса гемодиализа назначают дополнительную дозу (табл. 1).
Таблица 1
Подбор дозы прегабалина с учетом функции почек
| Cl креатинина, мл/мин | Суточная доза прегабалина | Кратность приема, сут | |
| Стартовая доза, мг/сут | Максимальная доза, мг/сут | ||
| ?60 | 150 | 600 | 2–3 |
| ?30–<60 | 75 | 300 | 2–3 |
| ?15–<30 | 25–50 | 150 | 1–2 |
| <15 | 25 | 75 | 1 |
| Дополнительная доза после диализа, мг | |||
| — | 25 | 100 | Однократно |
Нарушение функции печени. У больных с нарушением функции печени коррекция дозы не требуется (см. «Фармакокинетика»).
Дети до 12 лет и подростки (12–17 лет включительно). Безопасность и эффективность применения прегабалина у детей до 12 лет и подростков 12–17 лет не установлена. Применение препарата у детей не рекомендуется.
Пожилые люди (старше 65 лет). Пациентам пожилого возраста (старше 65 лет) может потребоваться снижение дозы прегабалина в связи со снижением функции почек.
В случае пропуска дозы прегабалина необходимо принять следующую дозу как можно скорее, однако не следует принимать пропущенную дозу, если время приема следующей уже подходит.
Побочные действия
По имеющемуся опыту клинического применения прегабалина более чем у 12000 пациентов, наиболее распространенными нежелательными явлениями были головокружение и сонливость. Наблюдаемые явления были обычно легкими или умеренными. Частота отмены прегабалина и плацебо из-за нежелательных реакций составила 14 и 7% соответственно. Основными нежелательными эффектами, требовавшими прекращения лечения, были головокружение (4%) и сонливость (3%), в зависимости от их субъективной переносимости.
Другие побочные эффекты, также приводящие к отмене препарата, — атаксия, спутанность сознания, астения, нарушение внимания, нечеткость зрения, нарушение координации, периферические отеки.
Ниже перечислены все нежелательные явления, частота которых превышала таковую в группе плацебо (наблюдавшиеся более чем у 1 человека). Они распределены по системно-органным классам и частоте: очень часто — ≥1/10; часто — ≥1/100, <1/10; нечасто — ≥1/1000, <1/100; редко — <1/1000.
Перечисленные нежелательные явления могли быть связаны с основным заболеванием и/или сопутствующей терапией.
Инфекции и инвазии: нечасто — назофарингит.
Со стороны системы крови и лимфатической системы: редко — нейтропения.
Нарушения метаболизма и питания: часто — повышение аппетита; нечасто — анорексия, гипогликемия.
Психические расстройства: часто — эйфория, спутанность сознания, снижение/увеличение либидо, раздражительность, усиление бессонницы/бессонница, дезориентация; нечасто — деперсонализация, аноргазмия, беспокойство, депрессия, ажитация, лабильность настроения, подавленное настроение, трудности в подборе слов, галлюцинации, необычные сновидения, панические атаки, апатия; редко — расторможенность, приподнятое настроение.
Неврологические расстройства: очень часто — головокружение, сонливость; часто — атаксия, нарушение внимания, нарушение координации, ухудшение памяти, тремор, дизартрия, парестезия, нарушение равновесия, амнезия, седация, летаргия; нечасто — когнитивные расстройства, гипестезия, нистагм, нарушение речи, миоклонические судороги, ослабление рефлексов, дискинезия, психомоторное возбуждение, постуральное головокружение, гиперестезия, потеря вкусовых ощущений, ощущение жжения на слизистых оболочках и коже, интенционный тремор, ступор, обморок; редко — гипокинезия, паросмия, дисграфия.
Со стороны органа зрения: часто — нечеткость зрения, диплопия; нечасто — сужение полей зрения, снижение остроты зрения, боль в глазах, астенопия, а также сухость в глазах, отечность глаз, повышенное слезотечение; редко — мелькание искр перед глазами, раздражение глаз, мидриаз, осциллопсия (субъективное ощущение колебания рассматриваемых предметов), нарушение восприятия зрительной глубины, утрата периферического зрения, косоглазие, усиление яркости зрительного восприятия.
Со стороны органа слуха и вестибулярного аппарата: часто — вертиго; нечасто — гиперакузия.
Со стороны ССС: нечасто — тахикардия, AV блокада I степени, приливы крови к лицу, снижение АД, похолодание конечностей, повышение АД, гиперемия кожи; редко — синусовая тахикардия, синусовая аритмия, синусовая брадикардия.
Со стороны дыхательной системы: нечасто — одышка, кашель, сухость слизистой оболочки носа; редко — заложенность носа, кровотечение из носа, ринит, храп, чувство стеснения в глотке.
Со стороны пищеварительной системы: часто — сухость во рту, запор, рвота, метеоризм, вздутие живота; нечасто — повышенное слюноотделение, гастроэзофагеальный рефлюкс, гипестезия слизистой оболочки полости рта; редко — асцит, дисфагия, панкреатит.
Со стороны кожных покровов: нечасто — потливость, папулезная сыпь; редко — холодный пот, крапивница.
Со стороны опорно-двигательного аппарата: нечасто — подергивания мышц, припухлость суставов, мышечные спазмы, миалгия, артралгия, боль в спине, боль в конечностях, скованность в мышцах; редко — спазм шейных мышц, боль в шее, рабдомиолиз.
Со стороны мочевыделительной системы: нечасто — дизурия, недержание мочи; редко — олигурия, почечная недостаточность.
Со стороны репродуктивной системы: часто — эректильная дисфункция; нечасто — задержка эякуляции, сексуальная дисфункция; редко — аменорея, боль в грудных железах, выделения из молочных желез, дисменорея, увеличение молочных желез в объеме.
Прочие: часто — утомляемость, отеки, в т.ч. периферические, чувство опьянения, нарушение походки; нечасто — астения, падения, жажда, чувство стеснения в груди, генерализованные отеки, озноб, боль, патологические ощущения; редко — гипертермия.
Лабораторные показатели и инструментальные данные: часто — увеличение массы тела; нечасто — повышение активности АЛТ, КФК, АСТ, снижение числа тромбоцитов; редко — повышение концентрации глюкозы и креатинина крови, снижение концентрации калия крови, снижение массы тела, снижение числа лейкоцитов в крови.
Эффекты, отмеченные при постмаркетинговом наблюдении (частота неизвестна)
Неврологические расстройства: головная боль, потеря сознания, когнитивные нарушения, судороги.
Со стороны пищеварительной системы: редкие случаи отека языка, тошнота, диарея.
Со стороны кожных покровов: редкие случаи отека лица, зуд, синдром Стивенса-Джонсона.
Со стороны органа зрения: кератит, потеря зрения.
Со стороны иммунной системы: ангионевротический отек, аллергические реакции, гиперчувствительность.
Со стороны ССС: ХСН, удлинение интервала QT.
Со стороны мочевыделительной системы: задержка мочи.
Со стороны дыхательной системы: отек легких.
Со стороны репродуктивной системы: гинекомастия.
Прочие: повышенная утомляемость.
Взаимодействие
Реклама: ООО «ВЕДАНТА», ИНН 7714886235, erid 4CQwVszH9pUkKJ7jUDd
Реклама: ООО «РЛС-Библиомед» ИНН 7714758963
Реклама: ООО «ВЕДАНТА», ИНН 7714886235, erid 4CQwVszH9pUkKJ7jUDd
Реклама: ООО «РЛС-Библиомед» ИНН 7714758963
Прегабалин выводится с мочой, в основном в неизмененном виде, подвергается минимальному метаболизму у человека (в виде метаболитов с мочой выводится менее 2% дозы), не ингибирует метаболизм других лекарственных веществ in vitro и не связывается с белками плазмы, поэтому он вряд ли способен вступать в фармакокинетическое взаимодействие.
Не обнаружены признаки клинически значимого фармакокинетического взаимодействия прегабалина с фенитоином, карбамазепином, вальпроевой кислотой, ламотриджином, габапентином, лоразепамом, оксикодоном или этанолом. Установлено, что пероральные гипогликемические препараты, диуретики, инсулин, фенобарбитал, тиагабин и топирамат не оказывают клинически значимое влияние на клиренс прегабалина.
При применении пероральных контрацептивов, содержащих норэтистерон и/или этинилэстрадиол, одновременно с прегабалином равновесная фармакокинетика препаратов не менялась.
Сообщалось о случаях нарушения дыхания и наступления комы при одновременном применении прегабалина с другими препаратами, угнетающими ЦНС. Также сообщалось об отрицательном влиянии прегабалина на деятельность ЖКТ (в т.ч. развитие кишечной непроходимости, паралитического илеуса, запора) при одновременном применении с ЛС, вызывающими запор (такими как ненаркотические анальгетики).
Повторное пероральное применение прегабалина с оксикодоном, лоразепамом или этанолом не оказывало клинически значимое влияние на дыхание. Прегабалин, по-видимому, усиливает нарушения когнитивной и двигательной функций, вызванные оксикодоном. Прегабалин может усилить эффекты этанола и лоразепама.
Передозировка
При передозировке препарата (до 15 г) каких-либо из неописанных выше нежелательных реакций зарегистрировано не было. В ходе постмаркетингового применения наиболее частыми нежелательными явлениями, развивавшимися при передозировке прегабалина, являлись: аффективные расстройства, сонливость, спутанность сознания, депрессия, ажитация и беспокойство.
Лечение: проводят промывание желудка, поддерживающую терапию и при необходимости — гемодиализ (см. «Способ применения и дозы», табл. 1).
Особые указания
У части больных сахарным диабетом в случае прибавки массы тела на фоне лечения прегабалином может потребоваться коррекция доз гипогликемических средств.
Прегабалин необходимо отменить в случае развития симптомов ангионевротического отека (таких как отек лица, периоральный отек или отечность тканей верхних дыхательных путей).
Противоэпилептические препараты, включая прегабалин, могут повышать риск возникновения суицидальных мыслей или поведения. Поэтому пациентов, получающих эти препараты, следует тщательно наблюдать на предмет возникновения или ухудшения депрессии, появления суицидальных мыслей или поведения.
Лечение прегабалином сопровождалось головокружением и сонливостью, которые повышают риск случайных травм (падений) у пожилых людей. В ходе постмаркетингового применения препарата отмечались также случаи потери сознания, спутанности сознания и нарушения когнитивных функций. Поэтому до тех пор, пока больные не оценят возможные эффекты препарата, они должны соблюдать осторожность.
Сведения о возможности отмены других противосудорожных средств при подавлении судорог прегабалином и целесообразности монотерапии этим препаратом недостаточны.
Имеются сообщения о развитии судорог, в т.ч. эпилептического статуса и малых припадков, на фоне применения прегабалина или сразу после окончания терапии.
При появлении в ответ на применение прегабалина таких нежелательных реакций, как нечеткость зрения или других нарушений со стороны органа зрения, отмена препарата может привести к исчезновению указанных симптомов.
Также отмечались случаи развития почечной недостаточности, в некоторых случаях после отмены прегабалина функция почек восстанавливалась.
В результате отмены прегабалина после длительной или краткосрочной терапии наблюдались следующие нежелательные явления: бессонница, головная боль, тошнота, диарея, гриппоподобный синдром, депрессия, потливость, головокружение, судороги и тревога. Сведения о частоте и выраженности проявлений синдрома отмены прегабалина в зависимости от длительности терапии последним и его дозы не имеется.
Нет данных о том, что прегабалин активен в отношении рецепторов, связанных с развитием злоупотребления препарата пациентами. Во время постмаркетинговых исследований отмечались случаи злоупотребления прегабалином. Как и при применении любого ЛС, влияющего на ЦНС, следует тщательно оценить анамнез пациента на предмет имеющихся случаев злоупотребления ЛС, а также наблюдать пациента в связи с возможностью злоупотребления прегабалином.
Имеются сообщения о случаях развития зависимости при применении прегабалина. Пациенты с лекарственной зависимостью в анамнезе нуждаются в тщательном медицинском наблюдении на предмет симптомов зависимости от прегабалина.
В ходе постмаркетингового применения препарата сообщалось о развитии ХСН на фоне терапии прегабалином у некоторых пациентов. Эти реакции преимущественно наблюдались у больных пожилого возраста, страдавших нарушениями функции сердца и получавших препарат по поводу нейропатии. Поэтому прегабалин у данной категории пациентов должен использоваться с осторожностью. После отмены прегабалина возможно исчезновение проявлений подобных реакций.
Частота нежелательных явлений со стороны ЦНС, особенно таких, как сонливость, повышается при лечении центральной нейропатической боли, обусловленной поражением спинного мозга, что, однако, может быть следствием суммации эффектов прегабалина и других параллельно принимаемых средств (например антиспастические). Это обстоятельство следует принимать во внимание при назначении прегабалина по данному показанию.
Отмечались случаи энцефалопатии, особенно у пациентов с сопутствующими заболеваниями, которые могут привести к развитию данного состояния.
Влияние на способность управлять транспортными средствами и работать с механизмами. Прегабалин может вызвать головокружение и сонливость и, соответственно, повлиять на способность управлять автомобилем и пользоваться сложной техникой. Больные не должны управлять автомобилем, пользоваться сложной техникой или выполнять другие потенциально опасные виды деятельности, пока не станет ясно, влияет ли этот препарат на выполнение ими таких задач.
Форма выпуска
Капсулы, 25 мг, 75 мг, 150 мг или 300 мг. В блистере из ПВХ и алюминиевой фольги, 10, 14 или 21 шт. 1 или 4 блистера по 14 шт., 4 блистера по 21 шт. или 10 блистеров по 10 шт. в картонной пачке.
Производитель
Пфайзер Мэньюфэкчеринг Дойчланд ГмбХ.
Моосвальдаллее, 1, 79090 Фрайбург, Германия.
Владелец регистрационного удостоверения: Пфайзер Инк. 235, Ист 42-я Стрит, Нью-Йорк, штат Нью-Йорк, 10017, США.
Претензии потребителей направлять по адресу представительства корпорации «Пфайзер Эйч. Си. Пи. Корпорэйшн», США.
Москва, 123317, Пресненская наб., 10, комплекс «Башня на набережной», блок С.
Тел.: (495) 258-55-35, факс: (495) 258-55-38.
Условия отпуска из аптек
По рецепту.
Условия хранения
При температуре не выше 25 °C.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности, указанного на упаковке.
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
По имеющемуся опыту клинического применения прегабалина более чем у 12000 пациентов, наиболее распространенными нежелательными явлениями были головокружение и сонливость. Наблюдаемые явления были обычно легкими или умеренными. Частота отмены прегабалина и плацебо из-за нежелательных реакций составила 14 и 7% соответственно. Основными нежелательными эффектами, требовавшими прекращения лечения, были головокружение (4%) и сонливость (3%), в зависимости от их субъективной переносимости.
Другие побочные эффекты, также приводящие к отмене препарата — атаксия, спутанность сознания, астения, нарушение внимания, нечеткость зрения, нарушение координации, периферические отеки.
Ниже перечислены все нежелательные явления, частота которых превышала таковую в группе плацебо (наблюдавшиеся более чем у 1 человека). Они распределены по системам и частоте (очень часто — ≥1/10; часто — ≥1/100, <1/10; нечасто — ≥1/1000, <1/100; редко — <1/1000).
Перечисленные нежелательные явления могли быть связаны с основным заболеванием и/или сопутствующей терапией.
Инфекции и инвазии: нечасто — назофарингит.
Со стороны системы крови и лимфатической системы: редко — нейтропения.
Нарушения метаболизма и питания: часто — повышение аппетита; нечасто — анорексия, гипогликемия.
Психические расстройства: часто — эйфория, спутанность сознания, снижение/увеличение либидо, раздражительность, усиление бессонницы /бессонница, дезориентация; нечасто — деперсонализация, аноргазмия, беспокойство, депрессия, ажитация, лабильность настроения, подавленное настроение, трудности в подборе слов, галлюцинации, необычные сновидения, панические атаки, апатия; редко — расторможенность, приподнятое настроение.
Неврологические расстройства: очень часто — головокружение, сонливость; часто — атаксия, нарушение внимания, нарушение координации, ухудшение памяти, тремор, дизартрия, парестезия, нарушение равновесия, амнезия, седация, летаргия; нечасто — когнитивные расстройства, гипестезия, нистагм, нарушение речи, миоклонические судороги, ослабление рефлексов, дискинезия, психомоторное возбуждение, постуральное головокружение, гиперестезия, потеря вкусовых ощущений, ощущение жжения на слизистых оболочках и коже, интенционный тремор, ступор, обморок; редко — гипокинезия, паросмия, дисграфия.
Изменения со стороны органа зрения: часто — нечеткость зрения, диплопия; нечасто — сужение полей зрения, снижение остроты зрения, боль в глазах, астенопия, а также сухость в глазах, отечность глаз, повышенное слезотечение; редко — мелькание искр перед глазами, раздражение глаз, мидриаз, осциллопсия (субъективное ощущение колебания рассматриваемых предметов), нарушение восприятия зрительной глубины, утрата периферического зрения, косоглазие, усиление яркости зрительного восприятия.
Изменения со стороны органа слуха и вестибулярного аппарата: часто — вертиго; нечасто — гиперакузия.
Со стороны ССС: нечасто — тахикардия, AV блокада I степени, приливы крови к лицу, снижение АД, похолодание конечностей, повышение АД, гиперемия кожи; редко — синусовая тахикардия, синусовая аритмия, синусовая брадикардия.
Со стороны дыхательной системы: нечасто — одышка, кашель, сухость слизистой оболочки носа; редко — заложенность носа, кровотечение из носа, ринит, храп, чувство стеснения в глотке.
Со стороны пищеварительной системы: часто — сухость во рту, запор, рвота, метеоризм, вздутие живота; нечасто — повышенное слюноотделение, гастроэзофагеальный рефлюкс, гипестезия слизистой оболочки полости рта; редко — асцит, дисфагия, панкреатит.
Со стороны кожных покровов: нечасто — потливость, папулезная сыпь; редко — холодный пот, крапивница.
Со стороны опорно-двигательного аппарата: нечасто — подергивания мышц, припухлость суставов, мышечные спазмы, миалгия, артралгия, боль в спине, боль в конечностях, скованность в мышцах; редко — спазм шейных мышц, боль в шее, рабдомиолиз.
Со стороны мочевыделительной системы: нечасто — дизурия, недержание мочи; редко — олигурия, почечная недостаточность.
Со стороны репродуктивной системы: часто — эректильная дисфункция; нечасто — задержка эякуляции, сексуальная дисфункция; редко — аменорея, боль в грудных железах, выделения из молочных желез, дисменорея, увеличение молочных желез в объеме.
Прочие: часто — утомляемость, отеки, в т.ч. периферические, чувство опьянения, нарушение походки; нечасто — астения, падения, жажда, чувство стеснения в груди, генерализованные отеки, озноб, боль, патологические ощущения; редко — гипертермия.
Лабораторные показатели и инструментальные данные: часто — увеличение массы тела; нечасто — повышение активности АЛТ, креатинфосфокиназы, АСТ, снижение числа тромбоцитов; редко — повышение концентрации глюкозы и креатинина крови, снижение концентрации калия крови, снижение массы тела, снижение числа лейкоцитов в крови.
Эффекты, отмеченные при постмаркетинговом наблюдении (частота неизвестна)
Неврологические расстройства: головная боль, потеря сознания, когнитивные нарушения, судороги.
Со стороны пищеварительной системы: редкие случаи отека языка, тошнота, диарея.
Со стороны кожных покровов: редкие случаи отека лица, зуд, синдром Стивенса-Джонсона.
Изменения со стороны органа зрения: кератит, потеря зрения.
Изменения со стороны иммунной системы: ангионевротический отек, аллергические реакции, гиперчувствительность.
Со стороны ССС: хроническая сердечная недостаточность, удлинение интервала QT.
Со стороны мочевыделительной системы: задержка мочи.
Со стороны дыхательной системы: отек легких.
Со стороны репродуктивной системы: гинекомастия.
Прочие: повышенная утомляемость.
Лирика® (75 мг)
МНН: Прегабалин
Анатомо-терапевтическо-химическая классификация: Pregabalin
Номер регистрации в РК:
№ РК-ЛС-5№011792
Информация о регистрации в РК:
02.05.2018 — 02.05.2023
Информация о реестрах и регистрах
Информация по ценам и ограничения
Предельная цена закупа в РК:
60.18 KZT
- Скачать инструкцию медикамента
Торговое название
Лирика®
Международное непатентованное название
Прегабалин
Лекарственная форма
Капсулы 75 мг, 150 мг, 300 мг
Состав
Одна капсула содержит:
активное вещество — прегабалин 75 мг, 150 мг, 300 мг,
вспомогательные вещества: лактозы моногидрат, крахмал кукурузный, тальк,
состав оболочки: желатин, титана диоксид Е 171, железа оксид красный Е 172, натрия лаурилсульфат, кремния диоксид коллоидный безводный,
состав черных чернил SW-9008/-9009: шеллак, железа оксид черный Е 172, пропиленгликоль, калия гидроксид.
Описание
Твердые желатиновые капсулы № 2 с корпусом и крышечкой белого цвета (для дозировки 150 мг) или капсулы № 4 и № 0 с корпусом белого цвета и крышечкой рыжевато-красного цвета (для дозировок 75 мг и 300 мг, соответственно).
На корпусах капсул черными чернилами указаны: дозировка и код продукта «PGN 75» (для дозировки 75 мг), «PGN 150» (для дозировки 150 мг), «PGN 300» (для дозировки 300 мг), на крышечках – «Pfizer».
Содержимое капсул – белый или почти белый порошок.
Фармакотерапевтическая группа
Противоэпилептические препараты другие. Прегабалин.
Код АТХ N03AX16
Фармакологические свойства
Фармакокинетика
Фармакокинетические показатели прегабалина в равновесном состоянии аналогичны у здоровых добровольцев, у пациентов с эпилепсией, принимающих противоэпилептические препараты, и у пациентов с хронической болью.
Всасывание
Прегабалин быстро всасывается натощак. Концентрация препарата в плазме крови достигает пика через один час как при однократном, так и многократном применении. Биодоступность прегабалина при приеме внутрь составляет
> 90 % и не зависит от принятой дозы. При повторном применении равновесное состояние достигается в течение 24-48 часов. Прием пищи ухудшает всасывание прегабалина. При этом Сmax снижается примерно на 25-30 %, а время достижения максимальной концентрации (tmax) увеличивается приблизительно до 2,5 ч. Однако, применение прегабалина с пищей не оказывает клинически значимого влияния на степень его всасывания.
Распределение
Объем распределения прегабалина после приема внутрь составляет примерно 0,56 л/кг. Препарат не связывается с белками плазмы крови.
Метаболизм
Прегабалин подвергается незначительному метаболизму. После приема дозы меченного радиоактивной меткой прегабалина приблизительно 98 % радиоактивного вещества, обнаруженного в моче, представляло собой неизмененный прегабалин. На долю N‑метилированного производного прегабалина, которое является основным метаболитом прегабалина, обнаруживаемым в моче, приходилось 0,9 % от принятой дозы препарата.
Выведение
Прегабалин выводится из системного кровотока преимущественно почками в неизмененном виде.
Средний период полувыведения прегабалина составляет 6,3 часа. Плазменный и почечный клиренс прегабалина прямо пропорциональны клиренсу креатинина.
Линейность/нелинейность
Фармакокинетика прегабалина в рекомендуемом диапазоне суточных доз имеет линейный характер. Межиндивидуальная вариабельность фармакокинетики прегабалина низкая (< 20 %). Фармакокинетику препарата при многократном приеме можно предсказать исходя из его фармакокинетики при однократном приеме. Поэтому необходимость в рутинном мониторинге концентрации прегабалина в плазме крови отсутствует.
Пол
Клинические исследования показывают, что пол не имеет клинически значимого влияния на концентрацию прегабалина в плазме.
Нарушение функции почек
Клиренс прегабалина прямо пропорционален клиренсу креатинина. Кроме того, прегабалин эффективно выводится из плазмы крови при гемодиализе (после 4 часов гемодиализа концентрация прегабалина в плазме крови уменьшается приблизительно на 50 %). Так как основным путем элиминации является выведение почками, у пациентов с нарушением функции почек требуется уменьшение дозы, а после гемодиализа необходим прием дополнительных доз.
Нарушение функции печени
Специальные фармакокинетические исследования у пациентов с нарушением функции печени не проводились. Поскольку прегабалин не подвергается значительному метаболизму и выделяется с мочой преимущественно в неизмененном виде, ожидается, что нарушение функции печени не будет значительно влиять на концентрацию прегабалина в плазме крови.
Пациенты детского возраста
Фармакокинетика прегабалина оценивалась у пациентов детского возраста с эпилепсией (возрастные группы: от 1 до 23 месяцев, от 2 до 6 лет, от 7 до 11 лет и от 12 до 16 лет) при уровне доз 2,5; 5; 10 и 15 мг/кг/сутки в исследовании фармакокинетики и переносимости.
После перорального приема прегабалина натощак пациентами детского возраста, как правило, время до достижения максимальной концентрации в плазме крови было аналогичным для всех возрастных групп и составляло от 0,5 до 2 часов после применения дозы.
Значения параметров Cmax и AUC увеличивались линейно при увеличении дозы в каждой возрастной группе. Значение AUC у пациентов детского возраста с массой тела до 30 кг было меньше на 30 % по причине увеличенного на 43 % скорректированного по массе тела клиренса у этих пациентов по сравнению с пациентами с массой тела ≥ 30 кг.
У пациентов детского возраста в возрасте до 6 лет терминальный период полувыведения прегабалина в среднем составлял от 3 до 4 часов, а у детей в возрасте 7 лет и старше — от 4 до 6 часов.
Популяционный фармакокинетический анализ продемонстрировал, что клиренс креатинина был значимой ковариатой клиренса прегабалина при пероральном приеме, масса тела была значимой ковариатой кажущегося объема распределения прегабалина при пероральном приеме, и эти зависимости были аналогичными для популяции пациентов детского возраста и популяции взрослых пациентов.
Фармакокинетика прегабалина у пациентов в возрасте младше 3 месяцев не изучалась.
Пациенты пожилого возраста (старше 65 лет)
Клиренс прегабалина имеет тенденцию к снижению в более пожилом возрасте. Это снижение клиренса при пероральном приеме прегабалина сопоставимо со снижением клиренса креатинина, что связано с более пожилым возрастом. Пациентам с возрастными нарушениями почечной функции может понадобиться снижение дозы прегабалина.
Кормящие женщины
Фармакокинетику прегабалина в дозе 150 мг каждые 12 часов (суточная доза 300 мг) оценивали у лактирующих женщин спустя по крайней мере 12 недель после родов. Лактация не оказывала влияния на фармакокинетику прегабалина или оказывала незначительное влияние. Прегабалин выделялся в грудное молоко со средним значением равновесных концентраций примерно 76 % от значений равновесных концентраций в плазме крови матери. Теоретическая средняя суточная доза прегабалина, поступающая ребенку с грудным молоком (предполагаемое среднее потребление молока: 150 мл/кг/сутки) женщин, принимающих 300 мг/сутки или максимальную дозу 600 мг/сутки, составляет от 0,31 до 0,62 мг/кг/сутки соответственно. Эти расчетные дозы составляют приблизительно 7 % от общей суточной дозы для матери из расчета в мг/кг массы тела.
Фармакодинамика
Действующим веществом препарата Лирика® является прегабалин — аналог гамма-аминомасляной кислоты ((S)-3-(аминометил)-5-метилгексановая кислота).
Механизм действия
Прегабалин связывается с дополнительной субъединицей (α2-дельта-белок) потенциал-зависимых кальциевых каналов в центральной нервной системе.
Показания к применению
-
лечение периферической и центральной нейропатической боли у взрослых
-
эпилепсия у взрослых с парциальными судорогами со вторичной генерализацией или без нее (в качестве вспомогательного средства)
-
лечение генерализованного тревожного расстройства у взрослых
Способ применения и дозы
Препарат применяют внутрь в дозе от 150 до 600 мг в сутки в два или три приема.
Препарат можно принимать независимо от приема пищи.
Нейропатическая боль
Лечение начинают с дозы 150 мг в сутки, разделенной на два или три приема. В зависимости от индивидуального ответа пациента и переносимости через 3-7 дней дозу можно увеличить до 300 мг в сутки, а при необходимости еще через 7 дней — до максимальной дозы 600 мг в сутки.
Эпилепсия
Лечение начинают с дозы 150 мг в сутки, разделенной на два или три приема. В зависимости от индивидуального ответа пациента и переносимости препарата через одну неделю дозу можно увеличить до 300 мг в сутки, а еще через одну неделю – до максимальной дозы 600 мг в сутки.
Генерализованные тревожные расстройства
Препарат применяют в дозе от 150 до 600 мг в сутки в два или три приема. Необходимость лечения должна пересматриваться регулярно.
Лечение начинают с дозы 150 мг в сутки. В зависимости от индивидуального ответа пациента и переносимости препарата через одну неделю дозу можно увеличить до 300 мг в сутки, еще через одну неделю дозу можно увеличить до 450 мг в сутки, а еще через неделю — до максимальной дозы 600 мг в сутки.
Отмена прегабалина
Если лечение необходимо прекратить, рекомендуется делать это постепенно в течение минимум одной недели, независимо от показания к применению.
Пациенты с нарушением функции почек
Прегабалин выводится из системного кровотока преимущественно почками в неизмененном виде. Поскольку клиренс прегабалина прямо пропорционален клиренсу креатинина, снижение дозы у пациентов с нарушением функции почек должно осуществляться в индивидуальном порядке по клиренсу креатинина (КлКр), как указано в таблице 1, и определяться по следующей формуле:
1,23 х [140 – возраст (лет)] х масса тела (кг)
(х 0,85 для женщин)
К
Сывороточный креатинин (мкмоль/л)
лКр (мл/мин) =
Прегабалин эффективно удаляется из плазмы крови с помощью гемодиализа (50 % препарата через 4 часа). У пациентов, получающих гемодиализ, суточную дозу препарата подбирают с учетом функции почек. В дополнение к суточной дозе препарата через каждые 4 часа гемодиализа назначают дополнительную дозу (см. табл. 1).
Таблица 1. Коррекция дозы прегабалина в зависимости от функции почек
|
Клиренс креатинина (мл/мин) |
Общая суточная доза прегабалина1 |
Режим дозирования |
|
|
Начальная доза (мг/сут.) |
Максимальная доза (мг/сут.) |
||
|
> 60 |
150 |
600 |
2 р./сут. или 3 р./сут. сутки |
|
от > 30 до < 60 |
75 |
300 |
2 р./сут. или 3 р./сут. |
|
от >15 до < 30 |
25-50 |
150 |
1 р./сут. или 2 р./сут. |
|
< 15 |
25 |
75 |
1 р./сут. |
|
Дополнительная доза после гемодиализа (мг) |
|||
|
25 |
100 |
Однократно2 |
1 Общая суточная доза (мг/сут.) должна быть разделена в соответствии с режимом дозирования для получения требуемого значения мг/дозу
2 Дополнительная доза — это разовая добавочная доза
Пациенты с нарушением функции печени
У пациентов с нарушением функции печени коррекции дозы не требуется.
Пациенты детского и подросткового возраста
Безопасность и эффективность препарата Лирика® у детей младше 12 лет и подростков (в возрасте 12-17 лет) не установлены. Имеющиеся данные приводятся в разделах «Побочные действия», «Фармакологические свойства», но дать по ним рекомендации по дозированию невозможно.
Пациенты пожилого возраста (старше 65 лет)
Пациентам пожилого возраста может потребоваться снижение дозы препарата в связи со снижением функции почек.
Побочные действия
При применении Лирики® зарегистрированы нежелательные эффекты, которые были классифицированы по частоте их проявления следующим образом: очень часто (≥ 1/10), часто (от ≥ 1/100 до < 1/10), нечасто (от ≥ 1/1000 до < 1/100) и редко (≥ 1/10 000 и < 1/1000) и неизвестно (невозможно определить по имеющимся данным).
Очень часто
— головокружение, головная боль, сонливость
Часто
— назофарингит
— повышение аппетита
— эйфория, спутанность сознания, раздражительность, дезориентация, бессонница, снижение либидо
— атаксия, нарушение координации, тремор, дизартрия, амнезия, ухудшение памяти, нарушение внимания, парестезия, гипестезия, седативный эффект, нарушение равновесия, заторможенность
— нечеткость зрения, диплопия
— вертиго
— сухость во рту, тошнота*, рвота, метеоризм, вздутие живота, запор, диарея*
— эректильная дисфункция
— повышенная утомляемость, периферический отек, отек, нарушение походки, падение, чувство опьянения, плохое самочувствие
— повышение массы тела
— мышечные судороги, артралгия, боль в спине, боль в конечностях, спазм мышц шейного отдела позвоночника
Нечасто
— нейтропения
— гиперчувствительность*
— анорексия, гипогликемия
— галлюцинации, приступ паники, беспокойство, тревожное возбуждение, депрессия, депрессивное настроение, приподнятое настроение, агрессия*, перемены в настроении, деперсонализация, затруднения с подбором слов, необычные сновидения, повышение либидо, аноргазмия, апатия
— обморок, ступор, миоклонус, потеря сознания*, психомоторная гиперактивность, дискинезия, постуральное головокружение, интенционный тремор, нистагм, когнитивное расстройство, психическое расстройство*, расстройство речи, гипорефлексия, гиперестезия, ощущение жжения, агевзия, недомогание*
— потеря периферического зрения, нарушение зрения, опухание глаза, дефект полей зрения, снижение остроты зрения, боль в глазах, астенопия, фотопсия, синдром сухого глаза, повышенное слезоотделение, раздражение глаз
— гиперакузия
— тахикардия, атриовентрикулярная блокада I степени, синусовая брадикардия, хроническая сердечная недостаточность*
— гипотензия, гипертензия, приливы жара, гиперемия, холодные руки и ноги
— одышка, носовое кровотечение, кашель, заложенность носа, ринит, храп, сухость слизистой носа
— гастроэзофагеальная рефлюксная болезнь, повышенное слюноотделение, оральная гипестезия
— папулезная сыпь, крапивница, гипергидроз, зуд*
— опухание суставов, миалгия, мышечные судороги, боль в шее, ригидность мышц
— недержание мочи, дизурия
— сексуальная дисфункция, задержка эякуляции, дисменорея, боль в молочных железах
— генерализованный отек, отек лица*, чувство стеснения в груди, боль, пирексия, жажда, озноб, астения
— повышение уровня креатинфосфокиназы крови, повышение уровня аланинаминотрансферазы, повышение уровня аспартатаминотрансферазы, повышение уровня глюкозы крови, снижение количества тромбоцитов, повышение уровня креатинина в крови, гипокалиемия, снижение массы тела
Редко
— ангионевротический отек*, аллергическая реакция*
— расторможенность
— судороги*, паросмия, гипокинезия, дисграфия
— потеря зрения*, кератит*, осциллопсия, изменение глубины зрительного восприятия, мидриаз, косоглазие, яркость зрительного восприятия
— удлинение интервала QT*, синусовая тахикардия, синусовая аритмия
— чувство стеснения в горле, отек легких*
— припухлость языка*, дисфагия, асцит, панкреатит
— синдром Стивенса-Джонсона*, холодный пот
— рабдомиолиз
— олигурия, задержка мочи*, почечная недостаточность
-
аменорея, увеличение молочных желез, выделения из молочных желез, гинекомастия*
— снижение количества лейкоцитов
* Дополнительные реакции, зарегистрированные во время пострегистрационного исследования препарата
Пациенты детского возраста
Профиль безопасности прегабалина, наблюдаемый в исследованиях у пациентов детского возраста, был аналогичен таковому у взрослых пациентов.
Сообщение сведений о предполагаемых нежелательных реакциях
Сообщение сведений о предполагаемых нежелательных реакциях, выявленных после регистрации лекарственного препарата, имеет большое значение. Это позволяет продолжать мониторинг соотношения пользы и риска лекарственного препарата.
Медицинских работников и пациентов просят сообщать о любых нежелательных реакциях по адресу, указанному в конце данной инструкции по медицинскому применению.
Противопоказания
— гиперчувствительность к активному веществу или к любому из вспомогательных веществ препарата
— детский и подростковый возраст до 18 лет
— беременность и период лактации
Лекарственные взаимодействия
Поскольку у человека прегабалин преимущественно выводится в неизмененном виде с мочой, подвергается незначительному метаболизму (< 2 % дозы выводится с мочой в виде метаболитов), не ингибирует in vitro метаболизм других препаратов и не связывается с белками плазмы крови, его фармакокинетическое взаимодействие с другими лекарственными препаратами маловероятно.
Исследования in vivo и популяционный фармакокинетический анализ
Не обнаружено признаков клинически значимого фармакокинетического взаимодействия Лирики® с фенитоином, карбамазепином, вальпроевой кислотой, ламотриджином, габапентином, лоразепамом, оксикодоном или этанолом. Установлено, что пероральные противодиабетические средства, диуретики, инсулин, фенобарбитал, тиагабин и топирамат не оказывают клинически значимого влияния на клиренс Лирики®.
Пероральные контрацептивы, норэтистерон и/или этинилэстрадиол
Одновременное применение прегабалина с пероральными контрацептивами, норэтистероном и/или этинилэстрадиолом не влияет на фармакокинетику этих веществ в равновесном состоянии.
Лекарственные препараты, влияющие на центральную нервную систему
Лирика® может усилить эффекты этанола и лоразепама.
В контролируемых клинических исследованиях при многократном пероральном приеме Лирики® с оксикодоном, лоразепамом или этанолом не наблюдалось клинически значимых эффектов на дыхательную функцию.
Имеются сообщения, полученные во время пострегистрационного применения препарата, о дыхательной недостаточности и коме у пациентов, получающих Лирику® и другие депрессанты центральной нервной системы.
Лирика®, по-видимому, аддитивно усиливает эффект оксикодона, состоящий в нарушении когнитивной и общей моторной функции.
Взаимодействия и пациенты пожилого возраста
Специальные исследования фармакодинамических взаимодействий у добровольцев пожилого возраста не проводились. Исследования межлекарственных взаимодействий проводились только с участием взрослых пациентов.
Особые указания
Пациенты с сахарным диабетом
Некоторым пациентам с сахарным диабетом, у которых наблюдается увеличение массы тела при применении прегабалина, может понадобиться коррекция дозы гипогликемических препаратов.
Реакции гиперчувствительности
Имеются сообщения о реакциях гиперчувствительности, включая случаи ангионевротического отека. При появлении симптомов ангионевротического отека, таких как отек лица, отек вокруг рта или отек верхних дыхательных путей, следует немедленно прекратить прием прегабалина.
Головокружение, сонливость, потеря сознания, спутанность сознания и психическое расстройство
Лечение прегабалином сопровождалось головокружением и сонливостью, которые могут повышать риск случайных травм (падений) у пациентов пожилого возраста. В ходе пострегистрационного применения препарата поступали сообщения о потере сознания, спутанности сознания и психическом расстройстве. Поэтому пациентам следует соблюдать осторожность до тех пор, пока им не станут известны потенциальные эффекты препарата.
Эффекты, связанные со зрением
В контролируемых исследованиях у пациентов, получавших лечение прегабалином, ухудшение четкости зрения наблюдалось чаще, чем у пациентов, получавших плацебо; в большинстве случаев этот побочный эффект исчезал при продолжении применения препарата. В клинических исследованиях, в которых проводилось офтальмологическое обследование, частота случаев снижения остроты зрения и изменения полей зрения была выше у пациентов, получавших прегабалин, по сравнению с пациентами, получавшими плацебо; частота изменений со стороны глазного дна была выше у пациентов, получавших плацебо.
В период пострегистрационного применения препарата также были зафиксированы нежелательные явления со стороны органа зрения, в том числе потеря зрения, нечеткое зрение или другие изменения остроты зрения, многие из которых имели кратковременный характер. Отмена препарата может привести к исчезновению или уменьшению выраженности этих симптомов со стороны зрения.
Почечная недостаточность
Сообщалось о случаях почечной недостаточности, и в некоторых случаях отмена прегабалина приводила к обратимости данной нежелательной реакции.
Отмена сопутствующих противоэпилептических лекарственных препаратов
Имеется недостаточно данных об отмене сопутствующих противоэпилептических препаратов после достижения контроля над судорожными приступами с помощью прегабалина в ситуации добавления этого препарата к противоэпилептической терапии с целью его применения в качестве монотерапии.
Симптомы отмены
После прекращения кратковременного и длительного лечения прегабалином у некоторых пациентов наблюдались симптомы отмены. Наблюдались следующие явления, свидетельствующие о физической зависимости: бессонница, головная боль, тошнота, тревога, диарея, гриппоподобный синдром, нервозность, депрессия, боль, судороги, гипергидроз и головокружение. Следует сообщить об этом пациенту в начале лечения.
В ходе применения прегабалина или вскоре после его отмены могут возникать судороги, включая эпилептический статус и развернутые судорожные приступы. Что касается прекращения длительного лечения прегабалином, то данные свидетельствуют, что частота и тяжесть симптомов отмены могут зависеть от дозы препарата.
Хроническая сердечная недостаточность
У некоторых пациентов, принимавших прегабалин в течение пострегистрационного периода, были зарегистрированы случаи хронической сердечной недостаточности. Эти реакции наблюдались преимущественно у пациентов пожилого возраста с сердечно-сосудистыми нарушениями во время применения прегабалина по нейропатическим показаниям. Прегабалин следует применять у таких пациентов с осторожностью. Отмена прегабалина может привести к разрешению реакции.
Лечение центральной нейропатической боли, обусловленной повреждением спинного мозга
Во время лечения центральной нейропатической боли, обусловленной повреждением спинного мозга, общая частота нежелательных реакций, частота нежелательных реакций со стороны центральной нервной системы и в особенности частота сонливости были повышены. Это может быть обусловлено аддитивным эффектом, вызванным сопутствующими лекарственными препаратами (например, противоспазматические препараты), необходимыми для лечения этого заболевания. Это следует учитывать при назначении прегабалина для лечения этого заболевания.
Суицидальное мышление и поведение
У пациентов, получавших противоэпилептические препараты по нескольким показаниям, были зарегистрированы суицидальные мысли и поведение. Мета-анализ рандомизированных плацебо-контролируемых исследований противоэпилептических лекарственных препаратов также продемонстрировал небольшое повышение риска возникновения суицидальных мыслей и суицидального поведения. Механизм этого риска неизвестен, и доступные данные не исключают возможности повышения риска при применении прегабалина. В связи с этим, пациенты должны находиться под мониторингом на предмет признаков появления суицидального мышления и поведения, и следует рассмотреть возможность
соответствующего лечения. Пациентам (а также лицам, осуществляющим уход за пациентами) следует рекомендовать обратиться за медицинской помощью в случае появления признаков суицидального мышления или поведения.
Снижение функции нижних отделов желудочно-кишечного тракта
В течение пострегистрационного периода были зарегистрированы явления, связанные со снижением функции нижних отделов желудочно-кишечного тракта (например, непроходимость кишечника, паралитическая непроходимость кишечника и запор), когда прегабалин применялся одновременно с лекарственными препаратами, которые могут вызывать запор, такими как опиоидные анальгетики. При одновременном применении прегабалина и опиоидных препаратов можно рассмотреть возможность применения мер для предотвращения запора (в особенности у пациентов женского пола и пожилого возраста).
Ненадлежащее применение, потенциальное злоупотребление и зависимость
Сообщалось о случаях ненадлежащего применения препарата, злоупотребления или зависимости от него. Пациентам со злоупотреблением псхоактивными веществами в анамнезе прегабалин следует назначать с осторожностью, и таких пациентов следует наблюдать с целью выявления симптомов ненадлежащего применения препарата, злоупотребления или зависимости от него (развитие толерантности, повышение дозы, поведение, направленное на поиск препарата).
Энцефалопатия
Сообщалось о случаях энцефалопатии, преимущественно у пациентов с основными заболеваниями, которые могут приводить к энцефалопатии.
Непереносимость лактозы
Лирика® содержит лактозы моногидрат. Препарат не следует назначать больным с редкой наследственной непереносимостью галактозы, лактазной недостаточностью Лаппа или синдромом мальабсорбции глюкозы и галактозы.
Беременность и период лактации
Женщины, способные к деторождению/контрацепция у мужчин и женщин
Поскольку потенциальный риск для человека неизвестен, женщинам, способным к деторождению, необходимо использовать эффективные методы контрацепции.
Беременность
Достаточные данные по применению прегабалина у беременных женщин отсутствуют.
Лирику® не следует применять во время беременности без явной необходимости (за исключением тех случаев, когда ожидаемая польза для матери явно превышает возможный риск для плода).
Период лактации
Прегабалин выделяется в грудное молоко. Влияние прегабалина на новорожденных/младенцев неизвестно. Решение о прекращении кормления грудью или прекращении терапии прегабалином должно приниматься с учетом преимущества грудного вскармливания для ребенка и пользы терапии для женщины.
Репродуктивная функция
Клинические данные о влиянии прегабалина на репродуктивную функцию женщин отсутствуют.
По данным клинического исследования влияния прегабалина на подвижность сперматозоидов у мужчин отсутствовало.
Особенности влияния лекарственного средства на способность управлять транспортным средством или потенциально опасными механизмами
Препарат Лирика® может оказывать незначительное или умеренное влияние на способность управлять транспортными средствами и работать с механизмами. Лирика® может вызывать головокружение и сонливость и тем самым влиять на способность управлять транспортными средствами и работать с механизмами. Пациентам рекомендуется избегать управления транспортными средствами, работы со сложными механизмами или осуществления любой другой потенциально опасной деятельности до тех пор, пока не будет выяснено, оказывает ли данный препарат влияние на их способность осуществлять эту деятельность.
Передозировка
Симптомы: сонливость, спутанность сознания, тревожное возбуждение, беспокойство, в редких случаях кома.
Лечение: общее поддерживающее лечение и при необходимости гемодиализ.
Форма выпуска и упаковка
По 14 капсул помещают в контурную ячейковую упаковку из пленки поливинилхлоридной и фольги алюминиевой.
По 1 или 4 контурные ячейковые упаковки помещают в картонную пачку вместе с инструкцией по применению на государственном и русском языках.
Условия хранения
Хранить при температуре не выше 25°С.
Хранить в недоступном для детей месте!
Срок хранения
3 года.
Не применять после истечения срока годности, указанного на упаковке.
Условия отпуска из аптек
По рецепту
Производитель и упаковщик
Пфайзер Мануфактуринг Дойчланд ГмбХ,
Моосвальдале 1, 79090 Фрайбург, Германия
Владелец регистрационного удостоверения
Пфайзер Эйч Си Пи Корпорэйшн, США
Адрес организации, принимающей на территории Республики Казахстан претензии от потребителей по качеству данного продукта и ответственной за пострегистрационное наблюдение за безопасностью лекарственного средства:
Представительство компании «Пфайзер Эйч Си Пи Корпорэйшн» (США) г.Алматы, ул. Фурманова, 100/4
тел.: (727) 250-09-16
факс: (727) 250-42-09
электронная почта: PfizerKazakhstan@pfizer.com
| 520578361477976825_ru.doc | 140 кб |
| 239140051477977983_kz.doc | 167.5 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники
Клинико-фармакологическая группа
Противосудорожный препарат
Действующее вещество
— прегабалин (pregabalin)
Форма выпуска, состав и упаковка
Капсулы твердые желатиновые, №4, с крышечкой белого цвета и корпусом белого цвета; черными чернилами на корпусе капсулы указаны дозировка и код продукта — «PGN 25», на крышечке — «Pfizer»; содержимое капсул — порошок белого или почти белого цвета.
Вспомогательные вещества: лактозы моногидрат — 35 мг, крахмал кукурузный — 20 мг, тальк — 20 мг.
Состав корпуса капсулы: титана диоксид — 0.557 мг (1.47%), натрия лаурилсульфат — 0.046 мг (0.12%) (max), вода — 3.306 мг (8.7%), желатин — 18.892 мг (49.72%) qsp до 100%.
Состав крышечки капсулы: титана диоксид — 0.371 мг (0.98%), натрия лаурилсульфат — 0.03 мг (0.08%) (max), вода — 2.204 мг (5.8%), желатин — 12.594 мг (33.14%) qsp до 100%.
Состав чернил: шеллак (24-27%), этанол (23-26%), изопропанол (0.5-3%), бутанол (0.5-3%), пропиленгликоль (3-7%), аммиака раствор концентрированный (1-2%), калия гидроксид (0.05-0.1%), вода очищенная (15-18%), краситель железа оксид черный (24-28%).
10 шт. — блистеры (10) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (1) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
21 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
Капсулы твердые желатиновые, №3, с крышечкой белого цвета и корпусом белого цвета с черной полосой; черными чернилами на корпусе капсулы указаны дозировка и код продукта — «PGN 50», на крышечке — «Pfizer»; содержимое капсул — порошок белого или почти белого цвета.
Вспомогательные вещества: лактозы моногидрат — 70 мг, крахмал кукурузный — 40 мг, тальк — 40 мг.
Состав корпуса капсулы: титана диоксид — 0.703 мг (1.46%), натрия лаурилсульфат — 0.058 мг (0.12%) (max), вода — 4.176 мг (8.7%), желатин — 23.863 мг (49.71%) qsp до 100%.
Состав крышечки капсулы: титана диоксид — 0.469 мг (0.98%), натрия лаурилсульфат — 0.038 мг (0.08%) (max), вода — 2.784 мг (5.8%), желатин — 15.909 мг (33.14%) qsp до 100%.
Состав чернил: шеллак (24-27%), этанол (23-26%), изопропанол (0.5-3%), бутанол (0.5-3%), пропиленгликоль (3-7%), аммиака раствор концентрированный (1-2%), калия гидроксид (0.05-0.1%), вода очищенная (15-18%), краситель железа оксид черный (24-28%).
10 шт. — блистеры (10) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (1) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
21 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
Капсулы твердые желатиновые, №4, с крышечкой от красно-коричневого до темно-красно-коричневого цвета* и корпусом белого цвета; черными чернилами на корпусе капсулы указаны дозировка и код продукта — «PGN 75», на крышечке — «Pfizer»; содержимое капсул — порошок белого или почти белого цвета.
Вспомогательные вещества: лактозы моногидрат — 8.25 мг, крахмал кукурузный — 8.375 мг, тальк — 8.375 мг.
Состав корпуса капсулы: титана диоксид — 0.557 мг (1.47%), натрия лаурилсульфат — 0.046 мг (0.12%) (max), вода — 3.306 мг (8.7%), желатин — 18.892 мг (49.72%) qsp до 100%.
Состав крышечки капсулы: краситель железа оксид красный — 0.264 мг (0.69%), титана диоксид — 0.062 мг (0.16%), натрия лаурилсульфат — 0.03 мг (0.08%) (max), вода — 2.204 мг (5.8%), желатин — 12.64 мг (33.26%) qsp до 100%.
Состав чернил: шеллак (24-27%), этанол (23-26%), изопропанол (0.5-3%), бутанол (0.5-3%), пропиленгликоль (3-7%), аммиака раствор концентрированный (1-2%), калия гидроксид (0.05-0.1%), вода очищенная (15-18%), краситель железа оксид черный (24-28%).
10 шт. — блистеры (10) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (1) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
21 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
Капсулы твердые желатиновые, №3, с крышечкой от красно-коричневого до темно-красно-коричневого цвета* и корпусом от красно-коричневого до темно-красно-коричневого цвета*; черными чернилами на корпусе капсулы указаны дозировка и код продукта — «PGN 100», на крышечке — «Pfizer»; содержимое капсул — порошок белого или почти белого цвета.
| 1 капс. | |
| прегабалин | 100 мг |
Вспомогательные вещества: лактозы моногидрат — 11 мг, крахмал кукурузный — 11.17 мг, тальк — 11.17 мг.
Состав корпуса капсулы: краситель железа оксид красный — 0.5 мг (1.04%), титана диоксид — 0.118 мг (0.25%), натрия лаурилсульфат — 0.058 мг (0.12%) (max), вода — 4.176 мг (8.7%), желатин — 23.949 мг (49.89%) qsp до 100%.
Состав крышечки капсулы: краситель железа оксид красный — 0.333 мг (0.69%), титана диоксид — 0.079 мг (0.16%), натрия лаурилсульфат — 0.038 мг (0.08%) (max), вода — 2.784 мг (5.8%), желатин — 15.966 мг (33.26%) qsp до 100%.
Состав чернил: шеллак (24-27%), этанол (23-26%), изопропанол (0.5-3%), бутанол (0.5-3%), пропиленгликоль (3-7%), аммиака раствор концентрированный (1-2%), калия гидроксид (0.05-0.1%), вода очищенная (15-18%), краситель железа оксид черный (24-28%).
10 шт. — блистеры (10) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (1) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
21 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
Капсулы твердые желатиновые, №2, с крышечкой белого цвета и корпусом белого цвета; черными чернилами на корпусе капсулы указаны дозировка и код продукта — «PGN 150», на крышечке — «Pfizer»; содержимое капсул — порошок белого или почти белого цвета.
| 1 капс. | |
| прегабалин | 150 мг |
Вспомогательные вещества: лактозы моногидрат — 16.5 мг, крахмал кукурузный — 16.75 мг, тальк — 16.75 мг.
Состав корпуса капсулы: титана диоксид — 0.894 мг (1.47%), натрия лаурилсульфат — 0.073 мг (0.12%) (max), вода — 5.307 мг (8.7%), желатин — 30.326 мг (49.71%) qsp до 100%.
Состав крышечки капсулы: титана диоксид — 0.596 мг (0.98%), натрия лаурилсульфат — 0.049 мг (0.08%) (max), вода — 3.538 мг (5.8%), желатин — 20.217 мг (33.14%) qsp до 100%.
Состав чернил: шеллак (24-27%), этанол (23-26%), изопропанол (0.5-3%), бутанол (0.5-3%), пропиленгликоль (3-7%), аммиака раствор концентрированный (1-2%), калия гидроксид (0.05-0.1%), вода очищенная (15-18%), краситель железа оксид черный (24-28%).
10 шт. — блистеры (10) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (1) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
21 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
Капсулы твердые желатиновые, №1, с крышечкой от светло-красно-коричневого до красно-коричневого цвета* и корпусом от светло-красно-коричневого до красно-коричневого цвета*; черными чернилами на корпусе капсулы указаны дозировка и код продукта — «PGN 200», на крышечке — «Pfizer»; содержимое капсул — порошок белого или почти белого цвета.
| 1 капс. | |
| прегабалин | 200 мг |
Вспомогательные вещества: лактозы моногидрат — 22 мг, крахмал кукурузный — 22.34 мг, тальк — 22.34 мг.
Состав корпуса капсулы: краситель железа оксид красный — 0.201 мг (0.26%), титана диоксид — 0.189 мг (0.25%), натрия лаурилсульфат — 0.091 мг (0.12%) (max), вода — 6.612 мг (8.7%), желатин — 38.507 мг (50.67%) qsp до 100%.
Состав крышечки капсулы: краситель железа оксид красный — 0.134 мг (0.18%), титана диоксид — 0.126 мг (0.17%), натрия лаурилсульфат — 0.061 мг (0.08%) (max), вода — 4.408 мг (5.8%), желатин — 25.672 мг (33.78%) qsp до 100%.
Состав чернил: шеллак (24-27%), этанол (23-26%), изопропанол (0.5-3%), бутанол (0.5-3%), пропиленгликоль (3-7%), аммиака раствор концентрированный (1-2%), калия гидроксид (0.05-0.1%), вода очищенная (15-18%), краситель железа оксид черный (24-28%).
10 шт. — блистеры (10) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (1) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
21 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
Капсулы твердые желатиновые, №0, с крышечкой от красно-коричневого до темно-красно-коричневого цвета* и корпусом белого цвета, черными чернилами на корпусе капсулы указаны дозировка и код продукта «PGN 300», на крышечке — «Pfizer»; содержимое капсул — порошок белого или почти белого цвета.
| 1 капс. | |
| прегабалин | 300 мг |
Вспомогательные вещества: лактозы моногидрат — 33 мг, крахмал кукурузный — 33.5 мг, тальк — 33.5 мг.
Состав корпуса капсулы: титана диоксид — 1.407 мг (1.47%), натрия лаурилсульфат — 0.115 мг (0.12%) (max), вода — 8.352 мг (8.7%), желатин — 47.726 мг (49.71%) qsp до 100%.
Состав крышечки капсулы: краситель железа оксид красный — 0.667 мг (0.69%), титана диоксид — 0.157 мг (0.16%), натрия лаурилсульфат — 0.077 мг (0.08%) (max), вода — 5.568 мг (5.8%), желатин — 31.931 мг (33.26%) qsp до 100%.
Состав чернил: шеллак (24-27%), этанол (23-26%), изопропанол (0.5-3%), бутанол (0.5-3%), пропиленгликоль (3-7%), аммиака раствор концентрированный (1-2%), калия гидроксид (0.05-0.1%), вода очищенная (15-18%), краситель железа оксид черный (24-28%).
10 шт. — блистеры (10) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (1) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
21 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
* в оригинальных сертификатах производителя данные цвета описаны так: «от красно-коричневого до темно-красно-коричневого цвета» — «orange», от светло-красно-коричневого до красно-коричневого цвета» — «light orange», что соответствует цвету понтонов сравнения, используемых в Европейском Союзе при проведении данного вида анализа.
Фармакологическое действие
Действующим веществом является прегабалин — аналог гамма-аминомасляной кислоты ((S)-3-(аминометил)-5-метилгексановая кислота).
Механизм действия
Было установлено, что прегабалин связывается с дополнительной субъединицей (α2-дельта-протеин) потенциал-зависимых кальциевых каналов в ЦНС, необратимо замещая [3Н]-габапентин. Предполагается, что такое связывание может способствовать проявлению его анальгетического и противосудорожного эффектов.
Нейропатическая боль
Эффективность прегабалина отмечена у пациентов с диабетической невропатией и постгерпетической невралгией.
Установлено, что при приеме прегабалина курсами до 13 недель по 2 раза/сут и до 8 недель по 3 раза/сут, в целом риск развития побочных эффектов и эффективность препарата при приемах по 2 или по 3 раза/сут одинаковы.
При приеме курсом продолжительностью до 13 недель боль уменьшалась в течение первой недели, а эффект сохранялся до конца лечения.
Отмечалось уменьшение индекса боли на 50% у 35% пациентов, получавших прегабалин, и 18% пациентов, принимавших плацебо. Среди пациентов, не испытывавших сонливости, эффект такого снижения боли отмечался у 33% пациентов группы прегабалина и 18% пациентов группы плацебо. У 48% пациентов, принимавших прегабалин, и у 16% пациентов, принимавших плацебо, возникала сонливость.
Фибромиалгия
Выраженное снижение болевой симптоматики, связанной с фибромиалгией, отмечается при применении прегабалина в дозах от 300 мг до 600 мг/сут. Эффективность доз 450 и 600 мг/сут сравнима, однако переносимость 600 мг/сут обычно хуже.
Также применение прегабалина связано с заметным улучшением в функциональной активности пациентов и снижением выраженности нарушений сна. Применение прегабалина в дозе 600 мг/сут приводило к более выраженному улучшению сна, по сравнению с дозой 300-450 мг/сут.
Эпилепсия
При приеме препарата в течение 12 недель по 2 или 3 раза/сут отмеченные риск развития побочных эффектов и эффективность препарата при этих режимах дозирования одинаковы. Уменьшение частоты судорог начиналось в течение первой недели.
Генерализованное тревожное расстройство
Уменьшение симптоматики генерализованного тревожного расстройства отмечается на первой неделе лечения. При применении препарата в течение 8 недель у 52% пациентов, получавших прегабалин, и у 38% пациентов, получавших плацебо, отмечалось 50% уменьшение симптоматики по шкале тревожности Гамильтона (HAM-A).
В клинических исследованиях у пациентов, постоянно получавших прегабалин, побочные реакции со стороны органа зрения (такие как затуманивание зрения, снижение остроты зрения, изменения полей зрения) отмечались чаще (за исключением изменений глазного дна), чем у пациентов, получавших плацебо (см. раздел «Особые указания»).
Фармакокинетика
Параметры фармакокинетики прегабалина в равновесном состоянии у здоровых добровольцев, у пациентов с эпилепсией, получавших противоэпилептическую терапию, и у пациентов, получавших его по поводу хронических болевых синдромов, были аналогичны.
Всасывание
Прегабалин быстро всасывается натощак. Сmax прегабалина в плазме достигается через 1 ч как при однократном, так и повторном применении. Биодоступность прегабалина при приеме внутрь составляет ≥90% и не зависит от дозы. При повторном применении Css достигается через 24-48 ч. При применении препарата после приема пищи Cmax снижается примерно на 25-30%, а Tmax увеличивается приблизительно до 2.5 ч. Однако прием пищи не оказывает клинически значимого влияния на общее всасывание прегабалина.
Распределение
Кажущийся Vd прегабалина после приема внутрь составляет примерно 0.56 л/кг. Прегабалин не связывается с белками плазмы.
В исследованиях прегабалина на животных отмечали, что он проникает через ГЭБ у мышей, крыс и обезьян. Также было показано, что прегабалин может проникать через плацентарный барьер, и обнаруживается в молоке у крыс во время лактации.
Метаболизм
Прегабалин практически не подвергается метаболизму. После приема меченного прегабалина примерно 98% радиоактивной метки определялось в моче в неизмененном виде. Доля N-метилированного производного прегабалина, который является основным метаболитом, обнаруживаемым в моче, составляла 0.9% дозы. В доклинических исследованиях не отмечено признаков рацемизации S-энантиомера прегабалина в R-энантиомер.
Выведение
Прегабалин выводится в основном почками в неизмененном виде.
Средний Т1/2 составляет 6.3 ч. Клиренс прегабалина из плазмы и почечный клиренс прямо пропорциональны КК. У пациентов с нарушенной функцией почек и пациентов, находящихся на гемодиализе, необходима коррекция дозы (см. раздел «Режим дозирования»).
Линейность/нелинейность
Фармакокинетика прегабалина в диапазоне рекомендуемых суточных доз носит линейный характер, межиндивидуальная вариабельность низкая (<20%). Фармакокинетику прегабалина при повторном применении можно предсказать на основании данных приема однократной дозы. Следовательно, необходимости в регулярном мониторировании концентрации прегабалина нет.
Фармакокинетика у особых групп пациентов
Пол. Пол пациента не оказывает клинически значимого влияния на концентрацию прегабалина в плазме.
Нарушение функции почек. Клиренс прегабалина прямо пропорционален КК. Учитывая, что прегабалин в основном выводится почками, у пациентов с нарушенной функцией почек рекомендуется снизить дозу прегабалина. Кроме того, прегабалин эффективно удаляется из плазмы при гемодиализе (после 4-часового сеанса гемодиализа концентрации прегабалина в плазме снижаются примерно на 50%), после гемодиализа необходимо назначить дополнительную дозу препарата (см. раздел «Режим дозирования»).
Нарушение функции печени. Фармакокинетика прегабалина у пациентов с нарушением функции печени специально не изучалась. Прегабалин практически не подвергается метаболизму и выводится в основном в неизмененном виде с мочой, поэтому нарушение функции печени не должно существенно изменять концентрации прегабалина в плазме.
Пожилые пациенты (старше 65 лет). Клиренс прегабалина с возрастом имеет тенденцию к снижению, что отражает возрастное снижение КК. Пациентам пожилого возраста с нарушенной функцией почек может потребоваться снижение дозы препарата (см. раздел «Режим дозирования»).
Показания
Нейропатическая боль:
- лечение нейропатической боли у взрослых.
Эпилепсия:
- в качестве дополнительной терапии у взрослых с парциальными судорожными приступами, сопровождающимися или не сопровождающимися вторичной генерализацией.
Генерализованное тревожное расстройство:
- лечение генерализованного тревожного расстройства у взрослых.
Фибромиалгия:
- лечение фибромиалгии у взрослых.
Противопоказания
- повышенная чувствительность к действующему веществу или любому другому компоненту препарата;
- редкие наследственные заболевания, в т.ч. непереносимость галактозы, лактазная недостаточность и нарушение всасывания глюкозы/галактозы;
- детский и подростковый возраст до 17 лет включительно (нет данных по применению).
С осторожностью: почечная недостаточность (см. раздел «Режим дозирования»); хроническая сердечная недостаточность (см. раздел «Особые указания»); одновременное применение с опиоидами (см. раздел «Особые указания»).
В связи с зарегистрированными единичными случаями бесконтрольного применения прегабалина, препарат необходимо назначать с осторожностью пациентам с лекарственной зависимостью в анамнезе (такие пациенты нуждаются в пристальном медицинском наблюдении во время лечения препаратом).
Дозировка
Препарат принимают внутрь независимо от приема пищи в суточной дозе от 150 до 600 мг в 2 или 3 приема.
При нейропатической боли лечение начинают с дозы 150 мг/сут. В зависимости от достигнутого эффекта и переносимости через 3-7 дней дозу можно увеличить до 300 мг/сут, а при необходимости еще через 7 дней — до максимальной дозы 600 мг/сут.
При эпилепсии лечение начинают с дозы 150 мг/сут. С учетом достигнутого эффекта и переносимости через 1 неделю дозу можно увеличить до 300 мг/сут, а еще через неделю — до максимальной дозы 600 мг/сут.
При фибромиалгии лечение начинают с дозы по 75 мг 2 раза/сут (150 мг/сут). В зависимости от достигнутого эффекта и переносимости через 7 дней дозу можно увеличить до 300 мг/сут (150 мг 2 раза/сут). При отсутствии положительного эффекта дозу увеличивают до 450 мг/сут (225 мг 2 раза/сут), а при необходимости еще через 7 дней — до максимальной дозы 600 мг/сут. Следует учитывать, что доза 600 мг/сут не дает дополнительных преимуществ, но хуже переносится.
При генерализованном тревожном расстройстве лечение начинают с дозы 150 мг/сут. В зависимости от достигнутого эффекта и переносимости через 7 дней дозу можно увеличить до 300 мг/сут. При отсутствии положительного эффекта дозу увеличивают до 450 мг/сут, а при необходимости еще через 7 дней — до максимальной дозы 600 мг/сут.
Следует регулярно оценивать необходимость продолжения терапии.
Отмена прегабалина
Если лечение необходимо прекратить, рекомендуется делать это постепенно в течение минимум 1 недели.
У пациентов с нарушенной функцией почек дозу подбирают индивидуально с учетом КК (табл. 1), который рассчитывают по следующей формуле:
Для мужчин:
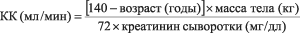
Для женщин:
КК (мл/мин)= значение КК для мужчин × 0.85
У пациентов, находящихся на гемодиализе, суточную дозу прегабалина подбирают с учетом функции почек. После 4-часового сеанса гемодиализа концентрации прегабалина в плазме крови снижаются примерно на 50%. Непосредственно после каждого 4-часового сеанса гемодиализа назначают дополнительную дозу (см. табл. 1).
Таблица 1. Подбор дозы прегабалина с учетом функции почек
| КК (мл/мин) |
Суточная доза прегабалина | Кратность приема в сутки |
|
| Стартовая доза (мг/сут) |
Максимальная доза (мг/сут) |
||
| ≥60 | 150 | 600 | 2-3 |
| ≥30-<60 | 75 | 300 | 2-3 |
| ≥15-<30 | 25-50 | 150 | 1-2 |
| <15 | 25 | 75 | 1 |
| Дополнительная доза после диализа (мг) | |||
| 25 | 100 | Однократно |
У пациентов с нарушением функции печени коррекции дозы не требуется (см. раздел «Фармакокинетика»).
Пациентам пожилого возраста (старше 65 лет) может потребоваться снижение дозы прегабалина в связи со снижением функции почек (см. раздел «Фармакокинетика»).
Применение у детей до 12 лет и подростков (12-17 лет, включительно) — безопасность и эффективность прегабалина не установлены. Применение препарата у детей не рекомендуется.
В случае пропуска дозы прегабалина необходимо принять следующую дозу как можно скорее, однако не следует принимать пропущенную дозу, если время приема следующей уже подходит.
Побочные действия
По имеющемуся опыту клинического применения прегабалина у более чем 12000 пациентов, наиболее распространенными нежелательными явлениями были головокружение и сонливость. Наблюдаемые явления были обычно легкими или умеренными. Частота отмены прегабалина и плацебо из-за нежелательных реакций составила 14% и 7% соответственно. Основными нежелательными эффектами, требовавшими прекращения лечения, были головокружение (4%) и сонливость (3%), в зависимости от их субъективной переносимости. Другие побочные эффекты, которые также приводили к отмене препарата: атаксия, спутанность сознания, астения, нарушение внимания, нечеткость зрения, нарушение координации, периферические отеки.
Также отмечались нежелательные реакции, возникающие после отмены прегабалина: бессонница, головная боль, тошнота, тревога, гриппоподобный синдром, судороги, повышенная возбудимость, депрессия, боль, гипергидроз и диарея.
На фоне терапии центральной нейропатической боли, связанной с повреждением спинного мозга, наблюдается увеличение частоты побочных реакций в целом, а также побочных реакций со стороны ЦНС, в особенности сонливости.
В таблице перечислены все нежелательные явления, частота которых превышала таковую в группе плацебо (наблюдавшиеся более чем у 1 человека). Они распределены по системно-органным классам. Частота встречаемости нежелательных реакций определялась по количеству нежелательных явлений в массиве данных клинических исследований независимо от оценки причинно-следственной связи: очень часто (≥1/10), часто (≥1/100, <1/10), нечасто (≥1/1000, <1/100) и редко (<1/1000). Реакции, наблюдавшиеся во время пострегистрационного применения препарата, выделены курсивом.
Перечисленные нежелательные явления могут также быть связаны с основным заболеванием и/или сопутствующей терапией.
| Частота | Нежелательные реакции |
| Инфекции и инвазии | |
| часто | назофарингит |
| Со стороны системы кроветворения | |
| нечасто | нейтропения |
| Со стороны обмена веществ и питания | |
| часто | повышение аппетита |
| нечасто | анорексия, гипогликемия |
| Психические нарушения | |
| часто | состояние эйфории, спутанность сознания, бессонница, раздражительность, депрессия, дезориентация, снижение либидо, паническая атака, апатия |
| нечасто | галлюцинации, беспокойство, тревожное возбуждение, подавленное настроение, приподнятое настроение, колебания настроения, агрессивность, деперсонализация, тревожные сновидения, затруднения с подбором слов, повышение либидо, аноргазмия, усиление бессонницы |
| редко | расторможенность |
| Со стороны нервной системы | |
| очень часто | головокружение, сонливость, головная боль |
| часто | атаксия, нарушение координации, тремор, дизартрия, амнезия, ухудшение памяти, нарушение внимания, парестезия, гипестезия, седативный эффект, нарушение равновесия, летаргия, агевзия |
| нечасто | обморочные состояния, миоклония, психомоторное возбуждение, дискинезия, ортостатическое головокружение, интенционный тремор, нистагм, нарушение речи, понижение рефлексов, ощущение жжения на коже и слизистых оболочках, гиперестезия, потеря сознания, когнитивные нарушения |
| редко | патологическое оцепенение, паросмия, гипокинезия, дисграфия, судороги |
| Со стороны органа зрения | |
| часто | нечеткость зрения, диплопия |
| нечасто | утрата периферического зрения, нарушение зрения, отечность в области глаза, дефект поля зрения, снижение остроты зрения, боль в глазах, астенопия, фотопсия, синдром сухого глаза, повышенное слезоотделение, раздражение слизистой оболочки глаз |
| редко | осциллопсия (колебание видимых предметов), изменение глубины зрительного восприятия, мидриаз, косоглазие, усиление яркости зрительного восприятия, кератит, потеря зрения |
| Со стороны органа слуха и вестибулярного аппарата | |
| часто | вертиго |
| нечасто | гиперакузия |
| Со стороны сердечно-сосудистой системы | |
| нечасто | тахикардия, AV-блокада I степени, синусовая брадикардия, хроническая сердечная недостаточность |
| редко | синусовая тахикардия, синусовая аритмия, удлинение интервала QT |
| Со стороны сосудов | |
| нечасто | гипотензия, гипертензия, гиперемия кожи, «приливы», холодные конечности |
| Со стороны дыхательной системы | |
| часто | сухость слизистой оболочки полости носа |
| нечасто | одышка, носовое кровотечение, кашель, заложенность носа, ринит, храп |
| редко | чувство стеснения в горле, отек легких |
| Со стороны пищеварительной системы | |
| часто | рвота, запор, метеоризм, вздутие живота, сухость во рту, тошнота, диарея |
| нечасто | гастроэзофагеальный рефлюкс, гиперсекреция слюнных желез, снижение чувствительности слизистой оболочки полости рта |
| редко | асцит, панкреатит, дисфагия, отек языка |
| Со стороны кожи и подкожных тканей | |
| нечасто | папулезная сыпь, крапивница, повышенная потливость, отек лица, кожный зуд |
| редко | Синдром Стивенса-Джонсона, холодный пот |
| Со стороны костно-мышечной системы | |
| часто | мышечные судороги, артралгия, боль в спине, боль в конечностях, спазм мышц шейного отдела позвоночника |
| нечасто | отек в области сустава, миалгия, мышечная судорога, боль в шее, скованность мышц |
| редко | рабдомиолиз |
| Со стороны мочевыделительной системы | |
| нечасто | недержание мочи, дизурия |
| редко | почечная недостаточность, олигурия, задержка мочи |
| Со стороны репродуктивной системы | |
| часто | боль в области молочных желез, эректильная дисфункция |
| нечасто | сексуальная дисфункция, отсроченная эякуляция, дисменорея |
| редко | аменорея, выделения из молочных желез, увеличение молочных желез, гинекомастия |
| Со стороны иммунной системы | |
| нечасто | реакции гиперчувствительности |
| редко | ангионевротический отек, аллергические реакции |
| Со стороны лабораторных показателей | |
| часто | увеличение массы тела, повышение концентрации креатинина в крови |
| нечасто | повышение активности КФК, АЛТ, АСТ, повышение концентрации глюкозы крови, снижение количества тромбоцитов, снижение содержания калия в крови, снижение массы тела |
| редко | снижение количества лейкоцитов в крови |
| Общие расстройства | |
| часто | периферический отек, нарушение походки, падение, чувство опьянения, плохое самочувствие, утомляемость |
| нечасто | генерализованный отек, чувство стеснения в груди, боль, лихорадка, жажда, озноб, общая слабость, недомогание |
Передозировка
Симптомы: при передозировке препарата (до 15 г) каких-либо из не описанных выше нежелательных реакций зарегистрировано не было. В ходе пострегистрационного применения наиболее частыми нежелательными явлениями, развивавшимися при передозировке прегабалина, являлись: аффективные расстройства, сонливость, спутанность сознания, депрессия, ажитация и беспокойство, в редких случаях были зарегистрированы случаи комы. Также отмечались судороги.
Лечение: проводят промывание желудка, поддерживающую терапию и при необходимости — гемодиализ (см. раздел «Режим дозирования» табл. 1).
Лекарственное взаимодействие
Прегабалин выводится с мочой в основном в неизмененном виде, подвергается минимальному метаболизму у человека (в виде метаболитов с мочой выводится менее 2% дозы), не ингибирует метаболизм других лекарственных веществ in vitro и не связывается с белками плазмы, поэтому вряд ли способен вступать в фармакокинетическое взаимодействие.
Исследования in vivo и популяционный фармакокинетический анализ
Не обнаружено признаков клинически значимого фармакокинетического взаимодействия прегабалина с фенитоином, карбамазепином, вальпроевой кислотой, ламотриджином, габапентином, лоразепамом, оксикодоном и этанолом. Установлено, что пероральные гипогликемические препараты, диуретики, инсулин, фенобарбитал, тиагабин и топирамат не оказывают клинически значимого влияния на клиренс прегабалина.
Пероральные контрацептивные препараты, норэтистерон и/или этинилэстрадиол
При применении пероральных контрацептивных препаратов, содержащих норэтистерон и/или этинилэстрадиол, одновременно с прегабалином равновесная фармакокинетика обоих препаратов не менялась.
Препараты, влияющие на ЦНС
Сообщалось о случаях нарушения дыхания, наступления комы и смерти при одновременном применении прегабалина с другими препаратами, угнетающими ЦНС, в т.ч. у пациентов, которые злоупотребляют психоактивными веществами.
Повторное пероральное применение прегабалина с оксикодоном, лоразепамом или этанолом не оказывало клинически значимого влияния на дыхание. Прегабалин, по-видимому, усиливает нарушения когнитивной и двигательной функций, вызванные оксикодоном. Прегабалин может усилить эффекты этанола и лоразепама.
Влияние на ЖКТ
Также сообщалось об отрицательном влиянии прегабалина на деятельность ЖКТ (в т.ч. развитие кишечной непроходимости, паралитического илеуса, запора) при одновременном применении с лекарственными средствами, вызывающими запор (такими как опиоиды) (см. раздел «Особые указания»).
Взаимодействие препаратов при применении у пожилых пациентов
Специальные исследования фармакодинамического взаимодействия с другими лекарственными средствами у пожилых пациентов не проводились.
Особые указания
Пациенты с сахарным диабетом
У части пациентов с сахарным диабетом в случае повышения массы тела на фоне лечения прегабалином может потребоваться коррекция доз гипогликемических препаратов.
Реакции гиперчувствительности
Прегабалин необходимо отменить в случае развития симптомов ангионевротического отека (таких как, отек лица, периоральный отек или отечность тканей верхних дыхательных путей).
Суицидальные мысли и поведение
Противоэпилептические препараты, включая прегабалин, могут повышать риск возникновения суицидальных мыслей или поведения. Поэтому пациентов, получающих эти препараты, следует тщательно наблюдать на предмет возникновения или ухудшения депрессии, появления суицидальных мыслей или поведения.
Снижение функции ЖКТ
При одновременном применении прегабалина и опиоидов следует рассмотреть необходимость проведения профилактических мер по предупреждению развития запоров (в особенности у пожилых пациентов и женщин).
Головокружение, сонливость, потеря сознания, спутанность сознания и нарушения когнитивных функций
Лечение прегабалином сопровождалось головокружением и сонливостью, которые повышают риск случайных травм (падений) у пожилых людей. В ходе пострегистрационного применения препарата отмечались также случаи потери сознания, спутанности сознания и нарушения когнитивных функций. Поэтому до тех пор, пока пациенты не оценят возможные эффекты препарата, они должны соблюдать осторожность.
Отмена сопутствующей терапии противосудорожными препаратами
Сведения о возможности отмены других противосудорожных средств при подавлении судорог прегабалином и целесообразности монотерапии этим препаратом недостаточны.
Имеются сообщения о развитии судорог, в т.ч. эпилептического статуса и малых припадков на фоне применения прегабалина или сразу после окончания терапии.
Влияние прегабалина на зрение
В клинических исследованиях у пациентов, постоянно получавших прегабалин, такой побочный эффект, как затуманивание зрения отмечался чаще, чем у пациентов, получавших плацебо. При этом указанный побочный эффект прекращался по мере продолжения лечения. В клинических исследованиях, во время которых проводили офтальмологическое обследование пациентов, снижение остроты зрения и изменения полей зрения чаще наблюдалось у пациентов, получающих прегабалин, чем у получающих плацебо. Частота изменений глазного дна была выше у пациентов, получающих плацебо.
Несмотря на то, что клиническое значение этих нарушений не установлено, пациентам следует сообщать врачу об изменениях зрения на фоне терапии прегабалином. В случае сохранения симптомов нарушения зрения следует продолжить наблюдение. Более частые проверки зрения следует проводить у пациентов, которые уже регулярно наблюдаются у офтальмолога. При появлении в ответ на применение прегабалина таких нежелательных реакций, как потеря зрения, нечеткость зрения или других нарушений со стороны органа зрения, отмена препарата может привести к исчезновению указанных симптомов.
Почечная недостаточность
Отмечались также случаи развития почечной недостаточности, в некоторых случаях после отмены прегабалина функция почек восстанавливалась.
Симптомы отмены прегабалина
В результате отмены прегабалина после длительной или краткосрочной терапии наблюдались следующие нежелательные явления: бессонница, головная боль, тошнота, диарея, гриппоподобный синдром, депрессия, потливость, головокружение, судороги и тревога. Имеющиеся данные свидетельствуют о том, что частота возникновения и тяжесть проявлений синдрома отмены могут зависеть от дозы прегабалина.
Злоупотребление прегабалином
Нет данных о том, что прегабалин активен в отношении рецепторов, отвечающих за развитие злоупотребления препаратом у пациентов. Во время пострегистрационных исследований отмечались случаи нарушения рекомендованного режима дозирования, злоупотребления и зависимости от прегабалина. Как и при применении любого лекарственного средства, влияющего на ЦНС, следует тщательно оценить анамнез пациента на предмет имеющихся случаев злоупотребления лекарственными средствами и/или психических расстройств. Пациенты должны наблюдаться на предмет нарушения рекомендованного режима дозирования, злоупотребления и зависимости от прегабалина (например, развитие устойчивости к терапии прегабалином, необоснованное повышение дозы препарата, аддиктивное поведение пациента).
Хроническая сердечная недостаточность
Несмотря на то, что очевидной взаимосвязи с концентрацией прегабалина в плазме крови и развитием сердечной недостаточности не отмечалось, в ходе пострегистрационного применения препарата сообщалось о развитии хронической сердечной недостаточности на фоне терапии прегабалином у некоторых пациентов. У пациентов без клинически выраженных признаков заболеваний сердца или сосудов не отмечалось связи между периферическими отеками и сердечно-сосудистыми осложнениями, такими как, повышение АД или хроническая сердечная недостаточность. Эти реакции преимущественно наблюдались у пациентов пожилого возраста, страдавших нарушениями функции сердца и получавших препарат по поводу невропатии. Поэтому прегабалин у данной категории пациентов следует применять с осторожностью. После отмены прегабалина возможно исчезновение проявлений подобных реакций.
Одновременное применение с опиоидами
Рекомендуется соблюдать осторожность при назначении прегабалина одновременно с опиоидами в связи с риском развития угнетения ЦНС. В наблюдательном исследовании с участием лиц, принимающих опиоиды, у пациентов, которые получали терапию прегабалином одновременно с опиоидом, наблюдался повышенный риск смертности, связанной с опиоидами, по сравнению с теми, кто принимал только опиоиды (скорректированное отношение шансов, 1.68 [95% ДИ, 1.19-2.36]).
Терапия центральной нейропатической боли, связанной с повреждением спинного мозга
Частота нежелательных явлений со стороны ЦНС, особенно таких как сонливость, повышается при лечении центральной нейропатической боли, обусловленной поражением спинного мозга, что, однако, может быть следствием суммирования эффектов прегабалина и других параллельно принимаемых средств (например, антиспастических). Это обстоятельство следует принимать во внимание при назначении прегабалина по данному показанию.
Энцефалопатия
Отмечались случаи энцефалопатии, особенно у пациентов с сопутствующими заболеваниями, которые могут привести к развитию данного состояния.
Женщины репродуктивного возраста/Контрацепция
Использование прегабалина в I триместре беременности может вызвать серьезные врожденные дефекты у будущего ребенка. Прегабалин не следует применять во время беременности, если польза для матери явно не превышает потенциальный риск для плода. Женщины репродуктивного возраста должны пользоваться адекватными методами контрацепции во время лечения (см. раздел «Беременность и лактация»).
Влияние на способность к управлению транспортными средствами и механизмами
Прегабалин может вызвать головокружение и сонливость и, соответственно, повлиять на способность управлять автомобилем и пользоваться сложной техникой. Пациенты не должны управлять автомобилем, пользоваться сложной техникой или выполнять другие потенциально опасные виды деятельности, пока не станет ясно, влияет ли этот препарат на выполнение ими таких задач.
Беременность и лактация
Беременность
Имеются ограниченные данные о применении прегабалина у беременных женщин.
Данные, полученные в ходе наблюдательного исследования, которое включало более случаев 2700 беременности, во время которых отмечалось воздействие прегабалина, на основании данных, регулярно собираемых из административных и медицинских реестров Дании, Финляндии, Норвегии и Швеции, не указывают на существенное повышение риска серьезных врожденных пороков развития, неблагоприятных исходов родов или патологических исходов в отношении развития нервной системы в постнатальном периоде для беременностей, во время которых отмечалось воздействие прегабалина.
Тяжелые врожденные пороки развития
Скорректированные отношения распространенности и 95% доверительные интервалы (ДИ) в стандартном мета-анализе для воздействия монотерапии прегабалином в I триместре по сравнению с отсутствием воздействия противоэпилептических препаратов составляли 1.13 (0.96-1.33).
Исходы родов и исходы в отношении развития нервной системы в постнатальном периоде
Статистически значимые данные для мертворождения, низкой массы тела при рождении, преждевременных родов, малых размеров плода для гестационного возраста, низкой оценки по шкале Апгар и микроцефалии отсутствовали.
Для популяции пациентов детского возраста, подвергшейся внутриутробному воздействию, исследование не выявило повышенного риска развития синдрома дефицита внимания и гиперактивности (СДВГ), расстройств аутистического спектра (РАС) и нарушений умственного развития.
При применении у животных препарат оказывал токсическое действие на репродуктивную функцию. Прегабалин не следует применять во время беременности, если польза для матери явно не превышает потенциальный риск для плода. При лечении прегабалином женщины репродуктивного возраста должны пользоваться адекватными методами контрацепции.
Период грудного вскармливания
Прегабалин выводится с грудным молоком. Т.к. безопасность применения прегабалина у новорожденных неизвестна, во время лечения прегабалином не рекомендуется кормить грудью. Следует прекратить грудное вскармливание или отменить терапию прегабалином, принимая во внимание необходимость терапии для матери и грудное вскармливание для новорожденного.
Фертильность
Клинических данных о влиянии прегабалина на фертильность женщин с сохраненной детородной функцией нет.
Применение в детском возрасте
Противопоказано применение в возрасте до 17 лет включительно (нет данных по применению).
При нарушениях функции почек
С осторожностью следует назначать препарат при почечной недостаточности. У пациентов с нарушенной функцией почек дозу подбирают индивидуально с учетом КК.
При нарушениях функции печени
У пациентов с нарушением функции печени коррекции дозы не требуется.
Применение в пожилом возрасте
Пациентам пожилого возраста (старше 65 лет) может потребоваться снижение дозы прегабалина в связи со снижением функции почек.
Условия отпуска из аптек
Препарат отпускают по рецепту.
Условия и сроки хранения
Препарат следует хранить в недоступном для детей месте при температуре не выше 25°C. Срок годности — 3 года. Не применять по истечении срока годности, указанного на упаковке.
Описание препарата ЛИРИКА основано на официально утвержденной инструкции по применению и утверждено компанией–производителем.
Предоставленная информация о ценах на препараты не является предложением о продаже или покупке товара. Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в соответствии со статьей 55 ФЗ «Об обращении лекарственных средств».
Обнаружили ошибку? Выделите ее и нажмите Ctrl+Enter.
Лирика® (Lyrica®) инструкция по применению
📜 Инструкция по применению Лирика®
💊 Состав препарата Лирика®
✅ Применение препарата Лирика®
📅 Условия хранения Лирика®
⏳ Срок годности Лирика®
Описание лекарственного препарата
Лирика®
(Lyrica®)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для печатного издания справочника Видаль 2023 года.
Дата обновления: 2023.09.25
Владелец регистрационного удостоверения:
Контакты для обращений:
ВИАТРИС ООО
(Россия)
Код ATX:
N03AX16
(Прегабалин)
Лекарственные формы
| Лирика® |
Капс. 25 мг: 14, 56, 84 или 100 шт. рег. №: ЛС-001752 |
|
|
Капс. 50 мг: 14, 56, 84 или 100 шт. рег. №: ЛС-001752 |
||
|
Капс. 75 мг: 14, 56, 84 или 100 шт. рег. №: ЛС-001752 |
||
|
Капс. 100 мг: 14, 56, 84 или 100 шт. рег. №: ЛС-001752 |
||
|
Капс. 150 мг: 14, 56, 84 или 100 шт. рег. №: ЛС-001752 |
||
|
Капс. 200 мг: 14, 56, 84 или 100 шт. рег. №: ЛС-001752 |
||
|
Капс. 300 мг: 14, 56, 84 или 100 шт. рег. №: ЛС-001752 |
Форма выпуска, упаковка и состав
препарата Лирика®
Капсулы твердые желатиновые, №4, с крышечкой белого цвета и корпусом белого цвета; черными чернилами на корпусе капсулы указаны дозировка и код продукта — «PGN 25», на крышечке — «Pfizer»; содержимое капсул — порошок белого или почти белого цвета.
Вспомогательные вещества: лактозы моногидрат — 35 мг, крахмал кукурузный — 20 мг, тальк — 20 мг.
Состав корпуса капсулы: титана диоксид — 0.557 мг (1.47%), натрия лаурилсульфат — 0.046 мг (0.12%) (max), вода — 3.306 мг (8.7%), желатин — 18.892 мг (49.72%) qsp до 100%.
Состав крышечки капсулы: титана диоксид — 0.371 мг (0.98%), натрия лаурилсульфат — 0.03 мг (0.08%) (max), вода — 2.204 мг (5.8%), желатин — 12.594 мг (33.14%) qsp до 100%.
Состав чернил: шеллак (24-27%), этанол (23-26%), изопропанол (0.5-3%), бутанол (0.5-3%), пропиленгликоль (3-7%), аммиака раствор концентрированный (1-2%), калия гидроксид (0.05-0.1%), вода очищенная (15-18%), краситель железа оксид черный (24-28%).
10 шт. — блистеры (10) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (1) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
21 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
Капсулы твердые желатиновые, №3, с крышечкой белого цвета и корпусом белого цвета с черной полосой; черными чернилами на корпусе капсулы указаны дозировка и код продукта — «PGN 50», на крышечке — «Pfizer»; содержимое капсул — порошок белого или почти белого цвета.
Вспомогательные вещества: лактозы моногидрат — 70 мг, крахмал кукурузный — 40 мг, тальк — 40 мг.
Состав корпуса капсулы: титана диоксид — 0.703 мг (1.46%), натрия лаурилсульфат — 0.058 мг (0.12%) (max), вода — 4.176 мг (8.7%), желатин — 23.863 мг (49.71%) qsp до 100%.
Состав крышечки капсулы: титана диоксид — 0.469 мг (0.98%), натрия лаурилсульфат — 0.038 мг (0.08%) (max), вода — 2.784 мг (5.8%), желатин — 15.909 мг (33.14%) qsp до 100%.
Состав чернил: шеллак (24-27%), этанол (23-26%), изопропанол (0.5-3%), бутанол (0.5-3%), пропиленгликоль (3-7%), аммиака раствор концентрированный (1-2%), калия гидроксид (0.05-0.1%), вода очищенная (15-18%), краситель железа оксид черный (24-28%).
10 шт. — блистеры (10) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (1) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
21 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
Капсулы твердые желатиновые, №4, с крышечкой от красно-коричневого до темно-красно-коричневого цвета* и корпусом белого цвета; черными чернилами на корпусе капсулы указаны дозировка и код продукта — «PGN 75», на крышечке — «Pfizer»; содержимое капсул — порошок белого или почти белого цвета.
Вспомогательные вещества: лактозы моногидрат — 8.25 мг, крахмал кукурузный — 8.375 мг, тальк — 8.375 мг.
Состав корпуса капсулы: титана диоксид — 0.557 мг (1.47%), натрия лаурилсульфат — 0.046 мг (0.12%) (max), вода — 3.306 мг (8.7%), желатин — 18.892 мг (49.72%) qsp до 100%.
Состав крышечки капсулы: краситель железа оксид красный — 0.264 мг (0.69%), титана диоксид — 0.062 мг (0.16%), натрия лаурилсульфат — 0.03 мг (0.08%) (max), вода — 2.204 мг (5.8%), желатин — 12.64 мг (33.26%) qsp до 100%.
Состав чернил: шеллак (24-27%), этанол (23-26%), изопропанол (0.5-3%), бутанол (0.5-3%), пропиленгликоль (3-7%), аммиака раствор концентрированный (1-2%), калия гидроксид (0.05-0.1%), вода очищенная (15-18%), краситель железа оксид черный (24-28%).
10 шт. — блистеры (10) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (1) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
21 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
Капсулы твердые желатиновые, №3, с крышечкой от красно-коричневого до темно-красно-коричневого цвета* и корпусом от красно-коричневого до темно-красно-коричневого цвета*; черными чернилами на корпусе капсулы указаны дозировка и код продукта — «PGN 100», на крышечке — «Pfizer»; содержимое капсул — порошок белого или почти белого цвета.
Вспомогательные вещества: лактозы моногидрат — 11 мг, крахмал кукурузный — 11.17 мг, тальк — 11.17 мг.
Состав корпуса капсулы: краситель железа оксид красный — 0.5 мг (1.04%), титана диоксид — 0.118 мг (0.25%), натрия лаурилсульфат — 0.058 мг (0.12%) (max), вода — 4.176 мг (8.7%), желатин — 23.949 мг (49.89%) qsp до 100%.
Состав крышечки капсулы: краситель железа оксид красный — 0.333 мг (0.69%), титана диоксид — 0.079 мг (0.16%), натрия лаурилсульфат — 0.038 мг (0.08%) (max), вода — 2.784 мг (5.8%), желатин — 15.966 мг (33.26%) qsp до 100%.
Состав чернил: шеллак (24-27%), этанол (23-26%), изопропанол (0.5-3%), бутанол (0.5-3%), пропиленгликоль (3-7%), аммиака раствор концентрированный (1-2%), калия гидроксид (0.05-0.1%), вода очищенная (15-18%), краситель железа оксид черный (24-28%).
10 шт. — блистеры (10) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (1) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
21 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
Капсулы твердые желатиновые, №2, с крышечкой белого цвета и корпусом белого цвета; черными чернилами на корпусе капсулы указаны дозировка и код продукта — «PGN 150», на крышечке — «Pfizer»; содержимое капсул — порошок белого или почти белого цвета.
Вспомогательные вещества: лактозы моногидрат — 16.5 мг, крахмал кукурузный — 16.75 мг, тальк — 16.75 мг.
Состав корпуса капсулы: титана диоксид — 0.894 мг (1.47%), натрия лаурилсульфат — 0.073 мг (0.12%) (max), вода — 5.307 мг (8.7%), желатин — 30.326 мг (49.71%) qsp до 100%.
Состав крышечки капсулы: титана диоксид — 0.596 мг (0.98%), натрия лаурилсульфат — 0.049 мг (0.08%) (max), вода — 3.538 мг (5.8%), желатин — 20.217 мг (33.14%) qsp до 100%.
Состав чернил: шеллак (24-27%), этанол (23-26%), изопропанол (0.5-3%), бутанол (0.5-3%), пропиленгликоль (3-7%), аммиака раствор концентрированный (1-2%), калия гидроксид (0.05-0.1%), вода очищенная (15-18%), краситель железа оксид черный (24-28%).
10 шт. — блистеры (10) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (1) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
21 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
Капсулы твердые желатиновые, №1, с крышечкой от светло-красно-коричневого до красно-коричневого цвета* и корпусом от светло-красно-коричневого до красно-коричневого цвета*; черными чернилами на корпусе капсулы указаны дозировка и код продукта — «PGN 200», на крышечке — «Pfizer»; содержимое капсул — порошок белого или почти белого цвета.
Вспомогательные вещества: лактозы моногидрат — 22 мг, крахмал кукурузный — 22.34 мг, тальк — 22.34 мг.
Состав корпуса капсулы: краситель железа оксид красный — 0.201 мг (0.26%), титана диоксид — 0.189 мг (0.25%), натрия лаурилсульфат — 0.091 мг (0.12%) (max), вода — 6.612 мг (8.7%), желатин — 38.507 мг (50.67%) qsp до 100%.
Состав крышечки капсулы: краситель железа оксид красный — 0.134 мг (0.18%), титана диоксид — 0.126 мг (0.17%), натрия лаурилсульфат — 0.061 мг (0.08%) (max), вода — 4.408 мг (5.8%), желатин — 25.672 мг (33.78%) qsp до 100%.
Состав чернил: шеллак (24-27%), этанол (23-26%), изопропанол (0.5-3%), бутанол (0.5-3%), пропиленгликоль (3-7%), аммиака раствор концентрированный (1-2%), калия гидроксид (0.05-0.1%), вода очищенная (15-18%), краситель железа оксид черный (24-28%).
10 шт. — блистеры (10) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (1) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
21 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
Капсулы твердые желатиновые, №0, с крышечкой от красно-коричневого до темно-красно-коричневого цвета* и корпусом белого цвета, черными чернилами на корпусе капсулы указаны дозировка и код продукта «PGN 300», на крышечке — «Pfizer»; содержимое капсул — порошок белого или почти белого цвета.
Вспомогательные вещества: лактозы моногидрат — 33 мг, крахмал кукурузный — 33.5 мг, тальк — 33.5 мг.
Состав корпуса капсулы: титана диоксид — 1.407 мг (1.47%), натрия лаурилсульфат — 0.115 мг (0.12%) (max), вода — 8.352 мг (8.7%), желатин — 47.726 мг (49.71%) qsp до 100%.
Состав крышечки капсулы: краситель железа оксид красный — 0.667 мг (0.69%), титана диоксид — 0.157 мг (0.16%), натрия лаурилсульфат — 0.077 мг (0.08%) (max), вода — 5.568 мг (5.8%), желатин — 31.931 мг (33.26%) qsp до 100%.
Состав чернил: шеллак (24-27%), этанол (23-26%), изопропанол (0.5-3%), бутанол (0.5-3%), пропиленгликоль (3-7%), аммиака раствор концентрированный (1-2%), калия гидроксид (0.05-0.1%), вода очищенная (15-18%), краситель железа оксид черный (24-28%).
10 шт. — блистеры (10) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (1) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
21 шт. — блистеры (4) — пачки картонные с контролем первого вскрытия.
* в оригинальных сертификатах производителя данные цвета описаны так: «от красно-коричневого до темно-красно-коричневого цвета» — «orange», от светло-красно-коричневого до красно-коричневого цвета» — «light orange», что соответствует цвету понтонов сравнения, используемых в Европейском Союзе при проведении данного вида анализа.
Фармакологическое действие
Действующим веществом является прегабалин — аналог гамма-аминомасляной кислоты ((S)-3-(аминометил)-5-метилгексановая кислота).
Механизм действия
Было установлено, что прегабалин связывается с дополнительной субъединицей (α2-дельта-протеин) потенциал-зависимых кальциевых каналов в ЦНС, необратимо замещая [3Н]-габапентин. Предполагается, что такое связывание может способствовать проявлению его анальгетического и противосудорожного эффектов.
Нейропатическая боль
Эффективность прегабалина отмечена у пациентов с диабетической невропатией и постгерпетической невралгией.
Установлено, что при приеме прегабалина курсами до 13 недель по 2 раза/сут и до 8 недель по 3 раза/сут, в целом риск развития побочных эффектов и эффективность препарата при приемах по 2 или по 3 раза/сут одинаковы.
При приеме курсом продолжительностью до 13 недель боль уменьшалась в течение первой недели, а эффект сохранялся до конца лечения.
Отмечалось уменьшение индекса боли на 50% у 35% пациентов, получавших прегабалин, и 18% пациентов, принимавших плацебо. Среди пациентов, не испытывавших сонливости, эффект такого снижения боли отмечался у 33% пациентов группы прегабалина и 18% пациентов группы плацебо. У 48% пациентов, принимавших прегабалин, и у 16% пациентов, принимавших плацебо, возникала сонливость.
Фибромиалгия
Выраженное снижение болевой симптоматики, связанной с фибромиалгией, отмечается при применении прегабалина в дозах от 300 мг до 600 мг/сут. Эффективность доз 450 и 600 мг/сут сравнима, однако переносимость 600 мг/сут обычно хуже.
Также применение прегабалина связано с заметным улучшением в функциональной активности пациентов и снижением выраженности нарушений сна. Применение прегабалина в дозе 600 мг/сут приводило к более выраженному улучшению сна, по сравнению с дозой 300-450 мг/сут.
Эпилепсия
При приеме препарата в течение 12 недель по 2 или 3 раза/сут отмеченные риск развития побочных эффектов и эффективность препарата при этих режимах дозирования одинаковы. Уменьшение частоты судорог начиналось в течение первой недели.
Генерализованное тревожное расстройство
Уменьшение симптоматики генерализованного тревожного расстройства отмечается на первой неделе лечения. При применении препарата в течение 8 недель у 52% пациентов, получавших прегабалин, и у 38% пациентов, получавших плацебо, отмечалось 50% уменьшение симптоматики по шкале тревожности Гамильтона (HAM-A).
В клинических исследованиях у пациентов, постоянно получавших прегабалин, побочные реакции со стороны органа зрения (такие как затуманивание зрения, снижение остроты зрения, изменения полей зрения) отмечались чаще (за исключением изменений глазного дна), чем у пациентов, получавших плацебо (см. раздел «Особые указания»).
Фармакокинетика
Параметры фармакокинетики прегабалина в равновесном состоянии у здоровых добровольцев, у пациентов с эпилепсией, получавших противоэпилептическую терапию, и у пациентов, получавших его по поводу хронических болевых синдромов, были аналогичны.
Всасывание
Прегабалин быстро всасывается натощак. Сmax прегабалина в плазме достигается через 1 ч как при однократном, так и повторном применении. Биодоступность прегабалина при приеме внутрь составляет ≥90% и не зависит от дозы. При повторном применении Css достигается через 24-48 ч. При применении препарата после приема пищи Cmax снижается примерно на 25-30%, а Tmax увеличивается приблизительно до 2.5 ч. Однако прием пищи не оказывает клинически значимого влияния на общее всасывание прегабалина.
Распределение
Кажущийся Vd прегабалина после приема внутрь составляет примерно 0.56 л/кг. Прегабалин не связывается с белками плазмы.
В исследованиях прегабалина на животных отмечали, что он проникает через ГЭБ у мышей, крыс и обезьян. Также было показано, что прегабалин может проникать через плацентарный барьер, и обнаруживается в молоке у крыс во время лактации.
Метаболизм
Прегабалин практически не подвергается метаболизму. После приема меченного прегабалина примерно 98% радиоактивной метки определялось в моче в неизмененном виде. Доля N-метилированного производного прегабалина, который является основным метаболитом, обнаруживаемым в моче, составляла 0.9% дозы. В доклинических исследованиях не отмечено признаков рацемизации S-энантиомера прегабалина в R-энантиомер.
Выведение
Прегабалин выводится в основном почками в неизмененном виде.
Средний Т1/2 составляет 6.3 ч. Клиренс прегабалина из плазмы и почечный клиренс прямо пропорциональны КК. У пациентов с нарушенной функцией почек и пациентов, находящихся на гемодиализе, необходима коррекция дозы (см. раздел «Режим дозирования»).
Линейность/нелинейность
Фармакокинетика прегабалина в диапазоне рекомендуемых суточных доз носит линейный характер, межиндивидуальная вариабельность низкая (<20%). Фармакокинетику прегабалина при повторном применении можно предсказать на основании данных приема однократной дозы. Следовательно, необходимости в регулярном мониторировании концентрации прегабалина нет.
Фармакокинетика у особых групп пациентов
Пол. Пол пациента не оказывает клинически значимого влияния на концентрацию прегабалина в плазме.
Нарушение функции почек. Клиренс прегабалина прямо пропорционален КК. Учитывая, что прегабалин в основном выводится почками, у пациентов с нарушенной функцией почек рекомендуется снизить дозу прегабалина. Кроме того, прегабалин эффективно удаляется из плазмы при гемодиализе (после 4-часового сеанса гемодиализа концентрации прегабалина в плазме снижаются примерно на 50%), после гемодиализа необходимо назначить дополнительную дозу препарата (см. раздел «Режим дозирования»).
Нарушение функции печени. Фармакокинетика прегабалина у пациентов с нарушением функции печени специально не изучалась. Прегабалин практически не подвергается метаболизму и выводится в основном в неизмененном виде с мочой, поэтому нарушение функции печени не должно существенно изменять концентрации прегабалина в плазме.
Пожилые пациенты (старше 65 лет). Клиренс прегабалина с возрастом имеет тенденцию к снижению, что отражает возрастное снижение КК. Пациентам пожилого возраста с нарушенной функцией почек может потребоваться снижение дозы препарата (см. раздел «Режим дозирования»).
Показания препарата
Лирика®
Нейропатическая боль:
- лечение нейропатической боли у взрослых.
Эпилепсия:
- в качестве дополнительной терапии у взрослых с парциальными судорожными приступами, сопровождающимися или не сопровождающимися вторичной генерализацией.
Генерализованное тревожное расстройство:
- лечение генерализованного тревожного расстройства у взрослых.
Фибромиалгия:
- лечение фибромиалгии у взрослых.
Режим дозирования
Препарат принимают внутрь независимо от приема пищи в суточной дозе от 150 до 600 мг в 2 или 3 приема.
При нейропатической боли лечение начинают с дозы 150 мг/сут. В зависимости от достигнутого эффекта и переносимости через 3-7 дней дозу можно увеличить до 300 мг/сут, а при необходимости еще через 7 дней — до максимальной дозы 600 мг/сут.
При эпилепсии лечение начинают с дозы 150 мг/сут. С учетом достигнутого эффекта и переносимости через 1 неделю дозу можно увеличить до 300 мг/сут, а еще через неделю — до максимальной дозы 600 мг/сут.
При фибромиалгии лечение начинают с дозы по 75 мг 2 раза/сут (150 мг/сут). В зависимости от достигнутого эффекта и переносимости через 7 дней дозу можно увеличить до 300 мг/сут (150 мг 2 раза/сут). При отсутствии положительного эффекта дозу увеличивают до 450 мг/сут (225 мг 2 раза/сут), а при необходимости еще через 7 дней — до максимальной дозы 600 мг/сут. Следует учитывать, что доза 600 мг/сут не дает дополнительных преимуществ, но хуже переносится.
При генерализованном тревожном расстройстве лечение начинают с дозы 150 мг/сут. В зависимости от достигнутого эффекта и переносимости через 7 дней дозу можно увеличить до 300 мг/сут. При отсутствии положительного эффекта дозу увеличивают до 450 мг/сут, а при необходимости еще через 7 дней — до максимальной дозы 600 мг/сут.
Следует регулярно оценивать необходимость продолжения терапии.
Отмена прегабалина
Если лечение необходимо прекратить, рекомендуется делать это постепенно в течение минимум 1 недели.
У пациентов с нарушенной функцией почек дозу подбирают индивидуально с учетом КК (табл. 1), который рассчитывают по следующей формуле:
Для мужчин:
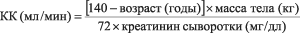
Для женщин:
КК (мл/мин)= значение КК для мужчин × 0.85
У пациентов, находящихся на гемодиализе, суточную дозу прегабалина подбирают с учетом функции почек. После 4-часового сеанса гемодиализа концентрации прегабалина в плазме крови снижаются примерно на 50%. Непосредственно после каждого 4-часового сеанса гемодиализа назначают дополнительную дозу (см. табл. 1).
Таблица 1. Подбор дозы прегабалина с учетом функции почек
У пациентов с нарушением функции печени коррекции дозы не требуется (см. раздел «Фармакокинетика»).
Пациентам пожилого возраста (старше 65 лет) может потребоваться снижение дозы прегабалина в связи со снижением функции почек (см. раздел «Фармакокинетика»).
Применение у детей до 12 лет и подростков (12-17 лет, включительно) — безопасность и эффективность прегабалина не установлены. Применение препарата у детей не рекомендуется.
В случае пропуска дозы прегабалина необходимо принять следующую дозу как можно скорее, однако не следует принимать пропущенную дозу, если время приема следующей уже подходит.
Побочное действие
По имеющемуся опыту клинического применения прегабалина у более чем 12000 пациентов, наиболее распространенными нежелательными явлениями были головокружение и сонливость. Наблюдаемые явления были обычно легкими или умеренными. Частота отмены прегабалина и плацебо из-за нежелательных реакций составила 14% и 7% соответственно. Основными нежелательными эффектами, требовавшими прекращения лечения, были головокружение (4%) и сонливость (3%), в зависимости от их субъективной переносимости. Другие побочные эффекты, которые также приводили к отмене препарата: атаксия, спутанность сознания, астения, нарушение внимания, нечеткость зрения, нарушение координации, периферические отеки.
Также отмечались нежелательные реакции, возникающие после отмены прегабалина: бессонница, головная боль, тошнота, тревога, гриппоподобный синдром, судороги, повышенная возбудимость, депрессия, боль, гипергидроз и диарея.
На фоне терапии центральной нейропатической боли, связанной с повреждением спинного мозга, наблюдается увеличение частоты побочных реакций в целом, а также побочных реакций со стороны ЦНС, в особенности сонливости.
В таблице перечислены все нежелательные явления, частота которых превышала таковую в группе плацебо (наблюдавшиеся более чем у 1 человека). Они распределены по системно-органным классам. Частота встречаемости нежелательных реакций определялась по количеству нежелательных явлений в массиве данных клинических исследований независимо от оценки причинно-следственной связи: очень часто (≥1/10), часто (≥1/100, <1/10), нечасто (≥1/1000, <1/100) и редко (<1/1000). Реакции, наблюдавшиеся во время пострегистрационного применения препарата, выделены курсивом.
Перечисленные нежелательные явления могут также быть связаны с основным заболеванием и/или сопутствующей терапией.
Противопоказания к применению
- повышенная чувствительность к действующему веществу или любому другому компоненту препарата;
- редкие наследственные заболевания, в т.ч. непереносимость галактозы, лактазная недостаточность и нарушение всасывания глюкозы/галактозы;
- детский и подростковый возраст до 17 лет включительно (нет данных по применению).
С осторожностью: почечная недостаточность (см. раздел «Режим дозирования»); хроническая сердечная недостаточность (см. раздел «Особые указания»); одновременное применение с опиоидами (см. раздел «Особые указания»).
В связи с зарегистрированными единичными случаями бесконтрольного применения прегабалина, препарат необходимо назначать с осторожностью пациентам с лекарственной зависимостью в анамнезе (такие пациенты нуждаются в пристальном медицинском наблюдении во время лечения препаратом).
Применение при беременности и кормлении грудью
Беременность
Имеются ограниченные данные о применении прегабалина у беременных женщин.
Данные, полученные в ходе наблюдательного исследования, которое включало более случаев 2700 беременности, во время которых отмечалось воздействие прегабалина, на основании данных, регулярно собираемых из административных и медицинских реестров Дании, Финляндии, Норвегии и Швеции, не указывают на существенное повышение риска серьезных врожденных пороков развития, неблагоприятных исходов родов или патологических исходов в отношении развития нервной системы в постнатальном периоде для беременностей, во время которых отмечалось воздействие прегабалина.
Тяжелые врожденные пороки развития
Скорректированные отношения распространенности и 95% доверительные интервалы (ДИ) в стандартном мета-анализе для воздействия монотерапии прегабалином в I триместре по сравнению с отсутствием воздействия противоэпилептических препаратов составляли 1.13 (0.96-1.33).
Исходы родов и исходы в отношении развития нервной системы в постнатальном периоде
Статистически значимые данные для мертворождения, низкой массы тела при рождении, преждевременных родов, малых размеров плода для гестационного возраста, низкой оценки по шкале Апгар и микроцефалии отсутствовали.
Для популяции пациентов детского возраста, подвергшейся внутриутробному воздействию, исследование не выявило повышенного риска развития синдрома дефицита внимания и гиперактивности (СДВГ), расстройств аутистического спектра (РАС) и нарушений умственного развития.
При применении у животных препарат оказывал токсическое действие на репродуктивную функцию. Прегабалин не следует применять во время беременности, если польза для матери явно не превышает потенциальный риск для плода. При лечении прегабалином женщины репродуктивного возраста должны пользоваться адекватными методами контрацепции.
Период грудного вскармливания
Прегабалин выводится с грудным молоком. Т.к. безопасность применения прегабалина у новорожденных неизвестна, во время лечения прегабалином не рекомендуется кормить грудью. Следует прекратить грудное вскармливание или отменить терапию прегабалином, принимая во внимание необходимость терапии для матери и грудное вскармливание для новорожденного.
Фертильность
Клинических данных о влиянии прегабалина на фертильность женщин с сохраненной детородной функцией нет.
Применение при нарушениях функции печени
У пациентов с нарушением функции печени коррекции дозы не требуется.
Применение при нарушениях функции почек
С осторожностью следует назначать препарат при почечной недостаточности. У пациентов с нарушенной функцией почек дозу подбирают индивидуально с учетом КК.
Применение у детей
Противопоказано применение в возрасте до 17 лет включительно (нет данных по применению).
Применение у пожилых пациентов
Пациентам пожилого возраста (старше 65 лет) может потребоваться снижение дозы прегабалина в связи со снижением функции почек.
Особые указания
Пациенты с сахарным диабетом
У части пациентов с сахарным диабетом в случае повышения массы тела на фоне лечения прегабалином может потребоваться коррекция доз гипогликемических препаратов.
Реакции гиперчувствительности
Прегабалин необходимо отменить в случае развития симптомов ангионевротического отека (таких как, отек лица, периоральный отек или отечность тканей верхних дыхательных путей).
Суицидальные мысли и поведение
Противоэпилептические препараты, включая прегабалин, могут повышать риск возникновения суицидальных мыслей или поведения. Поэтому пациентов, получающих эти препараты, следует тщательно наблюдать на предмет возникновения или ухудшения депрессии, появления суицидальных мыслей или поведения.
Снижение функции ЖКТ
При одновременном применении прегабалина и опиоидов следует рассмотреть необходимость проведения профилактических мер по предупреждению развития запоров (в особенности у пожилых пациентов и женщин).
Головокружение, сонливость, потеря сознания, спутанность сознания и нарушения когнитивных функций
Лечение прегабалином сопровождалось головокружением и сонливостью, которые повышают риск случайных травм (падений) у пожилых людей. В ходе пострегистрационного применения препарата отмечались также случаи потери сознания, спутанности сознания и нарушения когнитивных функций. Поэтому до тех пор, пока пациенты не оценят возможные эффекты препарата, они должны соблюдать осторожность.
Отмена сопутствующей терапии противосудорожными препаратами
Сведения о возможности отмены других противосудорожных средств при подавлении судорог прегабалином и целесообразности монотерапии этим препаратом недостаточны.
Имеются сообщения о развитии судорог, в т.ч. эпилептического статуса и малых припадков на фоне применения прегабалина или сразу после окончания терапии.
Влияние прегабалина на зрение
В клинических исследованиях у пациентов, постоянно получавших прегабалин, такой побочный эффект, как затуманивание зрения отмечался чаще, чем у пациентов, получавших плацебо. При этом указанный побочный эффект прекращался по мере продолжения лечения. В клинических исследованиях, во время которых проводили офтальмологическое обследование пациентов, снижение остроты зрения и изменения полей зрения чаще наблюдалось у пациентов, получающих прегабалин, чем у получающих плацебо. Частота изменений глазного дна была выше у пациентов, получающих плацебо.
Несмотря на то, что клиническое значение этих нарушений не установлено, пациентам следует сообщать врачу об изменениях зрения на фоне терапии прегабалином. В случае сохранения симптомов нарушения зрения следует продолжить наблюдение. Более частые проверки зрения следует проводить у пациентов, которые уже регулярно наблюдаются у офтальмолога. При появлении в ответ на применение прегабалина таких нежелательных реакций, как потеря зрения, нечеткость зрения или других нарушений со стороны органа зрения, отмена препарата может привести к исчезновению указанных симптомов.
Почечная недостаточность
Отмечались также случаи развития почечной недостаточности, в некоторых случаях после отмены прегабалина функция почек восстанавливалась.
Симптомы отмены прегабалина
В результате отмены прегабалина после длительной или краткосрочной терапии наблюдались следующие нежелательные явления: бессонница, головная боль, тошнота, диарея, гриппоподобный синдром, депрессия, потливость, головокружение, судороги и тревога. Имеющиеся данные свидетельствуют о том, что частота возникновения и тяжесть проявлений синдрома отмены могут зависеть от дозы прегабалина.
Злоупотребление прегабалином
Нет данных о том, что прегабалин активен в отношении рецепторов, отвечающих за развитие злоупотребления препаратом у пациентов. Во время пострегистрационных исследований отмечались случаи нарушения рекомендованного режима дозирования, злоупотребления и зависимости от прегабалина. Как и при применении любого лекарственного средства, влияющего на ЦНС, следует тщательно оценить анамнез пациента на предмет имеющихся случаев злоупотребления лекарственными средствами и/или психических расстройств. Пациенты должны наблюдаться на предмет нарушения рекомендованного режима дозирования, злоупотребления и зависимости от прегабалина (например, развитие устойчивости к терапии прегабалином, необоснованное повышение дозы препарата, аддиктивное поведение пациента).
Хроническая сердечная недостаточность
Несмотря на то, что очевидной взаимосвязи с концентрацией прегабалина в плазме крови и развитием сердечной недостаточности не отмечалось, в ходе пострегистрационного применения препарата сообщалось о развитии хронической сердечной недостаточности на фоне терапии прегабалином у некоторых пациентов. У пациентов без клинически выраженных признаков заболеваний сердца или сосудов не отмечалось связи между периферическими отеками и сердечно-сосудистыми осложнениями, такими как, повышение АД или хроническая сердечная недостаточность. Эти реакции преимущественно наблюдались у пациентов пожилого возраста, страдавших нарушениями функции сердца и получавших препарат по поводу невропатии. Поэтому прегабалин у данной категории пациентов следует применять с осторожностью. После отмены прегабалина возможно исчезновение проявлений подобных реакций.
Одновременное применение с опиоидами
Рекомендуется соблюдать осторожность при назначении прегабалина одновременно с опиоидами в связи с риском развития угнетения ЦНС. В наблюдательном исследовании с участием лиц, принимающих опиоиды, у пациентов, которые получали терапию прегабалином одновременно с опиоидом, наблюдался повышенный риск смертности, связанной с опиоидами, по сравнению с теми, кто принимал только опиоиды (скорректированное отношение шансов, 1.68 [95% ДИ, 1.19-2.36]).
Терапия центральной нейропатической боли, связанной с повреждением спинного мозга
Частота нежелательных явлений со стороны ЦНС, особенно таких как сонливость, повышается при лечении центральной нейропатической боли, обусловленной поражением спинного мозга, что, однако, может быть следствием суммирования эффектов прегабалина и других параллельно принимаемых средств (например, антиспастических). Это обстоятельство следует принимать во внимание при назначении прегабалина по данному показанию.
Энцефалопатия
Отмечались случаи энцефалопатии, особенно у пациентов с сопутствующими заболеваниями, которые могут привести к развитию данного состояния.
Женщины репродуктивного возраста/Контрацепция
Использование прегабалина в I триместре беременности может вызвать серьезные врожденные дефекты у будущего ребенка. Прегабалин не следует применять во время беременности, если польза для матери явно не превышает потенциальный риск для плода. Женщины репродуктивного возраста должны пользоваться адекватными методами контрацепции во время лечения (см. раздел «Беременность и лактация»).
Влияние на способность к управлению транспортными средствами и механизмами
Прегабалин может вызвать головокружение и сонливость и, соответственно, повлиять на способность управлять автомобилем и пользоваться сложной техникой. Пациенты не должны управлять автомобилем, пользоваться сложной техникой или выполнять другие потенциально опасные виды деятельности, пока не станет ясно, влияет ли этот препарат на выполнение ими таких задач.
Передозировка
Симптомы: при передозировке препарата (до 15 г) каких-либо из не описанных выше нежелательных реакций зарегистрировано не было. В ходе пострегистрационного применения наиболее частыми нежелательными явлениями, развивавшимися при передозировке прегабалина, являлись: аффективные расстройства, сонливость, спутанность сознания, депрессия, ажитация и беспокойство, в редких случаях были зарегистрированы случаи комы. Также отмечались судороги.
Лечение: проводят промывание желудка, поддерживающую терапию и при необходимости — гемодиализ (см. раздел «Режим дозирования» табл. 1).
Лекарственное взаимодействие
Прегабалин выводится с мочой в основном в неизмененном виде, подвергается минимальному метаболизму у человека (в виде метаболитов с мочой выводится менее 2% дозы), не ингибирует метаболизм других лекарственных веществ in vitro и не связывается с белками плазмы, поэтому вряд ли способен вступать в фармакокинетическое взаимодействие.
Исследования in vivo и популяционный фармакокинетический анализ
Не обнаружено признаков клинически значимого фармакокинетического взаимодействия прегабалина с фенитоином, карбамазепином, вальпроевой кислотой, ламотриджином, габапентином, лоразепамом, оксикодоном и этанолом. Установлено, что пероральные гипогликемические препараты, диуретики, инсулин, фенобарбитал, тиагабин и топирамат не оказывают клинически значимого влияния на клиренс прегабалина.
Пероральные контрацептивные препараты, норэтистерон и/или этинилэстрадиол
При применении пероральных контрацептивных препаратов, содержащих норэтистерон и/или этинилэстрадиол, одновременно с прегабалином равновесная фармакокинетика обоих препаратов не менялась.
Препараты, влияющие на ЦНС
Сообщалось о случаях нарушения дыхания, наступления комы и смерти при одновременном применении прегабалина с другими препаратами, угнетающими ЦНС, в т.ч. у пациентов, которые злоупотребляют психоактивными веществами.
Повторное пероральное применение прегабалина с оксикодоном, лоразепамом или этанолом не оказывало клинически значимого влияния на дыхание. Прегабалин, по-видимому, усиливает нарушения когнитивной и двигательной функций, вызванные оксикодоном. Прегабалин может усилить эффекты этанола и лоразепама.
Влияние на ЖКТ
Также сообщалось об отрицательном влиянии прегабалина на деятельность ЖКТ (в т.ч. развитие кишечной непроходимости, паралитического илеуса, запора) при одновременном применении с лекарственными средствами, вызывающими запор (такими как опиоиды) (см. раздел «Особые указания»).
Взаимодействие препаратов при применении у пожилых пациентов
Специальные исследования фармакодинамического взаимодействия с другими лекарственными средствами у пожилых пациентов не проводились.
Условия хранения препарата Лирика®
Препарат следует хранить в недоступном для детей месте при температуре не выше 25°C.
Срок годности препарата Лирика®
Срок годности — 3 года. Не применять по истечении срока годности, указанного на упаковке.
Условия реализации
Препарат отпускают по рецепту.
Контакты для обращений
ВИАТРИС ООО
(Россия)

|
|
ООО «Пфайзер» переименовано в ООО «Виатрис». ООО «Виатрис» 125315 Москва, Ленинградский пр-т, д. 72, к. 4 |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код