Форма выпуска, упаковка и состав
препарата Кломифен
10 шт. — банки темного стекла (1) — пачки картонные.
10 шт. — упаковки ячейковые контурные (1) — пачки картонные.
10 шт. — упаковки ячейковые контурные (2) — пачки картонные.
10 шт. — упаковки ячейковые контурные (3) — пачки картонные.
10 шт. — упаковки ячейковые контурные (4) — пачки картонные.
10 шт. — упаковки ячейковые контурные (10) — пачки картонные.
Фармакологическое действие
Стимулятор продукции гонадотропинов. Средство с антиэстрогенной и эстрогенной активностью. Имеет нестероидную структуру, которая близка к хлоротрианизену. Полагают, что действие кломифена обусловлено специфическим связыванием с эстрогенными рецепторами гипоталамуса и гипофиза, что повышает секрецию гонадотропных гормонов гипофиза. Это в свою очередь стимулирует созревание и эндокринную активность фолликула в яичнике, а также последующее образование и стимулирование функции желтого тела. В высоких дозах тормозит секрецию гонадотропинов. Не обладает гестагенной и андрогенной активностью.
Фармакокинетика
При приеме внутрь хорошо абсорбируется из ЖКТ. Метаболизируется в печени. Подвергается кишечно-печеночной рециркуляции. Т1/2 составляет 5-7 дней. Выводится в основном с желчью.
Показания активных веществ препарата
Кломифен
Ановуляторное бесплодие (индукция овуляции); аменорея (дисгонадотропная форма), вторичная аменорея, постконтрацептивная аменорея; синдром Штейна-Левенталя (синдром поликистозных яичников); олигоменорея; галакторея (на фоне опухоли гипофиза); синдром Киари-Фроммеля (синдром длительной послеродовой аменореи-галактореи); андрогенная недостаточность; у мужчин — олигоспермия.
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Принимают внутрь. Дозу и схему применения устанавливается индивидуально, в зависимости от показаний, схемы лечения и эффективности терапии.
Побочное действие
Со стороны пищеварительной системы: тошнота, рвота; редко — гастралгия, метеоризм, диарея, синдром острого живота.
Со стороны нервной системы: головная боль, головокружение, сонливость; редко — замедление скорости психических и двигательных реакций, повышенная возбудимость, депрессия, бессонница.
Со стороны органа зрения: нарушение восприятия света, двоение, размытость контуров, светобоязнь.
Со стороны мочевыделительной системы: учащение мочеиспускания; редко — полиурия.
Со стороны половой системы и молочных желез: уплотнение молочных желез, боли внизу живота, дисменорея, патологическое маточное кровотечение, увеличение размеров яичника (в т.ч. кистозное); редко — сухость влагалища, меноррагия.
Аллергические реакции: редко — сыпь, крапивница, аллергический дерматит, вазомоторные расстройства.
Прочие: редко — повышение аппетита, увеличение или снижение веса тела, алопеция, болезненность в области грудных желез, «приливы» крови к лицу.
Противопоказания к применению
Повышенная чувствительность к кломифену; печеночная и/или почечная недостаточность; беременность, период лактации (грудного вскармливания); киста яичников (за исключением синдрома поликистоза яичников); опухоль или гипофункция гипофиза; нарушения функции щитовидной железы или надпочечников; метроррагия неясной этиологии; длительно существующие или недавно развившиеся нарушения зрения; новообразования половых органов; эндометриоз; недостаточность яичников на фоне гиперпролактинемии.
Применение при беременности и кормлении грудью
Противопоказан к применению при беременности и в период лактации (грудного вскармливания).
Применение при нарушениях функции печени
Противопоказано применение при печеночной недостаточности.
Применение при нарушениях функции почек
Противопоказано применение при почечной недостаточности.
Особые указания
Рекомендуется до начала применения кломифена проверить функцию печени.
Перед применением кломифена следует обязательно провести тщательное гинекологическое обследование. Применение кломифена показано в случаях, когда суммарный уровень гонадотропина в моче ниже нижней границы нормы или на уровне нормы, пальпация яичников не выявляет отклонений от нормы, и функции щитовидной железы и надпочечников соответствуют норме.
При отсутствии созревания яйцеклетки следует до применения кломифена исключить или лечить все другие возможные причины бесплодия. Если обнаружено увеличение яичников или их кистозная трансформация, применение кломифена не разрешается до возвращения яичников к нормальным размерам. В дальнейшем следует уменьшить дозу или продолжительность лечения.
В процессе лечения необходимо постоянное наблюдение гинеколога, следует осуществлять контроль функции яичников, влагалищные исследования, наблюдать за феноменом «зрачка». Часто во время курса лечения трудно определить момент овуляции, а также часто наблюдается недостаточность желтого тела. Поэтому после зачатия рекомендуется начать профилактическое введение прогестерона.
При лечении кломифеном повышается вероятность многоплодной беременности, внематочной беременности, эндометриоза, роста имеющейся фибромы матки.
Горячие приливы, наблюдаемые во время курса лечения, прекращаются после окончания приема кломифена. Может также наблюдаться кистозное увеличение яичников, особенно при синдроме Штейна-Левенталя. В этих случаях размер яичников может достигать 4-8 см. При этом следует следить за температурой тела и прекращать лечение, как только она станет двухфазной.
Влияние на способность к управлению транспортными средствами и механизмами
В период лечения необходимо соблюдать осторожность при вождении автотранспорта и занятиях другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Лекарственное взаимодействие
Совместим с препаратами гонадотропных гормонов.
Состав
В одной таблетке содержится 50 мг активного вещества кломифена цитрата.
Дополнительными компонентами являются: желатин, лактоза, стеарат магния, крахмал, тальк.
Форма выпуска
Препарат выпускается в таблетированной форме.
Фармакологическое действие
Антиэстраген.
Фармакодинамика и фармакокинетика
Механизм действия основан на специфическом связывании рецепторов гипофиза и эстрогенных рецепторов яичников. При высоком содержании эстрогенов лекарственное средство оказывает антиэстрогенное влияние, при низком содержании эстрогенов проявляется умеренно выраженный эстрогенный эффект.
Малые дозы препарата Кломифен усиливают выработку ЛГ, ФСГ, пролактина и других гонадотропинов, усиливает овуляцию.
Большие дозировки лекарственного средства тормозят выработку гонадотропных гормонов. Кломифен не обладает андрогенной и гестагенной активностью.
Показания к применению
Кломифен назначают при дисфункциональных метроррагиях, синдроме поликистозных яичников, вторичной аменорее, галакторее, постконтрацептивной аменорее, синдроме Штейна-Левенталя, синдроме Киари-Фроммеля.
Лекарственное средство назначают для индукции овуляции при ановуляторном бесплодии, для диагностических целей при нарушениях в работе гипофиза (гонадотропная функция).
Противопоказания
Кломифен не назначают при метроррагиях неясного генеза, новообразованиях половых органов, при беременности, недостаточности яичников на фоне гиперпролактинемии, при эндометриозе, гипофункции гипофиза, новообразованиях гипофиза, при диагностированных кистах яичника, непереносимости активных компонентов, при патологии в работе почечной, печеночной систем.
Побочные действия
Пищеварительный тракт: диарея, метеоризм, гастралгия, рвота, тошнота, диспепсические расстройства.
Нервная система: сонливость, бессонница, повышенная возбудимость, головокружения, головные боли, замедление двигательной активности, снижение скорости психических реакций.
Мочеполовая система: увеличение размера яичников, меноррагия, дисменорея, боли внизу живота, полиурия, частое мочеиспускание.
Возможны аллергические реакции, алопеция, увеличение массы тела, ухудшение зрения, болезненность грудных желез.
Кломифен, инструкция по применению (Способ и дозировка)
Стимуляция овуляции: перед сном один раз в день принимают по 50 мг препарата Кломифен в течение пяти дней, начиная с пятого дня менструального цикла. При отсутствии менструации препарат принимают в любое время.
Если овуляция не развивается в течение месяца, то дозировку увеличивают до 150 мг в день, либо длительность терапии увеличивают на 10 дней. Максимальная курсовая доза – 1 грамм.
Овуляцию диагностируют по среднему, циклическому увеличению выработки ЛГ, наличию двухфазной базальной температуры, увеличению сывороточного прогестерона. Если беременность не наступает при диагностированной овуляции, то прием препарата Кломифен повторяют по схеме. Если после диагностированной овуляции не наступило менструальное кровотечение, то врач исключает/подтверждает беременность.
Лицам мужского пола назначают Кломифен в течение 3-4 месяцев 1-2 раза в сутки по 50 мг. Рекомендуется систематическая оценка спермограммы.
Передозировка
Проявляется нарушениями зрительного восприятия, «приливами» крови к лицу, тошнотой, рвотой, неврологической симптоматикой.
Требуется отмена препарата, указанные симптомы проходят самостоятельно.
Взаимодействие
Кломифен полностью совместим с лекарственными средствами гонадотропных гормонов.
Условия продажи
Требуется рецепт.
Условия хранения
В сухом, темном , недоступном для детей месте при температуре не более 25 градусов по Цельсию.
Срок годности
Не более трех лет.
Особые указания
Кломифен повышает вероятность многоплодной беременности. Эффективность препарата зависит от уровня эндогенных эстрогенов (при низкой концентрации гонадотропных гормонов гипофиза практически неэффективен; при достаточных концентрациях эндогенных эстрогенов эффективность высокая).
В период лечения требуется регулярное наблюдение гинеколога, оценка феномена «зрачка», контроль над работой яичников, оценка результатов влагалищного исследования.
Кломифен влияет на управление автотранспорта.
Аналоги
Совпадения по коду АТХ 4-го уровня:
Аналогами являются препараты: Кломид, Клостилбегит, Перготайм, Серофен, Серпафар.
Отзывы о Кломифене
Согласно отзывам, Кломифен эффективно помогает при ановуляторном бесплодии, дисфункциональных метроррагиях, синдроме поликистозных яичников, аменорее.
Цена Кломифена, где купить
Купить в аптеке Кломифена Цитрат довольно сложно. Чаще всего продаются такие аналоги лекарства, как, например, Клостилбегит. Цена в Украине данного средства около 640-700 гривен, в России — 550-700 рублей.
- Интернет-аптеки РоссииРоссия
ЛюксФарма* специальное предложение
-
Кломид (Кломифен) 50мг таб. №10
показать еще
Действующее вещество
— кломифена цитрат (clomifene)
Состав и форма выпуска препарата
| Таблетки | 1 таб. |
| кломифена цитрат | 50 мг |
10 шт. — банки темного стекла (1) — пачки картонные.
10 шт. — упаковки ячейковые контурные (1) — пачки картонные.
10 шт. — упаковки ячейковые контурные (2) — пачки картонные.
10 шт. — упаковки ячейковые контурные (3) — пачки картонные.
10 шт. — упаковки ячейковые контурные (4) — пачки картонные.
10 шт. — упаковки ячейковые контурные (10) — пачки картонные.
Фармакологическое действие
Стимулятор продукции гонадотропинов. Средство с антиэстрогенной и эстрогенной активностью. Имеет нестероидную структуру, которая близка к хлоротрианизену. Полагают, что действие кломифена обусловлено специфическим связыванием с эстрогенными рецепторами гипоталамуса и гипофиза, что повышает секрецию гонадотропных гормонов гипофиза. Это в свою очередь стимулирует созревание и эндокринную активность фолликула в яичнике, а также последующее образование и стимулирование функции желтого тела. В высоких дозах тормозит секрецию гонадотропинов. Не обладает гестагенной и андрогенной активностью.
Фармакокинетика
При приеме внутрь хорошо абсорбируется из ЖКТ. Метаболизируется в печени. Подвергается кишечно-печеночной рециркуляции. Т1/2 составляет 5-7 дней. Выводится в основном с желчью.
Показания
Ановуляторное бесплодие (индукция овуляции); аменорея (дисгонадотропная форма), вторичная аменорея, постконтрацептивная аменорея; синдром Штейна-Левенталя (синдром поликистозных яичников); олигоменорея; галакторея (на фоне опухоли гипофиза); синдром Киари-Фроммеля (синдром длительной послеродовой аменореи-галактореи); андрогенная недостаточность; у мужчин — олигоспермия.
Противопоказания
Повышенная чувствительность к кломифену; печеночная и/или почечная недостаточность; беременность, период лактации (грудного вскармливания); киста яичников (за исключением синдрома поликистоза яичников); опухоль или гипофункция гипофиза; нарушения функции щитовидной железы или надпочечников; метроррагия неясной этиологии; длительно существующие или недавно развившиеся нарушения зрения; новообразования половых органов; эндометриоз; недостаточность яичников на фоне гиперпролактинемии.
Дозировка
Принимают внутрь. Дозу и схему применения устанавливается индивидуально, в зависимости от показаний, схемы лечения и эффективности терапии.
Побочные действия
Со стороны пищеварительной системы: тошнота, рвота; редко — гастралгия, метеоризм, диарея, синдром острого живота.
Со стороны нервной системы: головная боль, головокружение, сонливость; редко — замедление скорости психических и двигательных реакций, повышенная возбудимость, депрессия, бессонница.
Со стороны органа зрения: нарушение восприятия света, двоение, размытость контуров, светобоязнь.
Со стороны мочевыделительной системы: учащение мочеиспускания; редко — полиурия.
Со стороны половой системы и молочных желез: уплотнение молочных желез, боли внизу живота, дисменорея, патологическое маточное кровотечение, увеличение размеров яичника (в т.ч. кистозное); редко — сухость влагалища, меноррагия.
Аллергические реакции: редко — сыпь, крапивница, аллергический дерматит, вазомоторные расстройства.
Прочие: редко — повышение аппетита, увеличение или снижение веса тела, алопеция, болезненность в области грудных желез, «приливы» крови к лицу.
Лекарственное взаимодействие
Совместим с препаратами гонадотропных гормонов.
Особые указания
Рекомендуется до начала применения кломифена проверить функцию печени.
Перед применением кломифена следует обязательно провести тщательное гинекологическое обследование. Применение кломифена показано в случаях, когда суммарный уровень гонадотропина в моче ниже нижней границы нормы или на уровне нормы, пальпация яичников не выявляет отклонений от нормы, и функции щитовидной железы и надпочечников соответствуют норме.
При отсутствии созревания яйцеклетки следует до применения кломифена исключить или лечить все другие возможные причины бесплодия. Если обнаружено увеличение яичников или их кистозная трансформация, применение кломифена не разрешается до возвращения яичников к нормальным размерам. В дальнейшем следует уменьшить дозу или продолжительность лечения.
В процессе лечения необходимо постоянное наблюдение гинеколога, следует осуществлять контроль функции яичников, влагалищные исследования, наблюдать за феноменом «зрачка». Часто во время курса лечения трудно определить момент овуляции, а также часто наблюдается недостаточность желтого тела. Поэтому после зачатия рекомендуется начать профилактическое введение прогестерона.
При лечении кломифеном повышается вероятность многоплодной беременности, внематочной беременности, эндометриоза, роста имеющейся фибромы матки.
Горячие приливы, наблюдаемые во время курса лечения, прекращаются после окончания приема кломифена. Может также наблюдаться кистозное увеличение яичников, особенно при синдроме Штейна-Левенталя. В этих случаях размер яичников может достигать 4-8 см. При этом следует следить за температурой тела и прекращать лечение, как только она станет двухфазной.
Влияние на способность к управлению транспортными средствами и механизмами
В период лечения необходимо соблюдать осторожность при вождении автотранспорта и занятиях другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Беременность и лактация
Противопоказан к применению при беременности и в период лактации (грудного вскармливания).
При нарушениях функции почек
Противопоказано применение при почечной недостаточности.
При нарушениях функции печени
Противопоказано применение при печеночной недостаточности.
Описание препарата КЛОМИФЕН основано на официально утвержденной инструкции по применению и утверждено компанией–производителем.
Предоставленная информация о ценах на препараты не является предложением о продаже или покупке товара. Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в соответствии со статьей 55 ФЗ «Об обращении лекарственных средств».
Обнаружили ошибку? Выделите ее и нажмите Ctrl+Enter.
МНН: Кломифен
Производитель: ФАРМАЦЕВТИЧЕСКИЙ ЗАВОД ЭГИС ЗАО
Анатомо-терапевтическо-химическая классификация: Clomifene
Номер регистрации в РК:
№ РК-ЛС-5№005861
Информация о регистрации в РК:
24.11.2016 — 24.11.2021
Номер регистрации в РБ:
2416/96/01/06/11/16
Информация о регистрации в РБ:
10.08.2016 — бессрочно
Информация о реестрах и регистрах
Информация по ценам и ограничения
Предельная цена закупа в РК:
361.21 KZT
- Скачать инструкцию медикамента
Торговое название
Клостилбегит ®
Международное непатентованное название
Кломифен
Лекарственная форма
Таблетки 50мг
Состав
Одна таблетка содержит
активное вещество — кломифена цитрат 50 мг,
вспомогательные вещества: лактозы моногидрат, крахмал картофельный, тальк Е-553b, желатин, магния стеарат Е-572, кислота стеариновая Е-570.
Описание
Круглые, плоские таблетки с фаской, с гравировкой в виде «CLO» на одной стороне, белого, желтовато-белого, или серовато-белого цвета; без или почти без запаха
Фармакотерапевтическая группа
Половые гормоны и модуляторы половой системы. Гонадотропины и другие стимуляторы овуляции. Стимуляторы овуляции синтетические. Кломифен
Код ATХ G03G B02
Фармакологические свойства
Фармакокинетика
После приема внутрь хорошо всасывается из желудочно-кишечного тракта. Кломифен метаболизируется в печени. Период полувыведения 5-7 дней. В течение 5 дней выводится 50% принятой внутрь дозы, главным образом через кишечник (42%) и мочой (8%). Кломифен обнаруживается в кале в течение 6 недель. Средний % выводимой дозы на 31-й – 35-й день после введения препарата меченого изотопом 14С в среднем составлял 0,73%, а на 42-й – 45-й день – 0,45%. Образцы кала и мочи брались у 6 испытуемых между 14 и 53 днями исследования. Не выведенное исходное вещество/метаболит медленно выводится в процессе энтерогепатической циркуляции. При длительном применении кломифен может измениться скорость синтеза холестерина. При длительном лечении кломифеном у пациентов может повыситься уровень холестерина в сыворотке крови.
Кломифена цитрат — рацемическая смесь цис-(зукломифен) и транс- (энкломифен) изомеров. Более активен цис-изомер, содержание которого в препарате составляет не менее 30-50%. Период полувыведения зукломифена более длительный, чем у транс-изомера. Зукломифен обнаруживается у здоровых добровольцев через месяц после приема. Этот факт указывает на кишечно-печеночную рециркуляцию препарата, которая обладает стереоспецифичностью. Кломифен может определяться в начале беременности у женщин, принимавших его для индукции овуляции.
Фармакодинамика
Клостилбегит — антиэстрогенный препарат нестероидной структуры. Механизм действия объясняется способностью специфически связываться с рецепторами эстрогенов в гипоталамусе, угнетая связывание эстрадиола с рецепторами. По принципу положительной обратной связи повышается выработка гонадотропина и, таким образом, происходит симуляция овуляции.
Показания к применению
— стимуляция овуляции у женщин с ановуляторным циклом с целью наступления беременности.
Таблетки Клостилбегит можно применять только пациенткам с доказанным нарушением овуляторного цикла. Перед назначением препарата Клостилбегит следует исключить или провести адекватное лечение других причин нарушения фертильности.
Способ применения и дозы
Препарат применяют строго по назначению врача!
1-ый курс лечения: рекомендуемая доза составляет 50 мг (1 таблетка) в сутки в течение 5 дней. При отсутствии недавнего маточного кровотечения лечение можно начинать в любой день.
Если планируется индукция кровотечения с помощью прогестина, либо при наличии спонтанных циклических кровотечениях рекомендуется начать лечение с 5-го дня цикла. Если овуляция наступает при применении дозы 50 мг, то дальнейшее повышение дозы в последующих циклах преимуществ не имеет.
2-ой курс лечения: эту схему следует применять при неэффективности 1-го курса лечения. Если овуляция не наступила после 1-го курса лечения, следует назначать ежедневно по 100 мг препарата (две таблетки 50 мг как однократную суточную дозу) в течение 5 дней, начиная с 5-го дня следующего цикла, то есть через 30 дней после предыдущего цикла. Не следует превышать дозу или длительность лечения (более, чем 100 мг/сут в течение 5 дней).
Большинство пациентов, способных реагировать на лечение, реагирует уже на первый курс лечения, Три курса лечения обычно можно считать адекватной терапевтической мерой. При отсутствии овуляционного кровотечения следует уточнить диагноз. У пациенток без признаков овуляции дальнейшее лечение не целесообразно.
Длительное лечение
Не рекомендуется
Специальные группы пациентов
У пациенток с повышенной чувствительностью к гипофизарному гонадотропину (например, при синдроме поликистозных яичников) следует соблюдать особую осторожность и, по возможности, назначать препарат в более низких дозах и в течение более короткого периода времени.
Побочные действия
Очень часто (1/10)
— вазомоторные приливы
— увеличение яичника
Часто (1/100 – <1/10)
— головная боль
— тошнота, рвота, метеоризм
— нарушение зрения (размытые пятна или вспышки в форме пятен, ощущение вибрирующего света в глазах — так называемые сцинтиллирующие скотомы, остаточное изображение)
— ощущение дискомфорта и болезненность молочных желез
— ациклическое маточное кровотечение, меноррагия
Нечасто (1/1000 –<1/100)
— депрессия
— головокружение
— вертиго (ощущение вращения)
— нервное напряжение, утомляемость
Редко (1/10 000 –<1/1000)
— катаракта, неврит зрительного нерва
— судорожные приступы
Частота неизвестна (нельзя определить на основании имеющихся данных)
— гормон-зависимые или связанные с гормонами новообразования/опухоли
— аллергические реакции
— гипертриглицеридемия
— параноидный психоз
— синкопальные состояния, острые нарушения мозгового кровообращения, тромбоз сосудов мозга
— нарушения функции нервной системы, дезориентация, нарушения речи
— панкреатит
— нарушение функции печени (изменение результатов бромсульфалеиновой пробы, желтуха)
— крапивница, сыпь, выпадение волос (алопеция)
— многоформная эритема, экхимозы, ангионевротический отек
— многоплодная беременность
— сочетание внематочной и маточной беременности
— внематочная беременность
— эндометриоз, ухудшение течения эндометриоза, уменьшение толщины эндометрия, значительное увеличение яичников
Проведенные исследования указывают, что побочные реакции развиваются более часто при длительном применении препарата и при использовании более высоких доз. При применении препарата в рекомендуемых дозах побочные реакции незначительны и лишь в редких случаях становятся помехой для лечения.
Увеличение яичников
При применении препарата в рекомендуемых дозах редко наблюдается увеличение яичников до патологических размеров, хотя в сравнении с обычными циклическими изменениями его размеров, увеличение может быть более выраженным. Аналогично, циклическая болезненность яичников может быть более выражена. При применении более высоких доз или продлении срока лечения увеличение яичников и формирование цист наблюдается более часто, кроме того, может удлиняться лютеиновая фаза овуляторного цикла.
В редких случаях сообщалось о выраженном увеличении яичников. Такой случай был описан у пациентки с синдромом поликистозных яичников, принимающей Клостилбегит в дозе 100 мг/сутки в течение 14 дней.
Не нормальное увеличение яичников обычно проходит спонтанно. У большинства пациенток с таким состоянием можно проводить консервативное лечение.
Нарушения со стороны органов зрения
С повышением общей дозы увеличивается частота развития симптомов, известных как «размытость» зрения, а также появление пятен или вспышек (мерцательная скотома). Также сообщалось о появлении последовательного образа («after-image»). Характерно, что первое появление или усиление этих симптомов со стороны органа зрения, в основном, наблюдается при ярком освещении. Имеются сообщения об офтальмологически подтвержденных скотомах, фосфенах и ухудшении остроты зрительного восприятия.
В редких случаях сообщалось о катаракте и неврите зрительного нерва. Эти зрительные нарушения обычно носят обратимый характер, хотя имелись сообщения о продолжительных нарушениях зрения после окончания лечения кломифеном. В некоторых случаях нарушение зрения может носить и необратимый характер, особенно при применении кломифена в высоких дозах или при его назначении в течение длительного периода времени.
Нарушения со стороны печени и желчевыводящих путей
С помощью бромсульфалеинового теста (БСФ) определяется количество выведенного из крови БСФ после внутривенного введения известного количества БСФ. Через 45 минут после внутривенного введения 5 мг/кг БСФ в крови остается только 5% дозы. Эта проба является эффективным методом выявления заболеваний, сопровождающихся поражением клеток печени и детоксицирующей функции печени, однако, этот метод не применим для диагностики внепеченочных заболеваний или для выявления внутрипеченочной обструктивной желтухи.
У 32 из 141 пациента, которым была проведена БСФ проба, задержка БСФ превышала 5%. Из входящих в эту группу 43 пациентов 5 человек принимали кломифен в рекомендованной в настоящее время дозе 50 мг. Ретенция БСФ обычно была минимальной, за исключением пациентов, постоянно принимавших кломифен на протяжении длительного времени или в случаях заболеваний печени, не связанных с приемом препарата. Результаты других печеночных проб обычно были нормальными.
В исследовании, в котором пациенты получали либо плацебо, либо кломифен в таблетках по 50 мг (по 3 дня в месяц в дозе 50 мг или 100 мг/сутки) в течение 6-месячного курса лечения БСФ тест проводился у 94 пациентов. Результаты, указывающие на задержку БСФ более 5%, были получены у 11 пациентов, 6 из которых принимали кломифен, а 5 – плацебо.
В другом исследовании сообщалось, что у одной пациентки, принимавшей кломифен таблетки в дозе 50 мг/сутки, на 19 день лечения развилась желтуха. Биопсия печени выявила холестаз без признаков гепатита.
Нарушения со стороны обмена веществ
Гипертриглицеридемия (в некоторых случаях с панкреатитом) наблюдалась у пациентов, страдавших или имевших в семейном анамнезе гипертриглицеридемию, и/или принимавших кломифен на протяжении периода времени или в дозах, превышающих рекомендуемые.
Противопоказания
— повышенная чувствительность к активному или вспомогательному веществу препарата
— нарушения функции печени или их наличие в анамнезе
— киста яичника (за исключением синдрома поликистоза яичников)
— метроррагия неясной этиологии
— гормон-зависимые опухоли
— эндометриоз
— дисгенез яичников, менопауза или любое состояние, при котором не ожидается ответа на лечение
— беременность
— детский и подростковый возраст до 18 лет
Лекарственные взаимодействия
Данные о лекарственном взаимодействии препарата Клостилбегит отсутствуют.
Особые указания
Рекомендуется регулярно контролировать функцию печени.
До начала лечения необходимо тщательное гинекологическое обследование пациентки.
Применение препарата должно быть под постоянным контролем гинеколога.
Необходимый уровень эндогенного эстрогена (определяемый на основании влагалищных мазков, биопсии эндометрия, определения уровня эстрогена в моче или эндометриального кровотечения в ответ на прогестерон) необходим для овуляции в ответ на лечение препаратом Клостилбегит. Пониженный уровень эстрогена — хотя с клинической точки зрения менее благоприятный – не исключает эффективность лечения. Лечение препаратом Клостилбегит не эффективно при первичной недостаточности гипофиза или яичников. Лечение препаратом Клостилбегит не замещает специального лечения недостаточности функции яичников, вызванной иными причинами, например, при заболеваниях щитовидной железы или надпочечников. Гиперпролактинемию также можно лечить другими методами. При бесплодии, связанном с низкой массой тела, Клостилбегит не является препаратом первого выбора, кроме того, этот препарат не влияет на повышенный уровень ФСГ, наблюдаемый при ранней менопаузе.
Синдром гиперстимуляции яичников (СГЯ)
Имеются сообщения о развитии СГЯ при назначении кломифена с целью индуцирования овуляции. При циклическом применении кломифена в некоторых случаях СГЯ развивался, когда кломифен комбинировали с гонадотропином. Симптомами этого синдрома, наблюдавшегося при применении кломифена, являются: перикардиальный выпот, анасарка, гидроторакс, острый живот, почечная недостаточность, отек легких, кровоизлияние в ткань яичника, тромбоз глубоких вен, перекручивание яичника и острая дыхательная недостаточность. При зачатии может начаться быстрое прогрессирование тяжелой формы синдрома.
С целью предотвращения опасности возможного увеличения яичников при лечении препаратом Клостилбегит, следует применять самые низкие дозы, достаточные для достижения хороших результатов лечения. Пациенток следует предупреждать, что в случае развития боли в области живота или в области органов малого таза, при увеличении массы тела, плохом самочувствии или метеоризме после приема таблеток Клостилбегит, следует сообщить врачу. Через несколько дней после отмены Клостилбегита, дальнейшее увеличение яичников не происходит. Пациентки с поликистозными яичниками с повышенной чувствительностью на гонадотропин, могут иметь и повышенную реакцию на обычно рекомендуемые дозы Клостилбегита.
Пациенток с жалобами на боли в области живота или в области органов малого таза, на увеличение массы тела, плохое самочувствие или метеоризм после приема таблеток Клостилбегит, необходимо обследовать по поводу возможной кисты яичника или других патологических изменений. Вследствие повышенной ранимости патологически увеличенных яичников, обследование области живота и таза следует проводить с исключительной осторожностью. При патологическом увеличении яичников Клостилбегит нельзя назначать до тех пор, пока размеры яичников не достигнут исходных (таковых до начала лечения). Увеличение и кисты яичников на фоне лечения кломифеном обычно спонтанно нормализуются через несколько дней или недель после отмены препарата. Большинству пациенток можно проводить консервативную терапию. В следующем цикле лечения дозу или продолжительность цикла следует уменьшить.
Изменение со стороны органа зрения
Пациенток следует предупреждать о возможном развитии размытости зрения или нарушения зрения типа точечной или мерцательной скотомы. Эти нарушения могут развиваться во время или вскоре после окончания лечения препаратом Клостилбегит. Обычно, эти изменения носят обратимый характер, хотя имелись сообщения о продолжительных нарушениях зрения после окончания лечения кломифеном. Нарушение зрения может носить и необратимый характер, особенно при применении кломифена в высоких дозах или при его назначении в течение длительного периода времени. Механизм таких нарушений зрения не известен. При жалобах на любое нарушение зрения лечение следует немедленно отменить и проконсультироваться с офтальмологом. Пациентов следует предупредить, что вследствие возможных нарушений зрения может возникнуть опасность при управлении транспортными средствами и работе с механизмами, особенно при неодинаковых световых условиях работы.
Гипертриглицеридемия
В пострегистрационном периоде сообщалось о случаях гипертриглицеридемии у пациенток, принимавших кломифен. Риск развития гипертриглицеридемии повышается у пациенток, страдавших или имевших в семейном анамнезе гипертриглицеридемию, и/или принимавших кломифен на протяжении более длительного периода времени или в дозах, превышающих рекомендуемые.
У таких пациенток рекомендуется регулярно определять уровень триглицеридов в плазме крови.
Многоплодная беременность
При зачатии на фоне лечения кломифеном повышается вероятность многоплодной беременности. Пациенток следует предупреждать о возможных осложнениях и рисках, связанных с многоплодной беременностью.
Эктопическая беременность
При зачатии на фоне лечения кломифеном в ряде случаев развивалась внематочная беременность (в яичниках или трубная). Имеются сообщения о случаях многоплодной беременности, при которых была внутри- и внематочная беременность.
Миома матки
Обследование пациенток с миомой матки, получавших Клостилбегит, следует проводить с осторожностью в связи с возможным дальнейшим ростом миомы.
Потеря беременности и врожденные дефекты
По литературным данным, средняя частота возникновения врожденных дефектов у матерей, получавших кломифен (до или после зачатия) не отличается от таковой, наблюдаемой в средней популяции сравнения. В опубликованных в литературе (спонтанные сообщения) случаях указывается, что при индукции овуляции кломифеном среди врожденных дефектов развития чаще встречаются дефекты развития нервной трубки, однако, исследования на популяционном уровне не подтверждают эти наблюдения.
Врачам следует в доступной для пациенток форме информировать их о возможной опасности и рисках, связанных как с естественной беременностью, так и при ее индукции с помощью кломифена. Пациенток следует информировать о том, что некоторые факторы и состояния могут стать факторами риска для их беременности. К таким факторам относятся: возраст женщины и мужчины, предыдущие спонтанные аборты, генотип Rh, нарушения менструального цикла и нарушения репродуктивной функции (независимо от причины) в анамнезе, органические заболевания сердца, диабет, возбудители инфекций (например, краснуха), наличие врожденных дефектов в семье и другие факторы риска. На основании результатов осмотра пациенток, им может быть показано генетическое обследование.
Были опубликованы результаты популяционных исследований о возможном повышении риска развития синдрома Дауна при индукции овуляции и о повышении частоты трисомии среди спонтанных абортов женщин с пониженной фертильностью, получавших лекарственные препараты для индукции овуляции (ни одна пациентка не получала монотерапию кломифеном без дополнительных индуцирующих препаратов). Однако количество сообщений еще недостаточно для того, чтобы подтвердить или опровергнуть повышенный риск. Этот вопрос можно решить с помощью амниоцентеза, проводимого по обычным показаниям (возраст, семейный анамнез).
В клинических исследованиях одноплодной или многоплодной беременности у пациенток, получавших кломифен, было установлено: потеря плода – 21,4% (частота абортов 19%), эктопическая беременность – 1,18%; молярная беременность – 0,17%; плод «бумажный» (foetus papyraceous) – 0,04%; беременности с одним или несколькими мертворождениями – 1,01%.
В клинических исследованиях кломифен применялся после зачатия в 158 случаях из 2369 закончившихся родами беременностей. Из этих 158 беременностей у 8 новорожденных (из 7 беременностей) были врожденные дефекты.
Не было выявлено различий в частоте врожденных дефектов у пациенток, которым кломифен назначался до 19 дня после зачатия или между 20-м и 35-м днями после зачатия. Эта частота соответствует ожидаемому частотному интервалу на общем популяционном уровне.
Рак яичника
Имеются редкие сообщения о развитии рака яичника при применении препаратов, улучшающих фертильность. Первичным фактором риска является само нарушение фертильности. Эпидемиологические данные указывают, что длительное применение Клостилбегита может повысить этот риск. Таким образом, не следует превышать рекомендуемую длительность лечения.
Лактоза
Каждая таблетка Клостилбегит содержит 100 мг лактозы. Это следует учитывать при назначении препарата пациентам с непереносимостью лактозы. При редких наследственных заболеваниях, в том числе лицам с непереносимостью фруктозы, дефицитом фермента Lapp-лактазы и мальабсорбцией глюкозы-галактозы препарат применять нельзя.
Беременность и период лактации
При подтверждении беременности прием препарата Клостилбегит следует отменить. Клостилбегит выделяется с грудным молоком, поэтому его применение в период лактации требует тщательного анализа риска и пользы.
Во избежании непреднамеренного назначения Клостилбегита на ранних стадиях беременности, во время каждого цикла лечения наличие овуляции следует определять с помощью соответствующих тестов. Перед каждым новым курсом лечения препаратом Клостилбегит следует проводить тест на беременность.
Особенности влияния лекарственного средства на способность управлять транспортным средством и потенциально опасными механизмами
В связи с преходящими нарушениями зрения в начале лечения препаратом, не рекомендуется управление транспортным средством и другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций, в особенности, при изменяющейся интенсивности освещения.
Передозировка
Симптомы: тошнота, рвота, вазомоторные приливы, нарушение зрения (снижение остроты зрения, вспышки света, скотома), увеличение яичников и боль в тазовых или брюшных органах.
Лечение: после отмены препарата рекомендуется симптоматическое лечение. Данных о возможном выведении препарата посредством диализа нет.
Форма выпуска и упаковка
По 10 таблеток во флаконе из коричневого стекла укупоренные ПЭ крышкой FG7 с контролем первого вскрытия и снабженные амортизатором-гармошкой.
На флакон наклеивают этикетку самоклеющуюся.
По 1 флакону вместе с инструкцией по медицинскому применению на государственном и русском языках помещают в картонную пачку.
Условия хранения
Хранить при температуре от 15°C до 25°C.
Хранить в недоступном для детей месте!
Срок хранения
5 лет
Не использовать по истечении срока годности.
Условия отпуска из аптек
По рецепту
Производитель
ЗАО «ФАРМАЦЕВТИЧЕСКИЙ ЗАВОД ЭГИС»
1106 БУДАПЕШТ, ул. Керестури, 30-38 Венгрия
Телефон: (36-1) 803-5555, факс: (36-1) 803-5529
Владелец регистрационного удостоверения
ЗАО «Фармацевтический завод ЭГИС», Венгрия
Адрес организации, принимающей на территории Республики Казахстан претензии от потребителей по качеству продукции (товара)
Представительство в РК ЗАО «Фармацевтический завод ЭГИС»
050060, г. Алматы, ул. Жарокова 286 Г
тел: + 7 (727) 247 63 34, + 7 (727) 247 63 33, факс: + 7 (727) 247 61 41,
e-mail: egis@egis.kz
| 039241071477977105_ru.doc | 98 кб |
| 375498211477978271_kz.doc | 111.5 кб |
| 2416_96_01_06_11_16_p.pdf | 0.38 кб |
| 2416_96_01_06_11_16_s.pdf | 0.66 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники. «Центр экспертиз и испытаний в здравоохранении» МЗ РБ
 |
|
 |
|
| Clinical data | |
|---|---|
| Trade names | Clomid, Serophene, others[1] |
| Other names | Clomiphene; Chloramifene; Chloramiphene; MRL-41; MRL/41; NSC-35770 |
| AHFS/Drugs.com | Monograph |
| Pregnancy category |
|
| Routes of administration |
By mouth |
| Drug class | Selective estrogen receptor modulator; Progonadotropin |
| ATC code |
|
| Legal status | |
| Legal status |
|
| Pharmacokinetic data | |
| Bioavailability | High (>90%) |
| Metabolism | Liver CYP2D6 (with enterohepatic circulation)[2] |
| Metabolites | 4-Hydroxyclomiphene (4-OH-CLO), 4-Hydroxy-N-desethylclomiphene (4-OH-DE-CLO) |
| Elimination half-life | 4 – 7 days [2][3][4]
active metabolites: 4-OH-DE-CLO : 15 — 37 hrs[2] |
| Excretion | Mainly feces, some in urine |
| Identifiers | |
|
IUPAC name
|
|
| CAS Number |
|
| PubChem CID |
|
| IUPHAR/BPS |
|
| DrugBank |
|
| ChemSpider |
|
| UNII |
|
| KEGG |
|
| ChEBI |
|
| ChEMBL |
|
| CompTox Dashboard (EPA) |
|
| ECHA InfoCard | 100.011.826 |
| Chemical and physical data | |
| Formula | C26H28ClNO |
| Molar mass | 405.966 g·mol−1 |
| 3D model (JSmol) |
|
|
SMILES
|
|
|
InChI
|
|
| |
Clomifene, also known as clomiphene, is a medication used to treat infertility in women who do not ovulate, including those with polycystic ovary syndrome.[5] Use results in a greater chance of twins.[5] It is taken by mouth once a day, with a course of treatment that usually lasts for five days.[5]
Common side effects include pelvic pain and hot flashes.[5] Other side effects can include changes in vision, vomiting, trouble sleeping, ovarian cancer, and seizures.[5][6] It is not recommended in people with liver disease or abnormal vaginal bleeding of unknown cause or who are pregnant.[6][7] Clomifene is in the selective estrogen receptor modulator (SERM) family of medication and is a nonsteroidal medication.[7][8] It works by causing the release of GnRH by the hypothalamus, and subsequently gonadotropin from the anterior pituitary.[6]
Clomifene was approved for medical use in the United States in 1967.[5] It is on the World Health Organization’s List of Essential Medicines, under the category «Ovulation inducers» (Complementary List).[9] Its introduction began the era of assisted reproductive technology.[10]
Clomifene (particularly the purified enclomiphene isomer) has also been found to have a powerful ability to boost or restore testosterone levels in hypogonadal men.[11]
Medical uses[edit]
Ovulation induction[edit]
Clomifene is one of several alternatives for ovulation induction in those who are infertile due to anovulation or oligoovulation.[12] Evidence is lacking for the use of clomifene in those who are infertile without a known reason.[13] In such cases, studies have observed a clinical pregnancy rate 5.6% per cycle with clomifene treatment vs. 1.3%–4.2% per cycle without treatment.[12]
Proper timing of the drug is important; it should be taken starting on about the fifth day of the cycle, and there should be frequent intercourse.[7][12][14]
The following procedures may be used to monitor induced cycles:[12]
- Follicular monitoring with vaginal ultrasound, starting 4–6 days after the last pill. Serial transvaginal ultrasound can reveal the size and number of developing follicles. It can also provide presumptive evidence of ovulation such as the sudden collapse of the preovulatory follicle, and an increase in fluid volume in the rectouterine pouch. After ovulation, it may reveal signs of luteinization such as loss of clearly defined follicular margins and appearance of internal echoes.
- Serum estradiol levels, starting 4–6 days after the last pill
- Adequacy of LH surge by urine LH surge tests 3 to 4 days after last clomifene pill
- Post-coital test 1–3 days before ovulation to check whether there are at least 5 progressive sperm per HPF
- Mid-luteal progesterone, with at least 10 ng/ml 7–9 days after ovulation being regarded as adequate.
Repeat dosing: This 5-day treatment course can be repeated every 30 days. The dosage may be increased by 50-mg increments in subsequent cycles until ovulation is achieved.[12] It is not recommended by the manufacturer to use clomifene for more than 6 cycles.[7][15]
It is no longer recommended to perform an ultrasound examination to exclude any significant residual ovarian enlargement before each new treatment cycle.[12]
Other uses[edit]
Clomifene has also been used with other assisted reproductive technology to increase success rates of these other modalities.[16]
Testosterone replacement therapy[edit]
Clomifene is sometimes used in the treatment of male hypogonadism as an alternative to testosterone replacement therapy.[17][non-primary source needed] The medication has been used at a dosage of 20 to 50 mg three times per week to once daily for this indication.[18] It has been found to increase testosterone levels by 2- to 2.5-times in hypogonadal men at such dosages.[17][18] Despite the use of questionnaires in testosterone replacement comparator trials being called into question, clomifene’s lower cost, therapeutic benefits, and greater value towards hypogonadism improvement have been noted.[19][non-primary source needed]
Clomifene consists of two stereoisomers in equal proportion: enclomifene and zuclomifene. Zuclomifene has pro-estrogenic properties, whereas enclomifene is pro-androgenic, i.e. it promotes testosterone production through stimulation of the HPG axis. For this reason, purified enclomifene isomer has been found to be twice as effective in boosting testosterone compared to the standard mix of both isomers.[11] Additionally, enclomifene has a half-life of just 10 hours,[4] but zuclomifene has a half-life on the order of several days to a week, so if the goal is to boost testosterone, taking regular clomifene may produce far longer-lasting pro-estrogenic effects than pro-androgenic effects.[20]
Gynecomastia[edit]
Clomifene has been used in the treatment of gynecomastia.[21] It has been found to be useful in the treatment of some cases of gynecomastia but it is not as effective as tamoxifen or raloxifene for this indication.[22] It has shown variable results for gynecomastia (probably because the zuclomifene isomer is estrogenic), and hence is not recommended for treatment of the condition.[23] Pure enclomifene isomer is likely to be more effective than clomifene at treating gynecomastia, because of the lack of the zuclomifene isomer (as noted above).
Due to its long half-life, zuclomifene can be detected in urine for at least 261 days after discontinuation[24] (261 days after discontinuation with a half-life of 30 days, there is still 0.24% of the peak level of zuclomifene being excreted, whereas with a half-life of 10 hours, enclomifene reaches the same 0.24% level in less than 4 days).
Because of its potential for boosting testosterone, clomifene is listed as banned for use by competitive sportsmen, both in and out of competition, by the World Anti-Doping Agency, absent an organic etiology of primary hypogonadism.
Contraindications[edit]
Contraindications include an allergy to the medication, pregnancy, prior liver problems, abnormal vaginal bleeding of unclear cause, ovarian cysts other than those due to polycystic ovarian syndrome, unmanaged adrenal or thyroid problems, and pituitary tumors.[7]
Side effects[edit]
The most common adverse drug reaction associated with the use of clomifene (>10% of people) is reversible ovarian enlargement.[7]
Less common effects (1–10% of people) include visual symptoms (blurred vision, double vision, floaters, eye sensitivity to light, scotomata), headaches, vasomotor flushes (or hot flashes), light sensitivity and pupil constriction, abnormal uterine bleeding and/or abdominal discomfort.[7]
Rare adverse events (<1% of people) include: high blood level of triglycerides, liver inflammation, reversible baldness and/or ovarian hyperstimulation syndrome.[7]
Clomifene can lead to multiple ovulation, hence increasing the chance of twins (10% of births instead of ~1% in the general population) and triplets.
Rates of birth defects and miscarriages do not appear to change with the use of clomifene for fertility.[7] Clomifene has been associated with liver abnormalities and a couple of cases of hepatotoxicity.[25]
Cancer risk[edit]
Some studies have suggested that clomifene if used for more than a year may increase the risk of ovarian cancer.[13] This may only be the case in those who have never been and do not become pregnant.[15] Subsequent studies have failed to support those findings.[12][26]
Clomifene has been shown to be associated with an increased risk of malignant melanomas and thyroid cancer.[3] Thyroid cancer risk was not associated with the number of pregnancies carried to viability.[27]
Pharmacology[edit]
Pharmacodynamics[edit]
Selective estrogen receptor modulator activity[edit]
Clomifene is a nonsteroidal triphenylethylene derivative that acts as a selective estrogen receptor modulator (SERM).[16] It consists of a non-racemic mixture of zuclomifene (~38%) and enclomifene (~62%), each of which has unique pharmacologic properties.[28] It is a mixed agonist and antagonist of the estrogen receptor (ER). Clomifene activates the ERα in the setting of low baseline estrogen levels and partially blocks the receptor in the context of high baseline estrogen levels.[18] Conversely, it is an antagonist of the ERβ.[18] Clomifene has antiestrogenic effects in the uterus.[29] There is little clinical research on the influence of clomifene in many target tissues, such as lipids, the cardiovascular system, and the breasts.[29][30] Positive effects of clomifene on bone have been observed.[18][29][30] Clomifene has been found to decrease insulin-like growth factor 1 (IGF-1) levels in women.[31]
Clomifene is a long-acting ER ligand, with a nuclear retention of greater than 48 hours.[32] Clomifene is a prodrug being activated via similar metabolic pathways as the related triphenylethylene SERMs tamoxifen and toremifene.[33][34] The affinity of clomifene for the ER relative to estradiol ranges from 0.1 to 12% in different studies, which is similar to the range for tamoxifen (0.06–16%).[35][36][37] 4-Hydroxyclomifene, a major active metabolite of clomifene, and afimoxifene (4-hydroxytamoxifen), a major active metabolite of tamoxifen, show 89–251% and 41–246% of the affinity of estradiol for the ER in human MCF-7 breast cancer cells, respectively.[38][39] The ER affinities of the isomers of 4-hydroxyclomifene were 285% for (E)-4-hydroxyclomifene and 16% for (Z)-4-hydroxyclomifene relative to estradiol.[38] 4-Hydroxy-N-desmethylclomifene has similar affinity to 4-hydroxyclomifene for the ER.[34] In one study, the affinities of clomifene and its metabolites for the ERα were ~100 nM for clomifene, ~2.4 nM for 4-hydroxyclomifene, ~125 nM for N-desmethylclomifene, and ~1.4 nM for 4-hydroxy-N-desmethylclomifene.[34]
Even though clomifene has some estrogenic effect, the antiestrogenic property is believed to be the primary source for stimulating ovulation.[5] Clomifene appears to act mostly in the hypothalamus where it depletes hypothalamic ERs and blocks the negative feedback effect of circulating endogenous estradiol, which in turn results in an increase in hypothalamic gonadotropin-releasing hormone (GnRH) pulse frequency and circulating concentrations of follicle-stimulating hormone (FSH) and luteinizing hormone (LH).
In normal physiologic female hormonal cycling, at 7 days past ovulation, high levels of estrogen and progesterone produced from the corpus luteum inhibit GnRH, FSH, and LH at the hypothalamus and anterior pituitary. If fertilization does not occur in the post-ovulation period the corpus luteum disintegrates due to a lack of human chorionic gonadotropin (hCG). This would normally be produced by the embryo in the effort of maintaining progesterone and estrogen levels during pregnancy.
Therapeutically, clomifene is given early in the menstrual cycle. It is typically prescribed beginning on day 3 and continuing for five days. By that time, FSH levels are rising steadily, causing the development of a few follicles. Follicles, in turn, produce the estrogen, which circulates in serum. In the presence of clomifene, the body perceives a low level of estrogen, similar to day 22 in the previous cycle. Since estrogen can no longer effectively exert negative feedback on the hypothalamus, GnRH secretion becomes more rapidly pulsatile, which results in increased pituitary gonadotropin release. (More rapid, lower amplitude pulses of GnRH lead to increased LH and FSH secretion, while more irregular, larger amplitude pulses of GnRH leads to a decrease in the ratio of LH to FSH.) Increased FSH levels cause the growth of more ovarian follicles, and subsequently rupture of follicles resulting in ovulation. Ovulation occurs most often 6 to 7 days after a course of clomifene.
In normal men, 50 mg/day clomifene for 8 months has been found to increase testosterone levels by around 870 ng/dL in younger men and by around 490 ng/dL in elderly men.[18] Estradiol levels increased by 62 pg/mL in younger men and by 40 pg/mL in elderly men.[18] These findings suggest that the progonadotropic effects of clomifene are stronger in younger men than in older men.[18] In men with hypogonadism, clomifene has been found to increase testosterone levels by 293 to 362 ng/dL and estradiol levels by 5.5 to 13 pg/mL.[18] In a large clinical study of men with low testosterone levels (<400 ng/dL), 25 mg/day clomifene increased testosterone levels from 309 ng/dL to 642 ng/dL after 3 months of therapy.[40] No significant changes in HDL cholesterol, triglycerides, fasting glucose, or prolactin levels were observed, although total cholesterol levels decreased significantly.[18][40]
| Medication | Breast | Bone | Liver | Uterus | Vagina | Brain | ||||
|---|---|---|---|---|---|---|---|---|---|---|
| Lipids | Coagulation | SHBGTooltip Sex hormone-binding globulin | IGF-1Tooltip Insulin-like growth factor 1 | Hot flashes | Gonadotropins | |||||
| Estradiol | + | + | + | + | + | + | + | + | + | + |
| «Ideal SERM» | – | + | + | ± | ± | ± | – | + | + | ± |
| Bazedoxifene | – | + | + | + | + | ? | – | ± | – | ? |
| Clomifene | – | + | + | ? | + | + | – | ? | – | ± |
| Lasofoxifene | – | + | + | + | ? | ? | ± | ± | – | ? |
| Ospemifene | – | + | + | + | + | + | ± | ± | – | ± |
| Raloxifene | – | + | + | + | + | + | ± | – | – | ± |
| Tamoxifen | – | + | + | + | + | + | + | – | – | ± |
| Toremifene | – | + | + | + | + | + | + | – | – | ± |
| Effect: + = Estrogenic / agonistic. ± = Mixed or neutral. – = Antiestrogenic / antagonistic. Note: SERMs generally increase gonadotropin levels in hypogonadal and eugonadal men as well as premenopausal women (antiestrogenic) but decrease gonadotropin levels in postmenopausal women (estrogenic). Sources: See template. |
Other activities[edit]
Clomifene is an inhibitor of the conversion of desmosterol into cholesterol by the enzyme 24-dehydrocholesterol reductase.[41][42] Concerns about possible induction of desmosterolosis and associated symptoms such as cataracts and ichthyosis with extended exposure precluded the use of clomifene in the treatment of breast cancer.[41][42] Continuous use of clomifene has been found to increase desmosterol levels by 10% and continuous high doses of clomifene (200 mg/day) have been reported to produce visual disturbances.[43][44]
Pharmacokinetics[edit]
Clomifene produces N-desmethylclomifene, clomifenoxide (clomifene N-oxide), 4-hydroxyclomifene, and 4-hydroxy-N-desmethylclomifene as metabolites.[2][45] Clomifene is a prodrug most importantly of 4-hydroxyclomifene and 4-hydroxy-N-desmethylclomifene, which are the most active of its metabolites.[33][34] In one study, the peak levels after a single 50 mg dose of clomifene were 20.37 nmol/L for clomifene, 0.95 nmol/L for 4-hydroxyclomifene, and 1.15 nmol/L for 4-hydroxy-N-desmethylclomifene.[2]
Clomifene has an onset of action of 5 to 10 days following course of treatment and an elimination half-life about 4 — 7days.[2][4] In one study, after a single 50 mg dose of clomifene, the half-life of clomifene was 128 hours (5.3 days), of 4-hydroxyclomifene was 13 hours, and of 4-hydroxy-N-desmethylclomifene was 15 hours.[2] Individuals with the CYP2D6*10 allele showed longer half-lives for 4-hydroxyclomifene and 4-hydroxy-N-desmethylclomifene.[2] Primarily due to differences in CYP2D6 genetics, steady state concentrations and individual response to clomifene are highly variable.[46]
Most clomifene metabolism occurs in the liver, where it undergoes enterohepatic recirculation. Clomifene and its metabolites are excreted primarily through feces (42%), and excretion can occur up to 6 weeks after discontinuation.[28]
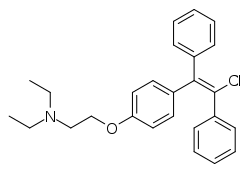
Chemistry[edit]
Clomifene is a triphenylethylene derivative. It is a mixture of two geometric isomers, the cis enclomifene ((E)-clomifene) form and trans zuclomifene ((Z)-clomifene) form. These two isomers contribute to the mixed estrogenic and antiestrogenic properties of clomifene.[10] The typical ratio of these isomers after synthesis is 38% zuclomiphene and 62% enclomiphene.[4] The United States Pharmacopeia specifies that clomifene preparations must contain between 30% and 50% zuclomiphene.[4]
History[edit]
A team at William S. Merrell Chemical Company led by Frank Palopoli synthesized clomifene in 1956; after its biological activity was confirmed a patent was filed and issued in November 1959.[10][47] Scientists at Merrell had previously synthesized chlorotrianisene and ethamoxytriphetol.[10] Clomifene was studied in the treatment of advanced breast cancer during the period of 1964 to 1974 and was found to be effective but was abandoned due to concerns about desmosterolosis with extended use.[41][48][49] Short-term use (e.g. days to months) did not raise the same concerns and clomifene continued to be studied for other indications.[42][43]
| Antiestrogen | Dosage | Year(s) | Response rate | Toxicity |
|---|---|---|---|---|
| Ethamoxytriphetol | 500–4,500 mg/day | 1960 | 25% | Acute psychotic episodes |
| Clomifene | 100–300 mg/day | 1964–1974 | 34% | Fears of cataracts |
| Nafoxidine | 180–240 mg/day | 1976 | 31% | Cataracts, ichthyosis, photophobia |
| Tamoxifen | 20–40 mg/day | 1971–1973 | 31% | Transient thrombocytopeniaa |
| Footnotes: a = «The particular advantage of this drug is the low incidence of troublesome side effects (25).» «Side effects were usually trivial (26).» Sources: [48][50] |
Clinical studies were conducted under an Investigational New Drug Application; clomifene was third drug for which an IND had been filed under the 1962 Kefauver Harris Amendment to the Federal Food, Drug, and Cosmetic Act that had been passed in response to the thalidomide tragedy.[10] It was approved for marketing in 1967 under the brand name Clomid.[10][51] It was first used to treat cases of oligomenorrhea but was expanded to include treatment of anovulation when women undergoing treatment had higher than expected rates of pregnancy.[52]
The drug is widely considered to have been a revolution in the treatment of female infertility, the beginning of the modern era of assisted reproductive technology, and the beginning of what in the words of Eli Y. Adashi, was «the onset of the US multiple births epidemic».[10][53]
The company was acquired by Dow Chemical in 1980,[54][55] and in 1989 Dow Chemical acquired 67 percent interest of Marion Laboratories, which was renamed Marion Merrell Dow.[54] In 1995 Hoechst AG acquired the pharmaceutical business of Marion Merrell Dow.[56] Hoechst in turn became part of Aventis in 1999,[57]: 9–11 and subsequently a part of Sanofi.[58] It became the most widely prescribed drug for ovulation induction to reverse anovulation or oligoovulation.[59]
Society and culture[edit]
Brand names[edit]
Clomifene is marketed under many brand names worldwide, including Beclom, Bemot, Biogen, Blesifen, Chloramiphene, Clofert, Clomene, ClomHEXAL, Clomi, Clomid, Clomidac, Clomifen, Clomifencitrat, Clomifene, Clomifène, Clomifene citrate, Clomifeni citras, Clomifeno, Clomifert, Clomihexal, Clomiphen, Clomiphene, Clomiphene Citrate, Cloninn, Clostil, Clostilbegyt, Clovertil, Clovul, Dipthen, Dufine, Duinum, Fensipros, Fertab, Fertec, Fertex, Ferticlo, Fertil, Fertilan, Fertilphen, Fertin, Fertomid, Ferton, Fertotab, Fertyl, Fetrop, Folistim, Genoclom, Genozym, Hete, I-Clom, Ikaclomin, Klofit, Klomen, Klomifen, Lomifen, MER 41, Milophene, Ofertil, Omifin, Ova-mit, Ovamit, Ovinum, Ovipreg, Ovofar, Ovuclon, Ovulet, Pergotime, Pinfetil, Profertil, Prolifen, Provula, Reomen, Serofene, Serophene, Serpafar, Serpafar, Surole, Tocofeno, and Zimaquin.[1]
Regulation[edit]
Clomifene is included on the World Anti-Doping Agency list of illegal doping agents in sport.[60] It is listed because it is an «anti-estrogenic substance».
Research[edit]
Clomifene has been used almost exclusively for ovulation induction in premenopausal women, and has been studied very limitedly in postmenopausal women.[61]
Clomifene was studied for treatment and prevention of breast cancer, but issues with toxicity led to abandonment of this indication, as did the discovery of tamoxifen.[62] Like the structurally related drug triparanol, clomifene is known to inhibit the enzyme 24-dehydrocholesterol reductase and increase circulating desmosterol levels, making it unfavorable for extended use in breast cancer due to risk of side effects like irreversible cataracts.[63][64]
References[edit]
- ^ a b «International brands of clomifene -«. Drugs.com. Archived from the original on 20 September 2016. Retrieved 11 September 2016.
- ^ a b c d e f g h i Kim MJ, Byeon JY, Kim YH, Kim SH, Lee CM, Jung EH, et al. (March 2018). «Effect of the CYP2D6*10 allele on the pharmacokinetics of clomiphene and its active metabolites». Archives of Pharmacal Research. 41 (3): 347–353. doi:10.1007/s12272-018-1005-7. PMID 29516347. S2CID 4034257.
- ^ a b Yilmaz S, Yilmaz Sezer N, Gönenç İM, İlhan SE, Yilmaz E (April 2018). «Safety of clomiphene citrate: a literature review». Cytotechnology. 70 (2): 489–495. doi:10.1007/s10616-017-0169-1. PMC 5851961. PMID 29159661.
- ^ a b c d e Mikkelson TJ, Kroboth PD, Cameron WJ, Dittert LW, Chungi V, Manberg PJ (September 1986). «Single-dose pharmacokinetics of clomiphene citrate in normal volunteers». Fertility and Sterility. 46 (3): 392–396. doi:10.1016/S0015-0282(16)49574-9. PMID 3091405.
- ^ a b c d e f g «Clomiphene Citrate». The American Society of Health-System Pharmacists. Archived from the original on 14 September 2017. Retrieved 8 December 2016.
- ^ a b c World Health Organization (2009). Stuart MC, Kouimtzi M, Hill SR (eds.). WHO Model Formulary 2008. World Health Organization. pp. 385–386. hdl:10665/44053. ISBN 9789241547659.
- ^ a b c d e f g h i «Clomiphene citrate tablets label» (PDF). FDA. Archived (PDF) from the original on September 27, 2016. Retrieved September 11, 2016.
- ^ Ghumman S (2015). Principles and Practice of Controlled Ovarian Stimulation in ART. Springer. p. 65. ISBN 9788132216865. Archived from the original on 2016-12-27.
- ^ World Health Organization (2019). World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. hdl:10665/325771. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ^ a b c d e f g Dickey RP, Holtkamp DE (1996). «Development, pharmacology and clinical experience with clomiphene citrate». Human Reproduction Update. 2 (6): 483–506. doi:10.1093/humupd/2.6.483. PMID 9111183.
- ^ a b Rodriguez KM, Pastuszak AW, Lipshultz LI (August 2016). «Enclomiphene citrate for the treatment of secondary male hypogonadism». Expert Opinion on Pharmacotherapy. 17 (11): 1561–7. doi:10.1080/14656566.2016.1204294. PMC 5009465. PMID 27337642.
- ^ a b c d e f g Practice Committee of the American Society for Reproductive Medicine (August 2013). «Use of clomiphene citrate in infertile women: a committee opinion». Fertility and Sterility. 100 (2): 341–8. doi:10.1016/j.fertnstert.2013.05.033. PMID 23809505.
- ^ a b Hughes E, Brown J, Collins JJ, Vanderkerchove P (January 2010). «Clomiphene citrate for unexplained subfertility in women». The Cochrane Database of Systematic Reviews. 2010 (1): CD000057. doi:10.1002/14651858.CD000057.pub2. PMC 7052733. PMID 20091498.
- ^ «Clomifene 50mg Tablets — Summary of Product Characteristics (SPC) — (eMC)». UK Electronic Medicines Compendium. Archived from the original on August 22, 2016. Retrieved September 11, 2016.
- ^ a b Trabert B, Lamb EJ, Scoccia B, Moghissi KS, Westhoff CL, Niwa S, Brinton LA (December 2013). «Ovulation-inducing drugs and ovarian cancer risk: results from an extended follow-up of a large United States infertility cohort». Fertility and Sterility. 100 (6): 1660–6. doi:10.1016/j.fertnstert.2013.08.008. PMC 3873340. PMID 24011610.
- ^ a b Seli E, Arici A. «Ovulation induction with clomiphene citrate». UpToDate. Retrieved 2019-07-30.
- ^ a b Bach PV, Najari BB, Kashanian JA (2016). «Adjunct Management of Male Hypogonadism». Current Sexual Health Reports. 8 (4): 231–239. doi:10.1007/s11930-016-0089-7. ISSN 1548-3584. S2CID 79220716.
- ^ a b c d e f g h i j Trost LW, Khera M (July 2014). «Alternative treatment modalities for the hypogonadal patient». Current Urology Reports. 15 (7): 417. doi:10.1007/s11934-014-0417-2. PMID 24817260. S2CID 20304701.
- ^ DiGiorgio L, Sadeghi-Nejad H (December 2016). «Off label therapies for testosterone replacement». Translational Andrology and Urology. 5 (6): 844–849. doi:10.21037/tau.2016.08.15. PMC 5182219. PMID 28078215.
- ^ Helo S, Mahon J, Ellen J, Wiehle R, Fontenot G, Hsu K, et al. (January 2017). «Serum levels of enclomiphene and zuclomiphene in men with hypogonadism on long-term clomiphene citrate treatment». BJU International. 119 (1): 171–176. doi:10.1111/bju.13625. PMID 27511863. S2CID 5538782.
- ^ Becker KL (2001). Principles and Practice of Endocrinology and Metabolism. Lippincott Williams & Wilkins. pp. 1206–. ISBN 978-0-7817-1750-2.
- ^ Agrawal S, Ganie MA, Nisar S (2017). «Gynaecomastia». Basics of Human Andrology. pp. 451–458. doi:10.1007/978-981-10-3695-8_26. ISBN 978-981-10-3694-1.
- ^ Nordt CA, DiVasta AD (August 2008). «Gynecomastia in adolescents». Current Opinion in Pediatrics. 20 (4): 375–82. doi:10.1097/MOP.0b013e328306a07c. PMID 18622190. S2CID 205834072.
- ^ Miller GD, Moore C, Nair V, Hill B, Willick SE, Rogol AD, Eichner D (March 2019). «Hypothalamic-Pituitary-Testicular Axis Effects and Urinary Detection Following Clomiphene Administration in Males». The Journal of Clinical Endocrinology and Metabolism. 104 (3): 906–914. doi:10.1210/jc.2018-01159. PMID 30295816.
- ^ Cameron R, Feuer G, de la Iglesia F (6 December 2012). Drug-Induced Hepatotoxicity. Springer Science & Business Media. pp. 565–. ISBN 978-3-642-61013-4.
- ^ Gadducci A, Guerrieri ME, Genazzani AR (January 2013). «Fertility drug use and risk of ovarian tumors: a debated clinical challenge». Gynecological Endocrinology. 29 (1): 30–5. doi:10.3109/09513590.2012.705382. PMID 22946709. S2CID 1240526.
- ^ Yu Q, Lv X, Liu K, Ma D, Wu Y, Dai W, Jiang H (2018). «Fertility Drugs Associated with Thyroid Cancer Risk: A Systematic Review and Meta-Analysis». BioMed Research International. 2018: 7191704. doi:10.1155/2018/7191704. PMC 5971354. PMID 29862285.
- ^ a b «ClomiPHENE (Professional Patient Advice)». Drugs.com. Retrieved 2019-07-30.
- ^ a b c Goldstein SR, Siddhanti S, Ciaccia AV, Plouffe L (2000). «A pharmacological review of selective oestrogen receptor modulators». Human Reproduction Update. 6 (3): 212–24. doi:10.1093/humupd/6.3.212. PMID 10874566.
- ^ a b Haskell SG (May 2003). «Selective estrogen receptor modulators». Southern Medical Journal. 96 (5): 469–76. doi:10.1097/01.SMJ.0000051146.93190.4A. PMID 12911186. S2CID 40607634.
- ^ Duarte FH, Jallad RS, Bronstein MD (November 2016). «Estrogens and selective estrogen receptor modulators in acromegaly». Endocrine. 54 (2): 306–314. doi:10.1007/s12020-016-1118-z. PMID 27704479. S2CID 10136018.
- ^ Runnebaum B, Rabe T (17 April 2013). Gynäkologische Endokrinologie und Fortpflanzungsmedizin: Band 1: Gynäkologische Endokrinologie. Springer-Verlag. pp. 88–. ISBN 978-3-662-07635-4.
- ^ a b Roche V, Zito WS, Lemke T, Williams DA (29 July 2019). Foye’s Principles of Medicinal Chemistry. Wolters Kluwer Health. pp. 3010–. ISBN 978-1-4963-8587-1.
- ^ a b c d Obach RS (April 2013). «Pharmacologically active drug metabolites: impact on drug discovery and pharmacotherapy». Pharmacological Reviews. 65 (2): 578–640. doi:10.1124/pr.111.005439. PMID 23406671. S2CID 720243.
- ^ Wittliff JL, Kerr II DA, Andres SA (2005). «Estrogens IV: Estrogen-Like Pharmaceuticals». In Wexler P (ed.). Encyclopedia of Toxicology, 2nd Edition. Vol. Dib–L. Elsevier. pp. 254–258. ISBN 9780080548005.
- ^ Blair RM, Fang H, Branham WS, Hass BS, Dial SL, Moland CL, et al. (March 2000). «The estrogen receptor relative binding affinities of 188 natural and xenochemicals: structural diversity of ligands». Toxicological Sciences. 54 (1): 138–53. doi:10.1093/toxsci/54.1.138. PMID 10746941.
- ^ Fang H, Tong W, Shi LM, Blair R, Perkins R, Branham W, et al. (March 2001). «Structure-activity relationships for a large diverse set of natural, synthetic, and environmental estrogens». Chemical Research in Toxicology. 14 (3): 280–94. doi:10.1021/tx000208y. PMID 11258977.
- ^ a b Baumann RJ, Bush TL, Cross-Doersen DE, Cashman EA, Wright PS, Zwolshen JH, et al. (March 1998). «Clomiphene analogs with activity in vitro and in vivo against human breast cancer cells». Biochemical Pharmacology. 55 (6): 841–51. doi:10.1016/s0006-2952(97)00574-1. PMID 9586957.
- ^ Sutherland RL, Watts CK, Ruenitz PC (October 1986). «Definition of two distinct mechanisms of action of antiestrogens on human breast cancer cell proliferation using hydroxytriphenylethylenes with high affinity for the estrogen receptor». Biochemical and Biophysical Research Communications. 140 (2): 523–9. doi:10.1016/0006-291x(86)90763-1. PMID 3778464.
- ^ a b Rambhatla A, Mills JN, Rajfer J (2016). «The Role of Estrogen Modulators in Male Hypogonadism and Infertility». Reviews in Urology. 18 (2): 66–72. doi:10.3909/riu0711 (inactive 1 August 2023). PMC 5010627. PMID 27601965.
{{cite journal}}: CS1 maint: DOI inactive as of August 2023 (link) - ^ a b c Zhang X (16 October 2018). Estrogen Receptor and Breast Cancer: Celebrating the 60th Anniversary of the Discovery of ER. Springer. pp. 153–. ISBN 978-3-319-99350-8.
- ^ a b c Maximov PY, McDaniel RD, Jordan VC (23 July 2013). Tamoxifen: Pioneering Medicine in Breast Cancer. Springer Science & Business Media. pp. 34–. ISBN 978-3-0348-0664-0.
- ^ a b Harper, Michael J.K. (21 December 2013). «Pharmacological Control of Reproduction in Women». In Jucker, Ernst (ed.). Progress in Drug Research / Fortschritte der Arzneimittelforschung / Progrès des recherches pharmaceutiques. Birkhäuser. pp. 69–. ISBN 978-3-0348-7065-8.
- ^ Hormones and Breast Cancer. Elsevier. 25 June 2013. pp. 13–. ISBN 978-0-12-416676-9.
- ^ Analytical Profiles of Drug Substances and Excipients. Academic Press. 20 March 1998. pp. 113–. ISBN 978-0-08-086120-3. Archived from the original on 5 November 2017.
- ^ Rostami-Hodjegan A, Lennard MS, Tucker GT, Ledger WL (May 2004). «Monitoring plasma concentrations to individualize treatment with clomiphene citrate». Fertility and Sterility. 81 (5): 1187–1193. doi:10.1016/j.fertnstert.2003.07.044. PMID 15136073.
- ^ Allen, R.E., Palopoli, F.P., Schumann, E.L. and Van Campen, M.G. Jr. (1959) U.S. Patent No. 2,914,563 Archived 2016-10-26 at the Wayback Machine, Nov. 24, 1959.
- ^ a b Jensen EV, Jordan VC (June 2003). «The estrogen receptor: a model for molecular medicine». Clin. Cancer Res. 9 (6): 1980–9. PMID 12796359.
- ^ Howell A, Jordan VC (2013). «Adjuvant Antihormone Therapy». In Craig JV (ed.). Estrogen Action, Selective Estrogen Receptor Modulators And Women’s Health: Progress And Promise. World Scientific. pp. 229–254. doi:10.1142/9781848169586_0010. ISBN 978-1-84816-959-3.
- ^ Howell A, Jordan VC (2013). «Adjuvant Antihormone Therapy». In Craig JV (ed.). Estrogen Action, Selective Estrogen Receptor Modulators And Women’s Health: Progress And Promise. World Scientific. pp. 229–254. doi:10.1142/9781848169586_0010. ISBN 978-1-84816-959-3.
- ^ Holtkamp DE, Greslin JG, Root CA, Lerner LJ (October 1960). «Gonadotrophin inhibiting and anti-fecundity effects of chloramiphene». Proceedings of the Society for Experimental Biology and Medicine. 105: 197–201. doi:10.3181/00379727-105-26054. PMID 13715563. S2CID 1448466.
- ^ Hughes E, Collins J, Vandekerckhove P (2000). «Clomiphene citrate for ovulation induction in women with oligo-amenorrhoea». The Cochrane Database of Systematic Reviews (2): CD000056. doi:10.1002/14651858.CD000056. PMID 10796477. (Retracted, see doi:10.1002/14651858.cd000056.pub2)
- ^ Adashi EY (Fall 2014). «Iatrogenic Birth Plurality: The Challenge and Its Possible Solution» (PDF). Harvard Health Policy Review. 14 (1): 9–10. Archived from the original (PDF) on 2016-10-06. Retrieved 2016-09-12.
- ^ a b Lee P (18 July 1989). «Dow Chemical to Get Control of Marion Labs : $5-Billion-Plus Deal Is an Effort to Diversify». Los Angeles Times. Archived from the original on 29 June 2016.
- ^ Williams W (11 February 1981). «Dow Broadens Product Lines». The New York Times. ISSN 0362-4331. Archived from the original on 6 October 2016.
- ^ «Hoechst AG to Buy Marion Merrell Dow / Acquisition worth over $7 billion». San Francisco Chronicle. Reuters. May 5, 1995. Archived from the original on October 6, 2016.
- ^ Arturo Bris and Christos Cabolis,
Corporate Governance Convergence Through Cross-Border Mergers The Case of Aventis Archived 2014-04-21 at the Wayback Machine, Chapter 4 in Corporate Governance and Regulatory Impact on Mergers and Acquisitions: Research and Analysis on Activity Worldwide Since 1990. Eds Greg N. Gregoriou, Luc Renneboog. Academic Press, 26 July 2007 - ^ Timmons H, Bennhold K (27 April 2004). «France Helped Broker the Aventis-Sanofi Deal». The New York Times. Archived from the original on 5 November 2017.
- ^ Strauss JF, Barbieri RL (13 September 2013). Yen and Jaffe’s Reproductive Endocrinology. Elsevier Health Sciences. pp. 518–. ISBN 978-1-4557-2758-2. Archived from the original on 5 November 2017.
- ^ The WADA Prohibited List 2016 (listed as clomiphene) Archived 2016-03-06 at the Wayback Machine
- ^ Palacios S (March 2007). «The future of the new selective estrogen receptor modulators». Menopause International. 13 (1): 27–34. doi:10.1258/175404507780456791. PMID 17448265. S2CID 29053109.
- ^ Maximov PY, Lee TM, Jordan VC (May 2013). «The discovery and development of selective estrogen receptor modulators (SERMs) for clinical practice». Current Clinical Pharmacology. 8 (2): 135–55. doi:10.2174/1574884711308020006. PMC 3624793. PMID 23062036.
- ^ Hormones and Breast Cancer. Elsevier. 25 June 2013. pp. 13–. ISBN 978-0-12-416676-9. Archived from the original on 5 November 2017.
- ^ Maximov PY, McDaniel RE, Jordan VC (2013). «Tamoxifen Goes Forward Alone». Tamoxifen. Milestones in Drug Therapy. pp. 31–46. doi:10.1007/978-3-0348-0664-0_2. ISBN 978-3-0348-0663-3. ISSN 2296-6064.
External links[edit]
- «Clomifene». Drug Information Portal. U.S. National Library of Medicine.
