Дата публикации 17 июня 2021Обновлено 13 апреля 2023
Определение болезни. Причины заболевания
Гиперплазия эндометрия (гиперпластические процессы эндометрия) — это патологическое разрастание желёз слизистой оболочки матки. Эндометрий состоит из желёз и стромы (основы). В норме строма занимает более половины площади эндометрия, при гиперплазии соотношение желёз к строме становится более 50 % [24].
Диагноз «гиперплазия эндометрия» ставится только по заключению гистологического исследования. Без своевременной диагностики и целенаправленного лечения повышается риск развития рака эндометрия.
Гиперплазию нужно отличать от пролифелирующего эндометрия, при котором эндометрий растёт, но не имеет структурных особенностей, характерных для ранней, средней или поздней стадии пролиферации в нормальном менструальном цикле. Также он отличается наличием участков кровоизлияний, дистрофических изменений и распадом [22].
Пролиферирующий эндометрий не является формой гиперплазии, так как соотношение желёз эндометрия к строме не изменяется. Однако если состояние не лечить, повышается риск развития гиперплазии [23].
Распространённость заболевания составляет 15–50 % от всех гинекологических патологий [7]. Гиперплазия эндометрия может возникнуть у женщин всех возрастов, но чаще развивается в 40-44 года, когда происходит гормональная перестройка из-за приближения менопаузы [1][6].
В составе маточного эндометрия есть специфические рецепторы, которые делают его органом-мишенью для половых гормонов. При гормональном сбое нарушается рост и дифференцировка эндометриальных клеток, что приводит к разрастанию эндометрия.
Факторы риска развития гиперплазии эндометрия [1][8][11]:
- ожирение и связанное с ним избыточное образование эстрогенов из андрогенов в жировой ткани [3];
- возраст старше 35 лет;
- наследственность и генетические мутации;
- злостное курение табака;
- раннее менархе (начало менструации) — до 12 лет;
- поздняя менопауза — позже 55 лет;
- затянувшийся период менопаузального перехода;
- хроническая ановуляция (отсутствие овуляции у женщины репродуктивного возраста более шести циклов подряд);
- сопутствующие заболевания: сахарный диабет 2-го типа, ожирение, синдром Линча (наследственный неполипозный колоректальный рак), синдром поликистозных яичников (СПКЯ), гормональные опухоли яичников, бесплодие, а также заболевания пищеварительного тракта, иммунной системы и щитовидной железы;
- приём некоторых лекарственных препаратов: менопаузальная заместительная гормональная терапия (ЗГТ), содержащая только эстрогены; длительная терапия Тамоксифеном. Этот препарат применяется в составе комплексного лечения рака молочной железы. Его побочным эффектом является влияние на слизистую оболочку матки с развитием гиперплазии [14].
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы гиперплазии эндометрия
В редких случаях гиперплазия эндометрия может протекать без симптомов [16][17]. Но обычно для гиперпластических процессов эндометрия характерны нарушения менструального цикла:
- интервал между менструациями более 35 дней или менее 21 дня;
- затяжные, обильные менструации;
- кровянистые выделения из половых путей между менструациями;
- отсутствие менструаций более шести месяцев вне беременности и лактации.
Пациентки репродуктивного возраста иногда жалуются на отсутствие беременности при регулярной половой жизни [15][18].
В период перехода к менопаузе основным симптомом заболевания являются нерегулярные обильные менструации, сменяющиеся длительными мажущими кровянистыми выделениями.
Женщины менопаузального возраста жалуются на скудные кровянистые выделения из половых путей. Они могут проявляться эпизодически либо быть продолжительными.
Иногда пациенток беспокоят симптомы, характерные для обменных и эндокринных нарушений: головные боли, избыточная прибавка веса, нарушение сна, периодически возникающая жажда, утомляемость, пониженная работоспособность и раздражительность, чрезмерный рост волос (в том числе на участках кожи, для которых это несвойственно) [2][11].
Патогенез гиперплазии эндометрия
Состояние эндометрия зависит от фазы менструального цикла:
- I фаза (фаза пролиферации) — продолжается до 14-го дня (при 28-дневном цикле). Под воздействием эстрогенов происходит пролиферация (рост) эндометрия. Его железы увеличиваются, слегка извиваются, их просвет расширяется, но секрета они ещё не содержат [3]. Максимальный рост наблюдается к концу фазы, когда в яичнике созревает один из фолликулов и происходит овуляция. Толщина функционального слоя эндометрия в этот период составляет 4–5 мм.
- II фаза (фаза секреции, или лютеиновая фаза) — продолжается с 14-го по 28-й день, совпадает с развитием жёлтого тела в яичнике на месте лопнувшего фолликула. Под влиянием гормонов жёлтого тела, в том числе прогестерона, железы эндометрия ещё больше извиваются и заполняются секретом. В них откладывается гликоген, фосфор и кальций, необходимые для питания и последующей имплантации эмбриона в слизистую оболочку матки. Толщина функционального слоя эндометрия в позднюю стадию фазы секреции (при отсутствии беременности) составляет 15 мм. Когда происходит обратное развитие жёлтого тела, уровень прогестерона и эстрогенов снижается, функциональный слой эндометрия отторгается и начинается менструация.
В патогенезе гиперплазии эндометрия выделяют два варианта развития событий:
- Гормонозависимый — избыточное влияние эстрогенов на слизистую оболочку матки при недостаточном воздействии прогестерона, который должен подавлять действие эстрогенов. Наблюдается при недостатке прогестерона или при избытке эстрогенов. В этом случае эстрогены провоцируют патологический рост эндометриальных желёз, при котором изменяется их форма и размер. Из-за недостатка прогестерона не наступает фаза секреции, поэтому эндометрий продолжает активно расти. Гиперплазия эндометрия почти всегда является гормонозависимой.
- Гормононезависимый — патологический ответ желёз и стромы эндометрия на нормальный уровень эстрогена. Может возникнуть из-за хронического воспаления эндометрия. В этом случае аномальное разрастание эндометрия связано с тем, что у рецепторов меняется структура и функции.
При гиперплазии эндометрия без клеточной атипии из-за гормонального дисбаланса увеличивается количество желёз. Их соотношение к строме эндометрия начинает превышать 50 % [3][7].
В случае гиперплазии эндометрия с атипией избыток желёз эндометрия сочетается с клеточными мутациями (атипическим перерождением). Атипическая гиперплазия эндометрия является предраковым состоянием.
Классификация и стадии развития гиперплазии эндометрия
Рассмотрим две основные международные классификации гиперплазии эндометрия, которые основаны на оценке строения ткани [4][9][12].
Международная классификация болезней 10-го пересмотра (МКБ-10):
- N85.0 Железистая гиперплазия эндометрия (кистозная, железисто-кистозная, полипоидная).
- N85.1 Аденоматозная (атипическая) гиперплазия эндометрия.
Пересмотренная классификация ВОЗ 2014 года:
- Гиперплазия эндометрия без атипии. Синонимы: доброкачественная, простая неатипическая, сложная неатипическая.
- Атипическая гиперплазия эндометрия. Синонимы: простая атипическая, сложная атипическая, эндометриальная интраэпителиальная неоплазия [25].
| Новый термин | Синонимы | Генетические изменения | Наличие рака эндометрия | Риск рака эндометрия |
|---|---|---|---|---|
| Гиперплазия эндометрия без атипии | 1. Простая неатипическая гиперпазия 2. Сложная гиперплазия без атипии |
Редко | Менее 1 % | 1,01–1,03 |
| Гиперплазия эндометрия с атипией | 1. Сложная атипическая гиперплазия эндометрия 2. Простая атипическая гиперплазия эндометрия 3. Эндометриальная интраэпителиальная неоплазия (EIN) |
Множество генетических изменений | от 25–33 до 59 % |
14–45 |
Основная цель этих классификаций — разграничить доброкачественную гиперплазию и гиперплазию с наличием атипических клеток. Это важно, чтобы определить дальнейшую тактику ведения пациенток, так как атипичная гиперплазия часто перерождается в рак [9].
Осложнения гиперплазии эндометрия
Анемия. Для гиперплазии эндометрия характерны аномальные маточные кровотечения. В связи с этим женщины часто страдают от хронического малокровия разной степени выраженности.
Бесплодие. Гормональные изменения отражаются на качестве эндометрия, что создаёт риск неудачной имплантации эмбриона. Помимо этого, гиперплазия эндометрия часто выявляется на фоне хронической ановуляции, при которой зачатие невозможно.
Перерождение в рак эндометрия. Самое грозное осложнение гиперплазии эндометрия. Согласно исследованию 2006 года, атипическая гиперплазия эндометрия перерождается в аденокарциному эндометрия в 29 % случаев. Гиперплазия без атипии становится злокачественной менее чем в 5 % случаев [4][10].
Риск озлокачествления зависит в первую очередь от выраженности клеточного атипизма, т. е. от степени изменения клеток. Возраст, состояние яичников, сопутствующие эндокринные заболевания, ожирение и приём гормональных препаратов не так сильно влияют на риск перерождения [10]. Поэтому так важна своевременная диагностика гиперплазии эндометрия и последующее выделение пациенток с этой патологией в группу онкологического риска [13].
Диагностика гиперплазии эндометрия
Диагностика основана на анализе данных анамнеза пациентки (истории болезни), клинической картины заболевания (жалоб и физикального осмотра), а также на результатах ультразвукового и гистероскопического исследования с обязательным патоморфологическим анализом соскоба из полости матки.
Диагноз «гиперплазия эндометрия» ставится только на основании гистологического исследования материала, полученного при диагностическом выскабливании слизистой оболочки матки или удалении матки.
Анамнез и клиническая картина
При сборе анамнеза врач-гинеколог задаёт пациентке вопросы:
- Были ли гинекологические проблемы у мамы, бабушки или других родственников по женской линии.
- Какой образ жизни ведёт пациентка.
- Есть ли вредные привычки.
- Какой характер питания.
- Как проходят менструации: длина цикла, характер и продолжительность менструаций.
- Бывают ли аномальные маточные кровотечения. Если да, каков их характер и продолжительность.
- Была ли беременность и роды, планируется ли беременность в будущем. Невозможность зачать ребёнка и невынашивание могут быть симптомом гиперплазии эндометрия [18].
- Есть ли сопутствующие заболевания из группы риска по развитию гиперплазии эндометрия.
- Принимает ли пациентка какие-либо гормональные препараты.
Физикальный осмотр включает в себя местный осмотр наружных половых органов, исследование влагалища и шейки матки в зеркалах, а также бимануальное (двумя руками) исследование матки и придатков. Осмотр проводится на первичном приёме, чтобы исключить воспалительные заболевания и/или объёмные опухолевые образования.
Инструментальная диагностика
Трансвагинальное ультразвуковое исследование (ТВУЗИ) органов малого таза. Толщина эндометрия по данным УЗИ не является надёжным критерием выявления гиперплазии эндометрия у женщин репродуктивного возраста [26]. Исследование проводят, чтобы исключить другие причины аномальных маточных кровотечений или оценить толщину эндометрия у женщин в постменопаузе [23][27].
У женщин репродуктивного и пременопаузального возрастов при подозрении на гиперплазию эндометрия ТВУЗИ органов малого таза проводится на 5–7-й день менструального цикла. В норме в это время толщина эндометрия не превышает 6 мм. Патологию эндометрия подозревают, когда его толщина не соответствует определённой фазе менструального цикла:
- на 5–7-й день цикла толщина эндометрия более 6 мм (в среднем 8–15 мм);
- в середине цикла (на 14–15-й день при 28-дневном цикле) толщина эндометрия более 15 мм [13][14].
В постменопаузе толщина эндометрия в норме должна быть не более 4–5 мм. Патологическое утолщение диагностируют, когда этот показатель превышает 5 мм [12]. Допустимая толщина эндометрия на фоне приёма Тамоксифена не больше 9 мм.
Помимо измерения толщины врач ультразвуковой диагностики оценивает кровоснабжение эндометрия, а также его контуры, однородность и соответствие фазе цикла у женщин репродуктивного возраста. Для атипической гиперплазии характерно более выраженное утолщение слизистого слоя матки, его неоднородность, неровные извилистые контуры и более интенсивная васкуляризация (кровоснабжение) [2][7].
В некоторых случаях, например при обильном кровотечении, которое угрожает здоровью пациентки, ТВУЗИ не проводится. Сразу принимается решение об обоснованном диагностическом выскабливании по жизненным показаниям [19].
Гистероскопия с раздельным диагностическим выскабливанием (РДВ) матки и цервикального канала — информативный метод в диагностике гиперпластических процессов эндометрия. При помощи гистероскопа (эндоскопического прибора для осмотра полости матки) врач оценивает состояние слизистой оболочки матки и цервикального канала. При необходимости удаляет локальные поражения и обязательно берёт материал для последующего гистологического исследования.
Если выскабливание проводят как лечебную процедуру при обильном маточном кровотечении, врач полностью удаляет слизистую оболочку матки под контролем гистероскопии.
Цитологическое исследование аспирата из полости матки. Пайпель-биопсия. Специальный зонд, введённый в полость матки, «всасывает» фрагменты эндометрия. В последующем специалист оценивает выраженность его пролиферативных изменений (т. е. новообразований клеток и клеточных структур). Пайпель-биопсия эндометрия — высокочувствительный метод диагностики гиперплазии и рака эндометрия [28].
У женщин репродуктивного возраста (15–49 лет) аспират берут на 2–26-й день менструального цикла. У женщин в пременопаузе (с 40–45 лет и до наступления менопаузы) и в менопаузальном возрасте (своевременная менопауза наступает в 46–54 года) пайпель-биопсию можно делать в любой день [20][21].
Дифференциальная диагностика гиперплазии эндометрия проводится с полипом эндометрия, субмукозной (подслизистой) миомой матки, эндометритом, прервавшейся беременностью и раком эндометрия.
Лечение гиперплазии эндометрия
Лечение патологии эндометрия основывается на трёх принципах:
- Предупредить развитие/прогрессирование злокачественного процесса эндометрия.
- Исключить сопутствующие злокачественные процессы в эндометрии.
- Выбрать наиболее подходящий пациентке план лечения [3].
Тактика лечения будет зависеть от результата гистологического исследования эндометрия, полученного в ходе выскабливания, от возраста женщины, сопутствующих заболеваний и репродуктивных планов.
Лечебная тактика в зависимости от наличия или отсутствия атипии [27][29].
Гиперплазия эндометрия без атипии:
- Консервативное лечение:
- нормализация менструального цикла;
- снижение веса;
- пероральные контрацептивы;
- циклические гестагены;
- внутриматочная система «Мирена».
- Хирургическое (только в исключительных случаях).
Гиперплазия эндометрия с атипией:
- Консервативное лечение проводится только у женщин, желающих сохранить способность к деторождению. Назначаются высокие дозы гестагенов и гистологический мониторинг.
- Хирургическое лечение. Выполняется пангистерэктомия — радикальная операция, при которой тело, шейка матки, маточные трубы и яичники удаляются через разрез в брюшной полости.
Наблюдение. У 70–80 % пациенток наблюдается самостоятельное исчезновение признаков гиперплазии. Поэтому если у женщины нет никаких симптомов и факторов риска, то врач наблюдает за состоянием эндометрия с помощью контрольных биопсий один раз в 6 месяцев. При получении двух последовательных негативных биопсий пациентку снимают с учёта [12].
Медикаментозное лечение гормональными препаратами проводится пациенткам репродуктивного возраста с неатипической гиперплазией эндометрия при наличии симптомов, факторов риска, отсутствии регресса за 6 месяцев наблюдения и при атипической гиперплазии эндометрия у женщин, планирующих беременность.
В периоды пери- и постменопаузы гормонотерапию проводят только при неатипических формах гиперплазии эндометрия [30].
Гормональную терапию назначают не менее чем на 6 месяцев:
- Внутриматочная гормональная контрацепция (ЛНГ-ВМС): спираль «Мирена», LNG-20.
- Прогестагены в циклическом (у менструирующих женщин) или непрерывном режиме (при сложной гиперплазии и при наличии сопутствующей патологии матки): Норколут (Норэтистерон), Дюфастон (Дидрогестерон), Утрожестан.
- Агонисты гонадотропин рилизинг-гормона (аГнРГ) применяются у пациенток с рецидивирующей гиперплазией эндометрия и у женщин репродуктивного возраста с атипической гиперплазией: Бусерелин-депо (Бусерелин).
После курса медикаментозной терапии необходимо сделать не менее двух контрольных биопсии эндометрия с интервалом один раз в 6 месяцев [3][11]. Критерием излеченности гиперплазии эндометрия будет отсутствие патологических изменений в биоптате.
В качестве негормональной терапии возможно применение препаратов:
- Циклодинон — негормональный лекарственный растительный препарат из плодов Витекса священного. Компоненты препарата нормализуют концентрацию половых гормонов.
- Мастодинон — комбинированный препарат на растительной основе [32].
Лечение нужно сочетать с низкокалорийной диетой и достаточной физической нагрузкой согласно общему физическому развитию женщины. При необходимости врач назначает препараты, которые нормализуют метаболизм углеводов в организме: подавляют образование глюкозы клетками печени, повышают чувствительность тканей к инсулину, расщепляют сложные сахара.
Хирургическое лечение. Атипическая гиперплазия эндометрия на начальном этапе требует обязательной консультации онкогинеколога, который должен установить, нужна ли операция и в каком объёме.
Чаще всего выполняется надвлагалищная ампутация матки — суправагинальная гистерэктомия (удаление тела и шейки матки). Вопрос о сохранении яичников решается строго индивидуально, зависит от возраста пациентки и факторов риска.
Показания к гистерэктомии:
- Атипический гиперпластический процесс эндометрия у пациенток старше 50 лет.
- Атипическая гиперплазия эндометрия, развившаяся в ходе лечения неатипической гиперплазии.
- Рецидивирующая гиперплазия эндометрия, особенно в сочетании с миомой матки и аденомиозом (эндометриоз тела матки) [3][11].
Прогноз. Профилактика
После успешного лечения пациентки должны находиться на диспансерном учёте: посещать гинеколога и делать ТВУЗИ органов малого таза один раз в пол года на протяжении пяти лет [11][12].
Применение прогестагенов в лечении гиперплазии эндометрия без атипии дают хорошие результаты: в 89–96 % случаев патологические изменения достаточно быстро регрессируют [3][5]. Рецидив заболевания при неатипическом процессе выявляют в 6 % случаев.
В случае атипической гиперплазии эффективность лечения составляет 50 %. Рецидив регистрируется в 25 % случаев, ещё в 25 % выявляется рак эндометрия [10].
Обследование для исключения гиперплазии или рака эндометрия показано в следующих случаях:
1. Если есть аномальные маточные кровотечения [29][31]:
- В постменопаузальном периоде показанием является любое маточное кровотечение, независимо от объёма и длительности. Первый шаг в этом случае — измерение толщины эндометрия с помощью ТВУЗИ:
- если этот показатель менее 5 мм — риск атипии минимальный;
- если толщина эндометрия более 5 мм — показана биопсия эндометрия.
- В период перименопаузы (от 45 лет и до менопаузы) обследование необходимо при частых, длительных или обильных аномальных маточных кровотечениях.
- До 45 лет:
- Показания у женщин с ожирением: частые, длительные или обильные аномальные маточные кровотечения.
- У женщин без ожирения: длительные аномальные маточные кровотечения в сочетании с хронической ановуляцией, монотерапией эстрогенами, эстрогенпродуцирующей опухолью, отсутствием эффекта от лечения аномальных маточных кровотечений, высоким риском развития рака эндометрия (синдром Линча), отсутствием менструации в течение шести и более месяцев с хронической ановуляцией.
2. Если по результатам цитологического исследования соскоба шейки матки отмечается:
- наличие атипических клеток эндометрия;
- наличие атипических клеток любой локализации у женщин старше 35 лет с факторами риска развития рака эндометрия;
- наличие клеток эндометрия с признаками доброкачественной гиперплазии у женщин старше 40 лет с нарушениями менструального цикла или факторами риска развития рака эндометрия.
Профилактика:
- Своевременно выявлять и лечить заболевания женских половых органов.
- Избегать искусственного прерывания беременности.
- Вести здоровый образ жизни с регуляцией диеты, снижением веса при ожирении, контролем уровня глюкозы в крови при сахарном диабете, отказом от курения.
- Полноценно питаться, отдыхать и заниматься спортом.
Библиографическое описание:
Каркусова, А. В. Гиперплазия эндометрия — проблема ХХI века / А. В. Каркусова, И. Р. Гудиева. — Текст : непосредственный // Молодой ученый. — 2019. — № 5 (243). — С. 57-61. — URL: https://moluch.ru/archive/243/56306/ (дата обращения: 24.09.2023).
В статье представлены данные о частоте встречаемости гиперплазии в РСО-Алании, также определен возраст встречаемости гиперпластических изменений в эндометрии.
Ключевые слова: гиперплазия, рак, матка, эндометрий, операции.
Введение
Гиперплазия эндометрия (ГПЭ) — нефизиологическая пролиферация эндометрия, сопровождающаяся структурной перестройкой железистого и, в меньшей степени, стромального компонента эндометрия на фоне избыточного влияния эстрогенов. К гиперпластическим процессам эндометрия относят различные варианты гиперплазии эндометрия и полипы эндометрия. [4].
Актуальность.
Гиперпластические процессы эндометрия остаются одной из наиболее актуальных проблем современной гинекологии в связи с неуклонным ростом заболеваемости раком эндометрия [1,2]. Известно, что фоном для развития рака эндометрия в периоде пре- и постменопаузы могут стать существующие в течение длительного времени и часто рецидивирующие гиперпластические процессы [3, 8]. Несмотря на довольно широкое освещение в литературе последних лет проблем патогенеза и ранней диагностики патологических состояний эндометрия, в частности, железистой гиперплазии и рака эндометрия, некоторые вопросы развития, своевременного выявления и прогноза течения пролиферативных процессов эндометрия с различной степенью функциональной активности клеток остаются недостаточно изученными [8].
Цель работы: Определить частоту выявления гиперплазии эндометрия среди женщин, поступивших в гинекологическое отделение ГБУЗ РКБ МЗ РСО-Алания.
Задачи исследования:
− провести анализ частоты выявления гиперплазии эндометрия среди женщин, поступивших в гинекологическое отделение РКБ.
− уточнить преимущественный возраст выявления гиперплазии эндометрия среди пациентов гинекологического отделения РКБ.
− изучить частоту выявляемости рака эндометрии и определить группу риска.
Материалы иметоды исследования.
Был проведен ретроспективный анализ журналов малых операций и журналов проведения гистероскопий за 2015–2017 гг. в гинекологическом отделении Республиканской клинической больницы РСО-Алания. Все больные поступали в стационар по поводу меноррагий, ациклических кровяных выделений из половых путей, а также по направлению женских консультаций с гиперплазией и полипом эндометрия для проведения гистероскопии. Возраст пациентов составлял от 18 до 80 лет. Женщины были поделены на 2 возрастные группы: репродуктивный период — 18–45 лет и пре- и постменопаузальный период — 46–80 лет.
Результаты исследования.
В ходе проведения ретроспективного анализа выявлено, что достоверно чаще гиперплазия эндометрия диагностировалась во второй возрастной группе (46–80 лет), чем в первой (18–45 лет) и составила соответственно 61 % и 39 %.
Частота гиперплазии эндометрия среди всех пациентов, которым были проведены гистероскопия и раздельное диагностическое выскабливание, составила 25 % (808 женщин) (рис. 1).
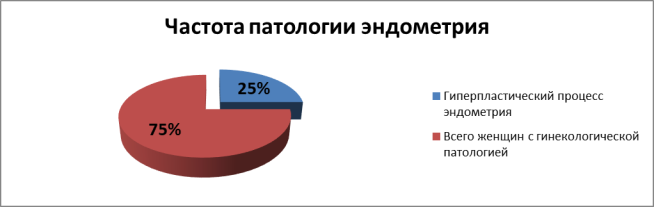
Для диагностики патологических процессов всем больным с подозрением на внутриматочную патологию проводили следующие методы исследования: гистероскопию — 2062 (63,7 %), раздельное диагностическое выскабливание (РДВ) — 1175 (36,3 %). Всего малых операций за трехлетний период в отделении гинекологии выполнено 3237 (рис. 2). Всем пациентам этой группы было также проведено гистологическое исследование соскобов эндометрия.
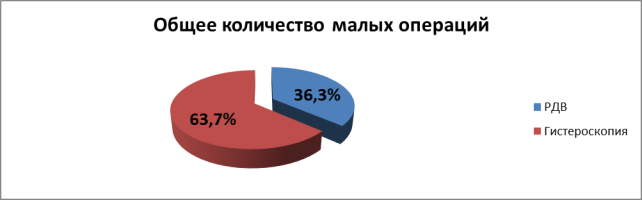
Далее представлены показатели отдельно по годам и отдельно по РДВ и гистероскопическим манипуляциям. Анализируя данные было определено, что в 2015 году выскабливаний по поводу ГПЭ было проведено — 537 (45,7 %), в 2016 году — 369 (31,4 %), в 2017 году — 269 (22,9 %) (рис. 3).
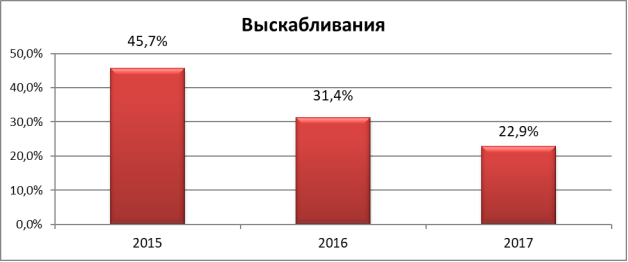
Гистероскопических манипуляций по причине ГПЭ было проведено в 2015 году — 642 (31,1 %), в 2016 году — 587 (28,5 %), в 2017 году — 833 (40,4 %) (рис. 4). Следует обратить внимание на то, что если в отношении РДВ с 2015 г. по 2017 г. отмечается снижение частоты проводимых манипуляции, то в отношении гистероскопии наоборот, наблюдается рост.
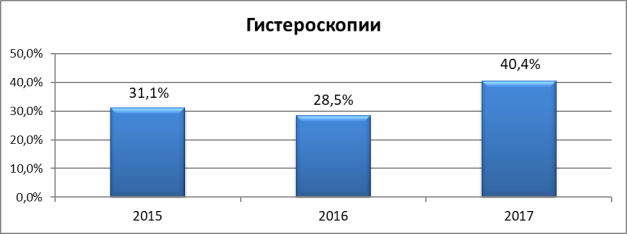
Также, были проанализированы показания к проведению малых операций. К показаниям были отнесены такие патологические состояния, как аномальное маточное кровотечение (АМК) — 22 %, гиперплазия эндометрия — 19 %, полипы эндометрия — 59 % (рис. 5). Малых операций по поводу ГПЭ за 2015- 2017г. было сделано 731. При этом следует отметить, что при аномальных маточных кровотечениях чаще проводили РДВ, а при полипах эндометрия — гистероскопии.
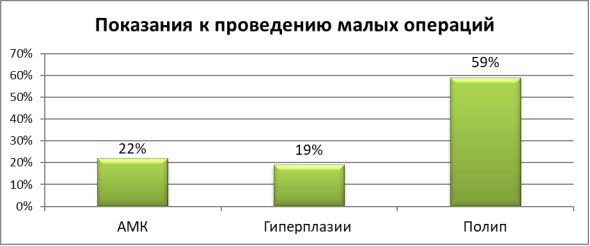
Рис. 5. Показания к проведению раздельного диагностического выскабливания и гистероскопии
Частота выявляемости рака эндометрия за 3 года в гинекологическом отделении РКБ составила 7,5 %. При анализе данного показателя по годам выявлено снижение частоты рака эндометрия с 3,3 % до 2,2 % (рис. 6).
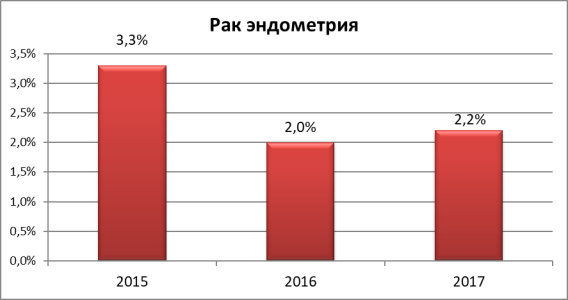
Рис. 6. Выявляемость рака эндометрия по годам с 2015 по 2017 гг.
Заключение.
Выводы:
- Частота развития ГПЭ среди пациентов, которым были проведены гистероскопия и раздельное диагностическое выскабливание, составила 808 случай (25 %).
- Преимущественный возраст развития гиперпластических процессов эндометрия составил от 46–80 лет (61 %).
- Частота выявляемости рака эндометрия за 3 года в гинекологическом отделении РКБ составила 7,5 %.
Литература:
- Бурлев, В. А. Микрососуды эндометрия у больных с гиперплазией и аденокарциномой / В. А. Бурлев, С. Э. Саркисов, Н. А. Ильясова, Е. Д. Дубинская, А. В. Бурлев / / Проблемы репродукции. — 2008. — № 4. — С.10–16.
- Сидорова, И. С. Патология эндометрия при наличии миомы матки / И. С. Сидорова, Н. А. Шешукова, С. В. Закаблукова // Гинекология. — 2006. — Т. 8, № 4. -С.57–6О.
- Кузнецова, И. В. Особенности менструального цикла и состояние эндометрия в пременопаузе: клинико-морфологические параллели / И. В. Кузнецова, О. А. Могиревская, Р. А. Вельхиева // Российский вестник акушера-гинеколога. — 2007. — № 3. — С. 30–33.
- Кулаков В. И., Прилепская В. Н. Практическая гинекология (клинические лекции). М.: МЕДпресс-информ, 2001. 720 с.
- Гинекология — национальное руководство под ред. В. И. Кулакова, Г. М. Савельевой, И. Б. Манухина. — 2009 г.
- Практическая гинекология Лихачев В. К. — 2007 г.
- https://meduniver.com/Medical/onkologia/klassifikacia_giperplazii_endometria.html
- Кулова Ф. Т. Некоторые аспекты патогенеза, диагностики, и ведения больных с железимтой гиперплазией эндометрия в период пери- и постменопаузы.// Автореф. дисс. канд мед. наук.- Москва-2001- 31 с.
Основные термины (генерируются автоматически): гинекологическое отделение, полип эндометрия, раздельное диагностическое выскабливание, гиперплазия эндометрия, гиперпластический процесс эндометрия, РСО-Алания, проведение малых операций, рак эндометрия, частота выявляемости рака эндометрия.
Клинические рекомендации, утвержденные МЗ РФ
ДОБРОКАЧЕСТВЕННАЯ ДИСПЛАЗИЯ МОЛОЧНОЙ ЖЕЛЕЗЫ
ЦЕРВИКАЛЬНАЯ ИНТРАЭПИТЕЛИАЛЬНАЯ НЕОПЛАЗИЯ, ЭРОЗИЯ И ЭКТРОПИОН ШЕЙКИ МАТКИ
ВНЕМАТОЧНАЯ (ЭКТОПИЧЕСКАЯ) БЕРЕМЕННОСТЬ
АНОМАЛЬНЫЕ МАТОЧНЫЕ КРОВОТЕЧЕНИЯ
ВОСПАЛИТЕЛЬНЫЕ БОЛЕЗНИ ЖЕНСКИХ ТАЗОВЫХ ОРГАНОВ
ВРОЖДЕННАЯ ДИСФУНКЦИЯ КОРЫ НАДПОЧЕЧНИКОВ (АДРЕНОГЕНИТАЛЬНЫЙ СИНДРОМ)
ВЫПАДЕНИЕ ЖЕНСКИХ ПОЛОВЫХ ОРГАНОВ
МЕНОПАУЗА И КЛИМАКТЕРИЧЕСКОЕ СОСТОЯНИЕ У ЖЕНЩИНЫ
СИНДРОМ ПОЛИКИСТОЗНЫХ ЯИЧНИКОВ
СИНДРОМ ГИПЕРСТИМУЛЯЦИИ ЯИЧНИКОВ
УРОГЕНИТАЛЬНЫЕ ЗАБОЛЕВАНИЯ, ВЫЗВАННЫЕ MYCOPLASMA GENITALIUM
УРОГЕНИТАЛЬНЫЙ ТРИХОМОНИАЗ
АНОГЕНИТАЛЬНАЯ ГЕРПЕТИЧЕСКАЯ ВИРУСНАЯ ИНФЕКЦИЯ
АНОГЕНИТАЛЬНЫЕ (ВЕНЕРИЧЕСКИЕ) БОРОДАВКИ
На Школах РОАГ новые клинические рекомендации представляют их разработчики – ведущие эксперты НМИЦ АГП им. В.И. Кулакова.
Предложения по внесению изменений в действующие клинические рекомендации
Сайт издательства «Медиа Сфера»
содержит материалы, предназначенные исключительно для работников здравоохранения. Закрывая это сообщение, Вы подтверждаете, что являетесь дипломированным медицинским работником или студентом медицинского образовательного учреждения.
ГБУЗ МО «Московский областной научно-исследовательский институт акушерства и гинекологии» Минздрава Московской области, Москва, Россия
Чечнева М.А.
Московский областной НИИ акушерства и гинекологии
Гиперплазия эндометрия в пери- и постменопаузе
Авторы:
Капитанова О.В., Чечнева М.А.
Как цитировать:
Капитанова О.В., Чечнева М.А. Гиперплазия эндометрия в пери- и постменопаузе. Российский вестник акушера-гинеколога.
2020;20(3):35‑40.
Kapitanova OV, Chechneva MA. Endometrial hyperplasia in peri- and postmenopausal women. Russian Bulletin of Obstetrician-Gynecologist. 2020;20(3):35‑40. (In Russ.)
https://doi.org/10.17116/rosakush20202003135

Читать метаданные
Большая клиническая значимость гиперпластических процессов в эндометрии заключается в том, что они являются одной из самых распространенных причин маточных кровотечений у женщин в возрасте 45—55 лет и их госпитализации в стационар. Гиперплазия эндометрия, особенно с атипией, является значительной клинической проблемой, поскольку может предшествовать раку эндометрия. За последние несколько лет оценка состояния эндометрия изменилась в признании того, что патология эндометрия не всегда носит глобальный характер. Толщина эндометрия не может быть единственным признаком гиперплазии эндометрия.
Авторы:
Капитанова О.В.
ГБУЗ МО «Московский областной научно-исследовательский институт акушерства и гинекологии» Минздрава Московской области, Москва, Россия
Чечнева М.А.
Московский областной НИИ акушерства и гинекологии
Список литературы:
- Макаров, И.О. Онкологические аспекты гиперпластических процессов в эндометрии. Российский вестник акушера-гинеколога. 2011;1:13-16.
- Максимов С.Я., Гусейнов К.Д., Косников А.Г. Факторы риска возникновения злокачественных новообразований органов репродуктивной системы женщин. Вопросы онкологии. 2013;53:4:496-501.
- Руководство по гинекологии. Под ред. акад. РАМН, проф. Айламазяна Э.К. М.: МЕДпресс-информ; 2012.
- Савельева Г.М., Бреусенко В.Г., Каппушева Л.М. Постменопауза. Физиология и патология. Вестник Российской ассоциации акушеров-гинекологов. 2008;2:56-59.
- Ашрафян Л.А., Новикова Е.Г. Гинекологические аспекты в тенденциях заболеваемости и смертности от рака органов репродуктивной системы. Журнал акушерских и женских болезней. 2011;1:XLX:27-33.
- Доброхотова Ю.Э., Сапрыкина Л.В. Гиперплазия эндометрия. М.: ГЭОТАР-Медиа; 2018.
- Вихляева Е.М. Руководство по эндокринной гинекологии. М.: МИА; 2006.
- Стрижаков А.Н., Давыдов А.И., Пашков В.М. Доброкачественные заболевания матки. М. 2011.
- Сидорова И.С., Унанян А.Д., Власов Р.С., Евкина И., Карпов Д. Гиперпластические процессы эндометрия: особенности клиники и терапии. Врач. 2011;3:40-42.
- Серов В.Н. Клинико-физиологические основы гинекологической эндокринологии. М. 2008.
- Ragupathy, K, Cawley, N, Ridout, A, Iqbal, P, Alloub, M. Nonassessable endometrium in women with post-menopausal bleeding: to investigate or ignore. Arch Gynecol Obstet. 2013;288:375-378.
- Манухин И.Б., Тактаров В.Г., Шмелева С.В. Здоровье женщины в климактерии. Руководство. (Серия «Практические руководства»). 2010.
- Серов В.Н., Сухих Г.Т., Прилепская В.Н., Радзинский В.Е. Руководство по амбулаторно-поликлинической помощи в акушерстве и гинекологии. М.: ГЕОТАР-Медиа; 2016.
- Аксель Е.М. Заболеваемость и смертность от злокачественных новообразований органов женской репродуктивной системы в России. Онкогинекология. 2015;1:4-13.
- Endometrial cancer. Practice Bulletin N 149. American College of Obstetricians and Gynecologists. Obstet Gynecol. 2015;125:1006-1026.
- Бохман Я.В. Лекции по онкогинекологии. М.: Медицинское информационное агентство; 2007.
- Бочкарева Н.В., Фомина С.В., Коломиец Л.А. Развитие рака эндометрия у больных разных возрастных групп с гиперпластическими процессами эндометрия. Медицинская радиология и радиационная безопасность. 2009;3:333-338.
- Кузнецов Р.Э., Чернеховская Н.Е., Андреев В.Г., Поваляев А.В. Заболевания матки и придатков. Диагностическая лапароскопия. М.: МЕДпресс-информ; 2009.
- Бабурин Д.В., Унанян А.Л. Тактика ведения пациенток с атипической гиперплазией эндометрия. Архив акушерства и гинекологии им. В.Ф. Снегирева. 2016;4:188-192.
- Epidemiology and investigations for suspected endometrial cancer. Joint SOGC-GOC-SCC Clinical Practice Guideline. J Obstet Gynaecol Canada. 2013;291:1-9.
- Timmermans A, Opmeer BC, Khan KS, Bachmann LM, Epstein E, Clark TJ, Gupta JK, Bakour SH, van den Bosch T, van Doorn HC, Cameron ST, Giusa MG, Dessole S, Dijkhuizen FP, Ter Riet G, Mol BW. Endometrial thickness measurement for detecting endometrial cancer in women with postmenopausal bleeding: a systematic review and metaanalysis. Obstet Gynecol. 2010;116:160-167. https://doi.org/10.1097/AOG.0b013e3181e3e7e8
- Colombo N, Preti E, Landoni F, Carinelli S, Colombo A, Marini C, Sessa C; ESMO Guidelines Working Group. Endometrial cancer: ESMO clinical practice guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2013;24:6:33-38. https://doi.org/10.1093/annonc/mdt353
- Giannella L, Cerami LB, Setti T, Bergamini E, Boselli F. Prediction of Endometrial Hyperplasia and Cancer among Premenopausal Women with Abnormal Uterine Bleeding. Biomed Res Int. 2019;2019:8598152. https://doi.org/10.1155/2019/8598152
- Trimble CL, Method M, Leitao M, Lu K, Ioffe O, Hampton M, Higgins R, Zaino R, Mutter GL. Society of Gynecologic Oncology Clinical Practice Committee. Management of endometrial precancers. Obstet Gynecol. 2012;120:1160-1175. https://doi.org/10.1097/aog.0b013e31826bb121
- Лучевая диагностика в гинекологии. Руководство для врачей. Под ред. Труфанова Г.Е., Панова В.О. СПб.: ЭЛБИ-СПб; 2008.
- Бенасэрраф Б., Голдстейн С., Гроцман И. Ультразвуковые исследования в гинекологии. М.: МЕДпресс-информ; 2016.
- Боровкова Л.В., Ершова В.О., Игнатьев А.А. Современные методы диагностики доброкачественных и злокачественных процессов эндометрия. Медицинский альманах. 2009;3:105-108.
- Буланов М.Н. Ультразвуковая гинекология: курс лекций в трех томах. М.: Видар-М; 2010.
- Сухих Г.Т., Сметник В.П., Андреева Е.Н., Балан В.Е., Гависова А.А., Григорян О.Р., Ермакова Е.И., Зайдиева Я.З., Ильина Л.М., Касян В.Н., Марченко Л.А., Подзолкова Н.М., Роговская С.И., Сметник А.А., Чернуха Г.Е., Юренева С.В. КР117 30 Менопаузальная гормонотерапия и сохранение здоровья женщин в зрелом возрасте. Клинические рекомендации. Проблемы репродукции. 2016;8-9.
- Baber RJ, Panay N, Fenton A, and the IMS Writing Group. 2016 IMS Recommendations on women’s midlife health and menopause hormone therapy. Climacteric. 2016;19:2:109-150. https://doi.org/10.3109/13697137.2015.1129166
- Демичева Т.В., Гришин Г.Н., Крикунова Л.И. Роль ультразвукового исследования в диагностике рака эндометрия и оценке стадии заболевания. Российский онкологический журнал. 2012;4:28-31.
- Jokubkiene L, Sladkevicius P, Valentin L. Transvaginal ultrasound examination of the endometrium in postmenopausal women without vaginal bleeding. Ultrasound Obstet Gynecol. 2016;48:3:390-396. PMID:26678251. https://doi.org/10.1002/uog.15841
- Сабанцев М.А., Баженова Л.Г., Шрамко С.В., Левченко В.Г., Маркина Л.А., Хвостова Е.П. Информативность стандартных методов диагностики пролиферативных заболеваний эндометрия. Российский вестник акушера-гинеколога. 2017;17:1:62-66.
- Breijer MC, Peeters JA, Opmeer BC, Clark TJ, Verheijen RH, Mol BW, Timmermans A. Capacity of endometrial thickness measurement to diagnose endometrial carcinoma in asymptomatic postmenopausal women: a systematic review and metaanalysis. Ultrasound Obstet Gynecol. 2012;40:621-629. https://doi.org/10.1002/uog.12306
- Озерская И.А. Эхография в гинекологии. М.: Видар-М; 2013.
- Lev-Sagie A, Hamani Y, Imbar T, Hurwitz A, Lavy Y. The significance of intrauterine lesions detected by ultrasound in asymptomatical postmenopausal women. Br J Obstet Gynaecol. 2005;112:379-382. https://doi.org/10.1111/j.1471-0528.2004.00444.x
- Ozelci R, Dilbaz B, Akpınar F, Kınay T, Baser E, Aldemir O, Altınbas SK. The significance of sonographically thickened endometrium in asymptomatic postmenopausal women. Obstet Gynecol Sci. 2019;62:4:273-279. https://doi.org/10.5468/ogs.2019.62.4.273
- Li Z, Li L. Risk of malignancies among asymptomatic postmenopausal women with thickened endometrium: A cohort study. Medicine (Baltimore). 2019;98:6:e14464. https://doi.org/10.1097/MD.0000000000014464
- Alcázar JL, Bonilla L, Marucco J, Padilla AI, Chacón E, Manzour N, Salas A. Risk of endometrial cancer and endometrial hyperplasia with atypia in asymptomatic postmenopausal women with endometrial thickness ≥11 mm: A systematic review and meta-analysis. J Clin Ultrasound. 2018;46:9:565-570. https://doi.org/10.1002/jcu.22631
- Ghoubara A, Emovon E, Sundar S, Ewies A. Thickened endometrium in asymptomatic postmenopausal women — determining an optimum threshold for prediction of atypical hyperplasia and cancer. J Obstet Gynaecol. 2018;38:8:1146-1149. https://doi.org/10.1080/01443615.2018.1458081
- Louie M, Canavan TP, Mansuria S. Threshold for endometrial sampling among postmenopausal patients without vaginal bleeding. Int J Gynaecol Obstet. 2016;132:3:314-317. https://doi.org/10.1016/j.ijgo.2015.07.023
- Wolfman W, Leyland N, Heywood M, Singh SS, Rittenberg DA, Soucy R, Allaire C, Awadalla A, Best C, Dunn S, Leroux N, Potestio F, Senikas V, Wallace S, Menzies R; Society of Obstetricians and Gynaecologists of Canada. Asymptomatic endometrial thickening. J Obstet Gynaecol Canada. 2009;32:10:990-999.
- Genc M, Genc B, Sahin N, Celik E, Turan GA, Gur EB, Guclu S. Endometrial pathology in postmenopausal women with no bleeding. Climacteric. 2015;18:2:241-245. https://doi.org/10.3109/13697137.2014.944152
- Адамян Л.В., Мельникова Н.С., Касян В.Н. Патология эндометрия в постменопаузе: нужен ли ультразвуковой скрининг? Проблемы репродукции. 2019;25:2:113-119. https://doi.org/10.17116/repro201925021113
- Litta P, Di Giuseppe J, Moriconi L, Delli Carpini G, Piermartiri MG, Ciavattini, A. Predictors of malignancy in endometrial polyps: a multi-institutional cohort study. Eur J Gynaecol Oncol. 2014;35:4:382-386.
- Ricciardi E, Vecchione A, Marci R, Schimberni M, Frega A, Maniglio P, Caserta D, Moscarini M. Clinical factors and malignancy in endometrial polyps. Analysis of 1027 cases. European J Obstet, Gynecol Reprod Biol. 2014;183:121-124. https://doi.org/10.1016/j.ejogrb.2014.10.021
- Gambadauro P, Martinez-Maestre MA, Schneider J, Torrejon R. Endometrial polyp or neoplasia? A case-control study in women with polyps at ultrasound. Climacteric. 2015;18:3:399-404. https://doi.org/10.3109/13697137.2014.967673
- Ferrazzi E, Zupi E, Leone FP, Savelli L, Omodei U, Moscarini M, Barbieri M, Cammareri G, Capobianco G, Cicinelli E, Coccia ME, Donarini G, Fiore S, Litta P, Sideri M, Solima E, Spazzini D, Testa AC, Vignali M. How often endometrial polyps malignant in asymptomatic postmenopausal women? A multicenter study. Am J Obstet Gynecol. 2009;200:3:235. https://doi.org/10.1016/j.ajog.2008.09.876
Рекомендуем статьи по данной теме:
Введение
Гиперпластические процессы в эндометрии представляют большую медико-биологическую и социально-экономическую проблему и занимают значительное место в структуре гинекологической заболеваемости [1—6]. Высокая распространенность гиперпластических процессов в эндометрии, отсутствие должной эффективности от гормональной терапии, а также вероятность озлокачествления ставят гиперплазию эндометрия (ГЭ) в ряд наиболее актуальных проблем современной медицины. По данным Е.М. Вихляевой, гиперплазией эндометрия страдают почти 50% женщин позднего репродуктивного возраста и в период перименопаузы [7].
Большая клиническая значимость гиперпластических процессов в эндометрии заключается в том, что они являются одной из наиболее частых причин маточных кровотечений у женщин в возрасте 45—55 лет и их госпитализации в стационар [8—12]. Другая причина пристального внимания к ГЭ — это возможность их злокачественной трансформации. По данным статистики РФ, рак эндометрия (РЭ) занимает 3-е место в структуре онкологической заболеваемости женского населения [13, 14]. Малигнизация железистой гиперплазии и полипа эндометрия встречается в 2—5% и достигает 10% в постменопаузе [15—17]. Атипическая гиперплазия прогрессирует в инвазивный рак с частотой до 50% наблюдений [18, 19]. Однако, по данным разных авторов, РЭ по результатам гистологического исследования подтверждается у 1—10% женщин, имеющих кровотечение в постменопаузе. Практически в 60% наблюдений выявляется атрофия эндометрия и примерно с одинаковой частотой — полипы эндометрия, ГЭ и другие доброкачественные изменения эндометрия [20, 21]. Таким образом, в большинстве случаев причиной кровотечений в постменопаузе служат изменения эндометрия доброкачественного характера.
Факторами риска развития РЭ являются пожилой возраст пациенток (старше 50 лет), ожирение, поздняя менопауза, сахарный диабет, длительная эстрогеновая стимуляция, прием тамоксифена [22, 23].
При ожирении и индексе массы тела (ИМТ) более 25 кг/м2 повышается риск развития РЭ на 200—400% [24]. Так как более 50% женщин в постменопаузе имеют избыточную массу тела, необходима онконастороженность в данной возрастной группе.
Диагностика патологии эндометрия
В скрининговой диагностике патологии эндометрия наиболее информативным неинвазивным методом обследования является лучевой — ультразвуковое исследование (УЗИ) — неинвазивный, легко выполнимый и высокоинформативный метод обследования больных для выявления количественных и качественных характеристик всех слоев эндометрия с оценкой их кровоснабжения, что позволяет современная аппаратура [25, 26]. Методами лучевой диагностики, в отсутствие клинических проявлений заболевания, могут выявляться различные признаки диффузных (гиперплазия) или очаговых (полипы) изменений эндометрия [27, 28].
В настоящее время согласно клиническим рекомендациям Министерства здравоохранения РФ [29] и международным протоколам [30] за верхнюю границу нормы толщины М-эха принимают 4 мм. Если она ниже этой границы, то вероятность РЭ составляет менее 1% [31—34], в таких случаях биопсия эндометрия не требуется. В ряде случаев увеличение толщины эндометрия по данным УЗИ выявляется у женщин в постменопаузе в отсутствие симптомов заболевания. Однако тактика ведения в таких случаях окончательно не определена. Последнее обстоятельство особенно важно, поскольку в настоящее время среди исследователей прочно укоренилось мнение, что толщина эндометрия является ведущим признаком гиперплазии [35]. Однако в литературе появляются данные о необходимости изменения ультразвуковых критериев толщины эндометрия для определения дальнейшей тактики ведения женщин в отсутствие клинических проявлений в постменопаузе, так как выбор метода лечения и его применение порой ограничены из-за сопутствующей соматической патологии больных. Особые трудности возникают при лечении больных с ГЭ старше 60 лет ввиду высокого риска развития осложнений при оперативном вмешательстве и применении анестезиологического пособия. Поэтому необходимо разграничить группы пациенток с утолщенным эндометрием (по УЗИ в отсутствие клинических проявлений), которым обязательно должны проводиться дальнейшая диагностика и лечение, и группы пациенток, которые могут находиться под динамическим наблюдением (без риска развития РЭ) в связи с возрастом, наличием соматической патологии или нежеланием (отказом) пациентки от дальнейшего лечения (диагностического обследования).
Современные данные литературы о дифференциальной диагностике и тактике ведения женщин в пери- и постменопаузе с патологией эндометрия
В исследовании A. Lev-Sagie и соавт. [36] под наблюдением находились 82 женщины в постменопаузе со случайно выявленным при УЗИ утолщением эндометрия, всем выполнена гистероскопия с выскабливанием стенок полости матки. По результатам гистологического исследования, у 67 (82%) пациенток выявлены неактивные полипы, у 7 — субмукозные узлы, у 6 — атрофия эндометрия, у 1 — простая гиперплазия, еще у 1 — полип с простой гиперплазией. Ни одного случая сложной гиперплазии или РЭ не было. При этом частота развития осложнений оперативного вмешательства составила 3,6%: 2 перфорации матки, 1 осложнение интубации.
R. Ozelci и соавт. [37] проанализировали истории болезни 266 женщин в постменопаузе, которым были выполнены гистероскопия и биопсия эндометрия. В исследование были включены пациентки с отсутствим симптомов, у которых, по данным трансвагинального ультразвукового исследования (ТВУИ), толщина эндометрия равна или превышает 6 мм. По результатам гистологического исследования, наиболее часто выявляемыми очаговыми поражениями у пациенток в отсутствие симптоматики были полипы эндометрия, диагностированные в 168 (63,1%) наблюдениях. У 24 (9%) пациенток была диагностирована простая гиперплазия, у 4 (1%) — атипичная гиперплазия и у 8 (3%) — аденокарцинома эндометрия. По мнению авторов обзора, при толщине эндометрия ≥10,5 мм рекомендованы гистероскопия и кюретаж стенок полости матки.
Другие исследователи [38] провели ретроспективный анализ (с января 2006 г. по январь 2017 г.) медицинских карт 488 женщин в постменопаузе, не имевших клинических проявлений, у которых при ТВУИ выявили эндометрий толщиной ≥5 мм и провели гистероскопию с последующей биопсией эндометрия. Наиболее частыми патологическими находками были полипы (51,0%) и нормальный эндометрий (34,2%). У 15 (3,1%) и 10 (2,0%) больных имелась интраэпителиальная неоплазия и карцинома соответственно. Однако пациентки с карциномой обладали более толстым эндометрием, в котором чаще определялся кровоток при цветовом допплеровском картировании (ЦДК). В исследовании отмечено, что при злокачественных новообразованиях толщина эндометрия была ≥12 мм, и при ЦДК определялись локусы кровотока в эндометрии.
J. Alcázar и соавт. [39] изучили результаты исследований, опубликованных в период с января 1990 г. по декабрь 2016 г., и оценили корреляцию между толщиной эндометрия, измеренной с помощью ТВУИ, и гистологическими находками у женщин, не имевших клинических проявлений в постменопаузе. Научные работы, включавшие исследования у пациенток, которые принимали заместительную гормональную терапию, тамоксифен или ингибиторы ароматазы, были исключены. Было выявлено 289 исследований, и оценены данные по 4751 женщине. Распространенность РЭ или ГЭ с атипией составила 2,4%. В результате исследователи пришли к выводу, что риск развития РЭ или ГЭ с атипией был в 2,6 раза выше у женщин с толщиной эндометрия ≥11 мм в отличие от такового у женщин с толщиной эндометрия 5—10 мм, хотя имелись значительные расхождения в разных исследованиях.
A. Ghoubara и соавт. в своем исследовании [40] также пришли к выводу, что использование порога толщины эндометрия ≥10 мм у женщин без клинических симптомов позволяет не упустить ни одного случая атипичной ГЭ или РЭ.
Целью исследования M. Louie и соавт. [41] было уточнение частоты внутриматочной патологии у 462 женщин с бессимтомно протекающей постменопаузой, не имевших клинических ее проявлений, и обеспечение оптимального порога для взятия у них биоптата эндометрия. В исследование включали женщин без симптомов заболевания эндометрия, если при ТВУИ у них была выявлена толщина эндометрия выше 4 мм.
Среди 462 женщин карцинома была выявлена у 9 (1,9%), атипичная гиперплазия — у 7 (1,5%). Толщина эндометрия, равная или превышающая 14 мм, достоверно ассоциировалась с типичной гиперплазией (отношение шансов — ОШ 4,29; 95% доверительный интервал — ДИ 1,30—14,20; p=0,02), с отрицательным прогностическим значением 98,3%. Толщина более 15 мм была ассоциирована с карциномой (ОШ — 4,53; 95% ДИ — 1,20—17,20; p=0,03), с прогностической значимостью отрицательного результата теста 98,5% и риском развития рака 0,06%. Таким образом, исследователи пришли к выводу, что случайно обнаруженное утолщение эндометрия менее 15 мм не может служить основанием для взятия биопсии эндометрия у женщин в постменопаузе, не имеющих вагинального кровотечения.
W. Wolfman и соавт. [42] изучили материалы публикаций, вышедших с 1970 по 2009 г., о результатах обследования женщин в постменопаузе без аномальных маточных кровотечений, у которых при УЗИ обнаружено утолщение эндометрия. При детальной оценке информативности, рисков и стоимости диагностического выскабливания авторы пришли к выводу, что применение инвазивных методов исследования только на основании увеличения показателя М-эхо является излишней (неоправданной) процедурой.
Однако некоторые исследователи придерживаются другой точки зрения. Целью исследования M. Genc и соавт. [43] было уточнение частоты внутриматочной патологии у 283 женщин в постменопаузе, госпитализированных в гинекологическое отделение для проведения гистерэктомии по причинам, не связанным с патологией эндометрия. По результатам гистологического исследования, у 75,6% из 209 пациенток, не имевших кровотечения в постменопаузе, обнаружена патология полости матки, о которой не подозревали на этапе предоперационной подготовки: ГЭ, полипы, миома матки, аденомиоз — в 1 (0,5%) наблюдение, аденокарциномы. У 87,8% из 74 женщин с кровотечением в постменопаузе обнаружена внутриматочная патология, в том числе 13 (17,6%; p=0,0001) наблюдений РЭ. Таким образом, патология полости матки может иметься и у женщин в постменопаузе, не имеющих симптомов заболевания, поэтому авторы настаивают на ежегодном скрининге и консультировании пациенток пожилого и старческого возраста, не дожидаясь у них эпизода кровотечения.
Л.В. Адамян и соавт. [44] в своем исследовании пациенток без клинических проявлений внутриматочных заболеваний в постменопаузе с подозрением на патологию эндометрия по данным ТВУЗ (толщина эндометрия более 4 мм), чаще всего выявляли полипы эндометрия (63,9%), атрофию эндометрия (30,5%), а частота аденокарциномы составила 2,1%. Авторы исследования акцентируют внимание на том, что риск возникновения злокачественных новообразований достаточно высок, что свидетельствует о важности адекватного обследования и своевременного лечения женщин этой возрастной группы, а также о необходимости скринингового обследования с применением УЗИ.
По данным литературы, у пациенток без клинических проявлений заболевания матки в постменопаузе с утолщеным эндометрием (по данным УЗИ) наиболее часто при гистероскопии и гистологическом исследовании выявляются полипы эндометрия. Однако частота РЭ у женщин с полипами эндометрия составляет 0,3—4,8% [45]. Большинство исследователей настаивают на обращении особого внимания на пациенток в постменопаузе с полипами, проявляющимися маточным кровотечением. Так, E. Ricciardi и соавт. [46] изучали распространенность полипов с атипией у пациенток в постменопаузе. В ретроспективном исследовании проанализированы данные 1027 женщин с полипами эндометрия в пери- и постменопаузе. Доброкачественные полипы выявлены в 95,8% случаев, предраковые — в 2,67% и с атипией — в 1,54% случаев. У женщин в постменопаузе (старше 60 лет) и старческом возрасте риск развития РЭ был выше (ОШ 3,05; 95% ДИ 1,54—6,19; p<0,001 и ОШ 2,8; 95% ДИ 1,38—5,56; p≤0,003 соответственно). У пациенток с кровотечением в постменопаузе риск развития РЭ повышался более чем в 30 раз (ОШ 31,1; 95% ДИ 10,3—111; p<0,001). По мнению авторов, на пациенток с кровотечением в постменопаузе следует обращать особое внимание, а женщины без симптомов заболевания в постменопаузе относятся к группе промежуточного риска, поэтому к ним необходим индивидуальный подход.
P. Gambadauro и соавт. [47] при анализе данных 1390 пациенток в постменопаузе с подозрением на полип эндометрия (по данным УЗИ) после гистероскопии установили, что все случаи неоплазии отмечены лишь у пациенток с кровотечением. У 40,6% женщин без кровотечения гистологически подтверждена доброкачественная структура полипа эндометрия. Пациентки, у которых диагностирован РЭ, были значительно старше пациенток с доброкачественной патологией, а также имели более высокий индекс массы тела. По мнению авторов, большое число женщин в постменопаузе без симптомов заболевания с подозрением на полип по данным УЗИ направляют на гистероскопию, хотя риск неоплазии в таких случаях крайне невысок.
E. Ferrazzi и соавт. [48] наблюдали 1152 женщины без симптомов заболевания в постменопаузе, у которых по данным УЗИ и соногистерографии выявлены полипы эндометрия, всем женщинам выполнены гистероскопия и кюретаж стенок полости матки. По данным гистологического исследования, выявлен 1 (менее 0,1%) случай РЭ в полипе диаметром более 4 мм, при этом частота неоплазии была в 10 раз ниже, чем у пациенток с кровотечением. Частота атипических гиперпластических полипов составила 1,2% у пациенток без симптомов заболевания и 2,2% — при наличии кровотечения. Выявлены 3 (0,3%) случая РЭ (не в полипе), которые в ходе гистероскопии визуализировались в виде полипоидных изменений. Риск выявления неоплазии у пациенток без клинических проявлений зависел от диаметра полипа (более 18 мм, ОШ 6,9; 95% ДИ 2,2—21,4 мм). При этом среди осложнений было 3 перфорации, 7 разрывов шейки матки, 3 ложных хода.
Заключение
У пациенток в пери- и постменопаузе патологические процессы в эндометрии протекают чаще всего бессимптомно, однако риск возникновения злокачественных новообразований выше общепопуляционных показателей, особенно при наличии кровотечений и рецидивов патологических процессов в эндометрии. Следует отметить, что диагноз может быть установлен на основании ультразвукового скрининга. При отсутствии единого мнения о рацио- нальных диагностике и наблюдении данного контингента женщин эта проблема требует дальнейшего изучения.
Участие авторов:
Концепция и дизайн исследования — М.А. Чечнева;
Сбор и обработка материала — О.В. Капитанова;
Статистическая обработка данных — О.В. Капитанова;
Написание текста — О.В. Капитанова;
Редактирование — М.А. Чечнева.
Авторы заявляют об отсутствии конфликта интересов.
Мы используем файлы cооkies для улучшения работы сайта. Оставаясь на нашем сайте, вы соглашаетесь с условиями
использования файлов cооkies. Чтобы ознакомиться с нашими Положениями о конфиденциальности и об использовании
файлов cookie, нажмите здесь.










