- Авторы
- Файлы
Парахонский А.П.
Тимофеев В.А.
На современном этапе иммунотерапия является неотъемлемой частью четвёртого направления в терапии опухолевых заболеваний. Большинство иммунотропных препаратов не обладает прямой противоопухолевой активностью, поэтому оптимальный клинический эффект может быть достигнут только при сочетании радикального противоопухолевого лечения с иммунотерапией. Существуют: специфическая иммунотерапия — инициирующая развитие специфических противоопухолевых иммунных реакций (так называемые противоопухолевые вакцины) и неспецифическая, восстанавливающая нарушенные количественные и функциональные показатели иммунной системы и повышающая в результате этого противоопухолевую резистентность организма в целом. Фармацевтический рынок предлагает большое количество лекарственных средств, влияющих на иммунную систему и на противоопухолевую резистентность организма. Среди них особого внимания заслуживает Галавит — отечественный иммуномодулятор с противовоспалительной активностью.
Цель работы — анализ механизмов иммуномодулирующих и противоопухолевых эффектов Галавита, который представляет собой аминодигидрофталазиндион натрия и является единственным иммуномодулятором с противовоспалительным механизмом действия, вследствие модуляции синтеза провоспалительных цитокинов гиперактивными макрофагами. Он способен, как супрессировать избыточные проявления иммунного ответа (обратимое ингибирование гиперактивированных макрофагов на 6-8 часов), так и повышать иммунную реакцию при недостаточной её активности. Основные механизмы действия Галавита осуществляются по следующим направлениям. Он регулирует активность макрофагов и синтез цитокинов (ИЛ-1, ИЛ-6, ФНО-α), повышает неспецифическую защиту организма за счёт усиления фагоцитарной активности нейтрофилов, повышает уровень иммуноглобулинов при их недостаточности, регулирует пролиферативную активность субпопуляций Т-лимфоцитов (Т-хелперы, Т-киллеры) регулирует пролиферативную активность NК-клеток, стимулирует синтез интерферонов, обладает антиоксидантным действием.
Установлено, что Галавит нормализует репрезентативную функцию макрофагов, синтез ими провоспалительных и противовоспалительных цитокинов, фагоцитарную активность нейтрофилов, цитотоксическую активность NK-клеток, усиливает продукцию ИЛ-2 Т-лимфоцитами и наработку лимфокинактивированных киллеров. Он регулирует пролиферацию Т- и В-лимфоцитов, синтез цитокинов (ИФ-α, ИФ-γ), опосредованно воздействует на гуморальное звено иммунитета, нормализуя продукцию антител и их функциональную активность. Отмечено, что на фоне применения Галавита повышается биодоступность опухоли для противоопухолевых препаратов и лучевой терапии. Характерно, что препарат не воздействует на нормально функционирующие клетки, что выгодно отличает его от большинства иммуномодулирующих препаратов. Доклинические исследования показали, что Галавит при концентрациях, не оказывающих цитотоксического действия на опухолевые клетки, ингибирует их инвазивную активность. Данный эффект проявляется как в отношении клеток экспериментальных опухолей мыши, так и опухолей человека. Клинические исследования подтвердили, что включение Галавита в традиционную схему послеоперационного лечения больных с гипернефроидным раком, инвазивным раком мочевого пузыря обеспечивает адекватную коррекцию иммунных нарушений и способствует снижению эндогенной токсемии, количества осложнений, летальности и длительности лечения больных в стационаре. Проведенный анализ наблюдения и терапии больных с диагнозом — аденома и рак простаты доказал, что у пациентов, которым к стандартной терапии добавлялся Галавит достоверно реже, по сравнению с контрольной группой, развивались не только иммунологические нарушения, опосредованные действием химиопрепаратов, но и была ниже частота таких побочных эффектов химиотерапии, как тошнота, рвота, диарея. Отмечено, что в группе «Галавит» частота возникновения отдалённых метастазов была достоверно ниже по сравнению с группой контроля. Коррекция иммунного статуса, и как результат, снижение частоты возникновения и тяжести протекания побочных эффектов привели к значительному улучшению общего состояния онкологических больных.
Таким образом, применение Галавита в комплексной терапии онкологических больных способствует нормализации иммунного статуса, повышению неспецифической резистентности, снижению частоты возникновения и тяжести инфекционных осложнений, длительности послеоперационного реабилитационного периода, улучшению переносимости химио- и радиотерапии, способствует формированию настроя на выздоровление и улучшает качество жизни онкологических больных.
Библиографическая ссылка
Парахонский А.П., Тимофеев В.А. ПРИМЕНЕНИЕ ГАЛАВИТА В ОНКОЛОГИЧЕСКОЙ ПРАКТИКЕ // Современные наукоемкие технологии. – 2008. – № 12.
– С. 34-35;
URL: https://top-technologies.ru/ru/article/view?id=24340 (дата обращения: 23.09.2023).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Роль иммуномодулятора Галавит в онкологической и хирургической практике
Статьи
Опубликовано в журнале:
РОССИЙСКИЙ БИОТЕРАПЕВТИЧЕСКИЙ ЖУРНАЛ »» N3/том3/2004
Л.И. Коробкова, Л.З. Велъшер, А.Б. Германов, Т.И. Гришина, А.И. Станулис, Г.П. Генc, Д. О. Щепеляев, Р.Е. Израилов
‘Московский Государственный Медико-Стоматологический Университет Центральная клиническая больница им. И.А. Семашко МНСРФ, Москва
РЕЗЮМЕ
Лекарственное средство Галавит — противовоспалительный и иммуномодулирующий препарат, который воздействует на иммунную систему опосредованно, через макрофаги. Препарат применяется в онкологической и хирургической практике
Ключевые слова: иммуномодулятор, Галавит, онкология, хирургия
В настоящее время большое внимание уделяется созданию иммунотропных препаратов и разработке адекватных методов направленной иммунокоррекции. Повышенный интерес к данному разделу медицины не случаен, поскольку различные компоненты иммунной системы участвуют в реакциях организма на внедрение чужеродных агентов и повреждения собственных тканей, в репаративных процессах, предотвращении опухолевого рост и элиминации трансформированных клеток, в кроветворении. При этом действие иммуннокомпетентных клеток может быть направлено на защиту организма от внешних и внутренних патогенных факторов и в то же время представлять ключевое звено развития значительного числа заболеваний человека.
Лекарственное средство Галавит, представляющее собой производное аминофталгидразида, разрешено к клиническому применению приказом МЗ РФ от 31 марта 1997 года в качестве противовоспалительного и иммуномодулирующего препарата [1].
Большинство иммуномодуляторов не проявляют прямого цитотоксического и противоопухолевого действия. Однако при доклиническом исследовании нового иммуномодулятора (зарегистрирован в 1997 г. под названием Галавит) была замечена его способность не только усиливать противоопухолевый иммунитет путем повышения и/или восстановления эффекторного механизма, опосредованного через презентативную функцию макрофагов, регуляцию синтеза интерлейкина-1 (ИЛ-1), фактора некроза опухоли (ФНО), интерлейкина-2 (ИЛ-2), естественных киллеров (NK- клеток) и др., но и модифицировать другие биологические аспекты взаимоотношений организма-носителя и опухоли.
Галавит воздействует на иммунную систему опосредованно, через макрофаги. Как известно, они занимают важное место в развитии процессов специфического иммунитета, находясь в самом начале активации каскада иммунокомпетентных клеток. Без макрофагов иммунный ответ обычно не развивается, это связано с тем, что макрофаги — абсолютно необходимые клетки для «презентации» антигена, т.е. представляют его иммунокомпетентным Т- и В-лимфоцитам в «удобном» виде: с антигенами комплекса гистосовместимости.
Одновременно макрофаги выделяют вещества-активаторы иммунитета — цитокины, влияющие на разные этапы иммунной реакции и на различные типы клеток.
Адгезия макрофагов наблюдается как к чужеродным, так и к собственным клеткам организма, так как они играют важную роль и в процессах распознавания «свое-чужое», оберегая организм от развития аутоагрессивных реакций и инициируя процесс иммунной элиминации измененных клеток при их опухолевом перерождении.
Первые исследования показали способность Галавита нормализовать скорость синтеза биологических макромолекул в макрофагах РНК, ДНК и белка. Так, препарат проявляет противовоспалительную активность вследствие способности обратимо (на 6-8 ч) ингибировать синтез гиперактивированными макрофагами провоспалительных цитокинов ФНО и ИЛ-1 или стимулировать их при исходной недостаточности. При этом Галавит способен восстановить угнетенную фагоцитарную функцию макрофагов и нейтрофилов и, следовательно, противоинфекционную защиту. Одновременно восстанавливается антиген-представляющая
функция макрофагов, активизируются процессы репарации поврежденных тканей, купируются клинические симптомы интоксикации и диарейного синдрома, восстанавливается адекватное
функционирование иммунной системы. Большинство фармакологических эффектов Галавита обусловлены модуляцией функциональной активности моноцитов/макрофагов и продукции ими некоторых ключевых цитокинов, в частности, интерлейкина-1 и фактора некроза опухолей, а также нитросоединений и реакционно-способных радикалов.
Принимая во внимание способность клеток моноцитарно-макрофагального ряда и их продуктов играть важную роль в противоопухолевом иммунном ответе, было изучено действие Галавита на опухолевый рост и метастазирование мышиной меланомы В16, а также на продолжительность жизни животных-опухоленосителей. Исследование проводилось в лаборатории клеточной иммунопатологии и биотехнологии НИИ морфологии человека РАМН.
В большинстве экспериментов Галавит в определенной степени угнетал рост подкожного узла меланомы и увеличивал продолжительность жизни мышей-опухоленосителей, но статистически значимых различий с контролем выявлено не было.
Интересные данные получены in vitro при изучении антиметастатической активности препарата. При введении 50 мкг Галавита 1 раз в 3 дня показано достоверное (р<0,05) снижение на 44% количества легочных метастазов на 28-й день эксперимента.
Вероятно, вышеописанные противоопухолевые эффекты препарата опосредованы стимуляцией макрофагов, являющихся основной мишенью биологического действия Галавита. Именно макрофаги реализуют процесс представления и, следовательно, точность распознавания антигена, т.е. решают ключевую задачу иммунной системы: различать «свое» и «чужое». Однако конкретные механизмы его антиметастатической активности требуют дальнейшего детального изучения.
В медицинском Радиологическом научном центре РАМН (г. Обнинск) было проведено экспериментальное изучение противоопухолевой активности влияния препарата Галавит на рост и метастазирование карциномы Льюиса у мышей-опухоленосителей. Исследована эффективность Галавита в качестве средства монотерапии, а также сочетание его с известным противоопухолевым препаратом циклофосфаном.
Применение Галавита в дозе 50 мкг/мышь способствовало статистически достоверному усилению антиметастатического действия циклофосфана — количество легочных метастазов снижалось в 4 раза по сравнению с уровнем метастазирования при применении только одного циклофосфана. Следует обратить внимание, что у 4 из 12 мышей группы “циклофосфан + Галавит 50 мкг/мышь» макроскопически видимые метастазы отсутствовали вообще.
Возможно, что эти эффекты опосредовались стимуляцией NK-клеток и CD8+ цитотоксических лимфоцитов, но в любом случае эти результаты достойны внимания клинических иммунологов и онкологов, в том числе для лечения больных генерализованным раком молочной железы.
Как известно, иммунная система онкологических больных чрезвычайно сложна и характеризуется дисбалансом различных ее звеньев. Снижение некоторых иммунологических показателей часто проявляется у генерализованных больных, перенесших в процессе противоопухолевого лечения: 1) цитостатическую терапию, 2) лучевую терапию, 3) оперативное вмешательство. Эти виды лечения способствуют различным нарушениям иммунитета. Очень часто у этой группы диагностируется вторичный иммунодефицит, вызванный предшествующим лечением, наблюдается гибель иммунных клеток по типу некроза или, чаще всего, апоптоза, а также дисбаланс эффекторных и супрессорных клеток. Так, лечение цитостатиками приводит к уничтожению покоящихся лимфоцитов по типу апоптоза, при котором итогом активации индукторов апоптоза является нарушение развития лимфоцитов и их гибель. Тип вторичного иммунодефицита, возникающий, при агрессивном химиотерапевтическом противоопухолевом лечении, относится к комбинированному. Проведен анализ наблюдения и лечения 65 больных с первично установленным диагнозом «метастатический рак молочной железы», или ранее получавших комбинированное или комплексное лечение по поводу данного заболевания, и у которых с течением времени выявлены отдаленные метастазы.
У всех больных диагноз был подтвержден результатами гистологических и цитологических исследований. Наличие отдаленных метастазов было установлено по данным клинического, лабораторного, рентгенологического, ультразвукового, радиоизотопного, компьютерно-томографического методов исследования.
Работа проводилась на основе требований и стандартов международных клинических исследований лекарственных средств «Качественная Клиническая Практика — Good Clinical Practice/GCP», которая позволяет регулировать применение клинических испытаний, обеспечивая надежность полученных данных, а также защищая права, неприкосновенность и конфиденциальность испытуемых.
При этом использовалось рандомизированное двойное слепое плацебо-контролируемое исследование, которое является своего рода «золотым стандартом» клинических испытаний, так как совместное применение технологий слепого исследования и рандомизации предотвращает воздействие на результаты наиболее грубых погрешностей.
Больные были разделены на 2 группы методом рандомизации: пациенты с четным годом рождения составляли первую группу, с нечетным — вторую. Обе группы больных получали одну и ту же схему полихимиотерапии — САР.
На фоне лечения цитостатиками больным обеих групп вводился препарат двух разных серий: №1 и №2; Первая группа получала полихимиотерапию по схеме CAF+ препарат серии № 1, вторая — полихимиотерапию по схеме CAF — препарат серии №2.
Как подразумевает методика двойного слепого рандомизированного плацебо-контролируемого исследования, ни пациент, ни врачи не знали до окончания работы, в какой из серий препарата находится Галавит, а в какой — плацебо. По окончании исследования конверты сданными были открыты, и оказалось, что препарат серии №1 — оригинальный, а препарат серии №2 — плацебо.
В обеих группах наблюдалось снижение уровня некоторых субпопуляций лимфоцитов до лечения, так как большинство включенных в исследование больных ранее получали комбинированное или комплексное лечение по поводу рака молочной железы. Данные представлены в табл. 1.
Как следует из табл. 1, более всего снижалось количество СОЗ+лимфоцитов и СО4+лимфоцитов в обеих группах. При анализе иммунологических показателей после цитостатического лечения на фоне плацебо динамики параметров Т-клеточного иммунитета отмечено не было. В другой группе, где пациенткам на фоне стандартной терапии CAF использовался Галавит, отмечается статистически значимая разница в нормализации иммунологических параметров. Так, содержание СОЗ+лимфоцитов увеличилось с 57,3±2,5 до 63,6±2,9 (р<0,05), СВ4+лимфоцитов — с 31,6+2,3 до 38,9+1,9 (р<0,05). Также отмечена статистически достоверная разница в изменении индекса CD4/CD8: произошла нормализация этого показателя с 1,2±0,1 до 1,9±0,2(р<0,05).
Полностью сохранился исходный уровень CD8 цитотоксических клеток и CD 16 (NK — естественных киллеров).
При этом у пациенток обеих групп определялась поликлональная гиперпродукция всех классов иммуноглобулинов.
Как видно из табл. 2, после лечения произошло снижение исходно повышенных уровней всех классов иммуноглобулинов в группе Галавита, однако в группе плацебо, наоборот, средний уровень иммуноглобулинов еще более возрос (кроме IgM, который изначально был в пределах нормы).
Таким образом, применение иммуномодулирующего препарата Галавит на фоне химиотерапии по схеме CAF в обследованиях больных диссеминированным раком молочной железы привело к улучшению иммунного статуса пациентов, что уменьшило восприимчивость пациентов к инфекционным агентам и повысило качество жизни больных.
Таблица 1
Динамика изменения состояния клеточного звена иммунитета у больных диссеминированным раком молочной железы под влиянием Галавита на фоне полихимиотерапии
|
Препарат |
Срок обсле- |
Субпопуляции лимфоцитов крови, % антиген-положительных клеток |
||||||
|
CD3+ |
CD4+ |
CD8+ |
CD20+ |
HLA-DR |
CD 16+ |
CD4+/CD8+ |
||
|
Галавит |
До лечения |
56,5±2,6 |
31,9+2,5 |
26,1±1,8 |
6,7±1,6 |
10,7±1 |
18,1+1,7 |
1,2+0,1 |
|
После лечения |
63,3±3* |
39,7+2** |
24,9±2 |
5,4±0,9 |
9,5+1,2 |
16,7+1,3 |
1,9+0,2** |
|
|
Плацебо |
До лечения |
61,2±2,8 |
34,4±2,4 |
28,8+4,6 |
8,8±1,4 |
15,4+2,1 |
21,4+2 |
1,2+ОД |
|
После лечения |
64,3+3,1 |
34,7+2,8 |
25,7+1,8 |
4,8+0,6* |
10+1,3* |
17,3+2,4* |
1,5+0,2 |
|
|
Норма |
60-75 |
35-46 |
25-30 |
5-15 |
7-15 |
10-20 |
1,2-2,4 |
|
|
* Различия достоверны: р<0,05 по отношению к соответствующим показателям до лечения; ** Различия достоверны: р<0,01 по отношению к соответствующим показателям до лечения |
Таблица 2
Динамика изменения состояния гуморального звена иммунитета у больных диссеминированным раком молочной железы под влиянием Галавита на фоне полихимиотерапии
|
Препарат |
Срок обследования |
Сывороточные иммуноглобулины, МЕ/мл |
||
|
IgG |
IgM |
|||
|
Галавит |
До лечения |
182±11 |
201123 |
200122 |
|
После лечения |
173i5,6 |
176+15 |
161±13,3 |
|
|
Плацебо |
До лечения |
188±7,4 |
196+-29 |
136112 |
|
После лечения |
195±15 |
220±39 |
126+12 |
|
|
Норма |
140-150 |
110-120 |
150-160 |
Следующим было исследование препарата Галавит в онкологической клинике у больных немелкоклеточным раком легкого (НМРЛ) III стадии в период операции и ближайшего послеоперационного периода, оценка его противовоспалительных и иммуномодулирующих свойств. Также при анализе лечения больных НМРЛ 2 групп исследовались и сравнивались послеоперационные осложнения и их длительность.
В первой группе больных, получающих Галавит, был 31 пациент (5 женщин и 26 мужчин, средний возраст которых составил 61,3+2,7 года), во второй группе (плацебо) — 29 больных (5 женщин и 25 мужчин, средний возраст -59,8+3,1 года). Диагноз «рак легкого» у всех пациентов был верифицирован до операции и представлен плоско -клеточным раком. Из 31 пациента первой группы 21 произведена пульмонэктомия, в ] 0 случаях выполнены билобэктомии. Из 29 больных второй группы в 18 случаях имела место пульмонэктомия и в 11 — билобэктомия.
При хирургическом лечении больных раком легкого одним из грозных осложнений является пневмония. Это осложнение было зарегистрировано в группе плацебо у 68,2% пациентов, причем длительность пневмонии составила в среднем 10 дней на фоне антибактериальной терапии, тогда как в группе больных, которым назначался Галавит, пневмония констатирована лишь у 27,5 % пациентов, то есть наблюдалась в 2,5 раза реже и купировалась в среднем за 5-7 дней на фоне той же антибактериальной терапии.
Важным показателем лечения больных раком легкого III стадии является длительность периода реабилитации, то есть времени до выписки из стационара. Так, больные, оперированные на фоне Галавита, выписывались в среднем через 20,7±4,1 день, тогда как на фоне плацебо — на 28,3+3,9 день (р<0,05).
При анализе иммунного статуса пациентов до начала лечения определялось существенное увеличение абсолютного содержания лимфоцитов (вследствие лейкоцитоза) в обеих группах — 34001190 кл/ мкл крови и 2100± 180 кл/мкл. При этом отмечалось снижение относительного содержания CD3+, CD4+, CD8+, CD20+- лимфоцитов, а также CD 16+ — клеток (NK -лимфоциты), а также HLA-DR — лимфоцитов.
Сразу после операции у пациентов двух групп выявлено еще большее углубление дефицита относительного содержания субпопуляции лимфоцитов, преимущественно за счет HLA-DR и CD20+ (В-лимфоцитов). Важно отметить, что после операции достоверно возросла субпопуляция CD4± лимфоцитов (Т-лимфоцитов-хелперов) и даже превысила норму. Сравнительный анализ иммунного статуса групп больных, получавших Галавит и плацебо, не выявил существенных различий между группами в первые сутки после операции.
Однако в последующем, через 51 день после операции, в иммунном статусе пациентов наблюдались значительные различия. Так, в группе больных, получавших плацебо, абсолютное и относительное содержание субпопуляций лимфоцитов оставалось практически таким же, как в первые сутки после операции. Исключением являлось лишь содержание CD20+ лимфоцитов, составившее 8,5±0,7 % после лечения и лишь 3,4+0,5 % в первые сутки после операции. Это же касалось содержания IgA, уровень которого составил 242±45 МЕ/мл против 339157 МЕ/мл сразу после операции.
Напротив, в группе больных раком легкого, получавших Галавит, все субпопуляции лимфоцитов практически нормализовались. Важным исключением явилось относительное и абсолютное число CD 16+ лимфоцитов — естественных киллеров, играющих особую роль в противоопухолевом иммунитете. При этом их относительное содержание составило 25,8+1,2 % при норме 15,1 % (р<0,05). Принципиально важным явилась нормализация всех трех классов иммуноглобулинов, соответственно IgA — 122+12 (в норме 110-120 МЕ/мл), IgM — 157+17 (в норме 150-160 МЕ/мл), IgG — 143+15 (в норме 140-150 МЕ/мл). Важно отметить, что это сопровождалось нормализацией содержания CD20 — лимфоцитов, составивших в этой группе 8,7+0,3 % при норме 5-15 % (табл.3). Это особенно важно, поскольку свидетельствует о нормализации продукции иммуноглобулинов, избыточное количество которых участвует в «механизме ускользания».
Таким образом, препарат Галавит в курсовой дозе 2000 мг у больных раком легкого Ш стадии показал себя высокоэффективным иммуномодулятором, в 2,5 раза уменьшал количество осложнений послеоперационного периода, сроки пребывания больного в стационаре, сокращал период послеоперационной реабилитации в среднем на 8 дней, не вызывал побочных эффектов.
Использование иммунотропных лекарственных средств с преимущественной направленностью действия на макрофагальное звено считается наиболее целесообразным у больных распространенным перитонитом [2; 3; 4].
Таблица 3
Содержание субпопуляций лимфоцитов у больных иемелкоклеточным раком легкого III стадии
| Срок обсле- дования |
Препарат | CD3 | CD4 | CD8 | CD 16 | CD20 | HLA-DR | IgA | IgM | IgG |
| До лечения | Плацебо | 51,3+3, | 40,8+3,4 | 14,1+3,8 | 5,4+3,6 | 2,8+3,7 | 5,2+3,5 | 351111 | 130113 | 152115 |
| Галавит | 50,4+ | 41,2+3,5 | 14,5+3,9 | 6,5+3,8 | 2,9+3,8 | 5,4+3,7 | 340+12 | 126+14 | 134+12 | |
| 1 день после операции | Плацебо | 5О,5± | 39,9+4,0 | 12,3+4,1 | 5,2+3,5 | 2,9+3,8 | 4,8+4,0 | 326±9 | 115+12 | 159+14 |
| Галавит | 51,2±3,7 | 38,7+3,8 | 13, | 7,7+3,7 | 3,4±3,7 | 5,1±3,9 | 332+10 | 122+13 | 126+11 | |
| 51 день после операции | Плацебо | 55,6+ | 32,1+3,5 | 14,5± | 8,2±3,7 | 4Д+4,0 | 8,1+3,5 | 243112 | 122114 | 142+14 |
| Галавит | 61,3+ | 36,7+3,8 | 18,7+4, | 12,3±4,0 | 5,7±3,3 | 10,1+3,3 | 121112 | 141+15 | 143+15 | |
| Норма | 60-75 | 35-46 | 25-30 | 10-20 | 5-15 | 7-15 | 110-120 | 150-160 | 140-150 |
Обследовано 66 больных с распространенной формой острого перитонита различной этиологии. В группе сравнения обследованы 34 пациента, которым проводилось традиционное лечение. Основная группа была представлена 32 пациентами, которым к комплексному послеоперационному лечению добавлялся новый отечественный иммуномодулятор Галавит.
Препарат вводился внутримышечно по 100 мг 3 раза в течение первых сут, и по 100 мг 2 раза в последующие 9 сут послеоперационного периода у больных основной группы в добавление к комплексной терапии. Среди всех больных распространенным перитонитом у 35 (53 %) пациентов он носил разлитой характер, у 31 (47 %) пациентов отмечалась диффузная стадия.
В 1 -е сутки послеоперационного периода выявлено достоверное снижение процентного содержания Т-лимфоцитов (СDЗ+-клеток), а также их субпопуляций -Т-хелперов/индукторов (CD4+), Т-супрессоров/цитотоксических лимфоцитов (CD8+), а также увеличение процентного числа В-лимфоцитов. Отмечалось снижение фагоцитарной активности и фагоцитарного числа.
У большинства больных были выявлены значительные гематологические сдвиги: анемия, повышенная СОЭ, лейкоцитоз, увеличение содержания креатинина и мочевины, гипопротеинемия, повышенное содержание билирубина, АлАТ, АсАТ.
В результате анализа динамики клинического течения больных первой группы (традиционная терапия) выявлено, что только по завершении курса лечения происходили незначительные позитивные сдвиги в субъективном состоянии больных и клиническом течении заболевания. Отмечалась некоторая положительная динамика клинико-биохимичсских показателей крови. Сохранялись признаки нарушения иммунного статуса. Всё это способствовало развитию специфических и неспецифических осложнений у 26,5 % больных. Летальность у больных этой группы составила 23,5 %, а средняя продолжительность пребывания больных в стационаре превышала 22 койко-дня. Приведенные данные позволили сделать вывод о недостаточной эффективности традиционных лечебных мероприятий больным распространенной формой острого перитонита.
Анализ клинической картины заболевания в основной группе больных, у которых послеоперационное лечение было дополнено введением Галавита, показал значительные положительные сдвиги на 10-е сут послеоперационного периода. Благоприятное действие иммунокоррекции проявлялось в более быстром темпе нормализации как общего состояния больных, так и лабораторных показателей. Анализ биохимических показателей продемонстрировал, что при использовании Галавита быстрее снижается уровень креатинина, мочевины, билирубина, АсАТ, АлАТ, растет протеинемия. Полученные данные свидетельствуют о более раннем завершении катаболической фазы послеоперационного периода у больных основной группы, что свидетельствовало о противовоспалительном и детоксицирующем действии препарата.
При анализе гемограмм было выявлено, что у больных, получавших Галавит, к 10-м сут отмечен рост гемоглобина и гематокрита. Более показательна была динамика изменения «белой» крови. Достоверное снижение лейкоцитоза у больных, входящих в основную группу, показывало явное противовоспалительное действие препарата.
Таблица 4
Результаты иммунофенотипироваиия лимфоцитов у исследованных больных с острым распространенным перитонитом
|
Показатели |
Течение послеоперационного периода |
Норма |
|||
|
Неосложненное |
Осложненное |
n=35 |
|||
|
Группы больных |
Группы больных |
Группы больных |
Группы больных |
||
|
Основная n=22 |
Сравнения n=17 |
Основная n=6 |
Сравнения n=9 |
||
|
CD3 |
* 47,18*1,23 |
** 50 45+0 99. |
*48,16±1,6 |
* 51,3+0,62 |
67,5±7,5 |
|
CD 4 |
* 30,25+1,17 |
* 31,27+0,52 |
* 28,611,05 |
* 30,7+1,16 |
44,5+5,5 |
|
CDS |
17,625±0,8 |
17,18+0,3 |
17,2±1Д |
*** 21,42+1,52 |
27+8 |
|
CD 16 |
18,31 ±1,04 |
16,9+1,14 |
17,8+2,5 |
16,71+1,91 |
13,5+3,5 |
|
CD 20 |
** 26,93+0,52 |
23,9+ 1,0 |
** 28+0,68 |
** **** 22,42+1,59 |
14+1,2 |
|
CD4/ CDS |
1,756+0,04 |
1,8+0,02 |
1,68+0,06 |
* 1,67+0,02 |
1,9+0,1 |
|
* Различие достоверно при сравнении с нормой, р<0,05; ** Различие достоверно при сравнении с нормой, р<0,01; *** Различие по отношению к показателю предыдущей подгруппы статистически достоверно, р<0,05; **** Различие по отношению к показателю предыдущей подгруппы статистически достоверно, р<0,01 |
К концу лечения анализ изменений Т-клеточного звена указывал на выраженное иммунокорригирующее действие Галавита (табл. 4). У больных отмечалось достоверное увеличение показателей по сравнению с исходными данными за счет CD3+, CD4+, CD8+ клеток. Важно подчеркнуть, что в основной группе была отмечена стабилизация CD20+.
При анализе сывороточных иммуноглобулинов класса IgG, IgM и IgA каких-либо достоверных изменений по сравнению с первой группой получено не было, что, видимо, требует более длительного наблюдения за состоянием гуморального иммунитета.
Со стороны фагоцитарного звена иммунитета по сравнению с контрольной группой выявлена явная тенденция к росту фагоцитарной активности нейтрофилов и фагоцитарного числа. Показатели NK-клеток (CD 16+) оставались в пределах нормальных, в связи с чем не отмечено какой-либо существенной динамики, что подчеркивает избирательность действия Галавита только в случае их недостаточности. Наряду с нормализацией показателей иммунного статуса позитивные сдвиги отмечены при оценке параметров эндогенной интоксикации. Более ранняя нормализация температурной реакции в основной группе указывала на противовоспалительное действие препарата. Количество осложнений со стороны органов брюшной полости, а также других органов и систем уменьшилось до 18,7%. Летальность в этой группе снизилась до 12,5 %. а время пребывания больных в стационаре уменьшилось на 5,9 койко-дня. Сравнительная характеристика 2 клинических групп больных распространенными формами перитонита показала, что добавление Галавита к традиционной схеме лечения обеспечивает адекватную коррекцию иммунопатологических нарушений, эндогенной токсемии и способствует снижению количества осложнений, летальности и длительности пребывания больных в стационаре.
Таким образом, отечественный препарат Галавит может быть рекомендован для применения в хирургической и онкологической практике как иммуномодулирующее и противовоспалительное средство, улучшающее результаты лечения и качество жизни больных.
Работа частично поддержана грантом РФФИ N02-06-8549
ЛИТЕРА ТУРА
- Добрица В.П., Ботерашаили Н.М., Добрица Е.В. Современные имуномодуляторы для клинического применения// Руководство для врачей. — СПб.: Политехника, 2001.-С. 164-165.
- Гришина Т.Н. Клиническое значение нарушения иммунитета при хирургических вмешательствах. (Обзор литературы) // Андрология и генитальная хирургия. -2000. -№ 2. -С. 35-38.
- Карсонова М.И., Пинегин Б. В., Хаитов P.M. Иммунокоррегирующая терапия при хирургической инфекции // Анналы хирургической гепатологии. — 1999. — Т. 4, №1,- С. 88-96.
- Хаитов P.M., Пинегин Б.В. Изменение иммунитета при хирургических вмешательствах // Анналы хирургической гепатологии. -1998. -Т. 3. — С. 100-110
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Галавит® (Galavit) инструкция по применению
📜 Инструкция по применению Галавит®
💊 Состав препарата Галавит®
✅ Применение препарата Галавит®
📅 Условия хранения Галавит®
⏳ Срок годности Галавит®
Описание лекарственного препарата
Галавит®
(Galavit)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для электронного издания справочника Видаль 2023
года, дата обновления: 2022.11.14
Владелец регистрационного удостоверения:
Контакты для обращений:
СЭЛВИМ ООО
(Россия)
Код ATX:
L03
(Иммуностимуляторы)
Лекарственная форма
| Галавит® |
Таб. подъязычные 25 мг: 10, 20, 30, 40, 60 или 80 шт. рег. №: ЛСР-008746/09 |
Форма выпуска, упаковка и состав
препарата Галавит®
Таблетки подъязычные белого цвета с желтоватым оттенком, двояковыпуклые, без риски, с запахом ментола.
Вспомогательные вещества: сорбитол — 0.315 г, крахмал — 0.14 г, лактоза — 0.1 г, кальция стеарат — 0.005 г, тальк — 0.015 г, рацементол (ментол) — 0.0001 г.
10 шт. — упаковки ячейковые контурные из пленки поливинилхлоридной и фольги алюминиевой (1) — пачки картонные.
10 шт. — упаковки ячейковые контурные из пленки поливинилхлоридной и фольги алюминиевой (2) — пачки картонные.
10 шт. — упаковки ячейковые контурные из пленки поливинилхлоридной и фольги алюминиевой (3) — пачки картонные.
10 шт. — упаковки ячейковые контурные из пленки поливинилхлоридной и фольги алюминиевой (4) — пачки картонные.
20 шт. — упаковки ячейковые контурные из пленки поливинилхлоридной и фольги алюминиевой (1) — пачки картонные.
20 шт. — упаковки ячейковые контурные из пленки поливинилхлоридной и фольги алюминиевой (2) — пачки картонные.
20 шт. — упаковки ячейковые контурные из пленки поливинилхлоридной и фольги алюминиевой (3) — пачки картонные.
20 шт. — упаковки ячейковые контурные из пленки поливинилхлоридной и фольги алюминиевой (4) — пачки картонные.
Фармакологическое действие
Механизм действия препарата связан с его способностью регулировать функционально-метаболическую активность врожденного и адаптивного иммунитета (моноцитов, макрофагов, нейтрофилов, натуральных киллеров и других). Галавит® нормализует фагоцитарную активность моноцитов/макрофагов, бактерицидную активность нейтрофилов и цитотоксическую активность NK-клеток. При этом, восстанавливая пониженную активность клеток врожденного и адаптивного иммунитета, препарат повышает резистентность организма к инфекционным заболеваниям бактериальной, вирусной и грибковой этиологии, способствует более быстрой элиминации возбудителя из организма, сокращает частоту, выраженность и длительность инфекций.
Кроме того, Галавит® нормализует антителообразование, повышает функциональную активность (аффинитет) антител, опосредованно регулирует выработку эндогенных интерферонов (ИФН-α, ИФН-γ) клетками-продуцентами.
При воспалительных заболеваниях препарат обратимо (на 6-8 ч) ингибирует избыточный синтез гиперактивированными макрофагами фактора некроза опухолей-α, интерлейкина-1, интерлейкина-6 и других провоспалительных цитокинов, уровень которых определяет степень воспалительных реакций, их цикличность, а также выраженность интоксикации организма. Галавит® снижает выработку гиперактивированными макрофагами активных форм кислорода, тем самым снижая уровень оксидантного стресса и защищая ткани и органы от разрушительного воздействия радикалов. Нормализация избыточно повышенной функциональной активности фагоцитарных клеток приводит к восстановлению их антиген-представляющей и регулирующей функции, снижению уровня аутоагрессии.
Препарат хорошо переносится, не оказывает аллергизирующего, мутагенного, эмбриотоксического, тератогенного и канцерогенного действия.
Фармакокинетика
Выводится из организма, в основном, почками. При подъязычном применении T1/2 составляет 30 мин.
Основные фармакологические эффекты наблюдаются в течение 72 ч.
Показания препарата
Галавит®
У взрослых и подростков старше 12 лет (в т.ч. у лиц с вторичной иммунной недостаточностью) в качестве иммуномодулирующего и противовоспалительного средства в комплексной терапии:
- острых респираторных инфекций, заболеваний дыхательных путей и ЛОР-органов (в т.ч. часто рецидивирующих) бактериальной и вирусной этиологии (ОРВИ, грипп, бронхит, пневмония, тонзиллиты, отит, аденоидиты) и их профилактике;
- воспалительных заболеваний слизистой оболочки полости рта и горла, заболеваниях пародонта;
- хронических рецидивирующих заболеваний, вызванных вирусом герпеса;
- снижения физической работоспособности (в т.ч. у спортсменов).
Режим дозирования
Подъязычно по 1 таб. ежедневно до 4 раз/сут или по 2 таб. до 2 раз/сут.
При острых респираторных инфекциях, гриппе, бронхите, пневмонии, тонзиллите, отите, аденоидите для лечения — по 1 таб. 4 раза/сут. Курс — 5 дней. При хроническом и частом рецидивирующем течении продолжить прием по 1 таб. 4 раза/сут через день курсом до 15 дней. Для профилактики по 1 таб. 2 раза/сут. Курс 5-10 дней.
При воспалительных заболеваниях слизистой оболочки полости рта и горла, заболеваниях пародонта — по 1 таб. 4 раза/сут в течение 5 дней. Затем по 1 таб. 4 раза/сут через 3 суток курсом до 3 недель.
При хронических рецидивирующих заболеваниях, вызванных вирусом герпеса, по 1 таб. 4 раза/сут в течение 10 дней. Затем по 1 таб. 4 раза/сут через сутки в течение 10 дней.
Для повышения физической работоспособности по 1 таб. 4 раза/сут в течение 10 дней, затем по 1 таблетке 4 раза/сут через 3 суток курсом до 3 недель.
Лечение препаратом Галавит® можно начать на любой стадии заболевания.
Препарат следует применять согласно тем показаниям, тому способу применения и в тех дозах, которые указаны в инструкции.
Если после указанных курсов лечения улучшения не наступает или симптомы усугубляются, или появляются новые симптомы, необходимо проконсультироваться с врачом.
Побочное действие
Редко: возможны аллергические реакции.
Если у пациента отмечаются побочные эффекты, указанные в инструкции, или они усугубляются, или отмечаются любые другие побочные эффекты, не указанные в инструкции, следует сообщить об этом врачу.
Противопоказания к применению
- детский возраст до 12 лет;
- беременность;
- период лактации;
- непереносимость галактозы, фруктозы, дефицит лактазы или глюкозо-галактозная мальабсорбция;
- индивидуальная непереносимость.
Применение при беременности и кормлении грудью
Препарат противопоказан беременным женщинам и женщинам в период грудного вскармливания.
Применение у детей
Противопоказано применение препарата в детском возрасте до 12 лет.
Особые указания
В состав препарата входит сорбитол, поэтому пациенты с редкими наследственными патологиями, связанными с непереносимостью фруктозы и сорбитола, не должны принимать препарат.
Влияние на способность к управлению транспортными средствами и механизмами
Препарат не оказывает влияния на способность к управлению транспортными средствами и работу с механизмами.
Передозировка
Случаи передозировки не отмечены.
Лекарственное взаимодействие
Галавит® позволяет повысить эффективность антибиотикотерапии и снизить ее побочные эффекты. При одновременном применении с препаратом Галавит® возможно снижение курсовых доз антибиотиков.
Случаи несовместимости с другими лекарственными препаратами не отмечены.
Условия хранения препарата Галавит®
Препарат следует хранить в недоступном для детей, защищенном от света месте при температуре не выше 25°С.
Срок годности препарата Галавит®
Срок годности — 3 года. Не использовать по истечении срока годности, указанного на картонной пачке.
Условия реализации
Препарат отпускается без рецепта.
Контакты для обращений
СЭЛВИМ ООО
(Россия)

|
|
123290 Москва, |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
В большинстве развитых стран рак легкого является наиболее распространенной формой опухоли и остается одной из важнейших медицинских и социально-экономических проблем. Ежегодно в мире регистрируется 1,04 млн. новых случаев рака легкого, из них 58% приходится на развитые страны (7).

Таблица 1
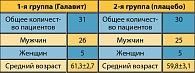
Таблица 2

Таблица 3

Таблица 4. Изменения субпопуляции лимфоцитов у пациентов группы сравнения, получавших плацебо, в разные сроки лечения

Таблица 5. Изменения содержания сывороточных иммуноглобулинов у пациентов группы сравнения, получавших плацебо, в разные сроки лечения

Таблица 6. Изменения субпопуляции лимфоцитов у пациентов группы, получавших Галавит, в разные сроки лечения

Таблица 7. Изменения в иммунном статусе у пациентов группы, получавших Галавит, в разные сроки лечения

Таблица 8. Сравнение частоты случаев нормализаций показателей иммунного статуса у больных обследованных групп на 51 день после операции
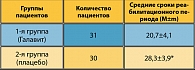
Таблица 9. Средние сроки реабилитационного периода
Накопленные многочисленные данные свидетельствуют о том, что одним из важных факторов, определяющих высокий риск развития рака легкого, является иммуносупрессия (5).
Немелкоклеточный рак легкого представляет собой морфологически неоднородную группу, включающую в основном плоскоклеточный рак (70-75%), аденокарциному (20-25%) различной дифференцировки и другие редкие формы рака. Они объединены в одну группу немелкоклеточного рака по органному принципу и близким отдаленным результатам. Единственным радикальным методом лечения немелкоклеточного рака легкого остается хирургический (2). В настоящее время основной контингент больных, подвергающихся хирургическому лечению – это больные с II–III стадией опухолевого процесса. При проведении хирургического лечения у больных немелкоклеточным раком легкого одним из осложнений является пневмония, которая чаще встречается у пациентов старше 60 лет (8,4%) по сравнению с возрастной группой моложе 60 лет (1,6%). Летальность при этом осложнении по различным литературным данным составляет до 66,7%.
Оперативное вмешательство и развивающиеся в послеоперационном периоде осложнения приводят к значительной иммуносупресии. Целью данной работы явилось исследование клинико-иммунологической эффективности применения иммуномодулятора Галавит у больных немелкоклеточным раком легкого II-III стадии в послеоперационном периоде.
Материалы и методы
Препарат Галавит представляет собой производное аминофталгидразида, он обладает выраженным противовоспалительным и иммуномодулирующим действием. С 1997 года препарат разрешен к клиническому применению приказом МЗ РФ (3). Курсовая доза Галавита составляет 2000 мг (8). Дизайн исследования: препарат применяем в дозе 100 мг внутримышечно в течение 3-х дней до хирургического вмешательства, включая день операции, в течение 2-х дней после операции и далее каждые 3 дня до 51-х суток после операции (таблица 1).
Больные были обследованы рандомизированным двойным слепым плацебо-контролируемым методом. В исследование был включен 61 пациент, находившийся на лечении в хирургическом торакальном отделении НУЗ ЦКБ №2 им. Н.А. Семашко ОАО «РЖД» в период с 2000 по 2004 гг. Диагноз «плоскоклеточный рак легкого» был верифицирован до оперативного лечения. Рандомизация больных осуществлялась путем распределения в основную группу (Галавит) и группу сравнения (плацебо) по четным и нечетным годам рождения пациентов, отобранных для исследования.
Характеристика групп пациентов, включенных в исследование, представлена в таблице 2.
В зависимости от распространенности опухолевого процесса хирургическое лечение производилось в различных объемах (таблица 3), однако частота применения разных видов операций в сравниваемых группах практически не различалась.
Иммунный статус пациентов в обеих группах оценивался до оперативного лечения, на 1-е и 51-е сутки после операции. Сравнительному анализу подвергались абсолютное и относительное содержание CD3, CD4, CD8, CD16, CD20, HLA-DR-лимфоцитов, а также содержание IgA, IgM, IgG-иммуноглобулинов (6,1).
Результаты исследования и их обсуждение
При сравнительном анализе результатов иммунологического исследования у всех пациентов непосредственно перед началом лечения выявляли значительное снижение относительного содержания CD3, CD4, CD8, CD20 – лимфоцитов, CD16 клеток и HLA-DR – лимфоцитов.
У пациентов группы сравнения, получавших плацебо, непосредственно перед операцией абсолютное содержание лимфоцитов составило 2100 ± 180 кл /мкл крови. Относительное содержание CD3 , CD4, CD8, CD16, CD20, HLA-DR лимфоцитов в крови представлены в таблице 4 .
В первые сутки после хирургического вмешательства у пациентов второй группы, получавших плацебо, как и первой группе, получающей Галавит, наблюдали увеличение дефицита относительного содержания HLA-DR и CD20, CD4 лимфоцитов. При сравнении полученных данных с показателями иммунограмм, полученных на 51-е сутки после хирургического лечения, достоверных различий средних величин значений абсолютного и относительного содержания субпопуляций лимфоцитов у больных данной группы по сравнению с результатами первых суток выявлено не было, что отражено в представленных данных таблицы 4. При проведении индивидуального анализа результатов больных отмечена нормализация показателей лишь у части больных данной группы: CD3 у 6 больных (20%); CD4 у 9 больных (30%); CD8 у 9 больных (30%); CD16 у 7 больных (23,3%); CD20 у 11 больных (36,6%); HLA-DR у 18 больных (60%).
При анализе содержания сывороточных иммуноглобулинов до операции у пациентов второй группы, получавших плацебо, так же, как и в первой группе, получавшей Галавит, отмечено значительное увеличение IgA, незначительное увеличение IgG и снижение IgM по отношению к норме (таблица 5).
При анализе изменения содержания сывороточных иммуноглобулинов в первые сутки после оперативного вмешательства достоверных различий выявлено не было по сравнению с предыдущим наблюдением в данной группе пациентов.
На 51-е сутки после хирургического лечения отмечено достоверное снижение среднегрупповых показателей IgA до 243 ± 12 (р≤0,05), содержание же IgM по сравнению с предыдущей иммунограммой, равно как и содержание IgG, достоверно не изменилось. Однако у небольшого числа пациентов отмечена нормализация показателей: IgA – у 3-х больных (10%); IgM – у 6 больных (20%); IgG – у 18 больных (60%).
В первой группе пациентов, получавших Галавит непосредственно перед операцией, абсолютное содержание лимфоцитов в среднем составило 2400 ± 190 кл/мкл крови, что не отличалось от средних значений показателей больных группы сравнения. Относительное содержание субпопуляций лимфоцитов представлено в таблице 6.
На первые сутки после хирургического вмешательства у пациентов первой группы, получавших Галавит, наблюдали отсутствие существенных изменений в соотношении фенотипов клеток по сравнению с исходными данными.
При последующем исследовании иммунного статуса, на 51-е сутки после оперативного вмешательства, были выявлены существенные изменения. Так, зарегистрировано значительное увеличение относительного и абсолютного содержания NK-клеток (CD16) и нормализация других субпопуляций лимфоцитов в среднем по группе (таблица 6). При этом нормализация показателей отмечена у большинства больных данной группы: CD3 – у 28 больных (90,3%); CD4 – у 25 больных (80,6%); CD8 – у 17 больных (54,8%); CD16 – у 14 больных (45,2%); CD20 – у 19 больных (61,3%); HLA-DR – у 20 больных (64,5%).
При оценке уровня сывороточных иммуноглобулинов до операции у пациентов первой группы при применении Галавита выявлено увеличение содержания IgA , содержание же IgM и IgG было снижено (таблица 7). На первые сутки после хирургического вмешательства у пациентов первой группы больных, получавших Галавит, содержание IgA оставалось повышенным и составляло 332 ± 10, содержание IgM и IgG продолжало оставаться ниже нормы: 122 ± 13 и 126 ± 11 соответственно.
В дальнейшем, на 51-е сутки после хирургического лечения, отмечали нормализацию содержания всех трех классов сывороточных иммуноглобулинов: IgA – у 25 больных (80,6%); IgM – у 28 больных (90,3%); IgG – у 26 больных (83,9%).
Сравнение положительных изменений показателей иммунного статуса у больных разных групп на 51-й день после операции представлены в таблице 8.
В процессе исследования отмечено, что в группе больных, получавших плацебо, пневмония, являющаяся одним из грозных осложнений хирургического лечения рака легкого, возникала в 68,9% случаев, причем её длительность в среднем составила 10-12 дней на фоне антибактериальной терапии. В группе больных, получавших Галавит, пневмония была констатирована только у 25,8% пациентов, т.е. наблюдалась в 2,5 раза реже и купировалась в среднем за 5-7 дней (в два раза реже) на фоне аналогичной антибактериальной терапии.
Большое значение в лечении рака легкого имеет длительность реабилитационного периода – время от момента оперативного вмешательства до выписки из стационара (таблица 9).
Полученные результаты позволяют сделать вывод о том, что включение в комплексное лечение больных в послеоперационном периоде препарата Галавит позволяет достоверно (р <0,05) сократить длительность реабилитационного периода.
Заключение
Таким образом, при использовании иммуномодулятора Галавит в комплексной терапии у больных с II–III стадией немелкоклеточного рака легкого после оперативного лечения на фоне применяемой стандартной терапии, значительно чаще наблюдается нормализация показателей клеточного и гуморального иммунитета, более чем вдвое уменьшается частота возникновения послеоперационных осложнений, что положительно влияет на течение послеоперационного и реабилитационного периодов, а следовательно и на качество жизни пациентов.
Аминодигидрофталазиндион натрия
Активное вещество — аминодигидрофталазиндион натрия (Галавит®) 0,025 г, вспомогательные вещества — сорбитол 0,315 г, крахмал 0,14 г, лактоза 0,1 г, кальция стеарат 0,005 г, тальк 0,015 г и рацементол (ментол) 0,0001 г.
Таблетки белого цвета с желтоватым оттенком, двояковыпуклые, без риски, с запахом ментола.
Иммуномодулирующее и противовоспалительное средство
АТХ L03 Иммуноcтимуляторы
Фармакодинамика
Механизм действия Галавита связан со способностью воздействовать на функционально-метаболическую активность макрофагов.
При воспалительных заболеваниях препарат обратимо на 6-8 часов ингибирует избыточный синтез фактора некроза опухолей, интерлейкина-1 и других провоспалительных цитокинов, активных форм кислорода гиперактивированными макрофагами, определяющими степень воспалительных реакций, их цикличность, а также выраженность интоксикации. Нормализация функционального состояния макрофагов приводит к восстановлению их антигенпредставляющей и регулирующей функции, снижению уровня аутоагрессии. Препарат стимулирует бактерицидную активность нейтрофильных гранулоцитов, усиливая фагоцитоз и повышая неспецифическую резистентность организма к инфекционным заболеваниям.
Фармакокинетика
Выводится из организма в основном через почки. При подъязычном применении период полувыведения составляет 30 минут. Основные фармакологические эффекты наблюдаются в течение 72 часов.
В качестве иммуномодулирующего и противовоспалительного средства в комплексной терапии иммунодефицитных состояний у взрослых и подростков старше 12 лет:
— инфекционные кишечные заболевания, сопровождающиеся интоксикацией и/или диареей;
— язвенная болезнь желудка и 12-перстной кишки;
— вирусные гепатиты;
— хронические рецидивирующие заболевания, вызванные вирусом герпеса;
— заболевания, вызванные вирусом папилломы человека;
— инфекционно-воспалительные урогенитальные заболевания (уретрит хламидийной и трихомонадной этиологии, хламидийный простатит, острый и хронический сальпингоофорит, эндометрит);
— гнойно-воспалительные заболевания органов малого таза;
— послеоперационная реабилитация больных с миомой матки;
— осложнения послеоперационного периода у женщин репродуктивного возраста;
— гнойные хирургические заболевания (ожоговые поражения, хронический остеомиелит, гангренозный аппендицит с оментитом, перитонит, гнойный плеврит);
— послеоперационные гнойно-септические осложнения и их профилактика (в том числе, у онкологических больных);
— хронический рецидивирующий фурункулез, рожа;
— астенические состояния, невротические и соматоформные расстройства, снижение физической работоспособности (в том числе, у спортсменов); психические, поведенческие и постабстинентные расстройства при алкогольной и наркотической зависимости;
— воспалительные заболевания слизистой оболочки полости рта и горла, заболевания пародонта;
— частые рецидивирующие заболевания дыхательных путей и ЛОР-органов бактериальной и вирусной этиологии (частые ОРВИ, бронхит, пневмония, хронический тонзиллит, хронический отит, хронический аденоидит) и их профилактика.
Индивидуальная непереносимость; беременность и лактация.
Подъязычно по 1-й таблетке ежедневно до 4-х раз в сутки или по 2 таблетки ежедневно до 2-х раз в сутки, в зависимости от диагноза и тяжести заболевания.
— При острых инфекционных кишечных заболеваниях, сопровождающихся диарейным синдромом: начальная доза составляет 2 таблетки — однократно, затем по 1 таблетке 3-4 раза в день до купирования симптомов интоксикации в течение 3-5 дней.
— При язвенной болезни желудка и 12-перстной кишки в остром периоде: первые 2 суток применять по 1 таблетке 4 раза в день, затем через каждые 3 суток по 1 таблетке 4 раза в день, курс 2-3 недели. В хроническом периоде применять: 5 суток по 1 таблетке 4 раза в день, затем через каждые 3 суток по 1 таблетке 4 раза в день курсом до 3-х недель.
— При вирусных гепатитах различной этиологии: в остром периоде заболевания начальная доза составляет по 2 таблетки 2 раза в день до купирования симптомов интоксикации и- воспаления. Возможно последующее продолжение курса по 1 таблетке 4 раза в день через каждые 3 суток курсом до 2-3-х недель.
— При хронических рецидивирующих заболеваниях, вызванных вирусом герпеса: по 1 таблетке 4 раза в день в течение 10 дней. Затем по 1 таблетке 4 раза в день через сутки в течение 10 дней.
— При заболеваниях, вызванных вирусом папилломы человека: 5 дней по 1 таблетке 4 раза в день, затем по 1 таблетке 4 раза в день через день курсом до 2-3-х недель.
— При урогенитальных заболеваниях — уретрите хламидийной и трихомонадной этиологии, хламидийном простатите: в первый день 2 раза по 2 таблетки, затем по 1 таблетке 4 раза в день через день курсом до 2- х недель (в зависимости от тяжести патологического процесса).
— При сальпингоофорите, эндометрите: в острый период 2 дня по 2 таблетки 2 раза в день, затем по 1 таблетке 4 раза в день через каждые 3 суток в течение 3 недель. В хроническом периоде — 5 дней по 1 таблетке 4 раза в день, затем по 1 таблетке 4 раза в день через каждые 3 суток курсом до 2-3-х недель.
— При острых и хронических гнойных заболеваниях органов малого таза: в остром периоде — В первый день по 2 таблетки 2 раза в день, затем 3 дня по 1 таблетке 4 раза в день, затем по 1 таблетке 4 раза в день через день в течение 10 дней. В хроническом периоде — 5 дней по 1 таблетке 4 раза в день, затем по 3-4 таблетки через каждые 3 суток курсом до 3-х недель.
— Для послеоперационной реабилитации больных с миомой матки и при осложнениях послеоперационного периода у женщин репродуктивного возраста: 5 дней по 1 таблетке 4 раза в день, затем по 1 таблетке 4 раза в день через день курсом до 2-х недель.
— При гнойных хирургических заболеваниях (ожоговые поражения, хронический остеомиелит, гангренозный аппендицит с оментитом, перитонит, гнойный плеврит): применять 4 раза в день по 1 таблетке в течение 5 дней, затем по 1 таблетке 4 раза через день курсом до 15 дней.
— Для профилактики и лечения хирургических осложнений в до- и послеоперационном периоде (в том числе, у онкологических больных) назначают по 1 таблетке 4 раза в день в течение 5 дней до операции, в течение 10 дней после операции по 1 таблетке 4 раза через день и в течение 3-х недель по 1 таблетке 4 раза через 3 суток. При тяжелом течении заболевания в первый день по 2 таблетки 2 раза в сутки.
— При хроническом рецидивирующем фурункулезе, роже: 5 дней по 1 таблетке 4 раза в день, затем по 1 таблетке 4 раза через день курсом до 3-х недель.
— При астенических состояниях, невротических и соматоформных расстройствах, при психических, поведенческих и постабстинентных расстройствах, у пациентов с алкогольной и наркотической зависимостью: 5 дней по 1 таблетке 4 раза в день, затем по 1 таблетке 4 раза через каждые 3 суток в течение 3-х недель. Для повышения физической работоспособности: по 1 таблетке 4 раза через день в течение 10 дней, затем по 1 таблетке 4 раза в день через 3 суток курсом до 3-х недель.
— При воспалительных заболеваниях слизистой оболочки полости рта и горла, заболеваниях пародонта: начальная доза 1 таблетка 4 раза в день в течение 5 дней, затем по 1 таблетке 4 раза в день через 3 суток курсом до 3-х недель
— При частых рецидивирующих заболеваниях дыхательных путей и ЛОР-органов бактериальной и вирусной этиологии (частые ОРВИ, бронхит, пневмония, хронический тонзиллит, хронический отит, хронический аденоидит): применять 4 раза в день по 1 таблетке в течение 5 дней, затем по 1 таблетке 4 раза через день курсом до 15 дней. Для профилактики острых респираторных инфекций и гриппа по 1 таблетке 2 раза в день. Курс 5-10 дней.
В редких случаях возможны аллергические реакции.
При одновременном применении возможно снижение курсовых доз антибиотиков. Случаи несовместимости с другими лекарственными препаратами не отмечены.
Таблетки, содержащие 25 мг Галавита®.
По 10 или 20 таблеток подъязычных в контурной ячейковой упаковке из пленки поливинилхлоридной и фольги алюминиевой. По 1, 2, 3 или 4 контурных упаковки вместе с инструкцией по применению в картонной пачке. 10, 20, 30, 40 или 50 контурных упаковок с равным количеством инструкций по применению в групповой упаковке.
Хранить при температуре не выше 25°С, в защищенном от света, недоступном для детей месте.
3 года.
Не использовать по истечении срока годности, указанного на картонной пачке.
Без рецепта
Регистрационный номер
ЛСР-008746/09
Дата регистрации
2009-11-02
Дата переоформления
2017-11-07
Владелец регистрационного удостоверения
Производитель
СЭЛВИМ ООО
Россия
ЦЕНТР СОВРЕМЕННОЙ МЕДИЦИНЫ МЕДИКОР ЗАО
Россия

