Описание препарата Дупиксент® (раствор для подкожного введения, 150 мг/мл) основано на официальной инструкции, утверждено компанией-производителем в 2021 году
Дата согласования: 10.09.2021
Особые отметки:
Содержание
- Фотографии упаковок
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Аналоги (синонимы) препарата Дупиксент®
- Заказ в аптеках Москвы
Фотографии упаковок
10.09.2021

10.09.2021
Действующее вещество
ATX
Фармакологическая группа
Состав
| Раствор для подкожного введения | 1 мл |
| активное вещество: | |
| дупилумаб | 150/175 мг |
| Ингредиент | Количество (дозировка 150 мг/мл) | Количество (дозировка 175 мг/мл) | ||
| в 1 мл | в 1 шприце1 | в 1 мл | в 1 шприце2 | |
| Действующее вещество | ||||
| Дупилумаб | 150 мг | 300 мг | 175 мг | 200 мг |
| Вспомогательные вещества | ||||
| L-Гистидин | 3,1 мг3 | 6,2 мг3 | 3,1 мг3 | 3,54 мг3 |
| L-Гистидина гидрохлорида моногидрат | ||||
| L-Аргинина гидрохлорид | 4,35 мг4 | 8,7 мг4 | 10,51 мг5 | 12,01 мг5 |
| Натрия ацетата тригидрат | 0,75 мг6 | 1,5 мг6 | 0,75 мг6 | 0,86 мг6 |
| Уксусная кислота ледяная | ||||
| Сахароза | 50 мг7 | 100 мг | 49,88 мг7 | 57,00 мг |
| Полисорбат 80 | 2 мг8 | 4 мг | 2 мг8 | 2,28 мг |
| Вода для инъекций | до 1,0 мл | до 2,0 мл | до 1,0 мл | до 1,14 мл |
1 В расчете на 2,0 мл препарата.
2 В расчете на 1,14 мл препарата.
3 Содержание L-гистидина и L-гистидина гидрохлорида приведено в пересчете на L-гистидин (М=155,16 г/моль), исходя из общей концентрации гистидина в препарате 20 мМ.
4 Содержание L-аргинина гидрохлорида приведено в пересчете на L-аргинин (М=174,20 г/моль), исходя из молярной концентрации L-аргинина в препарате 25 мМ. Номинальное содержание L-аргинина гидрохлорида (М=210,66 г/моль) в одном шприце составляет 10,5 мг.
5 Содержание L-аргинина гидрохлорида приведено в пересчете на L-аргинин (М=174,20 г/моль), исходя из молярной концентрации L-аргинина в препарате 50 мМ. Номинальное содержание L-аргинина гидрохлорида (М=210,66 г/моль) для дозировки 175 мг/мл составляет 9,93 мг.
6 Содержание натрия ацетата тригидрата и уксусной кислоты ледяной приведено исходя из общей концентрации ацетат-иона в препарате 12,5 мМ.
7 Содержание сахарозы приведено в пересчете на миллиграммы исходя из масса-объемной концентрации сахарозы в препарате 5%.
8 Содержание полисорбата 80 приведено в пересчете на миллиграммы исходя из масс-объемной концентрации полисорбата 80 в препарате 0,2%.
Описание лекарственной формы
Прозрачная или слегка опалесцирующая, бесцветная или желтоватого цвета жидкость.
Фармакологическое действие
Фармакологическое действие
—
противовоспалительное.
Фармакодинамика
Механизм действия
Препарат Дупиксент® является рекомбинантным человеческим моноклональным антителом (IgG4), которое блокирует передачу сигналов ИЛ-4 и ИЛ-13 путем специфического связывания с IL-4Rα-субъединицей, общей для рецепторных комплексов ИЛ-4 и ИЛ-13. Препарат Дупиксент® блокирует передачу сигналов ИЛ-4 через рецепторы I типа (IL-4Rα/γc) и общую передачу сигналов ИЛ-4 и ИЛ-13 через рецепторы II типа (IL-4Rα/IL-13Rα). ИЛ-4 и ИЛ-13 являются ключевыми цитокинами воспаления 2-го типа (в т.ч. продуцируемые и Тh2-лимфоцитами), вовлеченными в патогенез атопических заболеваний.
Воспаление 2-го типа играет важную роль в патогенезе многих атопических заболеваний, включая бронхиальную астму, способствует ограничению воздушного потока и увеличивает риск обострений. ИЛ-4 и ИЛ-13 выступают в качестве основных факторов воспаления 2-го типа, активируя множественные типы клеток (например, тучные клетки, лимфоциты, эозинофилы, нейтрофилы, макрофаги) и индуцируя множественные медиаторы (например, IgЕ, гистамин, эйкозаноиды, лейкотриены, хемокины и цитокины, включая эотаксин/CCL11, TARC/CCL17 и ИЛ-5), участвующие в воспалении 2-го типа. Блокирование пути передачи сигналов ИЛ-4/ИЛ-13 дупилумабом у пациентов снижает концентрации многих из этих маркеров воспаления 2-го типа, включая IgЕ, периостин и множественные провоспалительные цитокины и хемокины (например, эотаксин, TARC), а также снижает уровень фракции оксида азота в выдыхаемом воздухе (FeNO) — маркер воспаления в легких. Было показано, что блокирование пути передачи сигналов ИЛ-4/ИЛ-13 дупилумабом в гуманизированных моделях животных предотвращает последующие действия этих цитокинов и хемокинов, в т.ч. гиперплазию бокаловидных клеток, гиперреактивность гладкомышечных клеток дыхательных путей, эозинофильное воспаление в легких, другие воспалительные процессы в легких, а также предотвращает нарушение функции легких; при этом снижение выраженности эозинофильного воспаления в легких происходит независимо от нормального или повышенного уровня эозинофилов в крови.
Дупилумаб производится с помощью технологии рекомбинантной ДНК в суспензионной культуре клеток яичника китайского хомячка.
Дупилумаб имеет молекулярную массу приблизительно 147 кДа.
Фармакодинамика
Атопический дерматит
В клинических исследованиях лечение препаратом Дупиксент® приводило к снижению в сыворотке крови концентраций биомаркеров, связанных с цитокинами воспаления 2-го типа, таких как тимус-ассоциированный регуляторный хемокин (TARC/CCL17), общий сывороточный и аллергенспецифический IgЕ. Также наблюдалось снижение активности лактатдегидрогеназы (ЛДГ), биомаркера, связанного со степенью тяжести атопического дерматита и его активностью.
Препарат Дупиксент® уже в начале 2-й нед лечения вызывал супрессию хемокина TARC по сравнению с плацебо с тенденцией продолжения его снижения до максимальной и устойчивой супрессии к 12-й нед лечения.
У пациентов, получавших препарат Дупиксент® в дозе 300 мг 1 раз в 2 нед и в дозе 300 мг 1 раз в неделю, общий сывороточный IgЕ к 52-й нед терапии снизился на −74,8 и −73,9% (медиана изменения по сравнению с исходным уровнем), соответственно, по сравнению с −0% в группе плацебо. Аналогичные тенденции наблюдались в отношении антигенспецифических IgЕ, в т.ч. энтеротоксина А, специфического для золотистого стафилококка (S. aureus), аллергенов трав и деревьев.
Бронхиальная астма
В соответствии с ингибированием передачи сигналов ИЛ-4 и ИЛ-13 лечение дупилумабом заметно уменьшало уровень FeNO и концентрации эотаксина-3, общего IgЕ, аллергенспецифического IgЕ, TARC и периостина у пациентов с бронхиальной астмой по сравнению с плацебо. Эти снижения уровней биомаркеров воспаления были сопоставимы для режимов дозирования 200 мг 1 раз в 2 нед и 300 мг 1 раз в 2 нед и были близки к максимальному подавлению через 2 нед лечения, за исключением IgЕ, уровень которого уменьшался медленнее. Описанные эффекты были устойчивыми во время лечения.
Хронический полипозный риносинусит
У участников исследований с хроническим полипозным риносинуситом (ХПРС) на фоне лечения дупилумабом также наблюдалось снижение в моче уровня лейкотриена 4 (LTE4), маркера, связанного с активацией тучных клеток, базофилов и эозинофилов.
Клиническая эффективность
Атопический дерматит
Эффективность и безопасность препарата Дупиксент® в монотерапии или в сочетании с топическими ГКС оценивали в трех основных рандомизированных двойных слепых плацебо-контролируемых исследованиях (SOLO 1, SOLO 2 и CHRONOS) с участием 2119 пациентов в возрасте 18 лет и старше со среднетяжелым и тяжелым течением атопического дерматита.
16-недельные исследования монотерапии (SOLO 1 и SOLO 2)
Показателя общей оценки исследователя (IGA) 0 или 1 («чистая» или «почти чистая кожа») к 16-й нед лечения в клиническом исследовании SOLO 1 достигли 37,9% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 нед, и 37,2% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в неделю, против 10,3% пациентов в группе плацебо, а в исследовании SOLO 2 — 36,1 и 36,4% против 8,5% пациентов соответственно.
Улучшение не менее чем на 75% от исходного значения по индексу тяжести и площади экземы (EASI-75) к 16-й нед лечения в исследовании SOLO 1 достигли 51,3% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 нед, и 52,5% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в неделю, против 14,7% пациентов в группе плацебо, а в исследовании SOLO 2 — 44,2 и 48,1% против 11,9% соответственно.
Не менее чем 4-балльного уменьшения зуда по пиковым значениям числовой шкалы оценки выраженности зуда (NRS) к 16-й нед лечения в исследовании SOLO 1 достигли 40,8% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 нед, и 40,3% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в неделю, против 12,3% пациентов в группе плацебо, а в исследовании SOLO 2 — 36,0 и 39,0% пациентов против 9,5% соответственно. Значительно больший процент пациентов, получавших Дупиксент®, достигал быстрого улучшения по шкале NRS по сравнению с пациентами в группе плацебо (определяемого как ≥4-балльное улучшение уже на 2-й нед), причем процент пациентов, у которых наблюдалось уменьшение тяжести зуда по шкале NRS, продолжал увеличиваться в течение всего периода лечения.
Эффекты лечения в подгруппах (с распределением по массе тела, возрасту, полу, расе и сопутствующей терапии, в т.ч. с применением иммунодепрессантов) в исследованиях SOLO 1 и SOLO 2 в целом согласуются с результатами, полученными в общей исследуемой популяции.
52-недельное клиническое исследование с одновременным применением местных ГКС (CHRONOS)
Показателя IGA 0 или 1 к 16-й нед лечения достигли 38,7% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 нед + топические ГКС, и 39,2% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в неделю + топические ГКС, против 12,4% пациентов в группе плацебо, а к 52-й нед — 36,0 и 40,0% против 12,5% пациентов соответственно.
EASI-75 к 16-й нед лечения достигли 68,9% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 нед + топические ГКС, и 63,9% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в неделю + топические ГКС, против 23,2% пациентов в группе плацебо + топические ГКС, а к 52-й нед — 65,2 и 64,1% против 21,6% пациентов соответственно.
Не менее чем 4-балльного улучшения по шкале NRS к 16-й нед лечения достигли 58,8% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 нед + топические ГКС, и 50,8% пациентов, получавших препарат Дупиксент® в дозе 300 мг 1 раз в неделю + топические ГКС, против 19,7% пациентов в группе плацебо + топические ГКС, а к 52-й нед — 51,2 и 39,0% против 12,9% пациентов соответственно. Более значительный процент пациентов, получавших препарат Дупиксент® + топические ГКС, достигал быстрого улучшения по шкале NRS по сравнению с пациентами в группе плацебо + топические ГКС (определяемого как >4-балльное улучшение уже на 2-й нед; р <0,05), причем доля пациентов, у которых наблюдалось уменьшение тяжести зуда по шкале NRS, продолжала увеличиваться в течение всего периода лечения.
Эффекты лечения в подгруппах (с распределением по массе тела, возрасту, полу, расе и сопутствующей терапии, в т.ч. с применением иммунодепрессантов) в исследовании CHRONOS в целом согласуются с результатами, полученными в общей исследуемой популяции.
Клиническая эффективность у пациентов, которым не рекомендовалось лечение циклоспорином
У пациентов, которым не рекомендовалось лечение циклоспорином или у которых оно было неэффективно, монотерапия препаратом Дупиксент® в обеих группах лечения приводила к значительному улучшению признаков и симптомов атопического дерматита по сравнению с плацебо. Больший процент пациентов, получавших Дупиксент®, по сравнению с группой плацебо достигал показателя IGA 0 или 1 и снижения по сравнению с исходным значением на ≥2 балла к 16-й нед (29,5 против 6,8%), EASI-75 к 16-й нед (38 против 11,4%), а также снижения не менее чем на 4 балла индекса тяжести зуда от исходного значения к 16-й нед (34,9 по сравнению с 8%) (р <0,001 для всех 3 конечных точек). Аналогичные результаты наблюдались у пациентов, получавших Дупиксент® одновременно с топическими ГКС. Эффективность комбинации препарата Дупиксент® + топические ГКС сохранялась до 52-й нед терапии.
Подростки (от 12 до 17 лет)
Эффективность и безопасность применения препарата Дупиксент® в монотерапии у пациентов оценивалась в мультицентровом рандомизированном двойном слепом плацебо-контролируемом исследовании (AD-1526) с участием 251 пациента от 12 до 17 лет с атопическим дерматитом среднетяжелого и тяжелого течения. Соответствующие пациенты, включенные в данное исследование, продемонстрировали неадекватный ответ на предварительную терапию топическими препаратами.
Пациенты получали: начальную дозу 400 мг препарата Дупиксент® (2 инъекции по 200 мг) с последующим введением 200 мг каждые 2 нед для пациентов с базовой массой тела менее 60 кг, либо начальную дозу препарата Дупиксент® 600 мг (2 инъекции по 300 мг) с последующим введением 300 мг каждые 2 нед для пациентов с базовой массой тела более 60 кг, либо начальную дозу препарата Дупиксент® 600 мг (2 инъекции по 300 мг) с последующим введением 300 мг каждые 4 нед независимо от массы тела, либо плацебо.
Дупиксент® вводили подкожно. При необходимости контролировать недопустимые симптомы пациентам разрешалось получать скоропомощное лечение по решению исследователя. Пациенты, которые получали такое лечение, были оценены как не отвечающие на терапию препаратом Дупиксент®.
В данном исследовании средний возраст пациентов составлял 14,5 лет, средний вес — 59,4 кг, 41,0% — женщины, 62,5% — белокожие, 15,1% — азиаты и 12,0% — темнокожие. В целом 92,0% пациентов имели как минимум одно коморбидное аллергическое состояние; у 65,5% пациентов наблюдался аллергический ринит; у 53,6% — бронхиальная астма и у 68,5% — пищевая аллергия.
Клинический ответ. Показателя IGA 0 или 1 («чистая» или «почти чистая кожа») к 16-й нед лечения в исследовании AD-1526 достигли 24,4% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 нед (≥60 кг) или 200 мг 1 раз в 2 недели (<60 кг), против 2,4% пациентов в группе плацебо.
Улучшение не менее чем на 75% от исходного значения по индексу EASI-75 к 16-й неделе достигли 41,5% пациентов, получавших Дупиксент® против 8,2% пациентов в группе плацебо.
Не менее чем 4-балльного уменьшения зуда по пиковым значениям числовой шкалы NRS к 16-й нед лечения в исследовании достигли 36,6% пациентов, получавших Дупиксент®, против 4,8% пациентов в группе плацебо. Значительно больший процент пациентов, получавших Дупиксент®, достигал быстрого улучшения по шкале оценки тяжести зуда NRS по сравнению с пациентами в группе плацебо (определяемого как ≥4-балльное улучшение уже на 2-й нед), причем процент пациентов, у которых наблюдалось уменьшение тяжести зуда по шкале NRS, продолжал увеличиваться в течение всего периода лечения. Значительно больший процент пациентов, рандомизированных на терапию препаратом Дупиксент® достиг быстрого улучшения по шкале NRS по сравнению с плацебо (улучшение более чем в 4 раза уже на 4-й нед; номинальное значение р <0,001) и доля пациентов, ответивших на терапию по шкале NRS наблюдалась в сочетании с улучшением объективных признаков атопического дерматита.
Долгосрочные исследования эффективности терапии препаратом Дупиксент® у пациентов подросткового возраста с атопическим дерматитом среднетяжелого и тяжелого течения, которые принимали участие в предыдущих клинических исследованиях препарата Дупиксент® были оценены в открытом продолженном исследовании (AD-1434). Данные в отношении эффективности, полученные в данном исследовании, предполагают, что клиническое преимущество, полученное на 16-й нед терапии, является стабильным в течение 52 нед терапии.
Дети (от 6 до 11 лет)
Эффективность и безопасность применения препарата Дупиксент® у пациентов детского возраста в сочетании с топическими ГКС изучалась в многоцентровом рандомизированном двойном слепом плацебо-контролируемом исследовании (AD-1652) с участием 367 пациентов от 6 до 11 лет с атопическим дерматитом, характеризующимся IGA ≥4 (по шкале от 0 до 4), EASI ≥21 (по шкале от 0 до 72), а также минимальной пораженной площадью поверхности тела ≥15%. У подходящих пациентов, включенных в это исследование, ранее наблюдался недостаточный ответ на топические препараты. Пациентов стратифицировали в зависимости от массы тела на исходном уровне (<30 кг, ≥30 кг). Пациенты в группе, получавшей препарат Дупиксент® 1 раз в 2 недели + топические ГКС с исходной массой тела <30 кг получали начальную дозу препарата 200 мг в день и затем — по 100 мг 1 раз в 2 нед со 2-й по 14-ю нед, а пациенты с исходной массой тела ≥30 кг получали первоначальную дозу препарата Дупиксент® 400 мг в день и затем — 200 мг 1 раз в 2 нед со 2-й по 14-ю нед. Пациенты в группе, получавшей препарат Дупиксент® 1 раз в 4 нед + топические ГКС получали первоначальную дозу препарата 600 мг в день и затем — 300 мг 1 раз в 4 нед с 4-й по 12-ю нед, независимо от массы тела. Пациентам было разрешено получать резервную терапию по усмотрению исследователя. Пациенты, получавшие резервную терапию, расценивались как не отвечающие на терапию препаратом Дупиксент®.
В данном исследовании средний возраст составлял 8,5 лет, средний вес — 29,8 кг, 50,1% — женщины, 69,2% — белокожие, 16,9% — темнокожие и 7,6% — азиаты.
В целом 91,7% пациентов имели как минимум одно коморбидное аллергическое состояние; у 64,4% наблюдалась пищевая аллергия, у 62,7% — другие виды аллергии, у 60,2% — аллергический ринит, у 46,7% — бронхиальная астма.
Клинический ответ. Показателя IGA 0 или 1 («чистая» или «почти чистая кожа») к 16-й нед лечения в исследовании AD-1652 достигли 29,5% пациентов с массой тела <30 кг, получавших Дупиксент® в дозе 300 мг 1 раз в 4 нед, против 13,1% в группе плацебо; 39,0% пациентов с массой тела ≥30 кг, получавших Дупиксент® в дозе 200 мг 1 раз в 2 нед, против 9,7% в группе плацебо.
Улучшение не менее чем на 75% от исходного значения по индексу EASI-75 к 16-й нед лечения в исследовании AD-1652 достигли 75,4% пациента с массой тела <30 кг, получавших Дупиксент® в дозе 300 мг 1 раз в 4 нед, против 27,9% в группе плацебо; 74,6% пациентов с массой тела ≥30 кг, получавших Дупиксент® в дозе 200 мг 1 раз в 2 нед, против 25,8% в группе плацебо.
Не менее чем 4-балльного уменьшения зуда по пиковым значениям числовой шкалы NRS к 16-й нед лечения в исследовании AD-1652 достигли 54,1% пациента с массой тела <30 кг, получавших Дупиксент® в дозе 300 мг 1 раз в 4 нед, против 11,7% в группе плацебо; 61,4% пациента с массой тела ≥30 кг, получавших Дупиксент® в дозе 200 мг 1 раз в 2 нед, против 12,9% в группе плацебо.
Значительно больший процент пациентов, получавших Дупиксент®, достигал быстрого улучшения по шкале NRS по сравнению с пациентами в группе плацебо (определяемого как ≥4-балльное улучшение на 2-й нед), причем процент пациентов, у которых наблюдалось уменьшение тяжести зуда по шкале NRS, продолжал увеличиваться в течение всего периода лечения. Значительно больший процент пациентов, рандомизированных на терапию препаратом Дупиксент® в сочетании с топическими ГКС, достиг быстрого улучшения по шкале NRS по сравнению с плацебо (улучшение ≥4 балла на 4-й нед).
Долгосрочная эффективность терапии препаратом Дупиксент® в сочетании с топическими ГКС, у пациентов детского возраста с атопическим дерматитом, которые принимали участие в предшествующих клинических исследованиях препарата Дупиксент® в сочетании с топическими ГКС, изучалась в продолженном открытом исследовании (AD-1434). Данные по эффективности, полученные в этом исследовании позволяют предположить, что клиническое улучшение, наблюдавшееся на 16-й нед, сохранялось в течение 52 нед терапии включительно.
Бронхиальная астма
Было проведено три рандомизированных двойных слепых плацебо-контролируемых многоцентровых исследования в параллельных группах (DRI12544, QUEST и VENTURE) продолжительностью от 24 до 52 нед с участием 2888 пациентов от 12 лет и старше. Во все три исследования пациенты были включены независимо от минимального исходного уровня эозинофилов или другого биомаркера воспаления 2-го типа (например, уровня FeNO или IgЕ).
Обострения бронхиальной астмы
В исследованиях DRI12544, QUEST и VENTURE оценивали частоту тяжелых обострений астмы независимо от минимального количества эозинофилов или любых других биомаркеров воспаления 2-го типа (например, FeNO или IgЕ) в начале исследования. В общей популяции, независимо от содержания эозинофилов и других биомаркеров воспаления 2-го типа, у пациентов, получавших 200 или 300 мг препарата Дупиксент® один раз в 2 нед, произошло значительное снижение частоты тяжелых обострений астмы по сравнению с группой плацебо. В исследованиях DRI12544 и QUEST частота тяжелых обострений при применении препарата Дупиксент® в дозе 200 мг 1 раз в 2 нед снижалась на 70 и 48%, а при применении в дозе 300 мг 1 раз в 2 нед — на 70 и 46% соответственно и на 59% в исследовании VENTURE.
В объединенном анализе исследований DRI12544 и QUEST частота тяжелых обострений, приводящих к госпитализации и/или посещениям отделений неотложной помощи, снизилась на 25,5 и 46,9% при применении препарата Дупиксент® в дозах 200 или 300 мг 1 раз в 2 нед соответственно.
Кумулятивное среднее число тяжелых обострений было более низкое у пациентов, получавших препарат Дупиксент®, по сравнению с плацебо в исследованиях DRI12544, QUEST и VENTURE (в общей популяции и популяции с исходным числом эозинофилов ≥150 клеток/мкл или FeNO ≥25 ppb) в течение 24 нед или 52 нед лечения в обеих группах режимов дозирования препарата.
В исследовании QUEST у пациентов, получавших ингаляционные ГКС (ИКС) в средней дозе, наблюдалось сходное снижение частоты тяжелых обострений астмы по сравнению с пациентами, получавшими ИКС в высокой дозе.
Функция легких
Клинически значимое увеличение предбронходилатационного значения ОФВ за 1-ю секунду (ОФВ1) наблюдалось на 12-й нед в общей популяции независимо от уровня эозинофилов или других биомаркеров воспаления 2-го типа (например, FeNO или IgЕ).
В исследованиях DRI12544, QUEST и VENTURE по сравнению с плацебо большее увеличение ОФВ1 наблюдалось также у пациентов с FeNO ≥25·10−9. Улучшение ОФВ1 было одинаковым, независимо от того, получали ли пациенты ИКС в средней дозе, ИКС в высокой дозе или пероральные ГКС (ОКС).
Значительные улучшения ОФВ1 наблюдались уже в течение второй недели (DRI12544, QUEST и VENTURE) после первой инъекции препарата Дупиксент® в дозе как 200, так и 300 мг и сохранялись в течение 24 нед (DRI12544 и VENTURE) и 52 нед (QUEST).
Скорректированная средняя разность абсолютных значений ОФВ1 была 0,20 и 0,14 л в группах, получавших Дупиксент® 200 мг 1 раз в 2 нед, по сравнению с плацебо и 0,16 и 0,13 л в группах, получавших 300 мг 1 раз в 2 нед, по сравнению с плацебо соответственно в исследованиях DRI12544 и QUEST. Соответствующее процентное изменение ОФВ1 составляло от 9,2 до 11,9% для дозы 200 мг 1 раз в 2 нед и от 9,4 до 11,7% для дозы 300 мг 1 раз в 2 нед. Скорректированная средняя разность абсолютных значений предбронходилатационного ОФВ1 от исходного уровня к 24-й нед (достаточное время для достижения максимального снижения дозы ОКС) в исследовании VENTURE составила 0,22 л в группе применения препарата Дупиксент® по сравнению с плацебо, что соответствовало улучшению на 15,1% по сравнению с исходным уровнем.
Кроме того, у пациентов, получавших препарат Дупиксент®, значительно улучшился постбронходилатационный показатель ОФВ1 по сравнению с исходным уровнем на 12-й и 52-й нед по сравнению с плацебо, что указывает на то, что препарат Дупиксент® улучшает фиксированную обструкцию дыхательных путей. В группе применения препарата Дупиксент® в течение года наблюдения не было зарегистрировано снижения функции легких с учетом значения постбронходилатационного значения ОФВ1.
Снижение дозы ОКС
В исследовании VENTURE оценивалось влияние препарата Дупиксент® на снижение применения поддерживающих ОКС. Исходная средняя доза ОКС составляла 11,75 мг в группе плацебо и 10,75 мг в группе, получавшей препарат Дупиксент®. По сравнению с плацебо у пациентов, получавших Дупиксент®, отмечалось большее снижение ежедневной дозы ОКС при сохранении контроля над астмой.
Среднее общее снижение ежедневной дозы ОКС при сохранении контроля над астмой составляло 70,1% по сравнению с исходным уровнем у пациентов, получавших Дупиксент®, и 41,9% в группе плацебо.
Исходы, сообщаемые пациентами
Кроме того, во всех 3 исследованиях Дупиксент® обеспечил клинически значимое улучшение показателей контроля бронхиальной астмы в общей популяции по сравнению с группой плацебо, о чем свидетельствуют показатели ACQ-5 и соответствующее улучшение качества жизни, измеренное по шкале AQLQ(S). Улучшение показателей ACQ-5 и AQLQ(S) было зарегистрировано уже через 2 нед и сохранялось на протяжении 24 нед в исследовании DRI12544 и 52 нед в исследовании QUEST. В общей популяции исследования QUEST доля пациентов, ответивших на лечение, что выражалось в достижении минимального клинически значимого различия показателей ACQ-5 и AQLQ(S), была существенно выше к 52-й нед в группе, получавшей обе дозы препарата Дупиксент®.
Долгосрочное продленное исследование (TRAVERSE)
Долгосрочную эффективность препарата Дупиксент® у 2282 взрослых и подростков со среднетяжелой и тяжелой бронхиальной астмой, и у взрослых пациентов с гормонозависимой астмой, которые принимали участие в предыдущих клинических испытаниях препарата Дупиксент®, оценивали в рамках открытого продленного исследования (TRAVERSE). В данном исследовании препарата Дупиксент® улучшение клинических показателей, в т.ч. снижение количества обострений и улучшение функции легких, сохранялось в течение 96 нед. У пациентов с гормонозависимой астмой, несмотря на продолжающееся снижение или отмену ОКС, отмечалось снижение количества обострений и устойчивое улучшение функции легких в течение 96 нед. Частота тяжелых обострений в течение 96 нед составила 0,3 и 0,27; а улучшение ОФВ1 от исходного значения — 0,33 л (21,1%) и 0,42 л (27,3%) у пациентов с уровнем эозинофилов в крови ≥150 и ≥300 клеток/мкл соответственно. Аналогичное сохранение эффекта наблюдалось и по параметрам ACQ-5 и AQLQ(S). Аналогичные результаты отмечались и в подгруппе пациентов, получавших высокие дозы ИКС.
Хронический полипозный риносинусит
Программа клинических исследований применения препарата при ХПРС включала два рандомизированных двойных слепых многоцентровых плацебо-контролируемых исследования в параллельных группах (SINUS-24 и SINUS-52) с участием 724 пациентов в возрасте 18 лет и старше, получающих базисную терапию интраназальными кортикостероидами (ИНКС). Эти исследования включали пациентов с тяжелым течением ХПРС, несмотря на ранее проведенное хирургическое вмешательство на придаточных пазухах носа или лечение системными кортикостероидами на протяжении последних 2 лет. В ходе исследования было разрешено лечение системными кортикостероидами или хирургическое вмешательство по решению исследователя. В исследовании SINUS-24 в общей сложности 276 пациентов были рандомизированы либо в группу Дупиксент® 300 мг (N=143), либо в группу плацебо (N=133), инъекции осуществляли 1 раз в 2 нед на протяжении 24 нед. В исследовании SINUS-52 в общей сложности 448 пациентов были рандомизированы либо в группу препарата Дупиксент® 300 мг 1 раз в 2 нед на протяжении 52 нед (N=150), либо в группу препарата Дупиксент® 300 мг 1 раз в 2 нед на протяжении 24 нед, а затем 300 мг 1 раз в 4 нед до 52-й нед (N=145), либо в группу плацебо (N=153). При компьютерной томографии у всех пациентов было выявлено снижение пневматизации придаточных пазух носа, оценка проводилась по шкале Ланда-Маккея (ШЛМ), при этом у 73–90% пациентов отмечалось снижение пневматизации всех придаточных пазух носа. Пациенты были стратифицированы в зависимости от наличия в анамнезе хирургических вмешательств и бронхиальной астмы/аспирининдуцированного респираторного заболевания (АИРЗ, аспириновой астмы). Хирургическое вмешательство на придаточных пазухах носа ранее выполнялось у 63% пациентов, в среднем 2,0 хирургических вмешательства, 74% участников на протяжении последних 2 лет получали системные кортикостероиды, среднее количество курсов за последние 2 года составляло 1,6. У 59% пациентов имелась сопутствующая бронхиальная астма, а у 28% — АИРЗ.
Комбинированными первичными конечными точками было изменение балла выраженности полипоза при эндоскопической риноскопии (по шкале NPS от 0 до 8 баллов) относительно исходного уровня к 24-й нед (централизованная маскированная оценка результатов), а также изменение балла заложенности носа/назальной обструкции относительно исходного уровня к 24-й нед (усредненный балл за 28 дней, шкала NC от 0 до 3 баллов), определяемое самим пациентом на основании ежедневных записей в дневнике. В обоих исследованиях вторичные конечные точки на 24-й нед включали изменения по сравнению с исходным уровнем таких показателей, как балл по ШЛМ, оцененный при КТ придаточных пазух носа (КТ ППН), количественная оценка выраженности симптомов (TSS), тест на идентификацию запахов Пенсильванского университета (UPSIT), ежедневная оценка снижения обоняния и опросник для оценки исхода болезней носа и околоносовых пазух из 22 вопросов (SNOT-22). Была выполнена обобщающая результаты двух исследований оценка уменьшения доли пациентов, которым не требовалось неотложное применение курсов системных кортикостероидов и/или хирургических вмешательств на придаточных пазухах носа, а также улучшения показателя ОФВ1 в подгруппе пациентов с бронхиальной астмой. Статистически и клинически значимая эффективность наблюдалась в отношении улучшения выраженности полипоза носа по шкале NPS на 24-й нед в SINUS-24 (скорректированная средняя разность −2,06 по сравнению с группой плацебо) и в SINUS-52 на 24- и 52-й нед с дальнейшим прогрессивным улучшением (скорректированная средняя разность −1,8 и −2,4 по сравнению с группой плацебо при терапии препаратом Дупиксент® 300 мг 1 раз в 2 нед соответственно на 24- и 52-й нед). У пациентов, получавших препарат Дупиксент®, отмечалось значимое снижение заложенности носа/назальной обструкции по сравнению с плацебо на 24-й нед в SINUS-24 (скорректированная средняя разность −0,89 по сравнению с группой плацебо) и на 24- и 52-й нед в SINUS-52 (скорректированная средняя разность −0,87 и −0,98 по сравнению с группой плацебо при терапии препаратом Дупиксент® 300 мг 1 раз в 2 нед соответственно на 24- и 52-й нед). В обоих исследованиях значимое улучшение в отношении заложенности носа/назальной обструкции относительно исходного уровня по шкале NC и ежедневной оценки снижения обоняния отмечалось уже при первой оценке на 4-й нед. Значимое снижение балла по ШЛМ, оцененного при КТ ППН, наблюдалось на 24-й нед в SINUS-24 (скорректированная средняя разность −7,44 по сравнению с группой плацебо) и в SINUS-52 на 24-й нед с дальнейшим улучшением к 52-й нед (скорректированная средняя разность −5,13 и −6,94 по сравнению с группой плацебо при терапии препаратом Дупиксент® 300 мг 1 раз в 2 нед соответственно на 24- и 52-й нед). Обобщающая результаты двух исследований оценка продемонстрировала снижение доли пациентов, которым не требовалось неотложное применение курсов системных кортикостероидов, на 74%, хирургических вмешательств на придаточных пазухах носа — на 83% при применении препарата Дупиксент® по сравнению с плацебо. В подгруппе пациентов с сопутствующей бронхиальной астмой отмечалось значимое улучшение показателей предбронходилатационного ОФВ1 на 24-й нед терапии препаратом Дупиксент® вне зависимости от исходного уровня эозинофилов: скорректированная средняя разность от исходного уровня ОФВ1 на 24-й нед для дозы препарата Дупиксент® 300 мг 1 раз в 2 нед составила 0,14 л против −0,07 л в группе плацебо, разность — 0,21 л. Эффективность в отношении первичных конечных точек — изменение балла выраженности полипоза по шкале NPS и изменение балла заложенности носа/назальной обструкции по шкале NC относительно исходного уровня к 24-й нед и ключевой вторичной конечной точки (балл по ШЛМ, оцененный при КТ ППН) в подгруппах пациентов с сопутствующей бронхиальной астмой или АИРЗ была схожей с общей популяцией пациентов с ХПРС.
Фармакокинетика
Фармакокинетика дупилумаба аналогична у пациентов с атопическим дерматитом, бронхиальной астмой и ХПРС.
Абсорбция
После однократного п/к введения 75–600 мг дупилумаба медиана Tmax в сыворотке крови составляла 3–7 дней. Абсолютная биодоступность дупилумаба после введения п/к дозы сходна между пациентами с атопическим дерматитом, бронхиальной астмой и ХПРС и составляет 61–64% (установлена при популяционном фармакокинетическом анализе).
Введение однократной нагрузочной дозы в первый день приводит к быстрому достижению клинически эффективных концентраций в течение 2 нед.
При схеме лечения 200 или 300 мг 1 раз в 2 нед, начиная с нагрузочной дозы 400 или 600 мг, Css дупилумаба обычно достигается в среднем к 16-й нед лечения. В состоянии достижения Css средняя остаточная концентрация перед введением следующей дозы составляла 39 мг/л при применении 200 мг 1 раз в 2 нед и 70–80 мг/л при применении 300 мг 1 раз в 2 нед.
При еженедельном п/к введении 300 мг препарата Дупиксент®, начиная с нагрузочной дозы 600 мг, Css обычно достигается в среднем после 13 нед лечения. В состоянии достижения Css средняя остаточная концентрация перед введением следующей дозы составляла 189 мг/л.
Линейность дозы
Из-за нелинейности клиренса системная экспозиция дупилумаба, определяемая по AUC, увеличивается быстрее, непропорционально увеличению дозы после однократного п/к введения препарата в дозах от 75 до 600 мг.
Распределение
Vd дупилумаба составляет приблизительно 4,6 л, что указывает на его распределение главным образом в сосудистой системе.
Метаболизм
Поскольку дупилумаб является белком, специальных исследований его метаболизма не проводилось. Предполагается, что дупилумаб расщепляется до низкомолекулярных пептидов и отдельных аминокислот.
Выведение
Выведение дупилумаба осуществляется параллельно линейными и нелинейными путями. При более высоких концентрациях выведение дупилумаба осуществляется главным образом через ненасыщаемый протеолитический путь, в то время как при более низких концентрациях выведение препарата преимущественно происходит через нелинейное насыщаемое связывание с мишенью IL-4Rα.
После введения последней дозы в состоянии Css медиана времени до неопределяемых концентраций дупилумаба составляет 9 нед при введении 200 мг 1 раз в 2 нед, 10–12 нед при введении 300 мг 1 раз в 2 нед и 13 нед при введении 300 мг 1 раз в неделю.
Особые группы пациентов
Пол
Пол пациента не влиял на фармакокинетические показатели препарата Дупиксент®.
Возраст
Возраст пациента не влиял на фармакокинетические показатели препарата Дупиксент®.
Пациенты пожилого возраста
По данным популяционного анализа фармакокинетических показателей, возраст пациентов не влиял на эффективность и безопасность препарата Дупиксент®.
Пациенты детского возраста
Безопасность и эффективность препарата Дупиксент® были установлены у пациентов в возрасте 6 лет и старше со среднетяжелым и тяжелым атопическим дерматитом. Безопасность и эффективность у детей, подростков и взрослых были сопоставимы. Безопасность и эффективность у детей в возрасте младше 6 лет с атопическим дерматитом не изучена.
Бронхиальная астма. Долгосрочную безопасность и эффективность препарата Дупиксент® оценивали у 89 пациентов подросткового возраста со среднетяжелой и тяжелой бронхиальной астмой, которые были включены в открытое продленное исследование (TRAVERSE). В исследовании наблюдение продолжалось в течение 96 недель, что составило 99 пациенто-лет кумулятивного воздействия препарата Дупиксент®. Профиль безопасности препарата Дупиксент® в исследовании TRAVERSE соответствовал профилю безопасности, зарегистрированному в базовых исследованиях по лечению астмы в течение 52 нед терапии. Дополнительных нежелательных реакций выявлено не было. В этом исследовании клиническая польза препарата Дупиксент®, включая уменьшение количества обострений и улучшение функции легких, наблюдаемое в базовых исследованиях лечения пациентов с астмой, сохранялась до 96-й нед. Безопасность и эффективность препарата у детей (младше 12 лет) с бронхиальной астмой не изучалась. Профиль нежелательных явлений у подростков сопоставим с таковым у взрослых (см. «Побочные действия»).
ХПРС. Обычно ХПРС не встречается у детей. Фармакокинетика дупилумаба не изучалась у детей (пациентов младше 18 лет) с ХПРС.
Расовая принадлежность
Согласно результатам популяционного фармакокинетического анализа, расовая принадлежность не влияла на фармакокинетические показатели препарата Дупиксент®.
Печеночная недостаточность
Дупилумаб представляет собой моноклональное антитело, поэтому не ожидается, что он подвергается значительной печеночной элиминации. Клинические исследования для оценки влияния печеночной недостаточности на фармакокинетику дупилумаба не проводились.
Почечная недостаточность
Дупилумаб представляет собой моноклональное антитело, поэтому не ожидается, что он подвергается значительной почечной элиминации. Клинические исследования для оценки влияния почечной недостаточности на фармакокинетику дупилумаба не проводились. Результаты популяционных фармакокинетических анализов показали, что нарушение функции почек легкой и средней степени тяжести существенным образом не влияет на системную экспозицию дупилумаба. Нет данных о применении дупилумаба у пациентов с тяжелой почечной недостаточностью.
Масса тела
Не требуется коррекции режима дозирования в зависимости от массы тела для пациентов с бронхиальной астмой старше 12 лет и взрослых пациентов с атопическим дерматитом. Для пациентов 6–17 лет с атопическим дерматитом рекомендованная доза 300 мг каждые 4 нед (с массой тела 15 — <30 кг), 200 мг каждые 2 нед (с массой тела 30 — <60 кг) или 300 мг каждые 2 нед (с массой тела >60 кг).
Показания
- атопический дерматит среднетяжелого и тяжелого течения у пациентов от 6 лет и старше при недостаточном ответе на терапию топическими лекарственными препаратами или в случае, когда такие препараты не рекомендованы к применению. Препарат Дупиксент® может применяться в монотерапии или одновременно с топическими лекарственными препаратами;
- в качестве дополнительной поддерживающей терапии бронхиальной астмы среднетяжелого и тяжелого течения у пациентов в возрасте 12 лет и старше с эозинофильным фенотипом или у пациентов с гормональнозависимой бронхиальной астмой, получающих ОКС;
- в качестве дополнительной поддерживающей терапии взрослых пациентов с плохо контролируемым тяжелым хроническим полипозным риносинуситом.
Противопоказания
- повышенная чувствительность к дупилумабу или любому из вспомогательных веществ препарата (см. «Особые указания);
- детский возраст до 6 лет у пациентов с атопическим дерматитом среднетяжелого и тяжелого течения в связи с неустановленными эффективностью и безопасностью;
- детский возраст до 12 лет у пациентов с бронхиальной астмой среднетяжелого и тяжелого течения в связи с неустановленными эффективностью и безопасностью.
С осторожностью: при беременности (только если ожидаемая польза для матери превышает потенциальный риск для плода).
Применение при беременности и кормлении грудью
Беременность
Имеются лишь ограниченные данные по применению дупилумаба у беременных женщин. В исследованиях, проведенных на животных, прямых и косвенных неблагоприятных эффектов в отношении репродуктивной токсичности не обнаружено. Препарат Дупиксент® можно применять во время беременности только в том случае, если ожидаемая польза для матери превышает потенциальный риск для плода.
Период грудного вскармливания
Неизвестно, экскретируется ли дупилумаб в грудное молоко человека. Следует с учетом пользы грудного вскармливания для ребенка и преимущества дальнейшего применения препарата для матери принять решение о прекращении кормления грудью или отмене препарата Дупиксент® в течение периода грудного вскармливания.
Способ применения и дозы
Реклама: ООО «РЛС-Патент», ИНН 5044031277, erid=4CQwVszH9pUkpHxmQQo
Общие рекомендации
Препарат Дупиксент® вводится п/к.
Атопический дерматит
Рекомендуемая доза препарата Дупиксент® у взрослых пациентов:
— начальная доза 600 мг (2 инъекции по 300 мг), далее — по 300 мг каждые 2 нед. В зависимости от индивидуального терапевтического ответа доза может быть увеличена до 300 мг еженедельно.
Рекомендуемая доза препарата Дупиксент® у пациентов 6–17 лет:
— для пациентов с массой тела от 15 до <30 кг: начальная доза — 600 мг (2 инъекции по 300 мг), далее по 300 мг каждые 4 нед;
— для пациентов с массой тела от 30 до <60 кг: начальная доза — 400 мг (2 инъекции по 200 мг), далее по 200 мг каждые 2 нед;
— для пациентов с массой тела 60 кг и более: начальная доза — 600 мг (2 инъекции по 300 мг), далее по 300 мг каждые 2 нед.
Бронхиальная астма
Рекомендуемая доза препарата Дупиксент® у взрослых пациентов и детей (12 лет и старше):
— начальная доза — 400 мг (2 инъекции по 200 мг), далее — по 200 мг каждые 2 нед. В зависимости от индивидуального терапевтического ответа доза может быть увеличена до 300 мг каждые 2 нед;
— начальная доза — 600 мг (2 инъекции по 300 мг), далее — по 300 мг каждые 2 нед. для пациентов с глюкокортикостероидозависимой бронхиальной астмой или с сопутствующим среднетяжелым или тяжелым атопическим дерматитом, при котором показано применение препарата Дупиксент®.
ХПРС
Начальная рекомендуемая доза для взрослых пациентов — 300 мг, далее — 300 мг каждые 2 нед.
В случае пропуска дозы пациент должен получить инъекцию как можно скорее и затем продолжить лечение в соответствии с назначенным ему режимом введения препарата.
Особые группы пациентов
Дети. Безопасность и эффективность препарата Дупиксент® у детей и подростков до 6 лет с атопическим дерматитом, бронхиальной астмой и у пациентов с хроническим полипозным риносинуситом младше 18 лет не установлена.
Пациенты пожилого возраста. У пациентов пожилого возраста коррекции дозы не требуется (см. «Фармакокинетика»).
Печеночная недостаточность. Отсутствуют данные по применению препарата у пациентов с печеночной недостаточностью (см. «Фармакокинетика»).
Почечная недостаточность. У пациентов с легкой или средней степенью тяжести почечной недостаточности коррекции дозы не требуется. Отсутствуют данные по применению препарата у пациентов с тяжелой почечной недостаточностью (см. «Фармакокинетика»).
Масса тела. Не требуется коррекции режима дозирования в зависимости от массы тела для пациентов с бронхиальной астмой старше 12 лет и взрослых пациентов с атопическим дерматитом и с хроническим полипозным риносинуситом (см. «Фармакокинетика», «Способ применения и дозы»). Для пациентов 6–17 лет с атопическим дерматитом рекомендованная доза 300 мг каждые 4 нед (с массой тела 15 — <30 кг), 200 мг каждые две недели (с массой тела 30 — <60 кг) и 300 мг каждые 2 нед (с массой тела более 60 кг).
Способ применения
Перед введением препарата следует осмотреть его на предмет наличия в растворе твердых частиц или появления нехарактерной окраски раствора. Если в препарате содержатся твердые частицы или у раствора появилась нехарактерная окраска, вводить препарат нельзя.
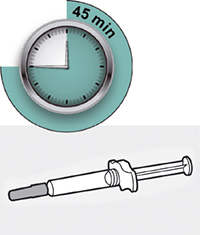
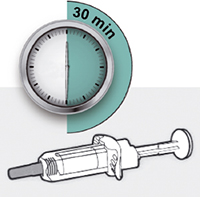
Раствор в предварительно заполненном шприце с системой защиты или предварительно заполненном шприце перед проведением инъекции препарата Дупиксент® должен нагреться до комнатной температуры. Для этого рекомендуется выдержать его при комнатной температуре в течение 45 мин (для дозировки 300 мг) или 30 мин (для дозировки 200 мг).
В случае необходимости предварительно заполненный шприц можно хранить при комнатной температуре (до 25 °C) в течение максимум 14 дней. Препарат нельзя хранить при температуре выше 25 °С. После извлечения из холодильника Дупиксент® должен быть использован в течение 14 дней или утилизирован.
Шприцы следует защищать от нагревания и воздействия прямого солнечного света.
Если начальная доза составляет 600 мг, следует сделать две инъекции по 300 мг в разные места для инъекций.
Если начальная доза составляет 400 мг, следует сделать две инъекции по 200 мг в разные места для инъекций.
Лечение препаратом Дупиксент® следует проводить под медицинским наблюдением. Инъекцию препарата может делать себе либо сам пациент, либо лицо, ухаживающее за ним.
Необходимо до начала применения препарата Дупиксент® обучить пациентов и/или ухаживающих за ними лиц подготовке и проведению инъекции препарата Дупиксент® согласно указаниям в «Инструкции по подготовке и проведению инъекции препарата Дупиксент® 300 мг в предварительно заполненном одноразовом шприце с системой защиты», «Инструкции по подготовке и проведению инъекции препарата Дупиксент® 300 мг в предварительно заполненном одноразовом шприце» и «Инструкции по подготовке и проведению инъекции препарата Дупиксент® 200 мг в предварительно заполненном одноразовом шприце с системой защиты».
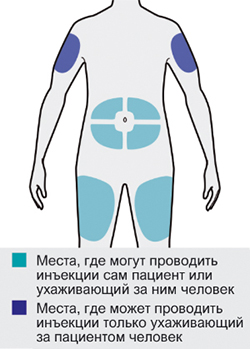
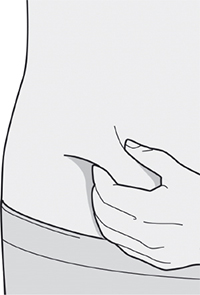
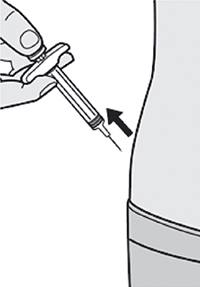
Препарат Дупиксент® может вводиться самим пациентом п/к с помощью предварительно заполненного одноразового шприца в область бедра или живота, за исключением области диаметром 5 см непосредственно вокруг пупка. Если инъекцию проводит другой человек, препарат также можно вводить в верхнюю часть плеча.
Рекомендуется менять места инъекций при каждом введении препарата.
Инъекцию препарата Дупиксент® не следует проводить в участки с болезненной и поврежденной кожей, в места с кровоподтеками или рубцами.
Все остатки неиспользованного препарата и расходные материалы должны утилизироваться в соответствии с требованиями местного законодательства.
Инструкция по подготовке и проведению инъекции препарата Дупиксент® 300 мг в предварительно заполненном одноразовом шприце с системой защиты
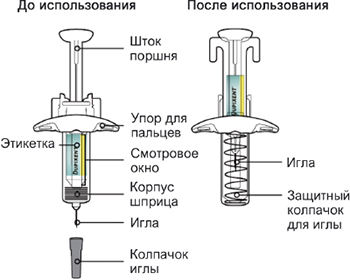
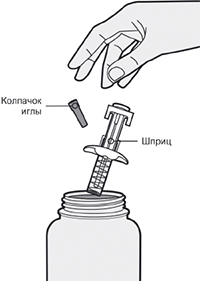
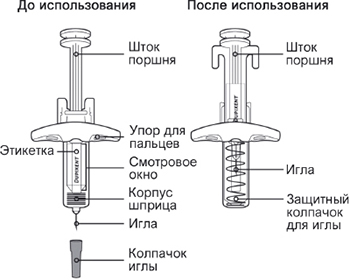
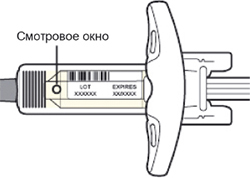
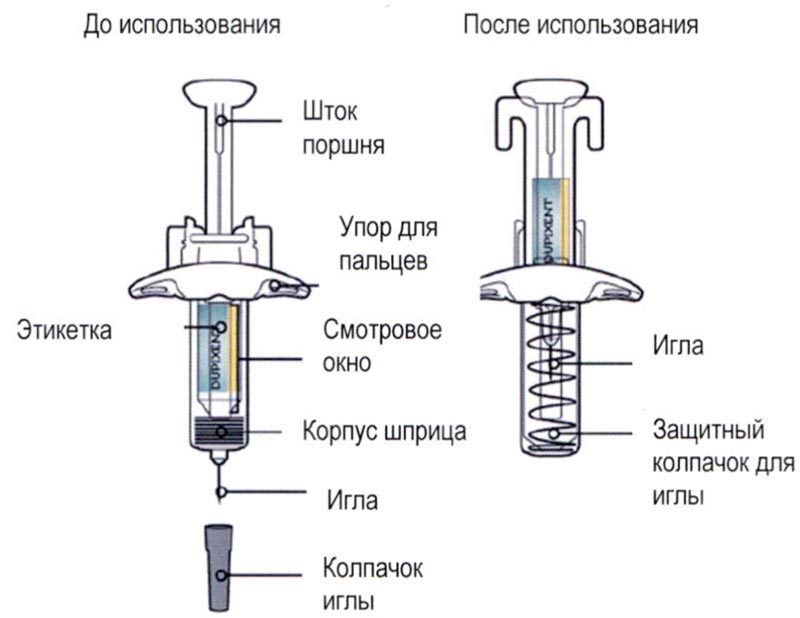
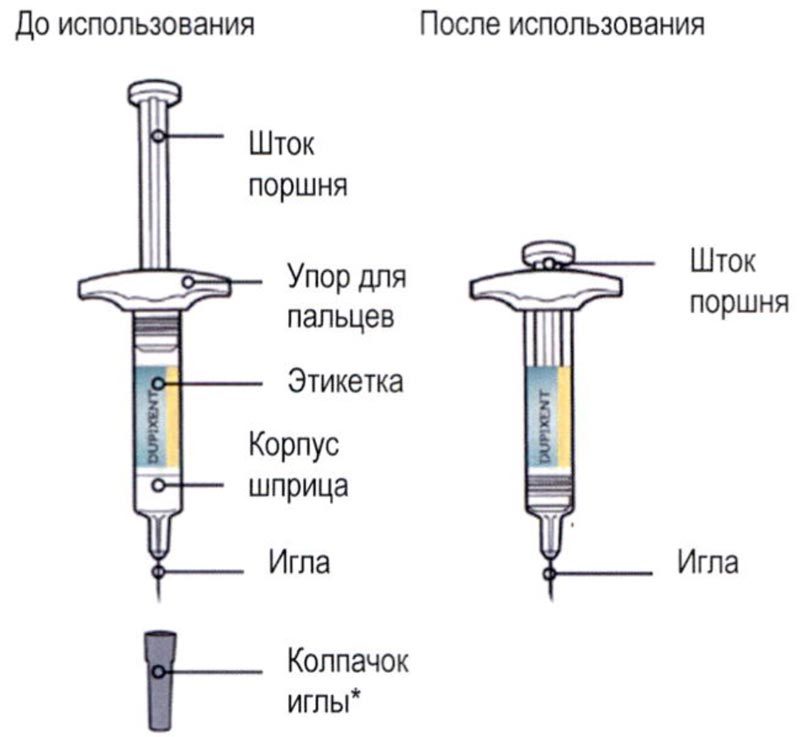
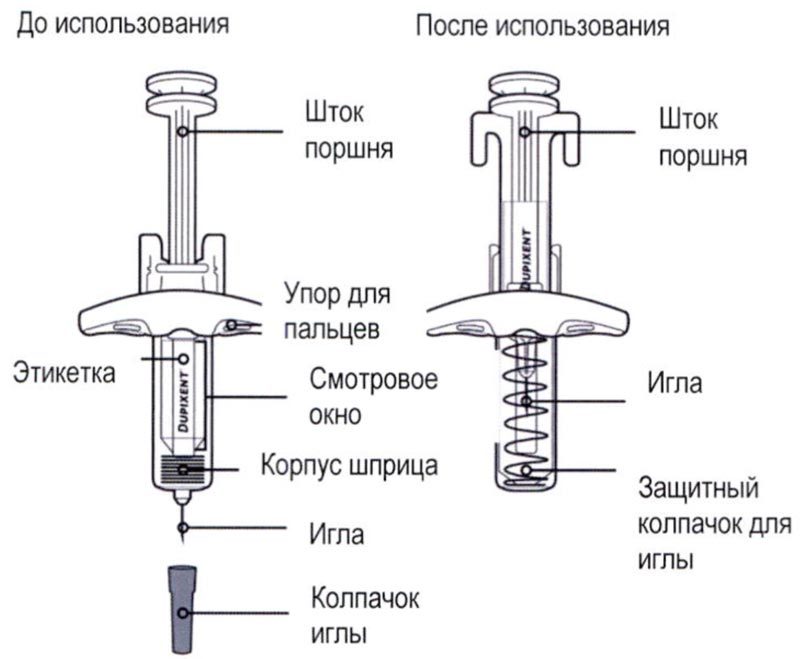
Перед началом применения препарата Дупиксент® в предварительно заполненном одноразовом шприце с системой защиты следует внимательно прочитать эту инструкцию. Элементы предварительно заполненного одноразового шприца с системой защиты показаны на рисунке ниже:
Данное устройство представляет собой предварительно заполненный одноразовый шприц с системой защиты (далее называется «шприц»). В нем содержится раствор для п/к введения, содержащий 300 мг препарата Дупиксент®.
Важная информация
— Не следует пытаться провести инъекцию самостоятельно или с помощью кого-то до тех пор, пока лечащий врач или медицинский работник не обучат пациента правильной технике проведения п/к инъекции.
— Перед использованием шприца следует внимательно прочитать информацию по его использованию.
— Следует узнать у своего лечащего врача, как часто пациенту необходимо проводить инъекции препарата Дупиксент®.
— Следует попросить своего лечащего врача или медицинского работника показать, как правильно пользоваться шприцем, перед тем как в первый раз самостоятельно провести инъекцию препарата Дупиксент®.
— Рекомендуется менять место инъекции при каждом введении препарата.
— Не использовать шприц, если он упал на твердую поверхность или поврежден.
— Нельзя использовать шприц, если отсутствует колпачок иглы или он не был надежно зафиксирован.
— Не дотрагиваться до штока поршня до тех пор, пока пациент не будет готов провести инъекцию.
— Не проводить инъекции через одежду.
— Не пытаться удалить воздушные пузырьки из шприца.
— Для того чтобы снизить риск случайного укола иглой, каждый предварительно заполненный одноразовый шприц оборудован устройством безопасности с системой защиты, которое автоматически активируется, закрывая иглу, после того, как проведена инъекция.
— Не тянуть шток поршня назад.
— Шприц не подлежит повторному использованию.
Как хранить шприц
— Хранить шприцы в недоступном для детей месте.
— Хранить неиспользуемые шприцы в оригинальной картонной упаковке в холодильнике при температуре от 2 до 8 °C.
— После извлечения из холодильника шприц следует оставить на 45 мин при комнатной температуре и дать возможность ему нагреться, перед тем как делать инъекцию препарата Дупиксент®.
— Шприцы можно хранить при комнатной температуре не более 14 дней.
— Не встряхивать шприц.
— Не подвергать шприц тепловому воздействию.
— Не замораживать шприц.
— Не допускать воздействия на шприц прямых солнечных лучей.
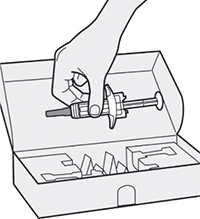
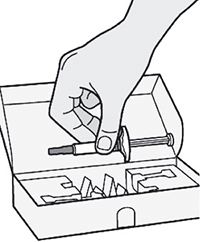
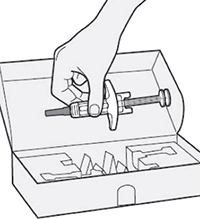
Шаг 1. Извлечение шприца из упаковки
Извлечь шприц из картонной упаковки, взяв его за середину корпуса.
Не снимать колпачок иглы до момента проведения инъекции.
Нельзя использовать шприц, если он упал на твердую поверхность или поврежден.
Шаг 2. Подготовка
Убедиться, что у пациента есть все необходимое для проведения инъекции:
— предварительно заполненный шприц;
— 1 салфетка, смоченная спиртом*;
— 1 ватный тампон или марлевая салфетка*;
— устойчивый к проколам контейнер* (см. Шаг 12).
* Не содержатся в картонной упаковке.
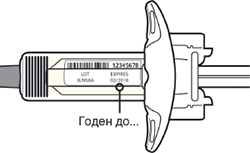
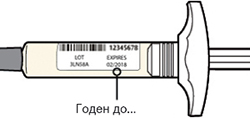
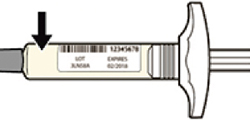
Внимательно проверить маркировку:
— проверить дату истечения срока годности;
— убедиться в том, что у пациента правильный препарат и правильная доза.
Нельзя использовать шприц после истечения срока годности, указанного на этикетке.
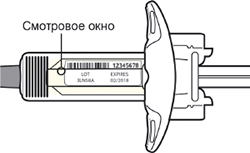
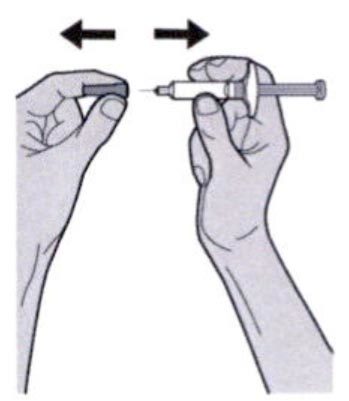
Шаг 3. Проверка
Осмотреть раствор через смотровое окно на шприце: проверить, является ли раствор прозрачным, бесцветным или имеет светло-желтый оттенок.
Примечание: Можно обнаружить воздушные пузырьки, это нормально.
Нельзя использовать шприц, если жидкость изменила цвет или помутнела, или если в ней есть заметные хлопья или частицы.
Шаг 4. Необходимо подождать 45 мин
Положить шприц на плоскую поверхность, не менее чем на 45 мин, чтобы шприц нагрелся до комнатной температуры.
Не нагревать шприц.
Не подвергать шприц прямому воздействию солнечных лучей.
Шприц нельзя хранить при комнатной температуре более 14 дней.
Шаг 5. Выбор места инъекции
Выбрать место инъекции:
— можно сделать инъекцию в наружную поверхность бедра или переднюю часть живота, за исключением области диаметром 5 см непосредственно вокруг пупка;
— если инъекцию осуществляет другой человек, для инъекции также можно использовать участок кожи в верхней части плеча.
Инъекции препарата Дупиксент® не следует осуществлять на участках с болезненной или поврежденной кожей, кровоподтеками или рубцами.
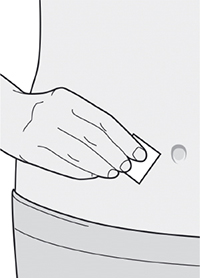
Шаг 6. Обработка места инъекции
— вымыть руки;
— протереть участок кожи, предназначенный для инъекции, салфеткой, смоченной спиртом;
— дать коже высохнуть перед проведением инъекции;
Не дотрагиваться до обработанного участка кожи руками и не дуть на него перед проведением инъекции.
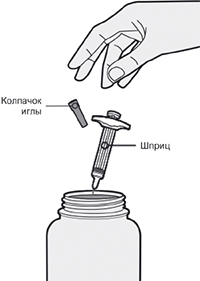
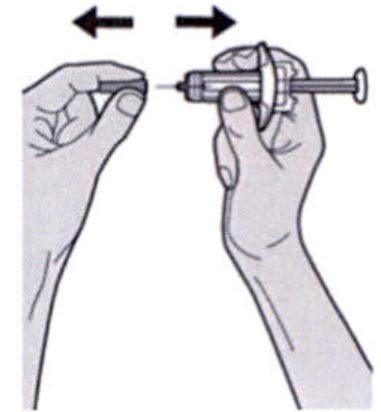
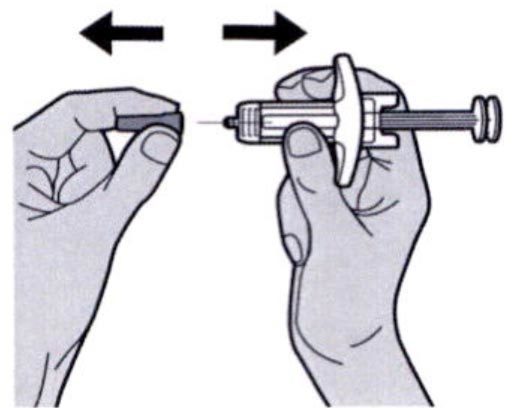
Шаг 7. Удаление колпачка иглы
Держать шприц за середину корпуса, игла должна быть направлена в сторону от пациента, и снять колпачок с иглы.
Не надевать колпачок обратно на иглу.
Не касаться иглы.
Лекарственный препарат необходимо ввести сразу же после удаления колпачка иглы.
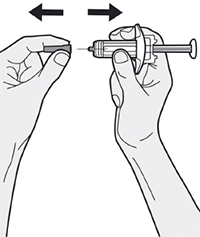
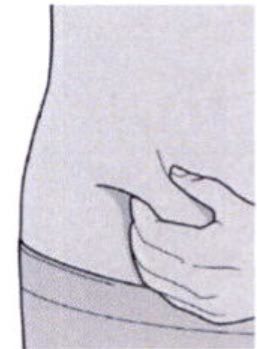
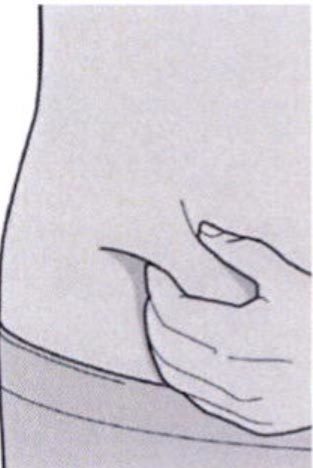
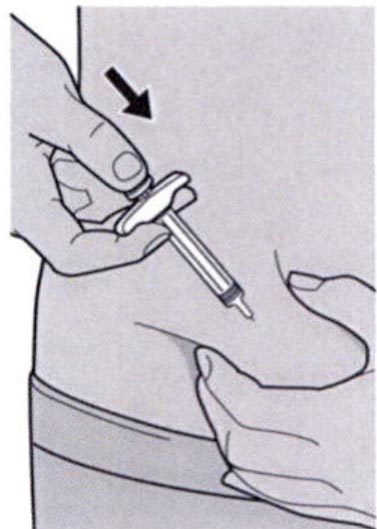
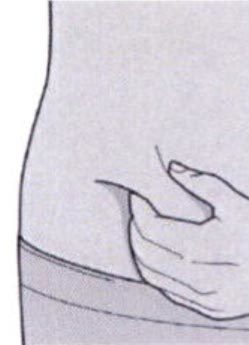
Шаг 8. Формирование складки кожи
Сформировать складку кожи в месте инъекции, как показано на рисунке.
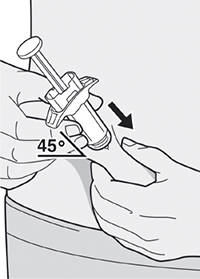
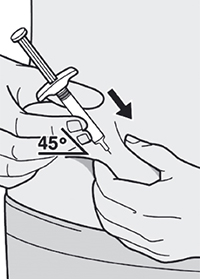
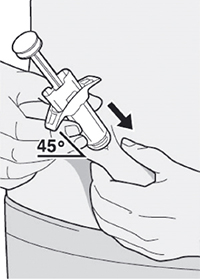
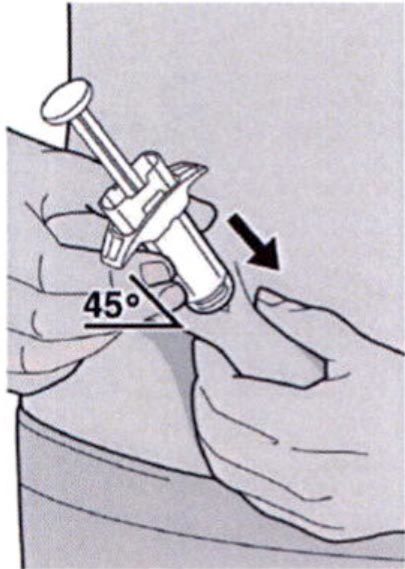
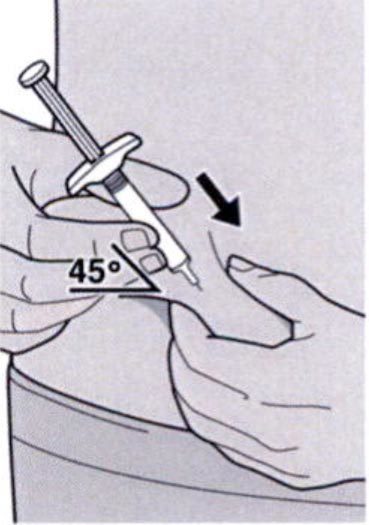
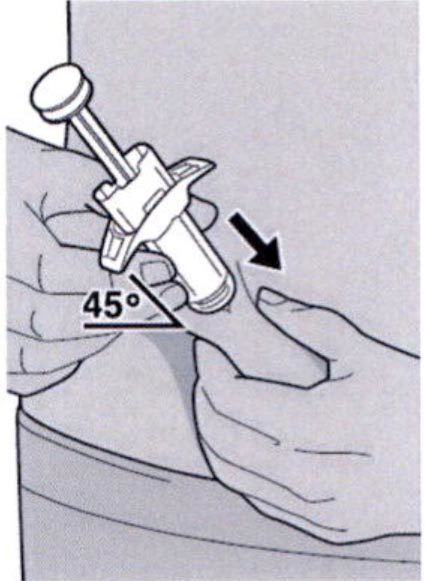
Шаг 9. Введение иглы
Полностью ввести иглу в сформированную складку кожи под углом приблизительно 45°.
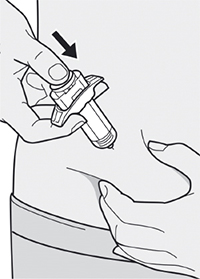
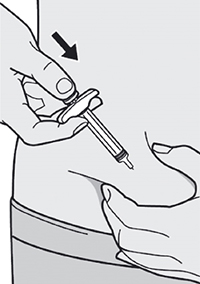
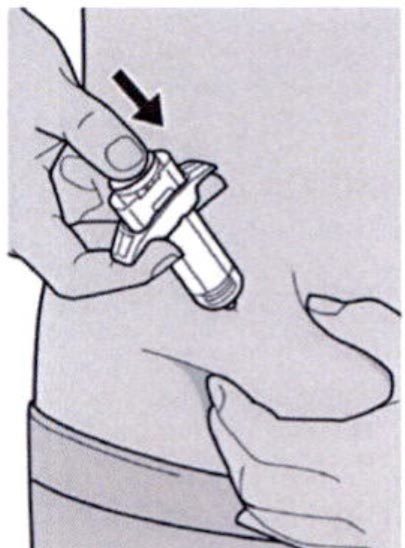
Шаг 10. Введение раствора
Ослабить сформированную складку кожи.
Медленно и непрерывно нажимать на шток поршня для введения всего раствора, пока шприц не опустеет.
Примечание: Может ощущаться некоторое сопротивление. Это нормально.
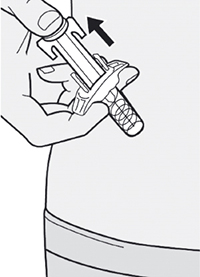
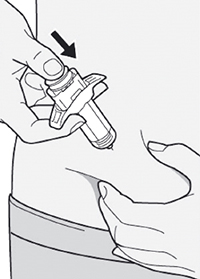
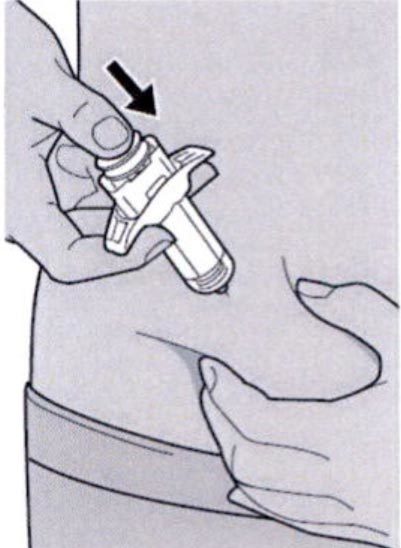
Шаг 11. Завершение инъекции и извлечение иглы
Поднять большой палец, снимая давление со штока поршня, игла будет втянута внутрь защитного колпачка для иглы, а затем удалить шприц из места инъекции.
Слегка прижать ватный тампон или марлевую салфетку к месту инъекции, если замечена кровь.
Не надевать колпачок иглы снова на иглу.
Не растирать кожу после инъекции.
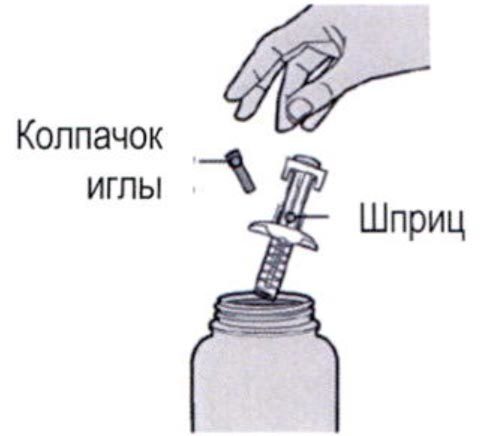
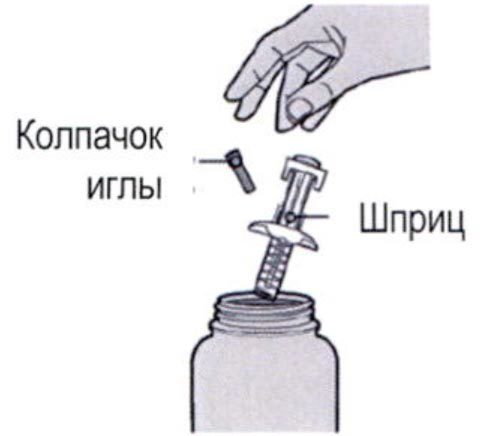
Шаг 12. Утилизация
После использования следует поместить шприц и колпачок иглы в устойчивый к проколам контейнер.
Хранить контейнер в недоступном для детей месте.
Инструкция по подготовке и проведению инъекции препарата Дупиксент® 300 мг в предварительно заполненном одноразовом шприце
Перед началом применения препарата Дупиксент® в предварительно заполненном одноразовом шприце внимательно прочитать эту инструкцию.
Элементы предварительно заполненного шприца показаны на рисунке ниже:
* Шприц может иметь твердый или мягкий колпачок иглы.
Данное устройство представляет собой предварительно заполненный одноразовый шприц (далее называется «шприц»). В нем содержится раствор для п/к введения, содержащий 300 мг препарата Дупиксент®.
Важная информация
— Пациенту не следует пытаться провести инъекцию самостоятельно или с помощью кого-то до тех пор, пока лечащий врач или медицинский работник не обучат пациента правильной технике проведения подкожной инъекции.
— Перед использованием шприца следует внимательно прочитать информацию по его использованию.
— Следует узнать у своего лечащего врача, как часто необходимо проводить инъекции препарата Дупиксент®.
— Пациенту следует попросить своего лечащего врача или медицинского работника показать, как правильно пользоваться шприцем, перед тем как в первый раз самостоятельно провести инъекцию препарата Дупиксент®.
— Рекомендуется менять место инъекции при каждом введении препарата.
— Не использовать шприц, если он поврежден.
— Нельзя использовать шприц, если отсутствует колпачок иглы или он не был надежно зафиксирован.
— Не дотрагиваться до штока поршня до тех пор, пока пациент не будет готов провести инъекцию.
— Не проводить инъекции через одежду.
— Не пытаться удалить воздушные пузырьки из шприца.
— Не тянуть шток поршня назад.
— Шприц не подлежит повторному использованию.
Как хранить шприц
— Хранить шприцы в недоступном для детей месте.
— Хранить неиспользуемые шприцы в оригинальной картонной упаковке в холодильнике при температуре от 2 до 8 °С.
— После извлечения из холодильника шприц следует оставить на 45 мин при комнатной температуре и дать возможность ему нагреться, перед тем как проводить инъекцию препарата Дупиксент®.
— Шприцы можно хранить при комнатной температуре не более 14 дней.
— Не встряхивать шприц.
— Не подвергать шприц тепловому воздействию.
— Не замораживать шприц.
— Не допускать воздействия на шприц прямых солнечных лучей.
Шаг 1. Извлечение шприца из упаковки
Извлечь шприц из картонной упаковки, взяв его за середину корпуса.
Не снимать колпачок иглы до момента проведения инъекции.
Нельзя использовать шприц, если он был поврежден.
Шаг 2. Подготовка
Убедиться, что у пациента есть все необходимое для проведения инъекции:
— предварительно заполненный шприц;
— 1 салфетка, смоченная спиртом*;
— 1 ватный тампон или марлевая салфетка*;
— устойчивый к проколам контейнер* (см. Шаг 12).
* Не содержатся в картонной упаковке.
Внимательно проверить маркировку:
— проверить дату истечения срока годности;
— убедиться в том, что у пациента правильный препарат и правильная доза.
Нельзя использовать шприц после истечения срока годности, указанного на этикетке.
Шаг 3. Проверка
Осмотреть раствор в шприце: проверить, является ли раствор прозрачным, бесцветным или имеет светло-желтый оттенок.
Примечание: Можно обнаружить воздушные пузырьки, это нормально.
Нельзя использовать шприц, если жидкость изменила цвет или помутнела, или если в ней есть заметные хлопья или частицы.
Шаг 4. Подождать 45 мин
Положить шприц на плоскую поверхность не менее чем на 45 мин, чтобы шприц нагрелся до комнатной температуры.
Не нагревать шприц.
Не подвергать шприц прямому воздействию солнечных лучей.
Шприц нельзя хранить при комнатной температуре более 14 дней.
Шаг 5. Выбор места инъекции
Выбрать место инъекции.
— можно сделать инъекцию в наружную поверхность бедра или в переднюю часть живота, за исключением области диаметром 5 см непосредственно вокруг пупка;
— если инъекцию осуществляет другой человек, для инъекции также можно использовать участок кожи в верхней части плеча.
Инъекции препарата Дупиксент® не следует осуществлять на участках с болезненной или поврежденной кожей, кровоподтеками или рубцами.
Шаг 6. Обработка участка инъекции
— вымыть руки;
— протереть участок кожи, предназначенный для инъекции, салфеткой, смоченной спиртом;
— дать коже высохнуть перед проведением инъекции;
— не дотрагиваться до обработанного участка кожи руками и не дуть на него перед проведением инъекции.
Шаг 7. Удаление колпачка иглы
Держать шприц за середину корпуса, игла должна быть направлена в сторону от пациента, и снять колпачок иглы.
Не надевать колпачок иглы обратно на иглу.
Не касаться иглы.
Лекарственный препарат необходимо ввести сразу же после удаления колпачка иглы.
Шаг 8. Формирование складки кожи
Сформировать складку кожи на участке инъекции, как показано на рисунке.
Шаг 9. Введение иглы
Полностью ввести иглу в сформированную складку под углом приблизительно 45°.
Шаг 10. Введение раствора
Ослабить сформированную складку кожи.
Медленно и непрерывно нажимать на шток поршня для введения всего раствора, пока шприц не опустеет.
Примечание: Может ощущаться некоторое сопротивление. Это нормально.
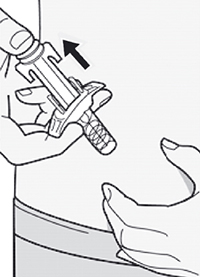
Шаг 11. Извлечение иглы
Извлечь иглу из кожи под тем же углом, под которым она была введена.
Не надевать колпачок иглы снова на иглу.
Слегка прижать ватный тампон или марлевую салфетку к месту инъекции, если замечена кровь.
Не растирать кожу после инъекции.
Шаг 12. Утилизация
После использования следует поместить шприц и колпачок иглы в устойчивый к проколам контейнер.
Не надевать колпачок иглы снова на иглу.
Хранить контейнер в недоступном для детей месте.
Инструкция по подготовке и проведению инъекции препарата Дупиксент® 200 мг в предварительно заполненном одноразовом шприце с системой защиты
Перед началом применения препарата Дупиксент® в предварительно заполненном одноразовом шприце с системой защиты следует внимательно прочитать эту инструкцию.
Элементы предварительно заполненного одноразового шприца с системой защиты показаны на рисунке ниже:
Данное устройство представляет собой предварительно заполненный одноразовый шприц с системой защиты (далее называется «шприц»). В нем содержится раствор для п/к введения, содержащий 200 мг препарата Дупиксент®.
Важная информация
— Пациенту не следует пытаться провести инъекцию самостоятельно или с помощью кого-то до тех пор, пока лечащий врач или медицинский работник не обучат пациента правильной технике проведения п/к инъекции.
— Перед использованием шприца следует внимательно прочитать информацию по его использованию.
— Следует узнать у своего лечащего врача, как часто необходимо проводить инъекции препарата Дупиксент®.
— Следует попросить своего лечащего врача или медицинского работника показать, как правильно пользоваться шприцем, перед тем как в первый раз самостоятельно провести инъекцию препарата Дупиксент®.
— Рекомендуется менять место инъекции при каждом введении препарата.
— Не использовать шприц, если он упал на твердую поверхность или поврежден.
— Нельзя использовать шприц, если отсутствует колпачок иглы или он не был надежно зафиксирован.
— Не дотрагиваться до штока поршня до тех пор, пока пациент не будет готов провести инъекцию.
— Не проводить инъекции через одежду.
— Не пытаться удалить воздушные пузырьки из шприца.
— Для того чтобы снизить риск случайного укола иглой, каждый предварительно заполненный одноразовый шприц оборудован устройством безопасности с системой защиты, которое автоматически активируется, закрывая иглу, после того как проведена инъекция.
— Не тянуть шток поршня назад.
— Шприц не подлежит повторному использованию.
Как хранить шприц
— Хранить шприцы в недоступном для детей месте.
— Хранить неиспользуемые шприцы в оригинальной картонной упаковке в холодильнике при температуре от 2 до 8 °С.
— После извлечения из холодильника шприц следует оставить на 30 мин при комнатной температуре и дать возможность ему нагреться, перед тем как делать инъекцию препарата Дупиксент®.
— Шприцы можно хранить при комнатной температуре не более 14 дней.
— Не встряхивать шприц.
— Не подвергать шприц тепловому воздействию.
— Не замораживать шприц.
— Не допускайте воздействия на шприц прямых солнечных лучей.
Шаг 1. Извлечение шприца из упаковки
Извлечь шприц из картонной упаковки, взяв его за середину корпуса.
Не снимать колпачок иглы до момента проведения инъекции.
Нельзя использовать шприц, если он упал на твердую поверхность или поврежден.
Шаг 2. Подготовка
Убедиться, что у пациента есть все необходимое для проведения инъекции:
— предварительно заполненный шприц;
— 1 салфетка, смоченная спиртом*;
— 1 ватный тампон или марлевая салфетка*;
— устойчивый к проколам контейнер* (см. Шаг 12).
* Не содержатся в картонной упаковке.
Внимательно проверить маркировку:
— проверить дату истечения срока годности;
— убедиться в том, что у пациента правильный препарат и правильная доза.
Нельзя использовать шприц после истечения срока годности, указанного на этикетке.
Шаг 3. Проверка
Осмотреть раствор через смотровое окно на шприце: проверить, является ли раствор прозрачным, бесцветным или имеет светло-желтый оттенок.
Примечание: Можно обнаружить воздушные пузырьки, это нормально.
Нельзя использовать шприц, если жидкость изменила цвет или помутнела, или если в ней есть заметные хлопья или частицы.
Шаг 4. Подождать 30 мин
Положить шприц на плоскую поверхность не менее чем на 30 мин, чтобы шприц нагрелся до комнатной температуры.
Не нагревать шприц.
Не подвергать шприц прямому воздействию солнечных лучей.
Шприц нельзя хранить при комнатной температуре более 14 дней.
Шаг 5. Выбор места инъекции
Выбрать место инъекции:
— можно сделать инъекцию в наружную поверхность бедра или переднюю часть живота, за исключением области диаметром 5 см непосредственно вокруг пупка;
— если инъекцию осуществляет другой человек, для инъекции также можно использовать участок кожи в верхней части плеча.
Инъекции препарата Дупиксент® не следует осуществлять на участках с болезненной или поврежденной кожей, кровоподтеками или рубцами.
Шаг 6. Обработка места инъекции
— вымыть руки;
— протереть участок кожи, предназначенный для инъекции салфеткой, смоченной спиртом;
— дать коже высохнуть перед проведением инъекции;
— не дотрагиваться до обработанного участка кожи руками и не дуть на него перед проведением инъекции.
Шаг 7. Удаление колпачка иглы
Держать шприц за середину корпуса, игла должна быть направлена в сторону от пациента, и снять колпачок с иглы.
Не надевать колпачок обратно на иглу.
Не касаться иглы.
Лекарственный препарат необходимо ввести сразу же после удаления колпачка иглы.
Шаг 8. Формирование складки кожи
Сформировать складку кожи в месте инъекции, как показано на рисунке.
Шаг 9. Введение иглы
Полностью ввести иглу в сформированную складку кожи под углом приблизительно 45°.
Шаг 10. Введение раствора
Ослабить сформированную складку кожи.
Медленно и непрерывно нажимать на шток поршня для введения всего раствора, пока шприц не опустеет.
Примечание: Может ощущаться некоторое сопротивление. Это нормально.
Шаг 11. Завершение инъекции и извлечение иглы
Поднять большой палец, снимая давление со штока поршня, игла будет втянута внутрь защитного колпачка для иглы, а затем удалить шприц из места инъекции.
Слегка прижать ватный тампон или марлевую салфетку к месту инъекции, если замечена кровь.
Не надевать колпачок иглы снова на иглу.
Не растирать кожу после инъекции.
Шаг 12. Утилизация
После использования следует поместить шприц и колпачок иглы в устойчивый к проколам контейнер.
Не надевать колпачок иглы снова на иглу.
Хранить контейнер в недоступном для детей месте.
Побочные действия
Для описания частоты встречаемости нежелательных реакций используется следующая классификация: очень часто (≥10 %); часто (≥1%, <10%); нечасто (≥0,1%, <1%); редко (≥0,01%, <0,1%); очень редко (<0,01%); частота неизвестна (невозможно определить по имеющимся данным частоту встречаемости нежелательной реакции).
Атопический дерматит
Таблица 1
Нежелательные реакции, наблюдавшиеся в клинических исследованиях у пациентов с атопическим дерматитом1
| Системно-органный класс | Частота | Нежелательные реакции |
| Инфекционные и паразитарные заболевания | Часто | Конъюнктивит (4,0%) |
| Герпес ротовой полости (3,8%) | ||
| Бактериальный конъюнктивит (1,9%) | ||
| Простой герпес (Herpes simplex)2 (1,7%) | ||
| Со стороны крови и лимфатической системы | Часто | Эозинофилия (1,7%) |
| Со стороны органа зрения | Часто | Аллергический конъюнктивит (7,0%) |
| Зуд в глазах (2,9%) | ||
| Блефарит (4,5%) | ||
| Синдром сухого глаза (1,8%) | ||
| Общие нарушения и нарушения в месте введения препарата | Очень часто | Реакции в месте инъекции (15,9%) |
1 Объединенные данные плацебо-контролируемых клинических исследований с проведением монотерапии (SOLO 1, SOLO 2 и исследования по подбору доз II фазы) и плацебо-контролируемого исследования CHRONOS с одновременным применением топических ГКС для лечения атопического дерматита; пациенты получали препарат в дозе 300 мг 1 раз в 2 нед и 300 мг 1 раз в неделю с или без топических ГКС в течение 16 нед.
2 В клинических исследованиях случаи с герпетическими инфекциями (Herpes simplex) проявлялись поражениями кожи и слизистых оболочек, обычно были легкой или средней степени тяжести и не включали герпетическую экзему. О случаях герпетической экземы сообщалось отдельно, частота таких случаев была ниже у пациентов, получавших препарат Дупиксент®, по сравнению с группой плацебо.
Подростки (от 12 до 17 лет)
Безопасность применения препарата Дупиксент® была оценена в исследовании с 250 пациентами от 12 до 17 лет с атопическим дерматитом среднетяжелого и тяжелого течения (AD-1526). Профиль безопасности в течение 16 нед был сравним с профилем безопасности взрослых пациентов, принимавших участие в исследованиях.
Безопасность при длительном применении препарата Дупиксент® была оценена в долгосрочном открытом продолженном исследовании с участием пациентов 12–17 лет с атопическим дерматитом среднетяжелого и тяжелого течения (AD-1434). Профиль безопасности в течение 52 нед был сравним с профилем безопасности пациентов, принимавших участие в 16-недельном исследовании (AD-1526). Профиль безопасности при длительном применении препарата Дупиксент® подростками соответствовал таковому у взрослых пациентов.
Профиль безопасности комбинированного лечения препаратом Дупиксент® + топические ГКС в течение 52 нед соответствует профилю его безопасности, наблюдавшемуся к 16-й нед.
Дети (от 6 до 11 лет)
Безопасность препарата Дупиксент® изучали в исследовании при участии 367 пациентов от 6 до 11 лет с тяжелым атопическим дерматитом (AD-1652). Профиль безопасности препарата Дупиксент® в сочетании с топическими ГКС у этих пациентов, наблюдение за которыми вели до 16-й нед включительно, оказался сопоставимым с профилем безопасности препарата в исследованиях с участием взрослых пациентов с атопическим дерматитом.
Долгосрочную безопасность препарата Дупиксент® в сочетании с топическими ГКС оценивали в открытом продолженном исследовании у 368 пациентов от 6 до 11 лет с атопическим дерматитом (AD-1434). На момент включения в исследование AD-1434 у 110 (29,9%) пациентов был среднетяжелый, а у 72 (19,6%) — тяжелый атопический дерматит. Профиль безопасности препарата Дупиксент® в сочетании с топическими ГКС у пациентов, наблюдение за которыми вели в течение 52 нед, был схожим с профилем безопасности, установленным на 16-й нед в исследовании AD-1652. Долгосрочный профиль безопасности препарата Дупиксент® в сочетании с топическими ГКС у детей был сопоставим с таковым у взрослых пациентов и подростков с атопическим дерматитом.
Бронхиальная астма
Таблица 2
Нежелательные реакции, наблюдавшиеся в клинических исследованиях у пациентов с бронхиальной астмой
| Системно-органный класс | Частота | Нежелательные реакции |
| Общие нарушения и нарушения в месте введения препарата | Очень часто | Эритема в месте инъекции (14,6%) |
| Часто | Отек в месте инъекции (4,8%) | |
| Часто | Зуд в месте инъекции (4,7%) | |
| Очень редко | Анафилаксия (0,04%) |
Долгосрочную безопасность препарата Дупиксент® оценивали в открытом продленном исследовании с участием 2282 пациентов в возрасте от 12 лет и старше со среднетяжелой и тяжелой бронхиальной астмой (TRAVERSE). В этом исследовании наблюдение продолжалось в течение 96 нед, что составило 3169 пациенто-лет кумулятивного воздействия препарата Дупиксент®. Профиль безопасности препарата Дупиксент® в исследовании TRAVERSE соответствовал профилю безопасности, зарегистрированному в базовых исследованиях по лечению астмы в течение 52 нед. Не было выявлено дополнительных нежелательных реакций.
ХПРС
Таблица 3
Нежелательные реакции, наблюдавшиеся в клинических исследованиях у пациентов с ХПРС
| Системно-органный класс | Частота | Нежелательные реакции |
| Инфекционные и паразитарные заболевания | Часто | Конъюнктивит (1,4%) |
| Общие нарушения и нарушения в месте введения препарата | Часто | Реакции в месте инъекции (3,4%) Отек в месте инъекции (1,4%) |
Описание отдельных нежелательных реакций
Явления, связанные с конъюнктивитом и кератитом
Конъюнктивит и кератит чаще всего наблюдались у пациентов с атопическим дерматитом, получавших препарат Дупиксент®. У большинства пациентов конъюнктивит или кератит разрешался полностью или частично в течение периода лечения. Среди пациентов с астмой частота конъюнктивита и кератита была низкой и сходной между группами, получавшими препарат Дупиксент® и плацебо. У пациентов с ХПРС частота конъюнктивита была низкой, хотя частота в группе получавших препарат Дупиксент® была выше, чем в группе плацебо. В программе клинических исследований у пациентов с ХПРС не было зарегистрировано ни одного случая кератита (см. «Особые указания»).
Герпетическая экзема и Herpes zoster
В клинических исследованиях у пациентов с атопическим дерматитом частота герпетической экземы была схожей в группах, получающих препарат Дупиксент®, и группе плацебо. По данным 16-недельных исследований монотерапии, Herpes zoster был зарегистрирован в <0,1% случаев в группе, получающей Дупиксент® (<1 на 100 пациенто-лет) и <1% в группе плацебо (1 на 100 пациенто-лет). В 52-недельном клиническом исследовании с одновременным применением топических ГКС (CHRONOS) Herpes zoster был зарегистрирован в 1% случаев в группе, получающей Дупиксент® + топические ГКС (1 на 100 пациенто-лет), и в 2% в группе плацебо (2 на 100 пациенто-лет). В клинических исследованиях у пациентов с бронхиальной астмой частота Herpes zoster была схожей в группах, получающих препарат Дупиксент® или плацебо.
Гиперчувствительность
Сообщалось о реакциях гиперчувствительности, включая анафилаксию и сывороточную болезнь, или реакциях, подобных сывороточной болезни (см. «Противопоказания» и «Особые указания»).
Эозинофилы
У пациентов, получавших препарат Дупиксент®, наблюдалось более высокое среднее начальное увеличение от исходного уровня количества эозинофилов по сравнению с пациентами, получавшими плацебо. Количество эозинофилов снижалось почти до базовых уровней во время исследования. В рамках открытого продленного исследования у пациентов с бронхиальной астмой количество эозинофилов продолжало снижаться ниже исходного уровня.
Частота развития эозинофилии (≥500 клеток/мкл), вызванной лечением, была сходной в группах пациентов, получавших препарат Дупиксент® и плацебо. Эозинофилия, вызванная лечением (≥5000 клеток/мкл), была зарегистрирована менее чем у 2% пациентов, получавших препарат Дупиксент®, и менее чем у 0,5% пациентов, получавших плацебо.
Инфекции
Количество серьезных инфекций у пациентов с атопическим дерматитом, бронхиальной астмой и ХПРС было сопоставимо у пациентов, принимавших Дупиксент® и плацебо.
В первичных клинических исследованиях безопасности у пациентов с атопическим дерматитом не наблюдалось увеличения общей частоты инфекций или серьезных инфекций во время лечения препаратом Дупиксент® по сравнению с плацебо. В 16-недельных первичных клинических исследованиях безопасности, в которых проводилась монотерапия препаратом Дупиксент®, были зарегистрированы серьезные инфекции у 0,5% пациентов, получавших дупилумаб, и у 1,0% пациентов, получавших плацебо. В 52-недельном исследовании CHRONOS серьезные инфекции были зарегистрированы у 0,2% пациентов, получавших препарат Дупиксент®, и у 0,6% пациентов, получавших плацебо.
В клинических исследованиях у пациентов с бронхиальной астмой не наблюдалось увеличения общей частоты инфекций или серьезных инфекций во время лечения препаратом Дупиксент® по сравнению с плацебо. В 24-недельном клиническом исследовании были зарегистрированы серьезные инфекции у 1,0% пациентов, получавших дупилумаб, и у 1,1% пациентов, получавших плацебо. В 52-недельном исследовании QUEST серьезные инфекции были зарегистрированы у 1,3% пациентов, получавших дупилумаб, и у 1,4% пациентов, получавших плацебо.
В клинических исследованиях у пациентов с ХПРС не наблюдалось увеличения общей частоты инфекций. В 24-недельном клиническом исследовании серьезные инфекции были зарегистрированы у 0,7% пациентов, получавших Дупиксент®, и у 1,1% пациентов, получавших плацебо.
Сердечно-сосудистые события
В однолетнем плацебо-контролируемом исследовании у пациентов с бронхиальной астмой (QUEST) сердечно-сосудистые тромбоэмболические события (сердечно-сосудистые смерти, нефатальные инфаркты миокарда и нефатальные инсульты) были зарегистрированы в 1 случае (0,2%) в группе пациентов, получавших Дупиксент® 200 мг 1 раз в 2 нед, в 4 случаях (0,6%) в группе пациентов, получавших Дупиксент® 300 мг 1 раз в 2 нед и в 2 случаях (0,3%) в группе плацебо. В однолетнем плацебо-контролируемом исследовании у пациентов с атопическим дерматитом (CHRONOS) сердечно-сосудистые тромбоэмболические события (сердечно-сосудистые смерти, нефатальные инфаркты миокарда и нефатальные инсульты) были зарегистрированы в 1 случае (0,9%) в группе пациентов, получавших Дупиксент® 300 мг 1 раз в 2 нед + топические ГКС, в 0 случаев (0,0%) в группе пациентов, получавших Дупиксент® 300 мг 1 раз в неделю + топические ГКС, и в 1 случае (0,3%) в группе плацебо + топические ГКС.
Иммуногенность
Как и все белковые лекарственные препараты, препарат Дупиксент® может вызывать аллергические реакции.
Примерно у 5% пациентов с атопическим дерматитом, бронхиальной астмой или ХПРС, которые получали препарат Дупиксент® в дозе 300 мг 1 раз в 2 нед в течение 52 нед, отмечалось образование антител (АТ) к дупилумабу, приблизительно у 2% пациентов АТ стойко сохранялись, приблизительно 2% имели нейтрализующие АТ. Аналогичные результаты наблюдались у пациентов детского возраста (от 6 до 11 лет) с атопическим дерматитом, которые получали препарат Дупиксент® в дозе 200 мг 1 раз в 2 нед или 300 мг 1 раз в 4 нед в течение 16 нед.
Приблизительно у 16% подростков с атопическим дерматитом, получавших препарат Дупиксент® в дозе 300 мг или 200 мг 1 раз в 2 нед в течение 16 недель, отмечалось образование антител к дупилумабу; приблизительно у 3% зарегистрирован стойкий ответ со стороны АТ, приблизительно у 5% пациентов были выявлены нейтрализующие АТ.
Примерно у 9% пациентов с бронхиальной астмой, которые получали препарат Дупиксент® в дозе 200 мг 1 раз в 2 нед в течение 52 нед, отмечалось образование АТ к дупилумабу, приблизительно у 4% АТ устойчиво сохранялись, приблизительно 4% имели нейтрализующие АТ.
Независимо от возраста и популяции примерно у 2–4% пациентов в группах плацебо в 52-недельных исследованиях имелись АТ к дупилумабу; приблизительно у 2% АТ устойчиво сохранялись и приблизительно 1% имели нейтрализующие АТ.
Реакция образования АТ обычно не влияла на системную экспозицию, безопасность или эффективность препарата Дупиксент®. Менее чем у 1% пациентов, получавших препарат Дупиксент® в зарегистрированной дозе, были выявлены высокие титры АТ к препарату, ассоциирующиеся со снижением его системной экспозиции и эффективности. Кроме того, у одного пациента была обнаружена сывороточная болезнь, а у другого реакция, подобная сывороточной болезни (<0,1%), ассоциировавшиеся с высокими титрами АТ (см. «Особые указания»).
Наблюдаемая частота стойкого сохранения АТ и нейтрализующей активности в значительной степени зависят от чувствительности и специфичности используемого аналитического метода. Кроме того, наблюдаемая частота АТ-положительного статуса в анализе может зависеть от нескольких факторов, в т.ч. методики анализа, способа обработки проб, времени сбора проб, сопутствующих препаратов, а также статуса основного заболевания в каждом отдельном случае. По этим причинам сравнение частоты образования АТ к дупилумабу с частотой выработки АТ к другим препаратам может ввести в заблуждение.
Взаимодействие
Реклама: ООО «ВЕДАНТА», ИНН 7714886235, erid 4CQwVszH9pUkKJ7jUDd
Реклама: ООО «РЛС-Библиомед» ИНН 7714758963
Реклама: ООО «ВЕДАНТА», ИНН 7714886235, erid 4CQwVszH9pUkKJ7jUDd
Реклама: ООО «РЛС-Библиомед» ИНН 7714758963
Живые вакцины
Применение препарата Дупиксент® с живыми вакцинами не изучалось. Во время лечения препаратом Дупиксент® не следует проводить вакцинацию живыми вакцинами.
Неживые (инактивированные) вакцины
Иммунные реакции на вакцинацию изучались в исследовании, в котором пациенты с атопическим дерматитом получали еженедельно препарат Дупиксент® в дозе 300 мг в течение 16 нед. После 12 нед терапии дупилумабом пациентов вакцинировали вакциной Tdap (Т-клеточнозависимая, Adacel®) и менингококковой полисахаридной вакциной (Т-клеточнонезависимая, Menomune®) и оценивали иммунные реакции по истечении 4 нед. У пациентов, получавших как дупилумаб, так и плацебо, реакции с образованием АТ к противостолбнячной и менингококковой полисахаридной вакцинам были сходными. В этом исследовании не было обнаружено нежелательных взаимодействий между любой из этих неживых вакцин и дупилумабом.
Взаимодействие с субстратами изоферментов CYP450
В клиническом исследовании, проведенном у пациентов с атопическим дерматитом, оценивались эффекты дупилумаба на фармакокинетику субстратов изоферментов CYP. Данные, полученные в этом исследовании, не указывают на клинически значимое влияние дупилумаба на активность изоферментов CYP1A2, CYP3A, CYP2C19, CYP2D6 или CYP2C9.
Взаимодействие с другими лекарственными средствами для лечения бронхиальной астмы
Влияние дупилумаба на фармакокинетику одновременно назначаемых препаратов не ожидается. Данные, полученные на основании популяционного анализа, не указывают на влияние одновременно назначаемых препаратов на фармакокинетику дупилумаба у пациентов со среднетяжелым или тяжелым течением бронхиальной астмы.
Передозировка
В клинических исследованиях не было выявлено проблем, связанных с безопасностью, при однократном в/в введении доз до 12 мг/кг. Специфического антидота при передозировке препарата Дупиксент® не существует. В случае передозировки необходимо контролировать состояние пациента для своевременного выявления признаков и симптомов нежелательных явлений и незамедлительно назначать соответствующее симптоматическое лечение.
Особые указания
Гиперчувствительность
При возникновении системной реакции гиперчувствительности лечение препаратом Дупиксент® должно быть немедленно прекращено и начата соответствующая терапия. В клинических исследованиях при применении препарата Дупиксент® при атопическом дерматите сообщалось об одном случае развития реакции, подобной сывороточной болезни, и одном случае развития сывороточной болезни после введения препарата (обе нежелательные реакции расценивались как серьезные). В исследовании при применении препарата при бронхиальной астме сообщалось об одном случае развития анафилаксии после введения препарата Дупиксент® (см. «Побочные действия»).
Конъюнктивит и явления, связанные с кератитом
Конъюнктивит и явления, связанные с кератитом, чаще встречались у пациентов с атопическим дерматитом, получавших препарат Дупиксент®. У некоторых пациентов наблюдалось нарушение зрения (например, затуманенное зрение), связанное с конъюнктивитом или кератитом (см. «Побочные действия»). Пациенты должны сообщать о первом появлении или ухудшении симптомов со стороны глаз своему лечащему врачу. Пациенты, получающие лечение препаратом Дупиксент®, у которых развивался конъюнктивит, не проходящий после стандартного лечения, или признаки и симптомы кератита, должны пройти соответствующее офтальмологическое обследование (см. «Побочные действия»).
Эозинофильные состояния
У пациентов с бронхиальной астмой может развиться серьезная системная эозинофилия, иногда в виде клинических признаков эозинофильной пневмонии или васкулита, соответствующих эозинофильному гранулематозу с полиангиитом, которые часто лечатся системными кортикостероидами. Эти события, как правило, но не всегда, могут быть связаны с сокращением приема ОКС. Врачи должны быть внимательны к васкулитной сыпи, ухудшающимся легочным симптомам, сердечным осложнениям и/или нейропатии, возникающим у их пациентов с эозинофилией. Сообщалось о случаях эозинофильной пневмонии и васкулита, соответствующих эозинофильному гранулематозу с полиангиитом, при применении препарата Дупиксент® у взрослых пациентов, которые участвовали в клиническом исследовании препарата при бронхиальной астме. Связь между применением препарата Дупиксент® и этими состояниями не была установлена.
Симптомы обострения бронхиальной астмы или ухудшающееся состояние
Препарат Дупиксент® не следует назначать для лечения симптомов остро возникшего ухудшения или обострений астмы. Препарат Дупиксент® не применяется для лечения острого бронхоспазма или астматического статуса.
Снижение дозы ГКС
Не следует резко прерывать применение системных, местных или ингаляционных ГКС после начала терапии препаратом Дупиксент®. Сокращение дозы ГКС при необходимости должно быть постепенным и выполняться под непосредственным наблюдением врача. Уменьшение дозы ГКС может сопровождаться системными симптомами отмены и/или манифестацией состояний, которые ранее не проявлялись из-за системной терапии ГКС.
Гельминтозы (глистные инвазии)
Пациенты с обнаруженным гельминтозом не включались в клинические исследования. Неизвестно, может ли препарат Дупиксент® повлиять на иммунный ответ при гельминтозах. Необходимо провести лечение пациентов с имеющимся гельминтозом перед тем, как начинать лечение препаратом Дупиксент®. Если во время лечения препаратом Дупиксент® пациент заражается гельминтозом, а антигельминтные препараты оказываются неэффективными, следует прекратить лечение препаратом Дупиксент® до излечения паразитарного заболевания.
Сопутствующие атопические заболевания
Пациентам с атопическим дерматитом и сопутствующей бронхиальной астмой следует рекомендовать не изменять своего лечения, не проконсультировавшись с лечащим врачом. Прекращая лечение препаратом Дупиксент®, следует принимать во внимание возможные эффекты на течение других атопических заболеваний.
Влияние на способность управлять транспортными средствами и механизмами. Препарат Дупиксент® не оказывает или оказывает незначительное влияние на способность управлять транспортными средствами и работать с другими механизмами.
Форма выпуска
Раствор для подкожного введения, 150 мг/мл, 175 мг/мл.
Для дозировки 150 мг/мл:
по 2,00 мл в одноразовом шприце/шприце с системой защиты из прозрачного стекла (тип I), снабженном несъемной иглой из нержавеющей стали, защищенной колпачком из мягкого эластомера с/без твердой крышкой(-и). По 1 или 2 шприца/шприца с системой защиты с инструкцией по применению в картонной пачке с заклеенными клапанами.
Или по 2 шприца/шприца с системой защиты в промежуточной картонной упаковке, по 3 промежуточных картонных упаковки в картонной пачке с заклеенными клапанами.
На каждую картонную пачку нанесен антиконтрафактный стикер.
Для дозировки 175 мг/мл:
по 1,14 мл в одноразовом шприце с системой защиты из прозрачного стекла (тип I), снабженном несъемной иглой из нержавеющей стали, защищенной колпачком из мягкого эластомера с/без твердой крышкой(-и). По 1 или 2 шприца с системой защиты в картонной пачке с заклеенными клапанами.
Или по 2 шприца с системой защиты в промежуточной картонной упаковке, по 3 промежуточных картонных упаковки в картонной пачке с заклеенными клапанами.
На каждую картонную пачку нанесен антиконтрафактный стикер.
Производитель
Санофи Винтроп Индустрия, Франция (150 мг/мл, 175 мг/мл; шприцы, шприцы с системой защиты).
Кук Фармика ЛЛС, США (150 мг/мл; шприцы).
Фасовщик (первичная упаковка):
Санофи Винтроп Индустрия, Франция (150 мг/мл, 175 мг/мл; шприцы, шприцы с системой защиты).
Кук Фармика ЛЛС, США (150 мг/мл; шприцы).
Упаковщик (вторичная (потребительская) упаковка):
Санофи Винтроп Индустрия, Франция (150 мг/мл, 175 мг/мл; шприцы, шприцы с системой защиты).
Кук Фармика ЛЛС, США (150 мг/мл; шприцы).
ЗАО «Санофи-Авентис Восток», 302516, Россия, Орловская область, Орловский район, с/п Большекуликовское, ул. Ливенская, 1.
Выпускающий контроль качества:
Санофи-Авентис Дойчланд ГмбХ, Германия (150 мг/мл, 175 мг/мл; шприцы, шприцы с системой защиты). Sanofi-Aventis Deutschland GmbH, Germany. Industriepark Hoechst — Brueningstrasse 50 H500, H590, H600 65926 Frankfurt am Main, Germany.
Санофи Винтроп Индустрия, Франция (150 мг/мл, 175 мг/мл; шприцы, шприцы с системой защиты). Sanofi Winthrop Industrie, France. 1051 boulevard Industriel 76580 Le Trait, France.
ЗАО «Санофи-Авентис Восток», 302516, Россия, Орловская область, Орловский район, с/п Большекуликовское, ул. Ливенская, 1.
Юридическое лицо, на имя которого выдано регистрационное удостоверение: АО Санофи-авентис груп, Франция.
Претензии потребителей направлять по адресу в России: АО «Санофи Россия», 125009, Москва, ул. Тверская, 22.
Телефон: (495) 721-14-00; факс: (495) 721-14-11.
Условия отпуска из аптек
По рецепту.
Условия хранения
При температуре 2–8 °C, в оригинальной упаковке для защиты от света.
(не замораживать)
Хранить в недоступном для детей месте.
Срок годности
36 мес.
Не применять по истечении срока годности, указанного на упаковке.
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
Дупиксент® (Dupixent) инструкция по применению
📜 Инструкция по применению Дупиксент®
💊 Состав препарата Дупиксент®
✅ Применение препарата Дупиксент®
📅 Условия хранения Дупиксент®
⏳ Срок годности Дупиксент®
Описание лекарственного препарата
Дупиксент®
(Dupixent)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для печатного издания справочника Видаль 2022 года.
Дата обновления: 2021.12.10
Владелец регистрационного удостоверения:
Контакты для обращений:
САНОФИ
Лекарственные формы
| Дупиксент® |
Р-р д/п/к введения 150 мг/1 мл: шприцы 2 мл 1, 2 или 6 шт. рег. №: ЛП-005440 |
|
|
Р-р д/п/к введения 175 мг/1 мл: шприцы 1.14 мл 1, 2 или 6 шт. рег. №: ЛП-005440 |
Форма выпуска, упаковка и состав
препарата Дупиксент®
Раствор для п/к введения прозрачный или слегка опалесцирующий, бесцветный или желтоватого цвета.
Вспомогательные вещества: L-гистидин и L-гистидина гидрохлорида моногидрат — 3.1 мгc, L-аргинина гидрохлорид — 4.35 мгd, натрия ацетата тригидрат и уксусная кислота ледяная — 0.75 мгf, сахароза — 50 мгg, полисорбат 80 — 2 мгh, вода д/и — до 1 мл.
2 мл — шприцы одноразовые (1) — пачки картонные с заклеенными клапанами×.
2 мл — шприцы одноразовые (2) — пачки картонные с заклеенными клапанами×.
2 мл — шприцы одноразовые (2) — упаковки картонные промежуточные (3) — пачки картонные с заклеенными клапанами×.
2 мл — шприцы с системой защиты из прозрачного стекла (тип I) (1) — пачки картонные с заклеенными клапанами×.
2 мл — шприцы с системой защиты из прозрачного стекла (тип I) (2) — пачки картонные с заклеенными клапанами×.
2 мл — шприцы с системой защиты из прозрачного стекла (тип I) (2) — упаковки картонные промежуточные (3) — пачки картонные с заклеенными клапанами×.
Раствор для п/к введения прозрачный или слегка опалесцирующий, бесцветный или желтоватого цвета.
Вспомогательные вещества: L-гистидин и L-гистидина гидрохлорида моногидрат — 3.1 мгc, L-аргинина гидрохлорид — 10.51 мгe, натрия ацетата тригидрат и уксусная кислота ледяная — 0.75 мгf, сахароза — 49.88 мгg, полисорбат 80 — 2 мгh, вода д/и — до 1 мл.
1.14 мл — шприцы одноразовые с системой защиты из прозрачного стекла (тип I) (1) — пачки картонные с заклеенными клапанами×.
1.14 мл — шприцы одноразовые с системой защиты из прозрачного стекла (тип I) (2) — пачки картонные с заклеенными клапанами×.
1.14 мл — шприцы одноразовые с системой защиты из прозрачного стекла (тип I) (2) — упаковки картонные промежуточные (3) — пачки картонные с заклеенными клапанами×.
× На каждую пачку картонную нанесен антиконтрафактный стикер.
a В расчете на 2 мл препарата.
b В расчете на 1.14 мл препарата.
c Содержание L-гистидина и L-гистидина гидрохлорида приведено в пересчете на L-гистидин (М=155.16 г/моль), исходя из общей концентрации гистидина в препарате 20 мМ.
d Содержание L-аргинина гидрохлорида приведено в пересчете на L-аргинин (М=174,2 г/моль), исходя из молярной концентрации L-аргинина в препарате 25 мМ. Номинальное содержание L-аргинина гидрохлорида (М=210.66 г/моль) в одном шприце составляет 10.5 мг.
e Содержание L-аргинина гидрохлорида приведено в пересчете на L-аргинин (М=174.2 г/моль), исходя из молярной концентрации L-аргинина в препарате 50 мМ. Номинальное содержание L-аргинина гидрохлорида (М=210.66 г/моль) в одном шприце составляет 9.93 мг.
f Содержание натрия ацетата тригидрата и уксусной кислоты ледяной приведено, исходя из общей концентрации ацетат иона в препарате 12.5 мМ.
g Содержание сахарозы приведено в пересчете на миллиграммы, исходя из масса-объемной концентрации сахарозы в препарате 5%.
h Содержание полисорбата 80 приведено в пересчете на миллиграммы, исходя из масса-объемной концентрации полисорбата 80 в препарате 0.2%.
Фармакологическое действие
Механизм действия
Препарат Дупиксент® является рекомбинантным человеческим моноклональным антителом (IgG4), которое блокирует передачу сигналов интерлейкина-4 (ИЛ-4) и интерлейкина-13 (ИЛ-13) путем специфического связывания с IL-4Rα-субъединицей, общей для рецепторных комплексов ИЛ-4 и ИЛ-13. Препарат Дупиксент® блокирует передачу сигналов ИЛ-4 через рецепторы I типа (IL-4Rα/γc) и общую передачу сигналов ИЛ-4 и ИЛ-13 через рецепторы II типа (IL-4Rα/IL-13Rα). ИЛ-4 и ИЛ-13 являются ключевыми цитокинами воспаления 2 типа (в т.ч. продуцируемые и Th2-лимфоцитами), вовлеченными в патогенез атопических заболеваний.
Воспаление 2 типа играет важную роль в патогенезе многих атопических заболеваний, включая бронхиальную астму, способствует ограничению воздушного потока и увеличивает риск обострений. ИЛ-4 и ИЛ-13 выступают в качестве основных факторов воспаления 2 типа, активируя множественные типы клеток (например, тучные клетки, лимфоциты, эозинофилы, нейтрофилы, макрофаги) и индуцируя множественные медиаторы (например, иммуноглобулин Е, гистамин, эйкозаноиды, лейкотриены, хемокины и цитокины, включая эотаксин/CCL11, TARC/CCL17 и ИЛ-5), участвующие в воспалении 2 типа. Блокирование пути передачи сигналов ИЛ-4/ИЛ-13 дупилумабом у пациентов снижает концентрации многих из этих маркеров воспаления 2 типа, включая иммуноглобулин Е, периостин и множественные провоспалительные цитокины и хемокины (например, эотаксин, TARC), а также снижает уровень фракции оксида азота в выдыхаемом воздухе (FeNO) — маркер воспаления в легких. Было показано, что блокирование пути передачи сигналов ИЛ-4/ИЛ-13 дупилумабом в гуманизированных моделях животных предотвращает последующие действия этих цитокинов и хемокинов, в т.ч. гиперплазию бокаловидных клеток, гиперреактивность гладкомышечных клеток дыхательных путей, эозинофильное воспаление в легких, другие воспалительные процессы в легких, а также предотвращает нарушение функции легких; при этом снижение выраженности эозинофильного воспаления в легких происходит независимо от нормального или повышенного уровня эозинофилов в крови.
Дупилумаб производится с помощью технологии рекомбинантной ДНК в суспензионной культуре клеток яичника китайского хомячка.
Дупилумаб имеет молекулярную массу приблизительно 147 кДа.
Фармакодинамика
Атопический дерматит
В клинических исследованиях лечение препаратом Дупиксент® приводило к снижению в сыворотке крови концентраций биомаркеров, связанных с цитокинами воспаления 2 типа, таких как тимус-ассоциированного регуляторного хемокина (TARC/CCL17), общего сывороточного иммуноглобулина Е и аллерген-специфического иммуноглобулина Е. Также наблюдалось снижение активности ЛДГ, биомаркера, связанного со степенью тяжести атопического дерматита и его активностью. Препарат Дупиксент® уже в начале 2-й недели лечения вызывал супрессию хемокина TARC по сравнению с плацебо, с тенденцией продолжения его снижения до максимальной и устойчивой супрессии к 12-й неделе лечения.
У пациентов, получавших препарат Дупиксент® в дозе 300 мг 1 раз в 2 недели и в дозе 300 мг 1 раз в неделю, общий сывороточный иммуноглобулин Е к 52-й неделе терапии снизился на -74.8% и -73.9% (медиана изменения по сравнению с исходным уровнем), соответственно, по сравнению с -0% в группе плацебо. Аналогичные тенденции наблюдались в отношении антиген-специфических иммуноглобулинов Е, в т.ч. энтеротоксина А, специфического для золотистого стафилококка (S. aureus), аллергенов трав и деревьев.
Бронхиальная астма
В соответствии с ингибированием передачи сигналов ИЛ-4 и ИЛ-13, лечение дупилумабом заметно уменьшало уровень FeNO и концентрации эотаксина-3, общего иммуноглобулина Е, аллерген-специфического иммуноглобулина Е, TARC и периостина у пациентов с бронхиальной астмой по сравнению с плацебо. Эти снижения уровней биомаркеров воспаления были сопоставимы для режимов дозирования 200 мг 1 раз в 2 недели и 300 мг 1 раз в 2 недели и были близки к максимальному подавлению через 2 недели лечения, за исключением иммуноглобулина Е, который уменьшался медленнее. Описанные эффекты были устойчивыми во время лечения.
Хронический полипозный риносинусит
У участников исследований с хроническим полипозным риносинуситом (ХПРС) на фоне лечения дупилумабом также наблюдалось снижение в моче уровня лейкотриена 4 (LTE4), маркера, связанного с активацией тучных клеток, базофилов и эозинофилов.
Клиническая эффективность
Атопический дерматит
Эффективность и безопасность препарата Дупиксент® в монотерапии или в сочетании с топическими ГКС оценивали в трех основных рандомизированных, двойных слепых, плацебо-контролируемых исследованиях (SOLO1, SOLO2 и CHRONOS) с участием 2119 пациентов в возрасте 18 лет и старше со среднетяжелым и тяжелым течением атопического дерматита.
16-недельные исследования монотерапии (SOLO1 и SOLO2)
Показателя общей оценки исследователя (IGA) 0 или 1 («чистая» или «почти чистая кожа») к 16-й неделе лечения в клиническом исследовании SOLO1 достигли 37.9% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 недели, и 37.2% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в неделю, против 10.3% пациентов в группе плацебо, а в исследовании SOLO2 — 36.1% и 36.4% против 8.5% пациентов соответственно.
Улучшение не менее чем на 75% от исходного значения по индексу тяжести и площади экземы (EASI-75) к 16-й неделе лечения в исследовании SOLO1 достигли 51.3% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 недели, и 52.5% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в неделю, против 14.7% пациентов в группе плацебо, а в исследовании SOLO2 — 44.2% и 48.1% против 11.9% соответственно.
Не менее чем 4-бального уменьшения зуда по пиковым значениям числовой шкалы оценки выраженности зуда NRS к 16-й неделе лечения в исследовании SOLO1 достигли 40.8% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 недели, и 40.3% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в неделю, против 12.3% пациентов в группе плацебо, а в исследовании SOLO2 — 36.0% и 39.0% пациентов против 9.5% соответственно. Значительно больший процент пациентов, получавших Дупиксент®, достигал быстрого улучшения по шкале оценки тяжести зуда NRS по сравнению с пациентами в группе плацебо (определяемого как ≥4-балльное улучшение уже на 2-й неделе), причем процент пациентов, у которых наблюдалось уменьшение тяжести зуда по шкале NRS, продолжал увеличиваться в течение всего периода лечения.
Эффекты лечения в подгруппах (с распределением на подгруппы по массе тела, возрасту, полу, расе и сопутствующей терапии, в т.ч. с применением иммунодепрессантов) в исследованиях SOLO1 и SOLO2 в целом согласуются с результатами, полученными в общей исследуемой популяции.
52-недельное клиническое исследование с одновременным применением топических ГКС (CHRONOS)
IGA 0 или 1 к 16-й неделе лечения достигли 38.7% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 недели + топические ГКС, и 39.2% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в неделю + топические ГКС, против 12.4% пациентов в группе плацебо, а к 52-й неделе — 36.0% и 40.0% против 12.5% пациентов соответственно.
EASI-75 к 16-й неделе лечения достигли 68.9% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 недели + топические ГКС, и 63.9% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в неделю + топические ГКС, против 23.2% пациентов в группе плацебо + топические ГКС, а к 52-й неделе — 65.2% и 64.1% против 21.6% пациентов соответственно.
Не менее чем 4-бального улучшения по шкале тяжести зуда NRS к 16-й неделе лечения достигли 58.8% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 недели + топические ГКС, и 50.8% пациентов, получавших препарат Дупиксент® в дозе 300 мг 1 раз в неделю + топические ГКС, против 19.7% пациентов в группе плацебо + топические ГКС, а к 52-й неделе — 51.2% и 39.0% против 12.9% пациентов соответственно. Более значительный процент пациентов, получавших препарат Дупиксент® + топические ГКС, достигал быстрого улучшения по шкале тяжести зуда NRS по сравнению с пациентами в группе плацебо + топические ГКС (определяемого как > 4-балльное улучшение уже на 2-й неделе; р <0.05), причем доля пациентов, у которых наблюдалось уменьшение тяжести зуда по шкале NRS, продолжала увеличиваться в течение всего периода лечения.
Эффекты лечения в подгруппах (с распределением по массе тела, возрасту, полу, расе и сопутствующей терапии, в т.ч. с применением иммунодепрессантов) в исследовании CHRONOS в целом согласуются с результатами, полученными в общей исследуемой популяции.
Клиническая эффективность у пациентов, которым не рекомендовалось лечение циклоспорином
У пациентов, которым не рекомендовалось лечение циклоспорином или оно было неэффективно, монотерапия препаратом Дупиксент® в обеих группах лечения, приводила к значительному улучшению признаков и симптомов атопического дерматита по сравнению с плацебо. Больший процент пациентов, получавших Дупиксент®, по сравнению с группой плацебо достигал IGA 0 или 1 и снижения по сравнению с исходным значением на ≥2 балла к 16-й неделе (29.5% против 6.8%), EASI-75 к 16-й неделе (38% против 11.4%), а также снижения не менее чем на 4 балла индекса тяжести зуда от исходного значения к 16-й неделе (34.9% по сравнению с 8%) (р <0.001 для всех 3 конечных точек). Аналогичные результаты наблюдались у пациентов, получавших Дупиксент® одновременно с топическими ГКС. Эффективность комбинации препарата Дупиксент® + топические ГКС сохранялась до 52-й недели терапии.
Подростки в возрасте от 12 до 17 лет
Эффективность и безопасность применения препарата Дупиксент® в монотерапии у пациентов оценивалась в мультицентровом, рандомизированном, двойном-слепом, плацебо-контролируемом исследовании (AD-1536) с участием 251 пациента в возрасте от 12 до 17 лет с атопическим дерматитом среднетяжелого и тяжелого течения. Соответствующие пациенты, включенные в данное исследование, продемонстрировали неадекватный ответ на предварительную терапию топическими препаратами.
Пациенты получали: начальную дозу 400 мг препарата Дупиксент® (2 инъекции по 200 мг) с последующим введением 200 мг каждые 2 недели для пациентов с базовой массой тела менее 60 кг или начальную дозу препарата Дупиксент® 600 мг (2 инъекции по 300 мг) с последующим введением 300 мг каждые 2 недели для пациентов с базовой массой тела более 60 кг; либо начальную дозу препарата Дупиксент® 600 мг (2 инъекции по 300 мг) с последующим введением 300 мг каждые 4 недели независимо от массы тела; либо плацебо.
Дупиксент® вводят п/к. При необходимости контролировать недопустимые симптомы пациентам разрешалось получать скоропомощное лечение по решению исследователя. Пациенты, которые получали такое лечение, были оценены как не отвечающие на терапию препаратом Дупиксент®.
В данном исследовании средний возраст пациентов составлял 14.5 лет, средний вес 59.4 кг, 41.0% пациентов были женщины, 62.5% белокожие, 15.1% азиаты и 12.0% темнокожие. В целом, 92.0% пациентов имели как минимум одно коморбидное аллергическое состояние; у 65.5% пациентов наблюдался аллергический ринит; у 53.6% пациентов была бронхиальная астма и у 68% пациентов наблюдалась пищевая аллергия.
Клинический ответ
Показателя общей оценки исследователя (IGA) 0 или 1 («чистая» или «почти чистая кожа») к 16-й неделе лечения в исследовании AD-1526 достигли 24.4% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 недели (≥ 60 кг) или 200 мг 1 раз в 2 недели (< 60 кг) против 2.4% пациентов в группе плацебо.
Улучшение не менее чем на 75% от исходного значения по индексу тяжести и площади экземы (EASI-75) к 16-й неделе достигли 41.5% пациентов, получавших Дупиксент® против 8.2% пациентов в группе плацебо.
Не менее чем 4-бального уменьшения зуда по пиковым значениям числовой шкалы оценки выраженности зуда (NRS) к 16-й неделе лечения в исследовании достигли 36,6 % пациентов, получавших Дупиксент®, против 4.8% пациентов в группе плацебо. Значительно больший процент пациентов, получавших Дупиксент®, достигал быстрого улучшения по шкале оценки тяжести зуда NRS по сравнению с пациентами в группе плацебо (определяемого как ≥ 4-балльное улучшение уже на 2-й неделе), причем процент пациентов, у которых наблюдалось уменьшение тяжести зуда по шкале NRS, продолжал увеличиваться в течение всего периода лечения.
Значительно большее соотношение пациентов, рандомизированных на терапию препаратом Дупиксент®, достигли быстрого улучшения по шкале оценки выраженности зуда (NRS) по сравнению с плацебо (улучшение более чем в 4 раза уже на 4-й неделе; номинальное значение p <0.001) и доля пациентов, ответивших на терапию по шкале NRS, наблюдалась в сочетании с улучшением объективных признаков атопического дерматита.
Долгосрочные исследования эффективности терапии препаратом Дупиксент® у пациентов подросткового возраста с атопическим дерматитом среднетяжелого и тяжелого течения, которые принимали участие в предыдущих клинических исследованиях препарата Дупиксент®, были оценены в открытом продолженном исследовании (AD-1434). Данные в отношении эффективности, полученные в данном исследовании, предполагают, что клиническое преимущество, полученное на 16-й неделе терапии, является стабильным в течение 52 недель терапии.
Дети в возрасте от 6 до 11 лет
Эффективность и безопасность применения препарата Дупиксент® у пациентов детского возраста в сочетании с топическими ГКС изучалась в многоцентровом рандомизированном двойном слепом плацебо-контролируемом исследовании (AD-1652) с участием 367 пациентов в возрасте от 6 до 11 лет с атопическим дерматитом, характеризующимся значениями IGA ≥4 (по шкале от 0 до 4), EASI ≥21 (по шкале от 0 до 72), а также минимальной пораженной площади поверхности тела ≥15%. У подходящих пациентов, включенных в это исследование, ранее наблюдался недостаточный ответ на топические препараты. Пациентов стратифицировали в зависимости от массы тела на исходном уровне (<30 кг, ≥30 кг).
Пациенты в группе, получавшей препарат Дупиксент® 1 раз в 2 недели + топические ГКС с исходной массой тела <30 кг получали начальную дозу препарата 200 мг/сут и затем по 100 мг 1 раз в 2 недели со 2 по 14 неделю, а пациенты с исходной массой тела ≥30 кг получали первоначальную дозу препарата Дупиксент® 400 мг/сут и затем 200 мг 1 раз в 2 недели со 2 по 14 неделю. Пациенты в группе, получавшей препарат Дупиксент® 1 раз в 4 недели + топические ГКС получали первоначальную дозу препарата 600 мг/сут и затем 300 мг 1 раз в 4 недели с 4 по 12 неделю, независимо от массы тела. Пациентам было разрешено получать резервную терапию по усмотрению исследователя. Пациенты, получавшие резервную терапию, расценивались как не отвечающие на терапию препаратом Дупиксент®.
В данном исследовании средний возраст составлял 8.5 лет, средняя масса тела 29.8 кг, 50.1% пациентов были женского пола, 69.2% были белыми, 16.9% были темнокожими и 7.6% были азиатами.
В целом, 91.7% пациентов имели как минимум одно коморбидное аллергическое состояние; у 64.4% наблюдалась пищевая аллергия, у 62.7% – другие виды аллергии, у 60.2% наблюдался аллергический ринит, у 46.7% пациентов наблюдалась бронхиальная астма.
Клинический ответ
Показателя общей оценки исследователя (IGA) 0 или 1 («чистая» или «почти чистая кожа») к 16-й неделе лечения в исследовании AD-1652 достигли 29.5% пациентов c массой тела менее 30 кг, получавших Дупиксент® в дозе 300 мг 1 раз в 4 недели, против 13.1% в группе плацебо; 39.0% пациентов с массой тела 30 и более кг, получавших Дупиксент® в дозе 200 мг 1 раз в 2 недели, против 9.7% в группе плацебо.
Улучшение не менее чем на 75% от исходного значения по индексу тяжести и площади экземы (EASI-75) к 16-й неделе лечения в исследовании AD-1652 достигли 75.4% пациентов c массой тела менее 30 кг, получавших Дупиксент® в дозе 300 мг 1 раз в 4 недели, против 27.9% в группе плацебо; 74.6% пациентов с массой тела 30 и более кг, получавших Дупиксент® в дозе 200 мг 1 раз в 2 недели, против 25.8% в группе плацебо.
Не менее чем 4-бального уменьшения зуда по пиковым значениям числовой шкалы оценки выраженности зуда (NRS) к 16-й неделе лечения в исследовании AD-1652 достигли 54.1% пациентов c массой тела менее 30 кг, получавших Дупиксент® в дозе 300 мг 1 раз в 4 недели, против 11.7% в группе плацебо; 61.4% пациентов с массой тела 30 и более кг, получавших Дупиксент® в дозе 200 мг 1 раз в 2 недели, против 12.9% в группе плацебо.
Значительно больший процент пациентов, получавших Дупиксент®, достигал быстрого улучшения по шкале оценки тяжести зуда NRS по сравнению с пациентами в группе плацебо (определяемого как ≥ 4-балльное улучшение уже на 2-й неделе), причем процент пациентов, у которых наблюдалось уменьшение тяжести зуда по шкале NRS, продолжал увеличиваться в течение всего периода лечения.
Значительно больший процент пациентов, рандомизированных на терапию препаратом Дупиксент® в сочетании с топическими ГКС, достиг быстрого улучшения по шкале оценки выраженности зуда (NRS) по сравнению с плацебо (улучшение ≥4 балла на 4-й неделе).
Долгосрочная эффективность терапии препаратом Дупиксент® в сочетании с топическими ГКС у пациентов детского возраста с атопическим дерматитом, которые принимали участие в предшествующих клинических исследованиях препарата Дупиксент® в сочетании с топическими ГКС изучалась в продолженном открытом исследовании (AD-1434). Данные по эффективности из этого исследования позволяют предположить, что клиническое улучшение, наблюдавшееся на 16 неделе, сохранялось в течение 52 недель терапии включительно.
Бронхиальная астма
Было проведено три рандомизированных, двойных слепых, плацебо-контролируемых, многоцентровых исследования в параллельных группах (DRI12544, QUEST и VENTURE) продолжительностью от 24 до 52 недель с участием 2888 пациентов (в возрасте 12 лет и старше). Во все три исследования пациенты были включены независимо от минимального исходного уровня эозинофилов или другого биомаркера воспаления 2 типа (например, уровня FeNO или иммуноглобулина Е).
Обострения бронхиальной астмы
В исследованиях DRI12544, QUEST и VENTURE оценивали частоту тяжелых обострений астмы независимо от минимального количества эозинофилов или любых других биомаркеров воспаления 2 типа (например, FeNO или иммуноглобулин Е) в начале исследования. В общей популяции, независимо от содержания эозинофилов и других биомаркеров воспаления 2 типа, у пациентов, получавших 200 или 300 мг препарата Дупиксент® 1 раз в 2 недели, произошло значительное снижение частоты тяжелых обострений астмы по сравнению с группой плацебо. В исследованиях DRI12544 и QUEST частота тяжелых обострений при применении препарата Дупиксент® в дозе 200 мг 1 раз в 2 недели снижалась на 70% и 48%; а при применении в дозе 300 мг 1 раз в 2 недели — на 70% и 46% соответственно; и на 59% в исследовании VENTURE.
В объединенном анализе исследований DRI12544 и QUEST частота тяжелых обострений, приводящих к госпитализации и/или посещениям отделений неотложной помощи, снизилась на 25.5% и 46.9% при применении препарата Дупиксент® в дозах 200 мг или 300 мг 1 раз в 2 недели соответственно.
Кумулятивное среднее число тяжелых обострений было более низкое у пациентов, получавших препарат Дупиксент® по сравнению с плацебо в исследованиях DRI12544, QUEST и VENTURE (в общей популяции и в популяции с исходным числом эозинофилов ≥150 клеток/мкл или FeNO ≥25 ppb) в течение 24- или 52-недельного периода лечения в обеих группах режимов дозирования препарата.
В исследовании QUEST у пациентов, получавших ингаляционные ГКС в средней дозе, наблюдалось сходное снижение частоты тяжелых обострений астмы по сравнению с пациентами, получавшими ингаляционные ГКС в высокой дозе.
Функция легких
Клинически значимое увеличение предбронходилатационного значения объема форсированного выдоха за 1-ю секунду (ОФВ1) наблюдалось на 12-й неделе в общей популяции независимо от уровня эозинофилов или других биомаркеров воспаления 2 типа (например, FeNO или иммуноглобулин Е). В исследованиях DRI12544, QUEST и VENTURE, по сравнению с плацебо, большее улучшение ОФВ1 наблюдалось также у пациентов с FeNO ≥25 ppb. Улучшение ОФВ1 было одинаковым, независимо от того, получали ли пациенты ингаляционные ГКС в средней дозе, ингаляционные ГКС в высокой дозе или пероральные ГКС.
Значительные улучшения ОФВ1 наблюдались уже в течение второй недели (DRI12544, QUEST и VENTURE) после первой инъекции препарата Дупиксент® в дозе как 200 мг, так и 300 мг и сохранялись в течение 24 недель (DRI12544 и VENTURE) и 52 недель (QUEST).
Скорректированная средняя разность абсолютных значений ОФВ1 была 0.20 л и 0.14 л в группах, получавших Дупиксент® 200 мг 1 раз в 2 недели, по сравнению с плацебо; 0.16 и 0.13 л в группах, получавших 300 мг 1 раз в 2 недели по сравнению с плацебо, соответственно в исследованиях DRI12544 и QUEST. Соответствующее процентное изменение ОФВ1 составляло от 9.2 до 11.9% для дозы 200 мг 1 раз в 2 недели и от 9.4 до 11.7% для дозы 300 мг 1 раз в 2 недели. Скорректированная средняя разность абсолютных значений пре-бронходилатационного ОФВ1 от исходного уровня к 24-й неделе (достаточное время для достижения максимального снижения дозы пероральных ГКС) в исследовании VENTURE составила 0.22 л в группе применения препарата Дупиксент® по сравнению с плацебо, что соответствовало улучшению на 15.1% по сравнению с исходным уровнем.
Кроме того, у пациентов, получавших препарат Дупиксент®, значительно улучшился постбронходилатационный показатель ОФВ1 по сравнению с исходным уровнем на 12-й и 52-й неделях по сравнению с плацебо, что указывает на то, что препарат Дупиксент® улучшает фиксированную обструкцию дыхательных путей. В группе применения препарата Дупиксент® в течение года наблюдения не было зарегистрировано снижения функции легких с учетом значения постбронходилатационного значения ОФВ1.
Снижение дозы пероральных ГКС
В исследовании VENTURE оценивалось влияние препарата Дупиксент® на снижение применения поддерживающих пероральных ГКС. Исходная средняя доза пероральных кортикостероидов составляла 11.75 мг в группе плацебо и 10.75 мг в группе, получавшей препарат Дупиксент®. По сравнению с плацебо, у пациентов, получавших Дупиксент®, отмечалось большее снижение ежедневной дозы пероральных ГКС при сохранении контроля над астмой. Среднее общее снижение ежедневной дозы пероральных ГКС при сохранении контроля над астмой составляло 70.1% по сравнению с исходным уровнем у пациентов, получавших Дупиксент® и 41.9% в группе плацебо.
Исходы, сообщаемые пациентами
Кроме того, во всех 3 исследованиях Дупиксент® обеспечил клинически значимое улучшение показателей контроля бронхиальной астмы в общей популяции по сравнению с группой плацебо, о чем свидетельствуют показатели ACQ-5 и соответствующее улучшение качества жизни, измеренное по шкале AQLQ(S). Улучшение показателей ACQ-5 и AQLQ(S) были зарегистрированы уже через 2 недели, и это улучшение сохранялось на протяжении 24 недель в исследовании DRI12544 и 52 недель в исследовании QUEST. В общей популяции исследования QUEST доля пациентов, ответивших на лечение, что выражалось в достижении минимального клинически значимого различия показателей ACQ-5 и AQLQ(S), была существенно выше к 52-й неделе в группе, получавшей обе дозы препарата Дупиксент®.
Долгосрочное продленное исследование (TRAVERSE)
Долгосрочную эффективность препарата Дупиксент® у 2282 взрослых и подростков со среднетяжелой и тяжелой бронхиальной астмой, и у взрослых пациентов с гормонозависимой астмой, которые принимали участие в предыдущих клинических исследованиях препарата Дупиксент®, оценивали в рамках открытого продленного исследования (TRAVERSE). В данном исследовании препарата Дупиксент® улучшение клинических показателей, в т.ч. снижение количества обострений и улучшение функции легких, сохранялось в течение 96 недель. У пациентов с гормонозависимой астмой, несмотря на продолжающееся снижение или отмену пероральных ГКС, отмечалось снижение количества обострений и устойчивое улучшение функции легких в течение 96 недель.
Частота тяжелых обострений в течение 96 недель составила 0.3 и 0.27; а улучшение ОФВ1 от исходного значения — 0.33 л (21.1%) и 0.42 л (27.3%) у пациентов с уровнем эозинофилов в крови ≥150 клеток/мкл и ≥300 клеток/мкл соответственно. Аналогичное сохранение эффекта наблюдалось и по параметрам ACQ-5 и AQLQ(S). Аналогичные результаты отмечались и в подгруппе пациентов, получавших высокие дозы ингаляционных кортикостероидов.
Хронический полипозный риносинусит
Программа клинических исследований применения препарата при ХПРС включала два рандомизированных двойных слепых многоцентровых плацебо-контролируемых исследования в параллельных группах (SINUS-24 и SINUS-52) с участием 724 пациентов в возрасте 18 лет и старше, получающих базисную терапию интраназальными кортикостероидами. Эти исследования включали пациентов с тяжелым течением ХПРС, несмотря на ранее проведенное хирургическое вмешательство на придаточных пазухах носа или лечение системными кортикостероидами на протяжении последних 2 лет. В ходе исследования было разрешено лечение системными кортикостероидами или хирургическое вмешательство по решению исследователя. В исследовании SINUS-24 в общей сложности 276 пациентов были рандомизированы либо в группу Дупиксент® 300 мг (n=143), либо в группу плацебо (n=133), инъекции осуществляли 1 раз в 2 недели на протяжении 24 недель. В исследовании SINUS-52 в общей сложности 448 пациентов были рандомизированы либо в группу препарата Дупиксент® 300 мг 1 раз в 2 недели на протяжении 52 недель (n=150), либо в группу препарата Дупиксент® 300 мг 1 раз в 2 недели на протяжении 24 недель, а затем 300 мг 1 раз в 4 недели до недели 52 (n=145), либо в группу плацебо (n=153). При компьютерной томографии у всех пациентов было выявлено снижение пневматизации придаточных пазух носа, оценка проводилась по шкале Лунда-Маккея (ШЛМ) при компьютерной томографии придаточных пазух носа, при этом у 73-90% пациентов отмечалось снижение пневматизации всех придаточных пазух носа. Пациенты были стратифицированы в зависимости от наличия в анамнезе хирургических вмешательств и бронхиальной астмы/аспирин-индуцированного респираторного заболевания (АИРЗ, аспириновой астмы). Хирургическое вмешательство на придаточных пазух носа ранее выполнялось у 63% пациентов, в среднем 2.0 хирургических вмешательства, 74% участников на протяжении последних 2 лет получали системные кортикостероиды, среднее количество курсов за последние 2 года составляло 1.6. У 59% пациентов имелась сопутствующая бронхиальная астма, а у 28% — АИРЗ.
Комбинированными первичными конечными точками было изменение балла выраженности полипоза при эндоскопической риноскопии (по шкале NPS от 0 до 8 баллов) относительно исходного уровня к 24-й неделе (централизованная маскированная оценка результатов), а также изменение балла заложенности носа/назальной обструкции относительно исходного уровня к 24-й неделе (усредненный балл за 28 дней, шкала NC от 0 до 3 баллов), определяемое самим пациентом на основании ежедневных записей в дневнике. В обоих исследованиях вторичные конечные точки на 24 неделе включали изменения по сравнению с исходным уровнем таких показателей, как: балл по ШЛМ, оцененный при компьютерной томографии придаточных пазух носа (КТ ППН), количественная оценка выраженности симптомов (TSS), тест на идентификацию запахов Пенсильванского университета (UPSIT), ежедневная оценка снижения обоняния и опросник для оценки исхода болезней носа и околоносовых пазух из 22 вопросов (SNOT-22). Была выполнена обобщающая результаты двух исследований оценка уменьшения доли пациентов, которым не требовалось неотложное применение курсов системных кортикостероидов и/или хирургических вмешательств на придаточных пазухах носа, а также улучшения показателя ОФВ1 в подгруппе пациентов с бронхиальной астмой. Статистически и клинически значимая эффективность наблюдалась в отношении улучшения выраженности полипоза носа по шкале NPS на 24 неделе в SINUS-24 (скорректированная средняя разность -2.06 по сравнению с группой плацебо) и в SINUS-52 на 24 и 52 неделе с дальнейшим прогрессивным улучшением (скорректированная средняя разность -1.8 и -2.4 по сравнению с группой плацебо при терапии препаратом Дупиксент® 300 мг 1 раз в 2 недели, соответственно на 24 и 52 неделях). У пациентов, получавших препарат Дупиксент®, отмечалось значимое снижение заложенности носа/назальной обструкции по сравнению с плацебо на 24 неделе в SINUS-24 (скорректированная средняя разность -0.89 по сравнению с группой плацебо) и на 24 и 52 неделе в SINUS-52 (скорректированная средняя разность -0,87 и -0.98 по сравнению с группой плацебо при терапии препаратом Дупиксент® 300 мг 1 раз в 2 недели, соответственно на 24 и 52 неделях). В обоих исследованиях значимое улучшение в отношении заложенности носа/назальной обструкции относительно исходного уровня по шкале NC и ежедневной оценки снижения обоняния отмечалось уже при первой оценке на 4 неделе. Значимое снижение балла по ШЛМ, оцененного при КТ ППН, наблюдалось на 24 неделе в SINUS-24 (скорректированная средняя разность -7.44 по сравнению с группой плацебо) и в SINUS-52 на 24 неделе с дальнейшим улучшением к 52 неделе (скорректированная средняя разность -5.13 и -6.94 по сравнению с группой плацебо при терапии препаратом Дупиксент® 300 мг 1 раз в 2 недели, соответственно на 24 и 52 неделях). Обобщающая результаты двух исследований оценка продемонстрировала снижение доли пациентов, которым не требовалось неотложное применение курсов системных кортикостероидов, на 74%, хирургических вмешательств на придаточных пазухах носа — на 83%, при применении препарата Дупиксент® по сравнению с плацебо. В подгруппе пациентов с сопутствующей бронхиальной астмой отмечалось значимое улучшение показателей предбронходилатационного ОФВ1 на 24 неделе терапии препаратом Дупиксент® вне зависимости от исходного уровня эозинофилов: скорректированная средняя разность от исходного уровня ОФВ1 на 24 неделе для дозы препарата Дупиксент® 300 мг 1 раз в 2 недели составила 0.14 л против -0.07 л в группе плацебо, разность 0.21 л. Эффективность в отношении первичных конечных точек — изменения балла выраженности полипоза по шкале NPS и изменение балла заложенности носа/назальной обструкции по шкале NC относительно исходного уровня к 24-й неделе — и ключевой вторичной конечной точки (балл по ШЛМ, оцененный при КТ ППН) в подгруппах пациентов с сопутствующей бронхиальной астмой или АИРЗ была схожей с общей популяцией пациентов с хроническим полипозным риносинуситом.
Фармакокинетика
Фармакокинетика дупилумаба аналогична у пациентов с атопическим дерматитом, бронхиальной астмой и хроническим полипозным риносинуситом.
Всасывание
После однократного п/к введения 75-600 мг дупилумаба медиана времени достижения Cmax в сыворотке крови (Tmax) составляла 3-7 дней. Абсолютная биодоступность дупилумаба после введения п/к дозы сходна между пациентами с атопическим дерматитом, бронхиальной астмой и хроническим полипозным риносинуситом и составляет 61-64% (установлена при популяционном фармакокинетическом анализе).
Введение однократной нагрузочной дозы в первый день приводит к быстрому достижению клинически эффективных концентраций в течение 2 недель.
При схеме лечения 200 мг или 300 мг 1 раз в 2 недели, начиная с нагрузочной дозы 400 мг или 600 мг, Css дупилумаба обычно достигаются в среднем к 16-й неделе лечения. В состоянии достижения Css средняя остаточная концентрация перед введением следующей дозы составляла 39 мг/л при применении 200 мг 1 раз в 2 недели и 70-80 мг/л при применении 300 мг 1 раз в 2 недели.
При еженедельном п/к введении 300 мг препарата Дупиксент®, начиная с нагрузочной дозы 600 мг, Css обычно достигаются в среднем после 13 недель лечения. В состоянии достижения Css средняя остаточная концентрация перед введением следующей дозы составляла 189 мг/л.
Линейность дозы
Из-за нелинейности клиренса системная экспозиция дупилумаба, определяемая по AUC, увеличивается быстрее, непропорционально увеличению дозы после однократного п/к введения препарата в дозах от 75 мг до 600 мг.
Распределение
Vd дупилумаба составляет приблизительно 4.6 л, что указывает на его распределение главным образом в сосудистой системе.
Метаболизм
Поскольку дупилумаб является белком, специальных исследований его метаболизма не проводилось. Предполагается, что дупилумаб расщепляется до низкомолекулярных пептидов и отдельных аминокислот.
Выведение
Выведение дупилумаба осуществляется параллельно линейными и нелинейными путями. При более высоких концентрациях выведение дупилумаба осуществляется главным образом через ненасыщаемый протеолитический путь, в то время как при более низких концентрациях выведение препарата преимущественно осуществляется через нелинейное насыщаемое связывание с мишенью IL-4Rα.
После введения последней дозы в состоянии равновесной концентрации медиана времени до неопределяемых концентраций дупилумаба, составляет 9 недель при введении 200 мг 1 раз в 2 недели, 10-12 недель при введении 300 мг 1 раз в 2 недели и 13 недель при введении 300 мг 1 раз в неделю.
Фармакокинетика у особых групп пациентов
Пол пациента не влиял на фармакокинетические показатели препарата Дупиксент®.
Возраст пациентов не влиял на фармакокинетические показатели препарата Дупиксент®.
Пациенты пожилого возраста. По данным популяционного анализа фармакокинетических показателей возраст пациентов не влиял на эффективность и безопасность препарата Дупиксент®.
Пациенты детского возраста. Безопасность и эффективность препарата Дупиксент® были установлены у пациентов в возрасте 6 лет и старше со среднетяжелым и тяжелым атопическим дерматитом. Безопасность и эффективность у детей, подростков и взрослых были сопоставимы. Безопасность и эффективность у детей в возрасте младше 6 лет с атопическим дерматитом не изучена.
Бронхиальная астма. Долгосрочную безопасность и эффективность препарата Дупиксент® оценивали у 89 пациентов подросткового возраста со среднетяжелой и тяжелой бронхиальной астмой, которые были включены в открытое продленное исследование (TRAVERSE). В исследовании наблюдение продолжалось в течение 96 недель, что составило 99 пациенто-лет кумулятивного воздействия препарата Дупиксент®. Профиль безопасности препарата Дупиксент® в исследовании TRAVERSE соответствовал профилю безопасности, зарегистрированному в базовых исследованиях по лечению астмы в течение 52 недель терапии. Дополнительных нежелательных реакций выявлено не было. В этом исследовании клиническая польза препарата Дупиксент®, включая уменьшение количества обострений и улучшение функции легких, наблюдаемое в базовых исследованиях лечения пациентов с астмой, сохранялась до 96-й недели.
Безопасность и эффективность препарата у детей младше 12 лет с бронхиальной астмой не изучалась. Профиль нежелательных реакций у подростков сопоставим с таковым у взрослых (см. раздел «Побочное действие»).
Хронический полипозный риносинусит. Обычно хронический полипозный риносинусит не встречается у детей. Фармакокинетика дупилумаба не изучалась у детей (пациентов младше 18 лет) с хроническим полипозным риносинуситом.
Расовая принадлежность. Согласно результатам популяционного фармакокинетического анализа расовая принадлежность не влияла на фармакокинетические показатели препарата Дупиксент®.
Печеночная недостаточность. Дупилумаб представляет собой моноклональное антитело, поэтому не ожидается, что он подвергается значительной печеночной элиминации. Клинические исследования для оценки влияния печеночной недостаточности на фармакокинетику дупилумаба не проводились.
Почечная недостаточность. Дупилумаб представляет собой моноклональное антитело, поэтому не ожидается, что он подвергается значительной почечной элиминации. Клинические исследования для оценки влияния почечной недостаточности на фармакокинетику дупилумаба не проводились. Результаты популяционных фармакокинетических анализов показали, что нарушение функции почек легкой и средней степени тяжести существенным образом не влияет на системную экспозицию дупилумаба. Нет данных о применении дупилумаба у пациентов с тяжелой почечной недостаточностью.
Масса тела. Не требуется коррекции режима дозирования в зависимости от массы тела для пациентов с бронхиальной астмой в возрасте старше 12 лет и взрослых пациентов с атопическим дерматитом.
Для пациентов в возрасте 6-17 лет с атопическим дерматитом рекомендованная доза 300 мг каждые 4 недели (с массой тела 15-<30 кг), 200 мг каждые 2 недели (с массой тела 30-<60 кг) и 300 мг каждые две недели (с массой тела более 60 кг).
Показания препарата
Дупиксент®
- атопический дерматит среднетяжелого и тяжелого течения у пациентов от 6 лет и старше при недостаточном ответе на терапию топическими лекарственными препаратами или в случае, когда такие препараты не рекомендованы к применению. Препарат Дупиксент® может применяться в монотерапии или одновременно с топическими лекарственными препаратами;
- в качестве дополнительной поддерживающей терапии бронхиальной астмы среднетяжелого и тяжелого течения у пациентов в возрасте 12 лет и старше с эозинофильным фенотипом или у пациентов с гормональнозависимой бронхиальной астмой, получающих пероральные ГКС;
- в качестве дополнительной поддерживающей терапии взрослых пациентов с плохо контролируемым тяжелым хроническим полипозным риносинуситом.
Режим дозирования
Препарат Дупиксент® вводят п/к.
Атопический дерматит
Рекомендуемая доза препарата Дупиксент® у взрослых пациентов:
- начальная доза — 600 мг (2 инъекции по 300 мг), далее — по 300 мг каждые 2 недели. В зависимости от индивидуального терапевтического ответа доза может быть увеличена до 300 мг еженедельно.
Рекомендуемая доза препарата Дупиксент® у пациентов в возрасте 6-17 лет:
- для пациентов с массой тела от 15 до <30 кг: начальная доза – 600 мг (2 инъекции по 300 мг), далее по 300 мг каждые 4 недели;
- для пациентов с массой тела от 30 до <60 кг: начальная доза — 400 мг (2 инъекции по 200 мг), далее по 200 мг каждые 2 недели;
- для пациентов с массой тела 60 кг и более: начальная доза — 600 мг (2 инъекции по 300 мг), далее по 300 мг каждые 2 недели.
Бронхиальная астма
Рекомендуемая доза препарата Дупиксент® у взрослых пациентов и детей (12 лет и старше):
- начальная доза — 400 мг (2 инъекции по 200 мг), далее — по 200 мг каждые 2 недели. В зависимости от индивидуального терапевтического ответа доза может быть увеличена до 300 мг каждые 2 недели;
- начальная доза — 600 мг (2 инъекции по 300 мг), далее — по 300 мг каждые 2 недели для пациентов с глюкокортикостероидозависимой бронхиальной астмой или сопутствующим среднетяжелым или тяжелым атопическим дерматитом, при котором показано применение препарата Дупиксент®.
Хронический полипозный риносинусит
В случае пропуска дозы пациент должен получить инъекцию как можно скорее и затем продолжить лечение в соответствии с назначенным ему режимом введения препарата.
Особые группы пациентов
Безопасность и эффективность препарата Дупиксент® у детей до 6 лет и подростков с атопическим дерматитом, бронхиальной астмой и у пациентов с хроническим полипозным риносинуситом младше 18 лет не установлена.
У пациентов пожилого возраста коррекции дозы не требуется.
Отсутствуют данные по применению препарата у пациентов с печеночной недостаточностью.
У пациентов с легкой или средней степенью тяжести почечной недостаточности коррекции дозы не требуется. Отсутствуют данные по применению препарата у пациентов с тяжелой почечной недостаточностью.
Не требуется коррекции режима дозирования в зависимости от массы тела для пациентов с бронхиальной астмой старше 12 лет и взрослых пациентов с атопическим дерматитом и хроническим полипозным риносинуситом.
Для пациентов 6-17 лет с атопическим дерматитом рекомендованная доза 300 мг каждые 4 недели (с массой тела 15-<30 кг), 200 мг каждые 2 недели (с массой тела 30-<60 кг) и 300 мг каждые 2 недели (с массой тела более 60 кг).
Способ применения
Перед введением препарата следует осмотреть его на предмет наличия в растворе твердых частиц или появления нехарактерной окраски раствора. Если в препарате содержатся твердые частицы или у раствора появилась нехарактерная окраска, вводить препарат нельзя.
Раствор в предварительно заполненном шприце с системой защиты или предварительно заполненном шприце перед проведением инъекции препарата Дупиксент® должен нагреться до комнатной температуры. Для этого рекомендуется выдержать его при комнатной температуре в течение 45 мин (для дозировки 300 мг) или 30 мин (для дозировки 200 мг).
В случае необходимости предварительно заполненный шприц можно хранить при комнатной температуре (до 25°С) в течение максимум 14 дней. Препарат нельзя хранить при температуре выше 25°С. После извлечения из холодильника Дупиксент® следует использовать в течение 14 дней или утилизировать.
Шприцы следует защищать от нагревания и воздействия прямого солнечного света.
Если начальная доза составляет 600 мг, следует сделать две инъекции по 300 мг в разные места для инъекций.
Если начальная доза составляет 400 мг, следует сделать две инъекции по 200 мг в разные места для инъекций.
Лечение препаратом Дупиксент® следует проводить под медицинским наблюдением. Инъекцию препарата может делать себе либо сам пациент, либо лицо, ухаживающее за ним.
Необходимо до начала применения препарата Дупиксент® обучить пациентов и/или ухаживающих за ними лиц подготовке и проведению инъекции препарата Дупиксент®, согласно указаниям в «Инструкции по подготовке и проведению инъекции препарата Дупиксент®, 300 мг в предварительно заполненном одноразовом шприце с системой защиты», «Инструкции по подготовке и проведению инъекции препарата Дупиксент®, 300 мг в предварительно заполненном одноразовом шприце» и «Инструкции по подготовке и проведению инъекции препарата Дупиксент®, 200 мг в предварительно заполненном одноразовом шприце с системой защиты».
Препарат Дупиксент® может вводиться самим пациентом п/к с помощью предварительно заполненного одноразового шприца в область бедра или живота, за исключением области диаметром 5 см непосредственно вокруг пупка. Если инъекцию проводит другой человек, препарат также можно вводить в верхнюю часть плеча.
Рекомендуется менять места инъекций при каждом введении препарата.
Инъекцию препарата Дупиксент® не следует проводить в участки с болезненной и поврежденной кожей, в места с кровоподтеками или рубцами.
Все остатки неиспользованного препарата и расходные материалы необходимо утилизировать в соответствии с требованиями местного законодательства.
Инструкция по подготовке и проведению инъекции препарата Дупиксент® 300 мг в предварительно заполненном одноразовом шприце с системой защиты
Перед началом применения препарата Дупиксент® в предварительно заполненном одноразовом шприце с системой защиты внимательно прочитайте эту инструкцию.
Элементы предварительно заполненного одноразового шприца с системой защиты показаны на рисунке ниже:
Данное устройство представляет собой предварительно заполненный одноразовый шприц с системой защиты (далее называется «шприц»). В нем содержится раствор для п/к введения, содержащий 300 мг препарата Дупиксент®.
Важная информация
- Не пытайтесь провести инъекцию самостоятельно или с помощью кого-то до тех пор, пока лечащий врач или медицинский работник не обучат Вас правильной технике проведения подкожной инъекции.
- Перед использованием шприца внимательно прочитайте информацию по его использованию.
- Узнайте у своего лечащего врача, как часто необходимо проводить инъекции препарата Дупиксент®.
- Попросите своего лечащего врача или медицинского работника показать, как правильно пользоваться шприцем, перед тем как в первый раз самостоятельно провести инъекцию препарата Дупиксент®.
- Рекомендуется менять место инъекции при каждом введении препарата.
- Не используйте шприц, если он упал на твердую поверхность или поврежден.
- Нельзя использовать шприц, если отсутствует колпачок иглы, или он не был надежно зафиксирован.
- Не дотрагивайтесь до штока поршня до тех пор, пока не будете готовы провести инъекцию.
- Не проводите инъекции через одежду.
- Не пытайтесь удалить воздушные пузырьки из шприца.
- Для того чтобы снизить риск случайного укола иглой, каждый предварительно заполненный одноразовый шприц оборудован устройством безопасности с системой защиты, которое автоматически активируется, закрывая иглу, после того, как проведена инъекция.
- Не тяните шток поршня назад.
- Шприц не подлежит повторному использованию.
Как хранить шприц
- Храните шприцы в недоступном для детей месте.
- Храните неиспользуемые шприцы в оригинальной картонной упаковке в холодильнике при температуре от 2°C до 8°C.
- После извлечения из холодильника шприц следует оставить на 45 мин при комнатной температуре и дать возможность ему нагреться перед тем, как делать инъекцию препарата Дупиксент®.
- Шприцы можно хранить при комнатной температуре в течение не более чем 14 дней.
- Не встряхивайте шприц.
- Не подвергайте шприц тепловому воздействию.
- Не замораживайте шприц.
- Не допускайте воздействия на шприц прямых солнечных лучей.
Шаг 1. Извлечение шприца из упаковки
Извлеките шприц из картонной упаковки, взяв его за середину корпуса.
Не снимайте колпачок иглы до момента проведения инъекции.
Нельзя использовать шприц, если он упал на твердую поверхность или поврежден.
Шаг 2. Подготовка
Убедитесь, что в наличии есть все необходимое для проведения инъекции:
- предварительно заполненный шприц;
- 1 салфетка, смоченная спиртом*;
- 1 ватный тампон или марлевая салфетка*;
- устойчивый к проколам контейнер* (см. Шаг 12).
* Не содержатся в картонной упаковке.
Внимательно проверьте маркировку:
- проверьте дату истечения срока годности;
- убедитесь в том, что у Вас правильный препарат и правильная доза.
Нельзя использовать шприц после истечения срока годности, указанного на этикетке.
Шаг 3. Проверка
Осмотрите раствор через смотровое окно на шприце: проверьте, является ли раствор прозрачным, является ли жидкость бесцветной или имеющей светло-желтый оттенок.
Примечание: Вы можете обнаружить воздушные пузырьки, это нормально.
Нельзя использовать шприц, если жидкость изменила цвет или помутнела, или если в ней есть заметные хлопья или частицы.
Шаг 4. Подождите 45 мин
Положите шприц на плоскую поверхность не менее чем на 45 мин, пусть шприц нагреется до комнатной температуры.
Не нагревайте шприц.
Не подвергайте шприц прямому воздействию солнечных лучей.
Шприц нельзя хранить при комнатной температуре более 14 дней.
Шаг 5. Выбор места инъекции
Выберите место инъекции
- Вы можете сделать инъекцию в наружную поверхность бедра или в переднюю часть живота, за исключением области диаметром 5 см непосредственно вокруг пупка;
- Если инъекцию осуществляет другой человек, для инъекции также можно использовать участок кожи в верхней части плеча.
Инъекции препарата Дупиксент® не следует осуществлять на участках с болезненной или поврежденной кожей, кровоподтеками или рубцами.
Шаг 6. Обработка места инъекции
- Вымойте руки.
- Протрите участок кожи, предназначенный для инъекции салфеткой, смоченной спиртом.
- Дайте коже высохнуть перед проведением инъекции.
Не дотрагивайтесь до обработанного участка кожи руками и не дуйте на него перед проведением инъекции.
Шаг 7. Удаление колпачка иглы
Держите шприц за середину корпуса, игла должна быть направлена в сторону от Вас; снимите колпачок с иглы.
Не надевайте колпачок обратно на иглу.
Не касайтесь иглы.
Лекарственный препарат необходимо ввести сразу же после удаления колпачка иглы.
Шаг 8. Формирование складки кожи
Сформируйте складку кожи в месте инъекции, как показано на рисунке.
Шаг 9. Введение иглы
Полностью введите иглу в сформированную складку кожи под углом приблизительно 45°.
Шаг 10. Введение раствора
Ослабьте сформированную складку кожи.
Медленно и непрерывно нажимайте на шток поршня для введения всего раствора, пока шприц не опустеет.
Примечание: Вы почувствуете некоторое сопротивление. Это нормально.
Шаг 11. Завершение инъекции и извлечение иглы
Поднимите большой палец, снимая давление со штока поршня, игла будет втянута внутрь защитного колпачка для иглы; затем удалите шприц из места инъекции.
Слегка прижмите ватный тампон или марлевую салфетку к месту инъекции, если заметите кровь.
Не надевайте колпачок иглы снова на иглу.
Не растирайте кожу после инъекции.
Шаг 12. Утилизация
После использования следует поместить шприц и колпачок иглы в устойчивый к проколам контейнер.
Не надевайте колпачок иглы снова на иглу.
Храните контейнер в недоступном для детей месте.
Инструкция по подготовке и проведению инъекции препарата Дупиксент® 300 мг в предварительно заполненном одноразовом шприце
Перед началом применения препарата Дупиксент® в предварительно заполненном одноразовом шприце внимательно прочитайте эту инструкцию.
Элементы предварительно заполненного шприца показаны на рисунке ниже:
*Шприц может иметь твердый или мягкий колпачок иглы
Данное устройство представляет собой предварительно заполненный одноразовый шприц (далее называется «шприц»). В нем содержится раствор для подкожного введения, содержащий 300 мг препарата Дупиксент®.
Важная информация
- Не пытайтесь провести инъекцию самостоятельно или с помощью кого-то до тех пор, пока лечащий врач или медицинский работник не обучат Вас правильной технике проведения подкожной инъекции.
- Перед использованием шприца внимательно прочитайте информацию по его использованию.
- Узнайте у своего лечащего врача, как часто Вам необходимо проводить инъекции препарата Дупиксент®.
- Попросите своего лечащего врача или медицинского работника показать, как правильно пользоваться шприцем, перед тем как в первый раз самостоятельно провести инъекцию препарата Дупиксент®.
- Рекомендуется менять место инъекции при каждом введении препарата.
- Не используйте шприц, если он поврежден.
- Нельзя использовать шприц, если отсутствует колпачок иглы или он не был надежно зафиксирован.
- Не дотрагивайтесь до штока поршня до тех пор, пока Вы не будете готовы провести инъекцию.
- Не проводите инъекции через одежду.
- Не пытайтесь удалить воздушные пузырьки из шприца.
- Не тяните шток поршня назад.
- Шприц не подлежит повторному использованию.
Как хранить шприц
- Храните шприцы в недоступном для детей месте.
- Храните неиспользуемые шприцы в оригинальной картонной упаковке в холодильнике при температуре от 2°C до 8°C.
- После извлечения из холодильника шприц следует оставить на 45 мин при комнатной температуре и дать возможность ему нагреться перед тем, как проводить инъекцию препарата Дупиксент®.
- Шприцы можно хранить при комнатной температуре в течение не более чем 14 дней.
- Не встряхивайте шприц.
- Не подвергайте шприц тепловому воздействию;
- Не замораживайте шприц.
- Не допускайте воздействия на шприц прямых солнечных лучей.
Шаг 1. Извлечение шприца из упаковки
Извлеките шприц из картонной упаковки, взяв его за середину корпуса.
Не снимайте колпачок иглы до момента проведения инъекции.
Нельзя использовать шприц, если он был поврежден.
Шаг 2. Подготовка
Убедитесь, что у Вас есть все необходимое для проведения инъекции:
- предварительно заполненный шприц;
- 1 салфетка, смоченная спиртом*;
- 1 ватный тампон или марлевая салфетка*;
- устойчивый к проколам контейнер* (см. Шаг 12).
* Не содержатся в картонной упаковке.
Внимательно проверьте маркировку:
- проверьте дату истечения срока годности;
- убедитесь в том, что у Вас правильный препарат и правильная доза.
Нельзя использовать шприц после истечения срока годности, указанного на этикетке.
Шаг 3. Проверка
Осмотрите раствор в шприце: проверьте, является ли раствор прозрачным, является ли жидкость бесцветной или имеющей светло-желтый оттенок.
Примечание: Вы можете обнаружить воздушные пузырьки, это нормально.
Нельзя использовать шприц, если жидкость изменила цвет или помутнела, или если в ней есть заметные хлопья или частицы.
Шаг 4. Подождите 45 мин
Положите шприц на плоскую поверхность не менее чем на 45 мин; пусть шприц нагреется до комнатной температуры.
Не нагревайте шприц.
Не подвергайте шприц прямому воздействию солнечных лучей.
Шприц нельзя хранить при комнатной температуре более 14 дней.
Шаг 5. Выбор места инъекции
Выберите место инъекции.
- Вы можете сделать инъекцию в наружную поверхность бедра или в переднюю часть живота, за исключением области диаметром 5 см непосредственно вокруг пупка.
- Если инъекцию осуществляет другой человек, для инъекции также можно использовать участок кожи в верхней части плеча.
Инъекции препарата Дупиксент® не следует осуществлять на участках с болезненной или поврежденной кожей, кровоподтеками или рубцами.
Этап 6. Обработка участка инъекции
- Вымойте руки.
- Протрите участок кожи, предназначенный для инъекции салфеткой, смоченной спиртом.
- Дайте коже высохнуть перед проведением инъекции.
- Не дотрагивайтесь до обработанного участка кожи руками и не дуйте на него перед проведением инъекции.
Шаг 7. Удаление колпачка иглы
Держите шприц за середину корпуса, игла должна быть направлена в сторону от Вас; снимите колпачок иглы.
Не надевайте колпачок иглы обратно на иглу.
Не касайтесь иглы.
Лекарственный препарат необходимо ввести сразу же после удаления колпачка иглы.
Шаг 8. Формирование складки кожи
Сформируйте складку кожи на участке инъекции, как показано на рисунке.
Шаг 9. Введение иглы
Полностью введите иглу в сформированную складку под углом приблизительно 45°.
Шаг 10. Введение раствора
Ослабьте сформированную складку кожи.
Медленно и непрерывно нажимайте на шток поршня для введения всего раствора, пока шприц не опустеет.
Примечание: Вы почувствуете некоторое сопротивление. Это нормально.
Шаг 11. Извлечение иглы
Извлеките иглу из кожи под тем же углом, под которым она была введена.
Не надевайте колпачок иглы снова на иглу.
Слегка прижмите ватный тампон или марлевую салфетку к месту инъекции, если Вы заметите кровь.
Не растирайте кожу после инъекции.
Шаг 12. Утилизация
После использования следует поместить шприц и колпачок иглы в устойчивый к проколам контейнер.
Не надевайте колпачок иглы снова на иглу.
Храните контейнер в недоступном для детей месте.
Инструкция по подготовке и проведению инъекции препарата Дупиксент® 200 мг в предварительно заполненном одноразовом шприце с системой защиты
Перед началом применения препарата Дупиксент® в предварительно заполненном одноразовом шприце с системой защиты внимательно прочитайте эту инструкцию.
Элементы предварительно заполненного одноразового шприца с системой защиты показаны на рисунке ниже:
Данное устройство представляет собой предварительно заполненный одноразовый шприц с системой защиты (далее называется «шприц»). В нем содержится раствор для подкожного введения, содержащий 200 мг препарата Дупиксент®.
Важная информация
- Не пытайтесь провести инъекцию самостоятельно или с помощью кого-то до тех пор, пока лечащий врач или медицинский работник не обучат Вас правильной технике проведения подкожной инъекции.
- Перед использованием шприца внимательно прочитайте информацию по его использованию.
- Узнайте у своего лечащего врача, как часто Вам необходимо проводить инъекции препарата Дупиксент®.
- Попросите своего лечащего врача или медицинского работника показать, как правильно пользоваться шприцем, перед тем как в первый раз самостоятельно провести инъекцию препарата Дупиксент®.
- Рекомендуется менять место инъекции при каждом введении препарата.
- Не используйте шприц, если он упал на твердую поверхность или поврежден.
- Нельзя использовать шприц, если отсутствует колпачок иглы, или он не был надежно зафиксирован.
- Не дотрагивайтесь до штока поршня до тех пор, пока вы не будете готовы провести инъекцию.
- Не проводите инъекции через одежду.
- Не пытайтесь удалить воздушные пузырьки из шприца.
- Для того чтобы снизить риск случайного укола иглой, каждый предварительно заполненный одноразовый шприц оборудован устройством безопасности с системой защиты, которое автоматически активируется, закрывая иглу, после того, как Вы провели инъекцию.
- Не тяните шток поршня назад.
- Шприц не подлежит повторному использованию.
Как хранить шприц
- Храните шприцы в недоступном для детей месте.
- Храните неиспользуемые шприцы в оригинальной картонной упаковке в холодильнике при температуре от 2°C до 8°C.
- После извлечения из холодильника шприц следует оставить на 30 мин при комнатной температуре и дать возможность ему нагреться перед тем, как делать инъекцию препарата Дупиксент®.
- Шприцы можно хранить при комнатной температуре в течение не более чем 14 дней.
- Не встряхивайте шприц.
- Не подвергайте шприц тепловому воздействию.
- Не замораживайте шприц.
- Не допускайте воздействия на шприц прямых солнечных лучей.
Шаг 1. Извлечение шприца из упаковки
Извлеките шприц из картонной упаковки, взяв его за середину корпуса.
Не снимайте колпачок иглы до момента проведения инъекции.
Нельзя использовать шприц, если он упал на твердую поверхность или поврежден.
Шаг 2. Подготовка
Убедитесь, что у Вас есть все необходимое для проведения инъекции:
- предварительно заполненный шприц;
- 1 салфетка, смоченная спиртом*;
- 1 ватный тампон или марлевая салфетка*;
- устойчивый к проколам контейнер* (см. Шаг 12).
* Не содержатся в картонной упаковке.
Внимательно проверьте маркировку:
- проверьте дату истечения срока годности;
- убедитесь в том, что у Вас правильный препарат и правильная доза.
Нельзя использовать шприц после истечения срока годности, указанного на этикетке.
Шаг 3. Проверка
Осмотрите раствор через смотровое окно на шприце: проверьте, является ли раствор прозрачным, является ли жидкость бесцветной или имеющей светло-желтый оттенок.
Примечание: Вы можете обнаружить воздушные пузырьки, это нормально.
Нельзя использовать шприц, если жидкость изменила цвет или помутнела, или если в ней есть заметные хлопья или частицы.
Шаг 4. Подождите 30 мин
Положите шприц на плоскую поверхность не менее чем на 30 мин; пусть шприц нагреется до комнатной температуры.
Не нагревайте шприц.
Не подвергайте шприц прямому воздействию солнечных лучей.
Шприц нельзя хранить при комнатной температуре более 14 дней.
Шаг 5. Выбор места инъекции
Выберите место инъекции.
- Вы можете сделать инъекцию в наружную поверхность бедра или в переднюю часть живота, за исключением области диаметром 5 см непосредственно вокруг пупка.
- Если инъекцию осуществляет другой человек, для инъекции также можно использовать участок кожи в верхней части плеча.
Инъекции препарата Дупиксент® не следует осуществлять на участках с болезненной или поврежденной кожей, кровоподтеками или рубцами.
Шаг 6. Обработка места инъекции
- Вымойте руки.
- Протрите участок кожи, предназначенный для инъекции салфеткой, смоченной спиртом.
- Дайте коже высохнуть перед проведением инъекции.
- Не дотрагивайтесь до обработанного участка кожи руками и не дуйте на него перед проведением инъекции.
Шаг 7. Удаление колпачка иглы
Держите шприц за середину корпуса, игла должна быть направлена в сторону от Вас; снимите колпачок с иглы.
Не надевайте колпачок обратно на иглу.
Не касайтесь иглы.
Лекарственный препарат необходимо ввести сразу же после удаления колпачка иглы.
Шаг 8. Формирование складки кожи
Сформируйте складку кожи в месте инъекции, как показано на рисунке.
Шаг 9. Введение иглы
Полностью введите иглу в сформированную складку кожи под углом приблизительно 45°.
Шаг 10. Введение раствора
Ослабьте сформированную складку кожи.
Медленно и непрерывно нажимайте на шток поршня для введения всего раствора, пока шприц не опустеет.
Примечание: Вы почувствуете некоторое сопротивление. Это нормально.
Шаг 11. Завершение инъекции и извлечение иглы
Поднимите большой палец, снимая давление со штока поршня, игла будет втянута внутрь защитного колпачка для иглы, а затем удалите шприц из места инъекции.
Слегка прижмите ватный тампон или марлевую салфетку к месту инъекции, если Вы заметите кровь.
Не надевайте колпачок иглы снова на иглу.
Не растирайте кожу после инъекции.
Шаг 12. Утилизация
После использования следует поместить шприц и колпачок иглы в устойчивый к проколам контейнер.
Не надевайте колпачок иглы снова на иглу.
Храните контейнер в недоступном для детей месте.
Побочное действие
Атопический дерматит
Для описания частоты встречаемости нежелательных реакций используется следующая классификация: очень часто (≥10%); часто (≥1% и <10%); нечасто (≥0.1% и <1%); редко (≥0.01% и <0.1%); очень редко (<0.01%); частота неизвестна (невозможно определить по имеющимся данным частоту встречаемости нежелательной реакции).
Таблица 1. Нежелательные реакции, наблюдавшиеся в клинических исследованиях у пациентов с атопическим дерматитомa
* Пострегистрационные данные.
a Объединенные данные плацебо-контролируемых клинических исследований с проведением монотерапии (SOLO1, SOLO2 и исследования по подбору доз 2 фазы) и плацебо-контролируемого исследования CHRONOS с одновременным применением топических ГКС для лечения атопического дерматита; пациенты получали препарат в дозе 300 мг 1 раз в 2 недели и 300 мг 1 раз в неделю с или без топических ГКС в течение 16 недель.
b В клинических исследованиях случаи с герпетическими инфекциями (Herpes simplex) проявлялись поражениями кожи и слизистых оболочек, обычно были легкой или средней степени тяжести и не включали герпетическую экзему. О случаях герпетической экземы сообщалось отдельно, частота таких случаев была ниже у пациентов, получавших препарат Дупиксент®, по сравнению с группой плацебо.
Подростки в возрасте от 12 до 17 лет
Безопасность применения препарата Дупиксент® была оценена в исследовании с 250 пациентами в возрасте от 12 до 17 лет с атопическим дерматитом среднетяжелого и тяжелого течения (AD-1526). Профиль безопасности в течение 16 недель был сопоставим с профилем безопасности взрослых пациентов, принимавших участие в исследованиях.
Безопасность при длительном применении препарата Дупиксент® была оценена в долгосрочном открытом продолженном исследовании с участием пациентов в возрасте 12-17 лет с атопическим дерматитом среднетяжелого и тяжелого течения (AD-1434). Профиль безопасности в течение 52 недель был сравним с профилем безопасности пациентов, принимавших участие в 16-недельном исследовании (AD-1526). Профиль безопасности при длительном применении препарата Дупиксент® подростками соответствовал таковому у взрослых пациентов. Профиль безопасности комбинированного лечения препаратом Дупиксент® в сочетании с топическими ГКС в течение 52 недель соответствует профилю его безопасности, наблюдавшемуся к 16-й неделе.
Дети в возрасте от 6 до 11 лет
Безопасность препарата Дупиксент® изучали в исследовании при участии 367 пациентов в возрасте от 6 до 11 лет с тяжелым атопическим дерматитом (AD-1652). Профиль безопасности препарата Дупиксент® в сочетании с топическими ГКС у этих пациентов, наблюдение за которыми вели до 16 недели включительно, оказался сопоставимым с профилем безопасности препарата в исследованиях с участием взрослых пациентов и подростков с атопическим дерматитом.
Долгосрочная безопасность препарата Дупиксент® в сочетании с топическими ГКС оценивали в открытом продолженном исследовании у 368 пациентов в возрасте от 6 до 11 лет с атопическим дерматитом (AD-1434). На момент включения в исследование AD-1434 у 110 (29.9%) пациентов был среднетяжелый атопический дерматит, а у 72 (19.6%) пациентов был тяжелый атопический дерматит. Профиль безопасности препарата Дупиксент® в сочетании с топическими ГКС у пациентов, наблюдение за которыми вели в течение 52 недель, был схожим с профилем безопасности, установленным на 16 неделе в исследовании AD-1652. Долгосрочный профиль безопасности препарата Дупиксент® в сочетании с топическими ГКС у детей был сопоставим с таковым у взрослых пациентов и подростков с атопическим дерматитом.
Бронхиальная астма
Таблица 2. Нежелательные реакции, наблюдавшиеся в клинических исследованиях у пациентов с бронхиальной астмой
* Пострегистрационные данные.
Долгосрочную безопасность препарата Дупиксент® оценивали в открытом продленном исследовании с участием 2282 пациентов в возрасте от 12 лет и старше со среднетяжелой и тяжелой бронхиальной астмой (TRAVERSE). В этом исследовании наблюдение продолжалось в течение 96 недель, что составило 3169 пациенто-лет кумулятивного воздействия препарата Дупиксент®. Профиль безопасности препарата Дупиксент® в исследовании TRAVERSE соответствовал профилю безопасности, зарегистрированному в базовых исследованиях по лечению астмы в течение 52 недель. Не было выявлено дополнительных нежелательных реакций.
Хронический полипозный риносинусит
Таблица 3. Нежелательные реакции, наблюдавшиеся в клинических исследованиях у пациентов с хроническим полипозным риносинуситом
* Пострегистрационные данные.
Описание отдельных нежелательных реакций
Явления, связанные с конъюнктивитом и кератитом
Конъюнктивит и кератит чаще всего наблюдались у пациентов с атопическим дерматитом, получавших препарат Дупиксент®. У большинства пациентов конъюнктивит или кератит разрешался полностью или частично в течение периода лечения. Среди пациентов с астмой частота конъюнктивита и кератита была низкой и сходной между группами, получавшим препарат Дупиксент® и плацебо. У пациентов с хроническим полипозным риносинуситом частота конъюнктивита была низкой, хотя частота в группе, получавших препарат Дупиксент® была выше, чем в группе плацебо. В программе клинических исследований у пациентов с хроническим полипозным риносинуситом не было зарегистрировано ни одного случая кератита (см. раздел «Особые указания»).
Герпетическая экзема и Herpes zoster
В клинических исследованиях у пациентов с атопическим дерматитом частота герпетической экземы была схожей в группах, получающих препарат Дупиксент® и в группе плацебо. По данным 16-недельных исследований монотерапии Herpes zoster был зарегистрирован в <0.1% случаев в группе, получающей Дупиксент® (<1 на 100 пациенто-лет) и <1% в группе плацебо (1 на 100 пациенто-лет). В 52-недельном клиническом исследовании с одновременным применением топических ГКС (CHRONOS) Herpes zoster был зарегистрирован в 1% случаев в группе, получающей Дупиксент® + топические ГКС (1 на 100 пациенто-лет) и в 2% в группе плацебо (2 на 100 пациенто-лет). В клинических исследованиях у пациентов с бронхиальной астмой частота Herpes zoster была схожей в группах, получающих препарат Дупиксент® или плацебо.
Гиперчувствительность
Сообщалось о реакциях гиперчувствительности, включая анафилаксию и сывороточную болезнь или реакциях, подобных сывороточной болезни (см. разделы «Противопоказания» и «Особые указания»).
Эозинофилы
У пациентов, получавших препарат Дупиксент®, наблюдалось более высокое среднее начальное увеличение от исходного уровня эозинофилов по сравнению с пациентами, получавшими плацебо. Количество эозинофилов снижалось почти до базовых уровней во время исследования. В рамках открытого продленного исследования у пациентов с бронхиальной астмой количество эозинофилов продолжало снижаться ниже исходного уровня.
Частота эозинофилии, вызванной лечением (≥500 клеток/мкл), была сходной в группах пациентов, получавших препарат Дупиксент® и плацебо. Эозинофилия, вызванная лечением (≥5000 клеток/мкл), была зарегистрирована менее чем у 2% пациентов, получавших препарат Дупиксент®, и менее чем у 0.5% пациентов, получавших плацебо.
Инфекции
Количество серьезных инфекций у пациентов с атопическим дерматитом, бронхиальной астмой и хроническим полипозным риносинуситом было сопоставимо у пациентов, принимавших Дупиксент® и плацебо.
В первичных исследованиях безопасности клинических исследованиях пациентов с атопическим дерматитом не наблюдалось увеличения общей частоты инфекций или серьезных инфекций во время лечения препаратом Дупиксент® по сравнению с плацебо. В 16-недельных первичных клинических исследованиях безопасности, в которых проводилась монотерапия препаратом Дупиксент®, были зарегистрированы серьезные инфекции у 0.5% пациентов, получавших дупилумаб и у 1.0% пациентов, получавших плацебо. В 52-недельном исследовании CHRONOS серьезные инфекции были зарегистрированы у 0.2% пациентов, получавших препарат Дупиксент® и у 0.6% пациентов, получавших плацебо.
В клинических исследованиях у пациентов с бронхиальной астмой не наблюдалось увеличения общей частоты инфекций или серьезных инфекций во время лечения препаратом Дупиксент® по сравнению с плацебо. В 24-недельном клиническом исследовании были зарегистрированы серьезные инфекции у 1.0% пациентов, получавших дупилумаб, и у 1.1% пациентов, получавших плацебо. В 52-недельном исследовании QUEST серьезные инфекции были зарегистрированы у 1.3% пациентов, получавших дупилумаб, и у 1.4% пациентов, получавших плацебо.
В клинических исследованиях у пациентов с хроническим полипозным риносинуситом не наблюдалось увеличения общей частоты инфекций. В 24-недельном клиническом исследовании серьезные инфекции были зарегистрированы у 0.7% пациентов, получавших Дупиксент® и у 1.1% пациентов, получавших плацебо.
В ходе исследования SINUS-52 продолжительностью 52 недели инфекции были зарегистрированы у 1.3% пациентов, получавших дупилумаб, и у 1.3% пациентов, получавших плацебо.
Сердечно-сосудистые события
В 1-летнем плацебо-контролируемом исследовании у пациентов с бронхиальной астмой (QUEST) сердечно-сосудистые тромбоэмболические события (сердечно-сосудистые смерти, нефатальные инфаркты миокарда и нефатальные инсульты) были зарегистрированы в 1 случае (0.2%) в группе пациентов, получавших Дупиксент® 200 мг 1 раз в 2 недели; в 4 случаях (0.6%) в группе пациентов, получавших Дупиксент® 300 мг 1 раз в 2 недели и в 2 случаях (0.3%) в группе плацебо. В 1-летнем плацебо-контролируемом исследовании у пациентов с атопическим дерматитом (CHRONOS) сердечно-сосудистые тромбоэмболические события (сердечно-сосудистые смерти, нефатальные инфаркты миокарда и нефатальные инсульты) были зарегистрированы в 1 случае (0.9%) в группе пациентов, получавших Дупиксент® 300 мг 1 раз в 2 недели + топические ГКС; в 0 случаев (0.0%) в группе пациентов, получавших Дупиксент® 300 мг 1 раз в неделю + топические ГКС и в 1 случае (0.3%) в группе плацебо + топические ГКС.
Иммуногенность
Как и все белковые лекарственные препараты, препарат Дупиксент® обладает потенциалом иммуногенности.
Примерно у 5% пациентов с атопическим дерматитом, бронхиальной астмой или хроническим полипозным риносинуситом, которые получали препарат Дупиксент® в дозе 300 мг 1 раз в 2 недели в течение 52 недель, отмечалось образование антител против дупилумаба (АТ); приблизительно у 2% пациентов АТ стойко сохранялись и приблизительно 2% имели нейтрализующие антитела. Аналогичные результаты наблюдались у пациентов детского возраста (от 6 до 11 лет) с атопическим дерматитом, которые получали препарат Дупиксент® в дозе 200 мг 1 раз в 2 недели или 300 мг 1 раз в 4 недели в течение 16 недель.
Приблизительно у 16% подростков с атопическим дерматитом, получавших препарат Дупиксент® в дозе 300 мг или 200 мг 1 раз в 2 недели в течение 16 недель, отмечалось образование антител к дупилумабу; приблизительно у 3% зарегистрирован стойкий ответ со стороны АТ, и приблизительно у 5% пациентов были выявлены нейтрализующие антитела.
Примерно у 9% пациентов с бронхиальной астмой, которые получали препарат Дупиксент® в дозе 200 мг 1 раз в 2 недели в течение 52 недель, отмечалось образование антител к дупилумабу; приблизительно у 4% АТ стойко сохранялись и приблизительно 4% имели нейтрализующие антитела.
Независимо от возраста и популяции примерно у 2-4% пациентов в группах плацебо в 52-недельных исследованиях имелись антитела к дупилумабу; приблизительно у 2% антитела устойчиво сохранялись и приблизительно 1% имел нейтрализующие антитела.
Реакция образования антител обычно не влияла на системную экспозицию, безопасность или эффективность препарата Дупиксент®. Менее чем у 1% пациентов, получавших препарат Дупиксент® в зарегистрированной дозе, были выявлены высокие титры антител к препарату, ассоциирующиеся со снижением его системной экспозиции и эффективности. Кроме того, у одного пациента была обнаружена сывороточная болезнь, а у другого реакция, подобная сывороточной болезни (<0.1%), ассоциировавшиеся с высокими титрами антител (см. раздел «Особые указания»).
Наблюдаемая частота стойкого сохранения АТ и нейтрализующей активности в значительной степени зависят от чувствительности и специфичности используемого аналитического метода. Кроме того, наблюдаемая частота АТ-положительного статуса в анализе может зависеть от нескольких факторов, в т.ч. методики анализа, способа обработки проб, времени сбора проб, сопутствующих препаратов, а также статуса основного заболевания в каждом отдельном случае. По этим причинам сравнение частоты образования антител к дупилумабу с частотой выработки антител к другим препаратам может ввести в заблуждение.
Противопоказания к применению
- повышенная чувствительность к дупилумабу или любому из вспомогательных веществ препарата;
- детский возраст до 6 лет у пациентов с атопическим дерматитом среднетяжелого и тяжелого течения и бронхиальной астмой среднетяжелого и тяжелого течения в связи с неустановленными эффективностью и безопасностью;
- детский возраст до 12 лет у пациентов с бронхиальной астмой среднетяжелого и тяжелого течения в связи с неустановленной эффективностью и безопасностью.
С осторожностью
При беременности (только если ожидаемая польза превышает потенциальный риск для плода).
Применение при беременности и кормлении грудью
Беременность
Имеются лишь ограниченные данные по применению дупилумаба у беременных женщин. В исследованиях, проведенных на животных, прямых и косвенных неблагоприятных эффектов в отношении репродуктивной токсичности не обнаружено. Препарат Дупиксент® можно применять во время беременности только в том случае, если ожидаемая польза для матери превышает потенциальный риск для плода.
Период грудного вскармливания
Неизвестно, экскретируется ли дупилумаб с грудным молоком человека. С учетом пользы грудного вскармливания для ребенка и преимущества дальнейшего применения препарата для матери следует принять решение о прекращении кормления грудью или отмене препарата Дупиксент® в течение периода грудного вскармливания.
Применение при нарушениях функции печени
У пациентов с легкой или средней степенью тяжести почечной недостаточности коррекции дозы не требуется. Отсутствуют данные по применению препарата у пациентов с тяжелой почечной недостаточностью.
Применение при нарушениях функции почек
Отсутствуют данные по применению препарата у пациентов с печеночной недостаточностью.
Применение у детей
Противопоказания: детский возраст до 6 лет у пациентов с атопическим дерматитом среднетяжелого и тяжелого течения и бронхиальной астмой среднетяжелого и тяжелого течения в связи с неустановленными эффективностью и безопасностью; детский возраст до 12 лет у пациентов с бронхиальной астмой среднетяжелого и тяжелого течения в связи с неустановленной эффективностью и безопасностью.
Применение у пожилых пациентов
У пациентов пожилого возраста коррекции дозы не требуется.
Особые указания
Гиперчувствительность
При возникновении системной реакции гиперчувствительности лечение препаратом Дупиксент® должно быть немедленно прекращено, и начата соответствующая терапия.
В клинических исследованиях при применении препарата Дупиксент® при атопическом дерматите сообщалось об одном случае развития реакции, подобной сывороточной болезни, и одном случае развития сывороточной болезни после введения препарата (обе нежелательные реакции расценивались как серьезные). В исследовании при применении препарата при бронхиальной астме сообщалось об одном случае развития анафилаксии после введения препарата Дупиксент® (см. раздел «Побочное действие»).
Конъюнктивит и явления, связанные с кератитом
Конъюнктивит и явления, связанные кератитом, чаще встречались у пациентов с атопическим дерматитом, получавших препарат Дупиксент®. У некоторых пациентов наблюдалось нарушение зрения (например, затуманенное зрение), связанное с конъюнктивитом или кератитом (см. раздел «Побочное действие»). Пациенты должны сообщать о первом появлении или ухудшении симптомов со стороны глаз своему лечащему врачу. Пациенты, получающие лечение препаратом Дупиксент®, у которых развивался конъюнктивит, не проходящий после стандартного лечения, или признаки и симптомы кератита, должны пройти соответствующее офтальмологическое обследование (см. раздел «Побочное действие»).
Эозинофильные состояния
У пациентов с бронхиальной астмой может развиться серьезная системная эозинофилия, иногда в виде клинических признаков эозинофильной пневмонии или васкулита, соответствующих эозинофильному гранулематозу с полиангиитом, которые часто лечатся системными кортикостероидами. Эти события, как правило, но не всегда, могут быть связаны с сокращением приема пероральных кортикостероидов. Врачи должны быть внимательны к васкулитной сыпи, ухудшающимся легочным симптомам, сердечным осложнениям и/или нейропатии, возникающим у их пациентов с эозинофилией. Сообщалось о случаях эозинофильной пневмонии и васкулита, соответствующих эозинофильному гранулематозу с полиангиитом, при применении препарата Дупиксент® у взрослых пациентов, которые участвовали в клиническом исследовании препарата при бронхиальной астме. Связь между применением препарата Дупиксент® и этими состояниями не была установлена.
Симптомы обострения бронхиальной астмы или ухудшающееся состояние
Препарат Дупиксент® не следует назначать для лечения симптомов остро возникшего ухудшения или обострений астмы. Препарат Дупиксент® не применяется для лечения острого бронхоспазма или астматического статуса.
Снижение дозы ГКС
Не следует резко прерывать применение системных, местных или ингаляционных ГКС после начала терапии препаратом Дупиксент®. Сокращение дозы ГКС, при необходимости, должно быть постепенным и должно выполняться под непосредственным наблюдением врача. Уменьшение дозы ГКС может сопровождаться системными симптомами отмены и/или манифестацией состояний, которые ранее не проявлялись из-за системной терапии ГКС.
Гельминтозы (глистные инвазии)
Пациенты с обнаруженным гельминтозом не включались в клинические исследования. Неизвестно, может ли препарат Дупиксент® повлиять на иммунный ответ при гельминтозах. Необходимо провести лечение пациентов с имеющимся гельминтозом перед тем, как начинать лечение препаратом Дупиксент®. Если во время лечения препаратом Дупиксент® пациент заражается гельминтозом, а антигельминтные препараты оказываются неэффективными, следует прекратить лечение препаратом Дупиксент® до излечения паразитарного заболевания.
Сопутствующие атопические заболевания
Пациентам с атопическим дерматитом или ХПРС и с сопутствующей бронхиальной астмой следует рекомендовать не изменять своего лечения, не проконсультировавшись с лечащим врачом. Прекращая лечение препаратом Дупиксент®, следует принимать во внимание возможные эффекты на течение других атопических заболеваний.
Влияние на способность к управлению транспортными средствами и механизмами
Препарат Дупиксент® не оказывает или оказывает незначительное влияние на способность управлять транспортными средствами и работать с другими механизмами.
Передозировка
В клинических исследованиях не было выявлено проблем, связанных с безопасностью, при однократном в/в введении в дозах до 12 мг/кг.
Лечение: специфического антидота при передозировке препаратом Дупиксент® не существует. В случае передозировки необходимо контролировать состояние пациента для своевременного выявления признаков и симптомов нежелательных явлений и незамедлительно назначать соответствующее симптоматическое лечение.
Лекарственное взаимодействие
Живые вакцины
Применение препарата Дупиксент® с живыми вакцинами не изучалось. Во время лечения препаратом Дупиксент® не следует проводить вакцинацию живыми вакцинами.
Неживые (инактивированные) вакцины
Иммунные реакции на вакцинацию изучались в исследовании, в котором пациенты с атопическим дерматитом получали еженедельно препарат Дупиксент® в дозе 300 мг в течение 16 недель. После 12 недель терапии дупилумабом пациентов вакцинировали вакциной Tdap (Т-клеточно-зависимая, Adacel®) и менингококковой полисахаридной вакциной (Т-клеточно-независимая, Menomune®) и оценивали иммунные реакции по истечении 4 недель. У пациентов, получавших как дупилумаб, так и плацебо, реакции с образованием антител к противостолбнячной и менингококковой полисахаридной вакцинам были сходными. В этом исследовании не было обнаружено нежелательных взаимодействий между любой из этих неживых вакцин и дупилумабом.
Взаимодействие с субстратами изоферментов CYP450
В клиническом исследовании, проведенном у пациентов с атопическим дерматитом, оценивались эффекты дупилумаба на фармакокинетику субстратов изоферментов CYP. Данные, полученные в этом исследовании, не указывают на клинически значимое влияние дупилумаба на активность изоферментов CYP1A2, CYP3A, CYP2C19, CYP2D6 или CYP2C9.
Взаимодействие с другими лекарственными средствами для лечения бронхиальной астмы
Влияние дупилумаба на фармакокинетику одновременно назначаемых препаратов не ожидается. Данные, полученные на основании популяционного анализа, не указывают на влияние одновременно назначаемых препаратов на фармакокинетику дупилумаба у пациентов со среднетяжелым или тяжелым течением бронхиальной астмы.
Условия хранения препарата Дупиксент®
Препарат следует хранить в недоступном для детей месте, в оригинальной упаковке для защиты от света, при температуре от 2° до 8°С; не замораживать.
Срок годности препарата Дупиксент®
Срок годности — 36 мес. Не использовать после окончания срока годности, указанного на упаковке.
Условия реализации
Препарат отпускается по рецепту.
Контакты для обращений
САНОФИ

|
|
Представительство |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Дупиксент — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-005440
Торговое наименование препарата:
Дупиксент®.
Международное непатентованное наименование:
дупилумаб.
Лекарственная форма:
раствор для подкожного введения.
Состав
| Ингредиент | Количество (дозировка 50 мг/мл) | Количество (дозировка 175 мг/мл) | ||
| в 1 мл | в шприцеa | в 1 мл | в шприцеb | |
| Действующее вещество | ||||
| Дупилумаб | 150 мг | 300 мг | 175 мг | 200 мг |
| Вспомогательные вещества | ||||
| L-гистидин | 3,1 мгc | 6,2 мгc | 3,1 мгc | 3,54 мгc |
| L-гистидина гидрохлорида моногидрат | ||||
| L-аргинина гидрохлорид | 4,35 мгd | 8,7 мгd | 10,51 мгe | 12,01 мгe |
| Натрия ацетата тригидрат | 0,75 мгf | 1,5 мгf | 0,75 мгf | 0,86 мгf |
| Уксусная кислота ледяная | ||||
| Сахароза | 50 мгg | 100 мг | 49,88 мгg | 57,00 мг |
| Полисорбат-80 | 2 мгi | 4 мг | 2 мгi | 2,28 мг |
| Вода для инъекций | до 1,0 мл | до 2,0 мл | до 1,0 мл | до 1,14 мл |
a) В расчете на 2,0 мл препарата.
b) В расчете на 1,14 мл препарата.
c) Содержание L-гистидина и L-гистидина гидрохлорида приведено в пересчете на L-гистидин (М=155,16 г/моль), исходя из общей концентрации гистидина в препарате 20 мМ.
d) Содержание L-аргинина гидрохлорида приведено в пересчете на L-аргинин (М=174,20 г/моль), исходя из молярной концентрации L-аргинина в препарате 25 мМ. Номинальное содержание L-аргинина гидрохлорида (М=210,66 г/моль) в одном шприце составляет 10,5 мг.
e) Содержание L-аргинина гидрохлорида приведено в пересчете на L-аргинин (М= 174,20 г/моль), исходя из молярной концентрации L-аргинина в препарате 50 мМ. Номинальное содержание L-аргинина гидрохлорида (М=210,66 г/моль) для дозировки 175 мг/мл составляет 9,93 мг.
f) Содержание натрия ацетата тригидрата и уксусной кислоты ледяной приведено, исходя из общей концентрации ацетат иона в препарате 12,5 мМ.
g) Содержание сахарозы приведено в пересчете на миллиграммы, исходя из масса-объемной концентрации сахарозы в препарате 5%.
h) Содержание полисорбата-80 приведено в пересчете на миллиграммы, исходя из масса-объемной концентрации полисорбата-80 в препарате 0,2%.
Описание
Прозрачная или слегка опалесцирующая, бесцветная или желтоватого цвета жидкость.
Фармакотерапевтическая группа:
ингибиторы интерлейкина.
Код ATX:
D11AH05.
Фармакологические свойства
Механизм действия
Препарат Дупиксент® является рекомбинантным человеческим моноклональным антителом (IgG4), которое блокирует передачу сигналов интерлейкина-4 (ИЛ-4) и интерлейкина-13 (ИЛ-13) путем специфического связывания с 1L-4Rа-субъединицей, общей для рецепторных комплексов ИЛ-4 и ИЛ-13. Препарат Дупиксент® блокирует передачу сигналов ИЛ-4 через рецепторы I типа (IL-4Rα/γc) и общую передачу сигналов ИЛ-4 и ИЛ-13 через рецепторы II типа (IL-4Rα/IL-13Ra). ИЛ-4 и ИЛ-13 являются ключевыми цитокинами воспаления 2-го типа (в том числе продуцируемые и Th2-лимфоцитами), вовлеченными в патогенез атопических заболеваний.
Воспаление 2-го типа играет важную роль в патогенезе многих атонических заболеваний, включая бронхиальную астму, способствует ограничению воздушного потока и увеличивает риск обострений. ИЛ-4 и ИЛ-13 выступают в качестве основных факторов воспаления 2-го типа, активируя множественные типы клеток (например, тучные клетки, лимфоциты, эозинофилы, нейтрофилы, макрофаги) и индуцируя множественные медиаторы (например, иммуноглобулин Е, гистамин, эйкозаноиды, лейкотриены, хемокины и цитокины, включая эотаксин/CCL11, TARC/CCL17 и ИЛ-5), участвующие в воспалении 2-го типа. Блокирование пути передачи сигналов ИЛ-4/ИЛ-13 дупилумабом у пациентов снижает концентрации многих из этих маркеров воспаления 2-го типа, включая иммуноглобулин Е, периостин и множественные провоспалительные цитокины и хемокины (например, эотаксин, TARC), а также снижает уровень фракции оксида азота в выдыхаемом воздухе (FeNO) – маркер воспаления в легких. Было показано, что блокирование пути передачи сигналов ИЛ-4/ИЛ-13 дупилумабом в гуманизированных моделях животных предотвращает последующие действия этих цитокинов и хемокинов, в том числе гиперплазию бокаловидных клеток, гиперреактивность гладкомышечных клеток дыхательных путей, эозинофильное воспаление в легких, другие воспалительные процессы в легких, а также предотвращает нарушение функции легких; при этом снижение выраженности эозинофильного воспаления в легких происходит независимо от нормального или повышенного уровня эозинофилов в крови.
Дупилумаб производится с помощью технологии рекомбинантной ДНК в суспензионной культуре клеток яичника китайского хомячка.
Дупилумаб имеет молекулярную массу приблизительно 147 кДа.
Фармакодинамика
Атопический дерматит
В клинических исследованиях лечение препаратом Дупиксент® приводило к снижению в сыворотке крови концентраций биомаркеров, связанных с цитокинами воспаления 2-го типа, таких как тимус ассоциированного регуляторного хемокина (TARC/CCL17), общего сывороточного иммуноглобулина Е и аллерген-специфического иммуноглобулина Е. Также наблюдалось снижение активности лактатдегидрогеназы (ЛДГ), биомаркера, связанного со степенью тяжести атопического дерматита и его активностью. Препарат Дупиксент® уже в начале 2-й недели лечения вызывал супрессию хемокина TARC по сравнению с плацебо, с тенденцией продолжения его снижения до максимальной и устойчивой супрессии к 12-й неделе лечения.
У пациентов, получавших препарат Дупиксент® в дозе 300 мг 1 раз в 2 недели и в дозе 300 мг 1 раз в неделю, общий сывороточный иммуноглобулин Е к 52-й неделе терапии снизился на -74,8% и -73,9% (медиана изменения по сравнению с исходным уровнем), соответственно, по сравнению с -0% в группе плацебо. Аналогичные тенденции наблюдались в отношении антиген-специфических иммуноглобулинов Е, в том числе энтеротоксина А, специфического для золотистого стафилококка (S. aureus), аллергенов трав и деревьев.
Бронхиальная астма
В соответствии с ингибированием передачи сигналов ИЛ-4 и ИЛ-13, лечение дупилумабом заметно уменьшало уровень FeNO и концентрации эотаксина-3, общего иммуноглобулина Е, аллерген-специфического иммуноглобулина Е, TARC и периостина у пациентов с бронхиальной астмой по сравнению с плацебо. Эти снижения уровней биомаркеров воспаления были сопоставимы для режимов дозирования 200 мг 1 раз в 2 недели и 300 мг 1 раз в 2 недели и были близки к максимальному подавлению через 2 недели лечения, за исключением иммуноглобулина Е, который уменьшался медленнее. Описанные эффекты были устойчивыми во время лечения.
Клиническая эффективность
Атонический дерматит
Эффективность и безопасность препарата Дупиксент® в монотерапии или в сочетании с топическими глюкокортикостероидами (ГКС) оценивали в трех основных рандомизированных, двойных слепых, плацебо-контролируемых исследованиях (SOLO 1, SOLO 2 и CHRONOS) с участием 2119 пациентов в возрасте 18 лет и старше со среднетяжелым и тяжелым течением атопического дерматита
16-недельные исследования монотерапии (SOLO 1 и SOLO 2)
Показателя общей оценки исследователя (IGA) 0 или 1 («чистая» или «почти чистая кожа») к 16-й неделе лечения в клиническом исследовании SOLO 1 достигли 37,9% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 недели, и 37,2% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в неделю, против 10,3% пациентов в группе плацебо, а в исследовании SOLO 2 – 36,1% и 36,4% против 8,5%, пациентов, соответственно.
Улучшение не менее чем на 75% от исходного значения по индексу тяжести и площади экземы (EASI-75) к 16-й неделе лечения в исследовании SOLO 1 достигли 51,3% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 недели, и 52,5% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в неделю, против 14,7% пациентов в группе плацебо, а в исследовании SOLO 2 – 44,2% и 48,1% против 11,9%, соответственно.
Не менее чем 4-бального уменьшения зуда по пиковым значениям числовой шкалы оценки выраженности зуда (NRS) к 16-й неделе лечения в исследовании SOLO 1 достигли 40,8% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 недели, и 40,3% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в неделю, против 12,3% пациентов в группе плацебо, а в исследовании SOLO 2 – 36,0% и 39,0% пациентов против 9,5%, соответственно. Значительно больший процент пациентов, получавших Дупиксент®, достигал быстрого улучшения по шкале оценки тяжести зуда NRS по сравнению с пациентами в группе плацебо (определяемого как ≥4-балльное улучшение уже на 2-й неделе), причем процент пациентов, у которых наблюдалось уменьшение тяжести зуда по шкале NRS, продолжал увеличиваться в течение всего периода лечения.
Эффекты лечения в подгруппах (с распределением на подгруппы по массе тела, возрасту, полу, расе и сопутствующей терапии, в том числе с применением иммунодепрессантов) в исследованиях SOLO 1 и SOLO 2 в целом согласуются с результатами, полученными в общей исследуемой популяции.
52-недельное клиническое исследование с одновременным применением топических ГКС (CHRONOS)
IGA 0 или 1 к 16-й неделе лечения достигли 38,7% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 недели + топические ГКС, и 39,2% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в неделю + топические ГКС, против 12,4% пациентов в группе плацебо, а к 52-й неделе – 36,0% и 40,0% против 12,5% пациентов, соответственно.
EASI-75 к 16-й неделе лечения достигли 68,9% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 недели + топические ГКС, и 63,9% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в неделю + топические ГКС, против 23,2% пациентов в группе плацебо + топические ГКС, а к 52-й неделе – 65,2% и 64,1% против 21,6% пациентов, соответственно.
Не менее чем 4-бального улучшения по шкале тяжести зуда NRS к 16-й неделе лечения достигли 58,8% пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 недели + топические ГКС, и 50,8% пациентов, получавших препарат Дупиксент® в дозе 300 мг 1 раз в неделю + топические ГКС, против 19,7% пациентов в группе плацебо + топические ГКС, а к 52-й неделе – 51,2% и 39,0% против 12,9% пациентов, соответственно. Более значительный процент пациентов, получавших препарат Дупиксент® + топические ГКС, достигал быстрого улучшения по шкале тяжести зуда NRS по сравнению с пациентами в группе плацебо + топические ГКС (определяемого как >4-балльное улучшение уже на 2-й неделе; р <0,05), причем доля пациентов, у которых наблюдалось уменьшение тяжести зуда по шкале NRS, продолжала увеличиваться в течение всего периода лечения.
Эффекты лечения в подгруппах (с распределением по массе тела, возрасту, полу, расе и сопутствующей терапии, в том числе с применением иммунодепрессантов) в исследовании CHRONOS в целом согласуются с результатами, полученными в общей исследуемой популяции.
Клиническая эффективность у пациентов, которым не рекомендовалось лечение циклоспорином
У пациентов, которым не рекомендовалось лечение циклоспорином или оно было неэффективно, монотерапия препаратом Дупиксент® в обеих группах лечения, приводила к значительному улучшению признаков и симптомов атопического дерматита по сравнению с плацебо. Больший процент пациентов, получавших Дупиксент®, по сравнению с группой плацебо достигал IGA 0 или 1 и снижения по сравнению с исходным значением на ≥2 балла к 16-й неделе (29,5% против 6,8%), EASI-75 к 16-й неделе (38% против 11,4%), а также снижения не менее чем на 4 балла индекса тяжести зуда от исходного значения к 16-й неделе (34,9% по сравнению с 8%) (р <0,001 для всех 3 конечных точек). Аналогичные результаты наблюдались у пациентов, получавших Дупиксент® одновременно с топическими ГКС. Эффективность комбинации препарата Дупиксент® + топические ГКС сохранялась до 52-й недели терапии.
Бронхиальная астма
Было проведено три рандомизированных, двойных слепых, плацебо-контролируемых, многоцентровых исследования в параллельных группах (DRI12544, QUEST и VENTURE) продолжительностью от 24 до 52 недель с участием 2888 пациентов (в возрасте 12 лет и старше). Во все три исследования пациенты были включены независимо от минимального исходного уровня эозинофилов или другого биомаркера воспаления 2-го типа (например, уровня FeNO или иммуноглобулина Е).
Обострения бронхиальной астмы
В исследованиях DRI12544, QUEST и VENTURE оценивали частоту тяжелых обострений астмы независимо от минимального количества эозинофилов или любых других биомаркеров воспаления 2-го типа (например, FeNO или иммуноглобулин Е) в начале исследования. В общей популяции, независимо от содержания эозинофилов и других биомаркеров воспаления 2-го типа, у пациентов, получавших 200 или 300 мг препарата Дупиксент® один раз в две недели, произошло значительное снижение частоты тяжелых обострений астмы по сравнению с группой плацебо. В исследованиях DRI12544 и QUEST частота тяжелых обострений при применении препарата Дупиксент® в дозе 200 мг 1 раз в 2 недели снижалась на 70% и 48%; а при применении в дозе 300 мг 1 раз в 2 недели – на 70% и 46%, соответственно; и на 59% в исследовании VENTURE.
В объединенном анализе исследований DRI12544 и QUEST частота тяжелых обострений, приводящих к госпитализации и/или посещениям отделений неотложной помощи, снизилась на 25,5% и 46,9% при применении препарата Дупиксент® в дозах 200 мг или 300 мг 1 раз в 2 недели, соответственно.
Кумулятивное среднее число тяжелых обострений было более низкое у пациентов, получавших препарат Дупиксент® по сравнению с плацебо в исследованиях DRI12544, QUEST и VENTURE (в общей популяции и в популяции с исходным числом эозинофилов ≥150 клеток/мкл или FeNO ≥25 ppb) в течение 24- или 52-недельного периода лечения в обеих группах режимов дозирования препарата.
В исследовании QUEST у пациентов, получавших ингаляционные глюкокортикостероиды (ИКС) в средней дозе, наблюдалось сходное снижение частоты тяжелых обострений астмы по сравнению с пациентами, получавшими ИКС в высокой дозе.
Функция легких
Клинически значимое увеличение предбронходилатационного значения объема форсированного выдоха за 1-ю секунду (ОФВ1) наблюдалось на 12-й неделе в общей популяции независимо от уровня эозинофилов или других биомаркеров воспаления 2-го типа (например, FeNO или иммуноглобулин Е). В исследованиях DRI12544, QUEST и VENTURE, по сравнению с плацебо, большее улучшение ОФВ1 наблюдалось также у пациентов с FeNO ≥25 ppb. Улучшение ОФВ1 было одинаковым, независимо от того, получали ли пациенты ИКС в средней дозе, ИКС в высокой дозе или пероральные глюкокортикостероиды (ОКС).
Значительные улучшения ОФВ1 наблюдались уже в течение второй недели (DRI12544, QUEST и VENTURE) после первой инъекции препарата Дупиксент® в дозе как 200 мг, так и 300 мг и сохранялись в течение 24 недель (DRI12544 и VENTURE) и 52 недель (QUEST).
Скорректированная средняя разность абсолютных значений ОФВ1 была 0,20 л и 0,14 л в группах, получавших Дупиксент® 200 мг 1 раз в 2 недели, по сравнению с плацебо; 0,16 и 0,13 л в группах, получавших 300 мг 1 раз в 2 недели по сравнениюс плацебо, соответственно в исследованиях DR112544 и QUEST. Соответствующее процентное изменение ОФВ1 составляло от 9,2 до 11,9% для дозы 200 мг 1 раз в 2 недели и от 9,4 до 11,7% для дозы 300 мг 1 раз в 2 недели. Скорректированная средняя разность абсолютных значений пре-бронходилатационного ОФВ1 от исходного уровня к 24-й неделе (достаточное время для достижения максимального снижения дозы пероральных глюкокортикостероидов) в исследовании VENTURE составила 0,22 л в группе применения препарата Дупиксент® по сравнению с плацебо, что соответствовало улучшению на 15,1% по сравнению с исходным уровнем.
Кроме того, у пациентов, получавших препарат Дупиксент®, значительно улучшился пост-бронходилатационный показатель ОФВ1 по сравнению с исходным уровнем на 12-й и 52-й неделях по сравнению с плацебо, что указывает на то, что препарат Дупиксент® улучшает фиксированную обструкцию дыхательных путей. В группе применения препарата Дупиксент® в течение года наблюдения не было зарегистрировано снижения функции легких с учетом значения пост-бронходилатационного значения ОФВ1.
Снижение дозы пероральных глюкокортикостероидов
В исследовании VENTURE оценивалось влияние препарата Дупиксент® на снижение применения поддерживающих пероральных глюкокортикостероидов. Исходная средняя доза пероральных кортикостероидов составляла 11,75 мг в группе плацебо и 10,75 мг в группе, получавшей препарат Дупиксент®. По сравнению с плацебо, у пациентов, получавших Дупиксент®, отмечалось большее снижение ежедневной дозы пероральных глюкокортикостероидов при сохранении контроля над астмой. Среднее общее снижение ежедневной дозы пероральных глюкокортикостероидов при сохранении контроля над астмой составляло 70,1% по сравнению с исходным уровнем у пациентов, получавших Дупиксент® и 41,9% в группе плацебо.
Исходы, сообщаемые пациентами
Кроме того, во всех 3-х исследованиях Дупиксент® обеспечил клинически значимое улучшение показателей контроля бронхиальной астмы в общей популяции по сравнению с группой плацебо, о чем свидетельствуют показатели ACQ-5 и соответствующее улучшение качества жизни, измеренное по шкале AQLQ(S). Улучшение показателей ACQ-5 и AQLQ(S) были зарегистрированы уже через 2 недели и это улучшение сохранялось на протяжении 24-х недель в исследовании DRI12544 и 52-х недель в исследовании QUEST. В общей популяции исследования QUEST доля пациентов, ответивших на лечение, что выражалось в достижении минимального клинически-значимого различия показателей ACQ-5 и AQLQ(S), была существенно выше к 52-й неделе в группе, получавшей обе дозы препарата Дупиксент®.
Фармакокинетика
Фармакокинетика дупилумаба аналогична у пациентов с атопическим дерматитом и бронхиальной астмой.
Абсорбция
После однократного подкожного введения 75-600 мг дупилумаба, медиана времени достижения максимальной концентрации в сыворотке крови (Тmax) составляла 3-7 дней. Абсолютная биодоступность дупилумаба после введения подкожной дозы сходна между пациентами с атопическим дерматитом и бронхиальной астмой и составляет 61-64% (установлена при популяционном фармакокинетическом анализе).
Введение однократной нагрузочной дозы в первый день приводит к быстрому достижению клинически эффективных концентраций в течение 2-х недель.
При схеме лечения 200 мг или 300 мг 1 раз в 2 недели, начиная с нагрузочной дозы 400 мг или 600 мг, равновесные концентрации дупилумаба обычно достигаются в среднем к 16-й неделе лечения. В состоянии достижения равновесных концентраций средняя остаточная концентрация перед введением следующей дозы составляла 39 мг/л при применении 200 мг 1 раз в 2 недели и 70-74 мг/л при применении 300 мг 1 раз в 2 недели.
При еженедельном подкожном введении 300 мг препарата Дупиксент®, начиная с нагрузочной дозы 600 мг, равновесные концентрации обычно достигаются в среднем после 13 недель лечения. В состоянии достижения равновесных концентраций средняя остаточная концентрация перед введением следующей дозы составляла 189 мг/л.
Линейность дозы
Из-за нелинейности клиренса системная экспозиция дупилумаба, определяемая по площади под фармакокинетической кривой «концентрация-время» (AUC), увеличивается быстрее, непропорционально увеличению дозы после однократного подкожного введения препарата в дозах от 75 мг до 600 мг.
Распределение
Объем распределения дупилумаба составляет приблизительно 4,6 л, что указывает на его распределение главным образом в сосудистой системе.
Метаболизм
Поскольку дупилумаб является белком, специальных исследований его метаболизма не проводилось. Предполагается, что дупилумаб расщепляется до низкомолекулярных пептидов и отдельных аминокислот.
Выведение
Выведение дупилумаба осуществляется параллельно линейными и нелинейными путями. При более высоких концентрациях выведение дупилумаба осуществляется главным образом через не насыщаемый протеолитический путь, в то время как при более низких концентрациях выведение препарата преимущественно осуществляется через нелинейное насыщаемое связывание с мишенью IL-4Rα.
После введения последней дозы в состоянии равновесной концентрации медиана времени до неопределяемых концентраций дупилумаба, составляет 9 недель при введении 200 мг 1 раз в 2 недели, 10-11 недель при введении 300 мг 1 раз в 2 недели и 13 недель при введении 300 мг 1 раз в неделю.
Особые группы пациентов
Пол
Пол пациента не влиял на фармакокинетические показатели препарата. Дупиксент®.
Возраст
Возраст пациента не влиял на фармакокинетические показатели препарата. Дупиксент®.
Пациенты пожилого возраста
По данным популяционного анализа фармакокинетических показателей возраст пациентов не влиял на эффективность и безопасность препарата Дупиксент®.
Пациенты детского возраста
Фармакокинетика дупилумаба у детей и подростков до 18 лет с атопическим дерматитом и у детей с бронхиальной астмой младше 12 лет не изучалась. Эффективность и профиль нежелательных реакций у подростков с бронхиальной астмой старше 12 лет были схожи с таковыми у взрослых.
Расовая принадлежность
Согласно результатам популяционного фармакокинетического анализа расовая принадлежность не влияла на фармакокинетические показатели препарата Дупиксент®.
Печеночная недостаточность
Дупилумаб представляет собой моноклональное антитело, поэтому не ожидается, что он подвергается значительной печеночной элиминации. Клинические исследования для оценки влияния печеночной недостаточности на фармакокинетику дупилумаба не проводились.
Почечная недостаточность
Дупилумаб представляет собой моноклональное антитело, поэтому не ожидается, что он подвергается значительной почечной элиминации. Клинические исследования для оценки влияния почечной недостаточности на фармакокинетику дупилумаба не проводились. Результаты популяционных фармакокинетических анализов показали, что нарушение функции почек легкой и средней степени тяжести существенным образом не влияет на системную экспозицию дупилумаба. Нет данных о применении дупилумаба у пациентов с тяжелой почечной недостаточностью.
Масса тела
Не требуется коррекции режима дозирования в зависимости от массы тела пациента.
Показания к применению
- Атопический дерматит среднетяжелого и тяжелого течения у взрослых пациентов при недостаточном ответе на терапию топическими лекарственными препаратами или в случае, когда такие препараты не рекомендованы к применению.
Препарат Дупиксент® может применяться в монотерапии или одновременно с топическими лекарственными препаратами. - В качестве дополнительной поддерживающей терапии бронхиальной астмы среднетяжелого и тяжелого течения у пациентов в возрасте 12 лет и старше с эозинофильным фенотипом или у пациентов с гормональнозависимой бронхиальной астмой, получающих пероральные глюкокортикостероиды.
- В качестве дополнительной поддерживающей терапии взрослых пациентов с плохо контролируемым тяжелым хроническим полипозным риносинуситом (ХПРС)
Противопоказания
Повышенная чувствительность к дупилумабу или любому из вспомогательных веществ препарата (см. раздел «Особые указания).
Детский возраст до 18 лет у пациентов с атопическим дерматитом среднетяжелого и тяжелого течения в связи с неустановленными эффективностью и безопасностью.
Детский возраст до 12 лет у пациентов с бронхиальной астмой среднетяжелого и тяжелого течения в связи с неустановленными эффективностью и безопасностью.
С осторожностью
При беременности (только если ожидаемая польза превышает потенциальный риск для плода).
Применение при беременности и в период грудного вскармливания
Беременность
Имеются лишь ограниченные данные по применению дупилумаба у беременных женщин. В исследованиях, проведенных на животных, прямых и косвенных неблагоприятных эффектов в отношении репродуктивной токсичности не обнаружено. Препарат Дупиксент® можно применять во время беременности только в том случае, если ожидаемая польза для матери превышает потенциальный риск для плода.
Период грудного вскармливания
Неизвестно, экскретируется ли дупилумаб в грудное молоко человека. Следует, с учетом пользы грудного вскармливания для ребенка и преимущества дальнейшего применения препарата для матери, принять решение о прекращении кормления грудью или отмене препарата Дупиксент® в течение периода грудного вскармливания.
Способ применения и дозы
Общие рекомендации
Препарат Дупиксент® вводится подкожно.
Атопический дерматит
• Рекомендуемая доза препарата Дупиксент® у взрослых пациентов: начальная доза – 600 мг (2 инъекции по 300 мг), далее – по 300 мг каждые 2 недели. В зависимости от индивидуального терапевтического ответа доза может быть увеличена до 300 мг еженедельно.
Бронхиальная астма
Рекомендуемая доза препарата Дупиксент® у взрослых пациентов и детей (12 лет и старше):
• начальная доза – 400 мг (2 инъекции по 200 мг), далее – по 200 мг каждые 2 недели. В зависимости от индивидуального терапевтического ответа доза может быть увеличена до 300 мг каждые 2 недели.
• начальная доза – 600 мг (2 инъекции по 300 мг), далее – по 300 мг каждые 2 недели для пациентов с глюкокортикостероидозависимой бронхиальной астмой или с сопутствующим среднетяжелым или тяжелым атопическим дерматитом, при котором показано применение препарата Дупиксент®.
В случае пропуска дозы пациент должен получить инъекцию как можно скорее и затем продолжить лечение в соответствии с назначенным ему режимом введения препарата.
Особые группы пациентов
Дети
Безопасность и эффективность препарата Дупиксент® у детей и подростков до 18 лет с атопическим дерматитом не установлена.
Безопасность и эффективность препарата Дупиксент® у детей в возрасте до 12 лет с бронхиальной астмой не установлена.
Пациенты пожилого возраста
У пациентов пожилого возраста коррекции дозы не требуется (см. раздел «Фармакокинетика»).
Печеночная недостаточность
Отсутствуют данные по применению препарата у пациентов с печеночной недостаточностью (см. раздел «Фармакокинетика»).
Почечная недостаточность
У пациентов с легкой или средней степенью тяжести почечной недостаточности коррекции дозы не требуется. Отсутствуют данные по применению препарата у пациентов с тяжелой почечной недостаточностью (см. раздел «Фармакокинетика»).
Масса тела
Не требуется коррекции режима дозирования в зависимости от массы тела пациента (см. раздел «Фармакокинетика»).
Способ применения
Перед введением препарата следует осмотреть его на предмет наличия в растворе твердых частиц или появления нехарактерной окраски раствора. Если в препарате содержатся твердые частицы или у раствора появилась нехарактерная окраска, вводить препарат нельзя.
Раствор в предварительно заполненном шприце с системой защиты или предварительно заполненном шприце перед проведением инъекции препарата Дупиксент® должен нагреться до комнатной температуры. Для этого рекомендуется выдержать его при комнатной температуре в течение 45 мин (для дозировки 300 мг) или 30 мин (для дозировки 200 мг).
В случае необходимости предварительно заполненный шприц можно хранить при комнатной температуре (до 25 °С) в течение максимум 14 дней. Препарат нельзя хранить при температуре выше 25 °С. После извлечения из холодильника Дупиксент® должен быть использован в течение 14 дней или утилизирован.
Шприцы следует защищать от нагревания и воздействия прямого солнечного света.
Если начальная доза составляет 600 мг, следует сделать две инъекции по 300 мг в разные места для инъекций.
Если начальная доза составляет 400 мг, следует сделать две инъекции по 200 мг в разные места для инъекций.
Лечение препаратом Дупиксент® следует проводить под медицинским наблюдением. Инъекцию препарата может делать себе либо сам пациент, либо лицо, ухаживающее за ним.
Необходимо до начала применения препарата Дупиксент® обучить пациентов и/или ухаживающих за ними лиц подготовке и проведению инъекции препарата Дупиксент®, согласно указаниям в «Инструкции по подготовке и проведению инъекции препарата Дупиксент®, 300 мг в предварительно заполненном одноразовом шприце с системой защиты», «Инструкции по подготовкеи проведению инъекции препарата Дупиксент®, 300 мг в предварительно заполненном одноразовом шприце» и «Инструкции по подготовке и проведению инъекции препарата Дупиксент®, 200 мг в предварительно заполненном одноразовом шприце с системой защиты».
Препарат Дупиксент® может вводиться самим пациентом подкожно с помощью предварительно заполненного одноразового шприца в область бедра или живота, за исключением области диаметром 5 см непосредственно вокруг пупка. Если инъекцию проводит другой человек, препарат также можно вводить в верхнюю часть плеча.
Рекомендуется менять места инъекций при каждом введении препарата.
Инъекцию препарата Дупиксент® не следует проводить в участки с болезненной и поврежденной кожей, в места с кровоподтеками или рубцами.
Все остатки неиспользованного препарата и расходные материалы должны утилизироваться в соответствии с требованиями местного законодательства.
Побочное действие
Атопический дерматит
Для описания частоты встречаемости нежелательных реакций используется следующая классификация: очень часто ≥10%; часто ≥1% и <10%; нечасто ≥0,1% и <1%; редко ≥0,01% и <0,1%; очень редко <0,01%; частота неизвестна (невозможно определить по имеющимся данным частоту встречаемости нежелательной реакции).
Табл. 1. Нежелательные реакции, наблюдавшиеся в клинических исследованиях у пациентов с атопическим дерматитомa
| Системно-органный класс | Частота | Нежелательные реакции |
| Инфекционные и паразитарные заболевания | Часто | Конъюнктивит (4,0%) |
| Герпес ротовой полости (3,8%) | ||
| Бактериальный конъюнктивит (1,9%) | ||
| Простой герпес (Herpes simplex)b (1,7%) | ||
| Нарушения со стороны крови и лимфатической системы | Часто | Эозинофилия (1,7%) |
| Нарушения со стороны органа зрения | Часто | Аллергический конъюнктивит (7,0%) |
| Зуд в глазах (2,9%) | ||
| Блефарит (4,5%) | ||
| Синдром сухого глаза (1,8%) | ||
| Общие нарушения и нарушения в месте введения препарата | Очень часто | Реакции в месте инъекции (15,9%) |
a Объединенные данные плацебо-контролируемых клинических исследований с проведением монотерапии (SOLO 1, SOLO 2 и исследования по подбору доз 2 фазы) и плацебо-контролируемого исследования CHRONOS с одновременным применением топических ГКС для лечения атопического дерматита: пациенты получали препарат в дозе 300 мг 1 раз в 2 недели и 300 мг 1 раз в неделю с или без топических ГКС в течение 16 недель.
b В клинических исследованиях случаи с герпетическими инфекциями (Herpes simplex) проявлялись поражениями кожи и слизистых оболочек, обычно были легкой или средней степени тяжести и не включали герпетическую экзему. О случаях герпетической экземы сообщалось отдельно, частота таких случаев была ниже у пациентов, получавших препарат Дупиксент®, по сравнению с группой плацебо.
Профиль безопасности комбинированного лечения препаратом Дупиксент® + топические ГКС в течение 52 недель соответствует профилю его безопасности, наблюдавшемуся к 16-й неделе.
Бронхиальная астма
Табл. 2. Нежелательные реакции, наблюдавшиеся в клинических исследованиях у пациентов с бронхиальной астмой
| Системно-органный класс | Частота | Нежелательные реакции |
| Общие нарушения и нарушения в месте введения препарата | Очень часто | Эритема в месте инъекции (14,6%) |
| Часто | Отек в месте инъекции (4,8%) | |
| Часто | Зуд в месте инъекции (4,7%) | |
| Очень редко | Анафилаксия (0,04%) |
Описание отдельных нежелательных реакций
Конъюнктивит
За время 52-недельного периода лечения в клиническом исследовании с одновременным применением топических ГКС (CHRONOS) конъюнктивит был зарегистрирован в 16% случаев в группе пациентов, получавших Дупиксент® в дозе 300 мг 1 раз в 2 недели + топические ГКС (20 на 100 пациенто-лет), и в 9% случаев, в группе плацебо + топические ГКС (10 на 100 пациенто-лет). В клинических исследованиях у пациентов с бронхиальной астмой частота конъюнктивита была схожей в группах, получающих препарат Дупиксент® или плацебо.
Герпетическая экзема и Herpes zoster
В клинических исследованиях у пациентов с атопическим дерматитом частота герпетической экземы была схожей в группах, получающих препарат Дупиксент® и в группе плацебо. По данным 16-недельных исследований монотерапии, Herpes zoster был зарегистрирован в <0,1% случаев в группе, получающей Дупиксент® (<1 на 100 пациенто-лет) и <1% в группе плацебо (1 на 100 пациенто-лет). В 52-недельном клиническом исследовании с одновременным применением топических ГКС (CHRONOS) Herpes zoster был зарегистрирован в 1% случаев в группе, получающей Дупиксент® + топические ГКС (1 на 100 пациенто-лет) и в 2% в группе плацебо (2 на 100 пациенто-лет). В клинических исследованиях у пациентов с бронхиальной астмой частота Herpes zoster была схожей в группах, получающих препарат Дупиксент® или плацебо.
Гиперчувствительность
В клинических исследованиях при атопическом дерматите сообщалось об одном случае развития сывороточной болезни и одном случае реакции, подобной сывороточной болезни, после введения препарата Дупиксент® (оба нежелательных явления оценивались как серьезные). В исследовании при применении препарата при бронхиальной астме сообщалось об одном серьезном случае развития анафилаксии после введения препарата Дупиксент® (см. раздел «Особые указания»).
Эозинофилы
У пациентов, получавших препарат Дупиксент®, наблюдалось более высокое среднее начальное увеличение от исходного уровня эозинофилов по сравнению с пациентами, получавшими плацебо. Количество эозинофилов снижалось почти до базовых уровней во время исследования.
Частота эозинофилии, вызванной лечением (≥ 500 клеток/мкл), была сходной в группах пациентов, получавших препарат Дупиксент® и плацебо.
Эозинофилия, вызванная лечением (≥5000 клеток/мкл), была зарегистрирована менее чем у 2% пациентов, получавших препарат Дупиксент®, и менее чем у 0,5% пациентов, получавших плацебо.
Инфекции
В клинических исследованиях не наблюдалось увеличения общей частоты инфекций или серьезных инфекций во время лечения препаратом Дупиксент® по сравнению с плацебо. В 16-недельных клинических исследованиях, в которых проводилась монотерапия препаратом Дупиксент®, были зарегистрированы серьезные инфекции у 1,0% пациентов, получавших плацебо, и у 0,5% пациентов, получавших дупилумаб. В 52-недельном исследовании CHRONOS серьезные инфекции были зарегистрированы у 0,6% пациентов, получавших плацебо, и у 0,2% пациентов, получавших препарат Дупиксент®.
В клинических исследованиях у пациентов с бронхиальной астмой не наблюдалось увеличения общей частоты инфекций или серьезных инфекций во время лечения препаратом Дупиксент® по сравнению с плацебо. В 24-недельном клиническом исследовании были зарегистрированы серьезные инфекции у 1,0% пациентов, получавших дупилумаб, и у 1,1% пациентов, получавших плацебо. В 52-недельном исследовании QUEST серьезные инфекции были зарегистрированы у 1,3% пациентов, получавших дупилумаб, и у 1,4% пациентов, получавших плацебо.
Сердечно-сосудистые события
В 1-летнем плацебо контролируемом исследовании у пациентов с бронхиальной астмой (QUEST) сердечно-сосудистые тромбоэмболические события (сердечно-сосудистые смерти, нефатальные инфаркты миокарда и нефатальные инсульты) были зарегистрированы в 1 случае (0,2%) в группе пациентов, получавших Дупиксент® 200 мг 1 раз в 2 недели; в 4 случаях (0,6%) в группе пациентов, получавших Дупиксент® 300 мг 1 раз в 2 недели и в 2 случаях (0,3%) в группе плацебо. В 1-летнем плацебо контролируемом исследовании у пациентов с атопическим дерматитом (CHRONOS) сердечно-сосудистые тромбоэмболические события (сердечно-сосудистые смерти, нефатальные инфаркты миокарда и нефатальные инсульты) были зарегистрированы в 1 случае (0,9%) в группе пациентов, получавших Дупиксент® 300 мг 1 раз в 2 недели + топические ГКС; в 0 случаев (0,0%) в группе пациентов, Дупиксент® 300 мг 1 раз в неделю + топические ГКС и в 1 случае (0,3%) в группе плацебо + топические ГКС.
Иммуногенность
Как и все белковые лекарственные препараты, препарат Дупиксент® может вызывать аллергические реакции.
Примерно у 6% пациентов с атопическим дерматитом или бронхиальной астмой, которые получали препарат Дупиксент® в дозе 300 мг 1 раз в 2 недели в течение 52 недель, отмечалось образование антител против дупилумаба (АТ); приблизительно у 2% пациентов АТ стойко сохранялись и приблизительно 2% имели нейтрализующие антитела.
Примерно у 9% пациентов с бронхиальной астмой, которые получали препарат Дупиксент® в дозе 200 мг 1 раз в 2 недели в течение 52 недель, отмечалось образование антител против дупилумаба; приблизительно у 4% АТ стойко сохранялись и приблизительно 4% имели нейтрализующие антитела.
Приблизительно 5% пациентов в группах плацебо в 52-недельных исследованиях имели положительные антитела к препарату Дупиксент®; приблизительно у 2% АТ стойко сохранялись и приблизительно 1% имел нейтрализующие антитела.
Реакция образования антител обычно не влияла на системную экспозицию дупилумаба, безопасность или эффективность препарата. Менее чем у 0,4% пациентов были выявлены высокие титры антител к дупилумабу, ассоциирующиеся со снижением его системной экспозиции и эффективности. Кроме того, у одного пациента была обнаружена сывороточная болезнь, а у другого реакция, подобная сывороточной болезни (<0,1%), ассоциировавшиеся с высокими титрами антител (см. раздел «Особые указания»).
Наблюдаемая частота стойкого сохранения АТ и нейтрализующей активности в значительной степени зависят от чувствительности и специфичности используемого аналитического метода. Кроме того, наблюдаемая частота АТ-положительного статуса в анализе может зависеть от нескольких факторов, в том числе методики анализа, способа обработки проб, времени сбора проб, сопутствующих препаратов, а также статуса основного заболевания в каждом отдельном случае. По этим причинам сравнение частоты образования антител к дупилумабу с частотой выработки антител к другим препаратам может ввести в заблуждение.
Передозировка
В клинических исследованиях не было выявлено проблем, связанных с безопасностью, при однократном внутривенном введении доз до 12 мг/кг.
Специфического антидота при передозировке препаратом Дупиксент® не существует. В случае передозировки необходимо контролировать состояние пациента для своевременного выявления признаков и симптомов нежелательных явлений и незамедлительно назначать соответствующее симптоматическое лечение.
Взаимодействие с другими лекарственными средствами
Живые вакцины
Применение препарата Дупиксент® с живыми вакцинами не изучалось.
Во время лечения препаратом Дупиксент® не следует проводить вакцинацию живыми вакцинами.
Неживые (инактивированные) вакцины
Иммунные реакции на вакцинацию изучались в исследовании, в котором пациенты с атопическим дерматитом получали еженедельно препарат Дупиксент® в дозе 300 мг в течение 16 недель. После 12 недель терапии дупилумабом пациентов вакцинировали вакциной Tdap (Т-клеточно-зависимая, Adacel®) и менингококковой полисахаридной вакциной (Т-клеточно-независимая, Menomune®) и оценивали иммунные реакции по истечении 4 недель. У пациентов, получавших как дупилумаб, так и плацебо, реакции с образованием антител к противостолбнячной и менингококковой полисахаридной вакцинам были сходными. В этом исследовании не было обнаружено нежелательных взаимодействий между любой из этих неживых вакцин и дупилумабом.
Взаимодействие с субстратами изоферментов СУР450
В клиническом исследовании, проведенном у пациентов с атопическим дерматитом, оценивались эффекты дупилумаба на фармакокинетику субстратов изоферментов CYP. Данные, полученные в этом исследовании, не указывают на клинически значимое влияние дупилумаба на активность изоферментов CYP1A2, CYP3A, CYP2C19, CYP2D6 или CYP2C9.
Взаимодействие с другими лекарственными средствами для лечения бронхиальной астмы
Влияние дупилумаба на фармакокинетику одновременно назначаемых препаратов не ожидается. Данные, полученные на основании популяционного анализа, не указывают на влияние одновременно назначаемых препаратов на фармакокинетику дупилумаба у пациентов со среднетяжелым или тяжелым течением бронхиальной астмы.
Особые указания
Гиперчувствительность
При возникновении системной реакции гиперчувствительности лечение препаратом Дупиксент® должно быть немедленно прекращено, и начата соответствующая терапия. В клинических исследованиях при применении препарата Дупиксент® при атопическом дерматите сообщалось об одном случае развития реакции, подобной сывороточной болезни, и одном случае развития сывороточной болезни после введения препарата (обе нежелательные реакции расценивались как серьезные). В исследовании при применении препарата при бронхиальной астме сообщалось об одном случае развития анафилаксии после введения препарата Дупиксент® (см. раздел «Побочное действие»).
Конъюнктивит
Конъюнктивит чаще встречался у пациентов с атопическим дерматитом, получавших препарат Дупиксент®. Большинство пациентов с конъюнктивитом выздоровели или выздоравливали в течение периода лечения. Среди пациентов с бронхиальной астмой частота конъюнктивита была низкой и сходной в группах, получавших препарат Дупиксент® и плацебо. Пациенты должны сообщать о первом появлении или ухудшении симптомов со стороны глаз своему лечащему врачу.
Эозинофильные состояния
У пациентов с бронхиальной астмой может развиться серьезная системная эозинофилия, иногда в виде клинических признаков эозинофильной пневмонии или васкулита, соответствующих эозинофильному гранулематозу с полиангиитом, которые часто лечатся системными кортикостероидами. Эти события, как правило, но не всегда, могут быть связаны с сокращением приема пероральных кортикостероидов. Врачи должны быть внимательны к васкулитной сыпи, ухудшающимся легочным симптомам, сердечным осложнениям и/или нейропатии, возникающим у их пациентов с эозинофилией. Сообщалось о случаях эозинофильной пневмонии и васкулита, соответствующих эозинофильному гранулематозу с полиангиитом, при применении препарата Дупиксент® у взрослых пациентов, которые участвовали в клиническом исследовании препарата при бронхиальной астме. Связь между применением препарата Дупиксент® и этими состояниями не была установлена.
Симптомы обострения бронхиальной астмы или ухудшающееся состояние
Препарат Дупиксент® не следует назначать для лечения симптомов остро возникшего ухудшения или обострений астмы. Препарат Дупиксент® не применяется для лечения острого бронхоспазма или астматического статуса.
Снижение дозы глюкокортикостероидов
Не следует резко прерывать применение системных, местных или ингаляционных глюкокортикостероидов после начала терапии препаратом Дупиксент®. Сокращение дозы глюкокортикостероидов, при необходимости, должно быть постепенным и должно выполняться под непосредственным наблюдением врача. Уменьшение дозы глюкокортикостероидов может сопровождаться системными симптомами отмены и/или манифестацией состояний, которые ранее не проявлялись из-за системной терапии глюкокортикостероидами.
Гельминтозы (глистные инвазии)
Пациенты с обнаруженным гельминтозом не включались в клинические исследования. Неизвестно, может ли препарат Дупиксент® повлиять на иммунный ответ при гельминтозах. Необходимо провести лечение пациентов с имеющимся гельминтозом перед тем, как начинать лечение препаратом Дупиксент®. Если во время лечения препаратом Дупиксент® пациент заражается гельминтозом, а антигельминтные препараты оказываются неэффективными, следует прекратить лечение препаратом Дупиксент® до излечения паразитарного заболевания.
Сопутствующие атопические заболевания
Пациентам с атопическим дерматитом и с сопутствующей бронхиальной астмой следует рекомендовать не изменять своего лечения, не проконсультировавшись с лечащим врачом. Прекращая лечение препаратом Дупиксент®, следует принимать во внимание возможные эффекты на течение других атопических заболеваний.
Влияние на способность управлять транспортными средствами и механизмами
Препарат Дупиксент® не оказывает или оказывает незначительное влияние на способность управлять транспортными средствами и работать с другими механизмами.
Форма выпуска
Раствор для подкожного введения, 150 мг/мл, 175 мг/мл.
Для дозировки 150 мг/мл:
По 2,00 мл в одноразовый шприц/шприц с системой защиты из прозрачного стекла (тип I), снабженный несъемной иглой из нержавеющей стали, защищенной колпачком из мягкого эластомера с/без твердой крышкой(-и).
По 1 или 2 шприца/шприца с системой защиты с инструкцией по применению в картонную пачку с заклеенными клапанами.
Или
По 2 шприца/шприца с системой защиты в промежуточную картонную упаковку, по 3 промежуточных картонных упаковки с инструкцией по применению в картонную пачку с заклеенными клапанами.
На каждую картонную пачку нанесен анти контрафактный стикер.
Для дозировки 175 мг/мл:
По 1,14 мл в одноразовый шприц с системой защиты из прозрачного стекла (тип I), снабженный несъемной иглой из нержавеющей стали, защищенной колпачком из мягкого эластомера с/без твердой крышкой(-и).
По 1 или 2 шприца с системой защиты с инструкцией по применению в картонную пачку с заклеенными клапанами.
Или
По 2 шприца с системой защиты в промежуточную картонную упаковку, по 3 промежуточных картонных упаковки с инструкцией по применению в картонную пачку с заклеенными клапанами.
На каждую картонную пачку нанесен анти контрафактный стикер.
Условия хранения
Хранить при температуре от 2 до 8 °С в оригинальной упаковке для защиты от света. Не замораживать.
Хранить в недоступном для детей месте.
Срок годности
Для дозировки 150 мг/мл – 24 мес.
Для дозировки 175 мг/мл – 18 мес.
Не использовать после окончания срока годности, указанного на упаковке.
Условия отпуска
Отпускают по рецепту.
Юридическое лицо, на имя которого выдано регистрационное удостоверение
АО Санофи-авентис груп, Франция.
Производитель
Санофи Винтроп Индустрия, Франция (150 мг/мл, 175 мг/мл; шприцы, шприцы с системой защиты)
Кук Фармика ЛЛС, США (150 мг/мл; шприцы)
Фасовщик (первичная упаковка)
Санофи Винтроп Индустрия, Франция (150 мг/мл, 175 мг/мл; шприцы, шприцы с системой защиты)
Кук Фармика ЛЛС, США (150 мг/мл; шприцы)
Упаковщик (вторичная (потребительская) упаковка)
Санофи Винтроп Индустрия, Франция (150 мг/мл, 175 мг/мл; шприцы, шприцы с системой защиты)
Кук Фармика ЛЛС, США (150 мг/мл; шприцы)
Выпускающий контроль качества
Санофи-Авентис Дойчланд ГмбХ, Германия (150 мг/мл, 175 мг/мл; шприцы, шприцы с системой защиты)
Sanofi-Aventis Deutschland GmbH, Germany.
Industriepark Hoechst – Brueningstrasse 50
H500, H590, H600 65926 Frankfurt am Main, Germany.
Санофи Винтроп Индустрия, Франция (150 мг/мл, 175 мг/мл; шприцы, шприцы с системой защиты)
Sanofi Winthrop Industrie, France.
1051 boulevard Industriel 76580 Le Trait, France.
Претензии потребителей направлять по адресу в России:
АО «Санофи Россия».
125009, г. Москва, ул. Тверская, 22.
В случае использования одноразового шприца с системой защиты, содержащего 300 мг препарата Дупиксент®, к инструкции по медицинскому применению лекарственного препарата прилагается «Инструкция по подготовке и проведению инъекции препарата Дупиксент®, 300 мг в предварительно заполненном одноразовом шприце с системой защиты»
Инструкция по подготовке и проведению инъекции препарата Дупиксент®, 300 мг в предварительно заполненном одноразовом шприце с системой защиты
Перед началом применения препарата Дупиксент® в предварительно заполненном одноразовом шприце с системой защиты внимательно прочитайте эту инструкцию.
Элементы предварительно заполненного одноразового шприца с системой защиты показаны на рисунке ниже:
Данное устройство представляет собой предварительно заполненный одноразовый шприц с системой защиты (далее называется «шприц»). В нём содержится раствор для подкожного введения, содержащий 300 мг препарата Дупиксент®.
Важная информация
- Не пытайтесь провести инъекцию самостоятельно или с помощью кого-то до тех пор, пока лечащий врач или медицинский работник не обучат Вас правильной технике проведения подкожной инъекции.
- Перед использованием шприца внимательно прочитайте информацию по его использованию.
- Узнайте у своего лечащего врача, как часто Вам необходимо проводить инъекции препарата Дупиксент®.
- Попросите своего лечащего врача или медицинского работника показать, как правильно пользоваться шприцем, перед тем как в первый раз самостоятельно провести инъекцию препарата Дупиксент®.
- Рекомендуется менять место инъекции при каждом введении препарата.
- Не используйте шприц, если он упал на твердую поверхность или поврежден.
- Нельзя использовать шприц, если отсутствует колпачок иглы, или он не был надежно зафиксирован.
- Не дотрагивайтесь до штока поршня до тех пор, пока вы не будете готовы провести инъекцию.
- Не проводите инъекции через одежду.
- Не пытайтесь удалить воздушные пузырьки из шприца.
- Для того чтобы снизить риск случайного укола иглой, каждый предварительно заполненный одноразовый шприц оборудован устройством безопасности с системой защиты, которое автоматически активируется, закрывая иглу, после того, как Вы провели инъекцию.
- Не тяните шток поршня назад.
- Шприц не подлежит повторному использованию.
Как хранить шприц
- Храните шприцы в недоступном для детей месте.
- Храните неиспользуемые шприцы в оригинальной картонной упаковке в холодильнике при температуре от 2 °С до 8 °С.
- После извлечения из холодильника, шприц следует оставить на 45 мин при комнатной температуре и дать возможность ему нагреться перед тем, как делать инъекцию препарата Дупиксент®.
- Шприцы можно хранить при комнатной температуре в течение не более чем 14 дней.
- Не встряхивайте шприц.
- Не подвергайте шприц тепловому воздействию.
- Не замораживайте шприц.
- Не допускайте воздействия на шприц прямых солнечных лучей.
Шаг 1: Извлечение шприца из упаковки
Извлеките шприц из картонной упаковки, взяв его за середину корпуса.
Не снимайте колпачок иглы до момента проведения инъекции.
Нельзя использовать шприц, если он упал на твёрдую поверхность или повреждён.
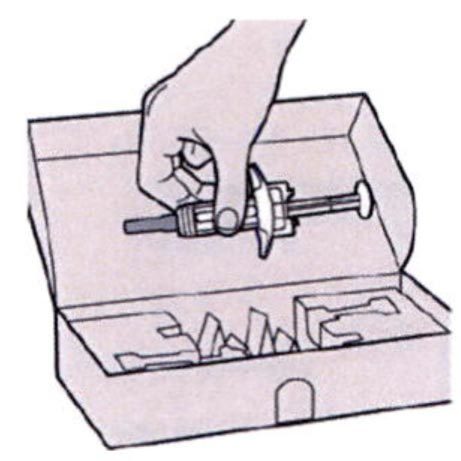
Шаг 2: Подготовка
Убедитесь, что у Вас есть все необходимое для проведения инъекции:
— предварительно заполненный шприц;
— 1 салфетка, смоченная спиртом;*
— 1 ватный тампон или марлевая салфетка;*
— устойчивый к проколам контейнер* (см. Шаг 12).
* не содержатся в картонной упаковке.
Внимательно проверьте маркировку:
— проверьте дату истечения срока годности;
— убедитесь в том, что у Вас правильный препарат и правильная доза.
Нельзя использовать шприц после истечения срока годности, указанного на этикетке.
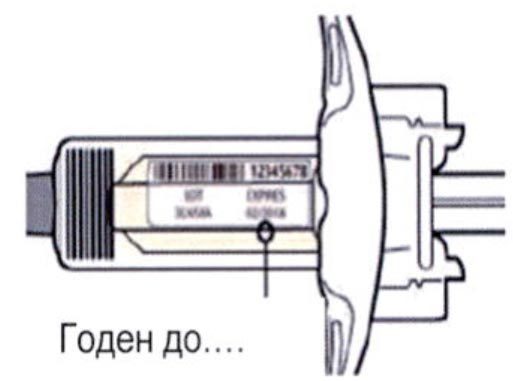
Шаг 3. Проверка
Осмотрите раствор через смотровое окно на шприце: проверьте, является ли раствор прозрачным, является ли жидкость бесцветной или имеющей светло-желтый оттенок.
Примечание: Вы можете обнаружить воздушные пузырьки, это нормально.
Нельзя использовать шприц, если жидкость изменила цвет или помутнела, или если в ней есть заметные хлопья или частицы.
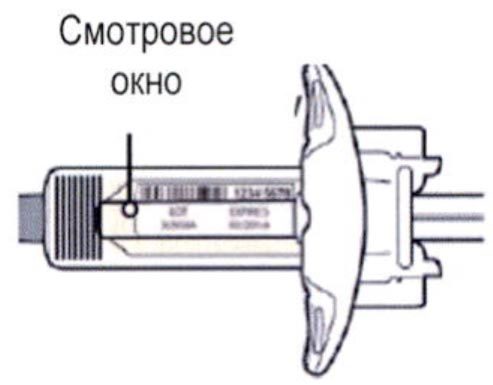
Шаг 4: Подождите 45 мин
Положите шприц на плоскую поверхность, не менее чем на 45 мин, пусть шприц нагреется до комнатной температуры.
Не нагревайте шприц.
Не подвергайте шприц прямому воздействию солнечных лучей.
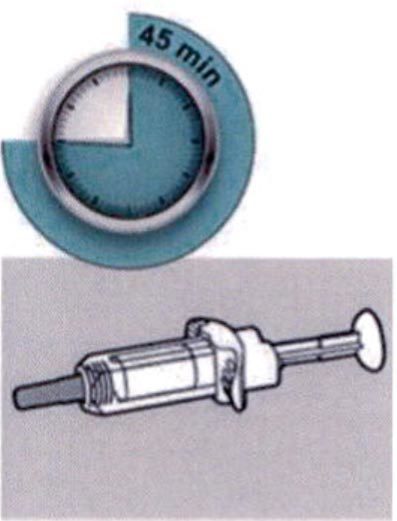
Шаг 5: Выбор места инъекции
Выберите место инъекции.
— Вы можете сделать инъекцию в наружную поверхность бедра или в переднюю часть живота, за исключением области диаметром 5 см непосредственно вокруг пупка.
— Если инъекцию осуществляет другой человек, для инъекции также можно использовать участок кожи в верхней части плеча.
Инъекции препарата Дупиксент® не следует осуществлять на участках с болезненной или поврежденной кожей, кровоподтеками или рубцами.

Шаг 6: Обработка места инъекции
- Вымойте руки.
- Протрите участок кожи, предназначенный для инъекции салфеткой, смоченной спиртом.
- Дайте коже высохнуть перед проведением инъекции.
Не дотрагивайтесь до обработанного участка кожи руками и не дуйте на него перед проведением инъекции.
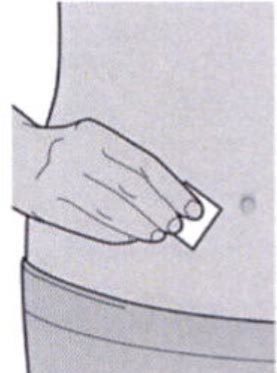
Шаг 7: Удаление колпачка иглы
Держите шприц за середину корпуса, игла должна быть направлена в сторону от Вас, и снимите колпачок с иглы.
Не надевайте колпачок обратно на иглу.
Не касайтесь иглы.
Лекарственный препарат необходимо ввести сразу же после удаления колпачка иглы.
Шаг 8: Формирование складки кожи
Сформируйте складку кожи в месте инъекции, как показано на рисунке.
Шаг 9: Введение иглы
Полностью введите иглу в сформированную складку кожи под углом приблизительно 45°.
Шаг 10: Введение раствора
Ослабьте сформированную складку кожи.
Медленно и непрерывно нажимайте на шток поршня для введения всего раствора, пока шприц не опустеет.
Примечание: Вы почувствуете некоторое сопротивление. Это нормально.
Шаг 11: Завершение инъекции и извлечение иглы
Поднимите большой палец, снимая давление со штока поршня, игла будет втянута внутрь защитного колпачка для иглы, а затем удалите шприц из места инъекции.
Слегка прижмите ватный тампон или марлевую салфетку к месту инъекции, если Вы заметите кровь.
Не надевайте колпачок иглы снова на иглу.
Не растирайте кожу после инъекции.
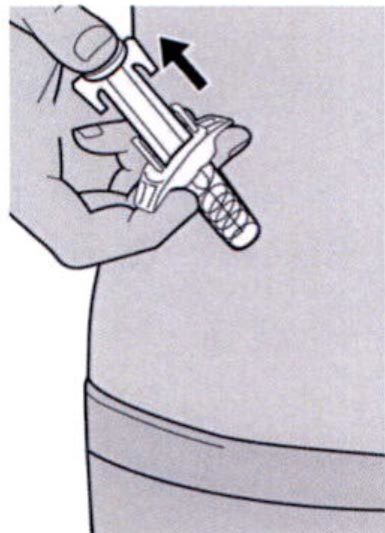
Шаг 12: Утилизация
После использования следует поместить шприц и колпачок иглы в устойчивый к проколам контейнер.
Не надевайте колпачок иглы снова на иглу.
Храните контейнер в недоступном для детей месте.
В случае использования одноразового шприца, содержащего 300 мг препарата Дупиксент®, к инструкции по медицинскому применению лекарственного препарата прилагается «Инструкция по подготовке и проведению инъекции препарата Дупиксент®, 300 мг в предварительно заполненном одноразовом шприце»
Инструкция по подготовке и проведению инъекции препарата Дупиксент®, 300 мг в предварительно заполненном одноразовом шприце
Перед началом применения препарата Дупиксент® в предварительно заполненном одноразовом шприце внимательно прочитайте эту инструкцию. Элементы предварительно заполненного шприца показаны на рисунке ниже:
* Шприц может иметь твердый или мягкий колпачок иглы.
Данное устройство представляет собой предварительно заполненный одноразовый шприц (далее называется «шприц»). В нём содержится раствор для подкожного введения, содержащий 300 мг препарата Дупиксент®.
Важная информация
- Не пытайтесь провести инъекцию самостоятельно или с помощью кого-то до тех пор, пока лечащий врач или медицинский работник не обучат Вас правильной технике проведения подкожной инъекции.
- Перед использованием шприца внимательно прочитайте информацию по его использованию.
- Узнайте у своего лечащего врача, как часто Вам необходимо проводить инъекции препарата Дупиксент®.
- Попросите своего лечащего врача или медицинского работника показать, как правильно пользоваться шприцем, перед тем как в первый раз самостоятельно провести инъекцию препарата Дупиксент®.
- Рекомендуется менять место инъекции при каждом введении препарата.
- Не используйте шприц, если он поврежден.
- Нельзя использовать шприц, если отсутствует колпачок иглы или он не был надежно зафиксирован.
- Не дотрагивайтесь до штока поршня до тех пор, пока Вы не будете готовы провести инъекцию.
- Не проводите инъекции через одежду.
- Не пытайтесь удалить воздушные пузырьки из шприца.
- Не тяните шток поршня назад.
- Шприц не подлежит повторному использованию.
Как хранить шприц
- Храните шприцы в недоступном для детей месте.
- Храните неиспользуемые шприцы в оригинальной картонной упаковке в холодильнике при температуре от 2 °С до 8 °С.
- После извлечения из холодильника, шприц следует оставить на 45 мин при комнатной температуре и дать возможность ему нагреться перед тем, как проводить инъекцию препарата Дупиксент®.
- Шприцы можно хранить при комнатной температуре в течение не более чем 14 дней.
- Не встряхивайте шприц.
- Не подвергайте шприц тепловому воздействию.
- Не замораживайте шприц.
- Не допускайте воздействия на шприц прямых солнечных лучей.
Шаг 1: Извлечение шприца из упаковки
Извлеките шприц из картонной упаковки, взяв его за середину корпуса.
Не снимайте колпачок иглы до момента проведения инъекции.
Нельзя использовать шприц, если он был повреждён.
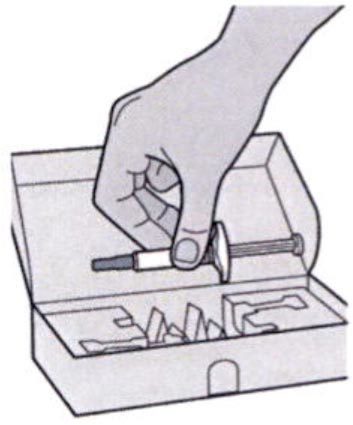
Шаг 2: Подготовка
Убедитесь, что у Вас есть все необходимое для проведения инъекции:
— предварительно заполненный шприц;
— 1 салфетка, смоченная спиртом;*
— 1 ватный тампон или марлевая салфетка;*
— устойчивый к проколам контейнер* (см. Шаг 12).
* не содержатся в картонной упаковке.
Внимательно проверьте маркировку:
— проверьте дату истечения срока годности;
— убедитесь в том, что у Вас правильный препарат и правильная доза.
Нельзя использовать шприц после истечения срока годности, указанного на этикетке.
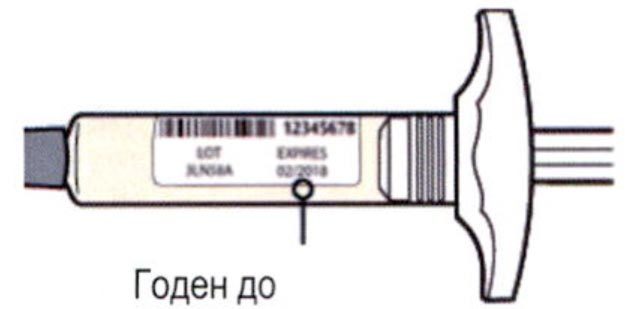
Шаг 3. Проверка
Осмотрите раствор в шприце: проверьте, является ли раствор прозрачным, является ли жидкость бесцветной или имеющей светло-желтый оттенок. Примечание: Вы можете обнаружить воздушные пузырьки, это нормально.
Нельзя использовать шприц, если жидкость изменила цвет или помутнела, или если в ней есть заметные хлопья или частицы.
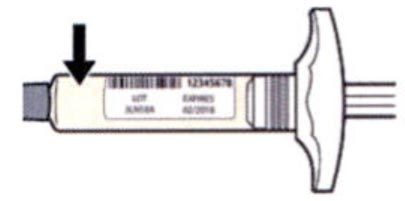
Шаг 4: Подождите 45 мин
Положите шприц на плоскую поверхность, не менее чем на 45 мин, пусть шприц нагреется до комнатной температуры.
Не нагревайте шприц.
Не подвергайте шприц прямому воздействию солнечных лучей. Шприц нельзя хранить при комнатной температуре более 14 дней.
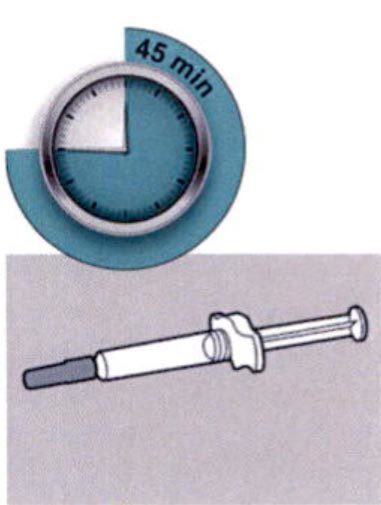
Шаг 5: Выбор места инъекции
Выберите место инъекции.
— Вы можете сделать инъекцию в наружную поверхность бедра или в переднюю часть живота, за исключением области диаметром 5 см непосредственно вокруг пупка.
— Если инъекцию осуществляет другой человек, для инъекции также можно использовать участок кожи в верхней части плеча.
Инъекции препарата Дупиксент® не следует осуществлять на участках с болезненной или поврежденной кожей, кровоподтеками или рубцами.

Этап 6: Обработка участка инъекции
- Вымойте руки.
- Протрите участок кожи, предназначенный для инъекции салфеткой, смоченной спиртом.
- Дайте коже высохнуть перед проведением инъекции.
Не дотрагивайтесь до обработанного участка кожи руками и не дуйте на него перед проведением инъекции.
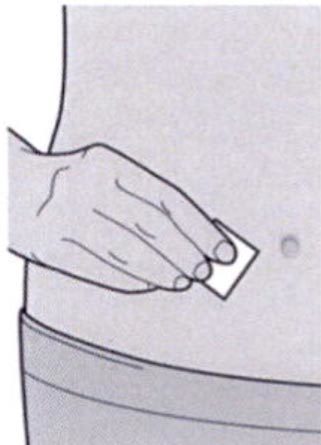
Шаг 7: Удаление колпачка иглы
Держите шприц за середину корпуса, игла должна быть направлена в сторону от Вас, и снимите колпачок иглы.
Не надевайте колпачок иглы обратно на иглу.
Не касайтесь иглы.
Лекарственный препарат необходимо ввести сразу же после удаления колпачка иглы.
Шаг 8: Формирование складки кожи
Сформируйте складку кожи на участке инъекции, как показано на рисунке.
Шаг 9: Введение иглы
Полностью введите иглу в сформированную складку под углом приблизительно 45°.
Шаг 10: Введение раствора
Ослабьте сформированную складку кожи.
Медленно и непрерывно нажимайте на шток поршня для введения всего раствора, пока шприц не опустеет.
Примечание: Вы почувствуете некоторое сопротивление. Это нормально.
Шаг 11: Извлечение иглы
Извлеките иглу из кожи под тем же углом, под которым она была введена.
Не надевайте колпачок иглы снова на иглу.
Слегка прижмите ватный тампон или марлевую салфетку к месту инъекции, если Вы заметите кровь.
Не растирайте кожу после инъекции.
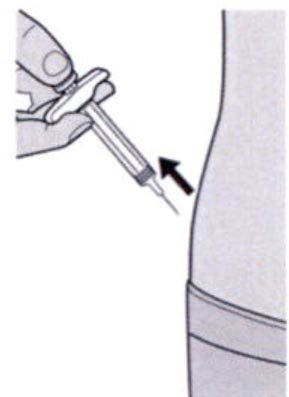
Шаг 12: Утилизация
После использования следует поместить шприц и колпачок иглы в устойчивый к проколам контейнер.
Не надевайте колпачок иглы снова на иглу.
Храните контейнер в недоступном для детей месте.
В случае использования одноразового шприца с системой защиты, содержащего 200 мг препарата Дупиксент®, к инструкции по медицинскому применению лекарственного препарата прилагается «Инструкция по подготовке и проведению инъекции препарата Дупиксент®, 200 мг в предварительно заполненном одноразовом шприце с системой защиты»
Инструкция по подготовке и проведению инъекции препарата Дупиксент®, 200 мг в предварительно заполненном одноразовом шприце с системой защиты
Перед началом применения препарата Дупиксент® в предварительно заполненном одноразовом шприце с системой защиты внимательно прочитайте эту инструкцию.
Элементы предварительно заполненного одноразового шприца с системой защиты показаны на рисунке ниже:
Данное устройство представляет собой предварительно заполненный одноразовый шприц с системой защиты (далее называется «шприц»). В нём содержится раствор для подкожного введения, содержащий 200 мг препарата Дупиксент®.
Важная информация
- Не пытайтесь провести инъекцию самостоятельно или с помощью кого-то до тех пор, пока лечащий врач или медицинский работник не обучат Вас правильной технике проведения подкожной инъекции.
- Перед использованием шприца внимательно прочитайте информацию по его использованию.
- Узнайте у своего лечащего врача, как часто Вам необходимо проводить инъекции препарата Дупиксент®.
- Попросите своего лечащего врача или медицинского работника показать, как правильно пользоваться шприцем, перед тем как в первый раз самостоятельно провести инъекцию препарата Дупиксент®.
- Рекомендуется менять место инъекции при каждом введении препарата.
- Не используйте шприц, если он упал на твердую поверхность или поврежден.
- Нельзя использовать шприц, если отсутствует колпачок иглы, или он не был надежно зафиксирован.
- Не дотрагивайтесь до штока поршня до тех пор, пока вы не будете готовы провести инъекцию.
- Не проводите инъекции через одежду.
- Не пытайтесь удалить воздушные пузырьки из шприца.
- Для того чтобы снизить риск случайного укола иглой, каждый предварительно заполненный одноразовый шприц оборудован устройством безопасности с системой защиты, которое автоматически активируется, закрывая иглу, после того, как Вы провели инъекцию.
- Не тяните шток поршня назад.
- Шприц не подлежит повторному использованию.
Как хранить шприц
- Храните шприцы в недоступном для детей месте.
- Храните неиспользуемые шприцы в оригинальной картонной упаковке в холодильнике при температуре от 2 °С до 8 °С.
- После извлечения из холодильника, шприц следует оставить на 30 мин при комнатной температуре и дать возможность ему нагреться перед тем, как делать инъекцию препарата Дупиксент®.
- Шприцы можно хранить при комнатной температуре в течение не более чем 14 дней.
- Не встряхивайте шприц.
- Не подвергайте шприц тепловому воздействию.
- Не замораживайте шприц.
- Не допускайте воздействия на шприц прямых солнечных лучей.
Шаг 1: Извлечение шприца из упаковки
Извлеките шприц из картонной упаковки, взяв его за середину корпуса.
Не снимайте колпачок иглы до момента проведения инъекции.
Нельзя использовать шприц, если он упал на твёрдую поверхность или повреждён.
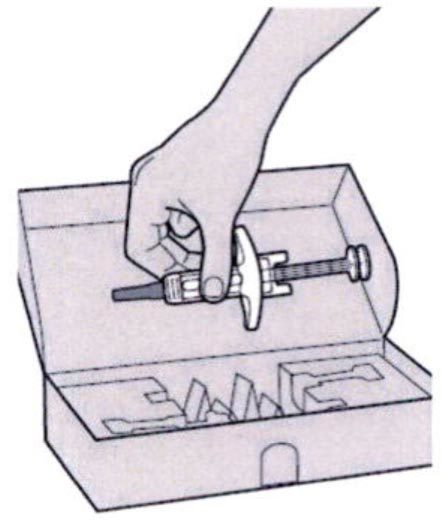
Шаг 2: Подготовка
Убедитесь, что у Вас есть все необходимое для проведения инъекции:
— предварительно заполненный шприц;
— 1 салфетка, смоченная спиртом;*
— 1 ватный тампон или марлевая салфетка;*
— устойчивый к проколам контейнер* (см. Шаг 12).
* не содержатся в картонной упаковке.
Внимательно проверьте маркировку:
— проверьте дату истечения срока годности;
— убедитесь в том, что у Вас правильный препарат и правильная доза.
Нельзя использовать шприц после истечения срока годности, указанного на этикетке.
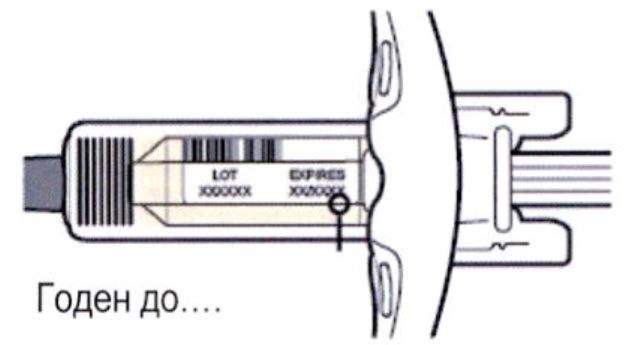
Шаг 3. Проверка
Осмотрите раствор через смотровое окно на шприце: проверьте, является ли раствор прозрачным, является ли жидкость бесцветной или имеющей светло-желтый оттенок.
Примечание: Вы можете обнаружить воздушные пузырьки, это нормально.
Нельзя использовать шприц, если жидкость изменила цвет или помутнела, или если в ней есть заметные хлопья или частицы.
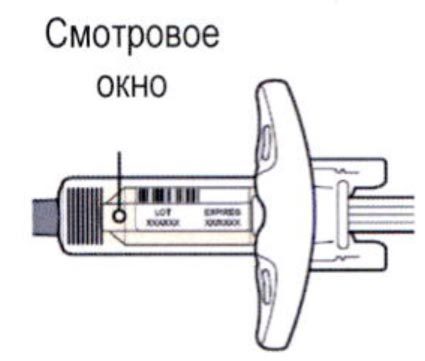
Шаг 4: Подождите 30 мин
Положите шприц на плоскую поверхность, не менее чем на 30 мин, пусть шприц нагреется до комнатной температуры.
Не нагревайте шприц.
Не подвергайте шприц прямому воздействию солнечных лучей.
Шприц нельзя хранить при комнатной температуре более 14 дней.
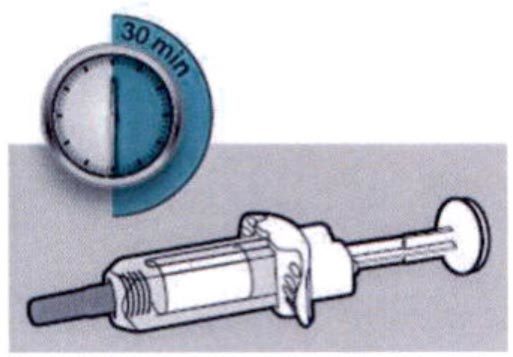
Шаг 5: Выбор места инъекции
Выберите место инъекции.
— Вы можете сделать инъекцию в наружную поверхность бедра или в переднюю часть живота, за исключением области диаметром 5 см непосредственно вокруг пупка.
— Если инъекцию осуществляет другой человек, для инъекции также можно использовать участок кожи в верхней части плеча.
Инъекции препарата Дупиксент® не следует осуществлять на участках с болезненной или поврежденной кожей, кровоподтеками или рубцами.

Шаг 6: Обработка места инъекции
- Вымойте руки.
- Протрите участок кожи, предназначенный для инъекции салфеткой, смоченной спиртом.
- Дайте коже высохнуть перед проведением инъекции.
Не дотрагивайтесь до обработанного участка кожи руками и не дуйте на него перед проведением инъекции.
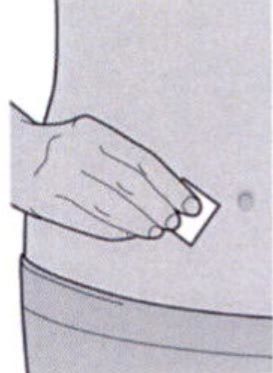
Шаг 7: Удаление колпачка иглы
Держите шприц за середину корпуса, игла должна быть направлена в сторону от Вас, и снимите колпачок с иглы.
Не надевайте колпачок обратно на иглу.
Не касайтесь иглы.
Лекарственный препарат необходимо ввести сразу же после удаления колпачка иглы.
Шаг 8: Формирование складки кожи
Сформируйте складку кожи в месте инъекции, как показано на рисунке.
Шаг 9: Введение иглы
Полностью введите иглу в сформированную складку кожи под углом приблизительно 45°.
Шаг 10: Введение раствора
Ослабьте сформированную складку кожи.
Медленно и непрерывно нажимайте на шток поршня для введения всего раствора, пока шприц не опустеет.
Примечание: Вы почувствуете некоторое сопротивление. Это нормально.
Шаг 11: Завершение инъекции и извлечение иглы
Поднимите большой палец, снимая давление со штока поршня, игла будет втянута внутрь защитного колпачка для иглы, а затем удалите шприц из места инъекции.
Слегка прижмите ватный тампон или марлевую салфетку к месту инъекции, если Вы заметите кровь.
Не надевайте колпачок иглы снова на иглу.
Не растирайте кожу после инъекции.
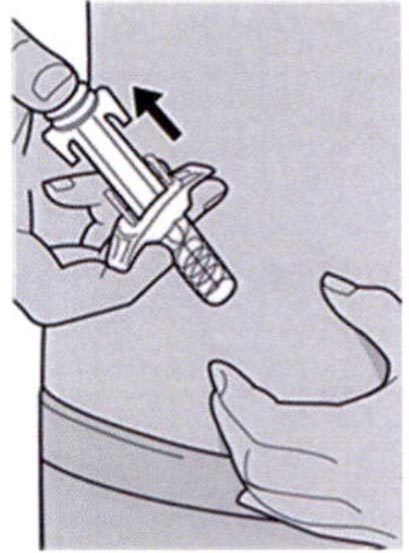
Шаг 12: Утилизация
После использования следует поместить шприц и колпачок иглы в устойчивый к проколам контейнер.
Не надевайте колпачок иглы снова на иглу.
Храните контейнер в недоступном для детей месте.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Сергиев Посад-6, 1А, Сергиево-Посадский р-н, МО (на въезде в Военный городок, на территории рынка)
г.Сергиев Посад, площадь Красногорская, д. 1
Никольская ул, 10, Москва
г.Жуковский, Чкалова, д. 41
Курыжова, 7, Южный мкр, Домодедово, МО
Энтузиастов ш, 3 к 1, Москва
Семеновская пл, 7 к 17А, Москва
Юшуньская малая. ул, 3, Москва
Нахимовский пр, 22, Москва
Шелепихинская наб, 34 к 2, Москва
Армавирская ул, 3, Москва
Пресненский Вал ул, 7c1, Москва
Авиаконструктора Миля ул, 4А, Москва
Новоугличское ш, 46, Сергиево-Посадский р-н, Сергиев Посад, МО
Вучетича ул, 22, Москва
г.Москва, Михайлова, д. 8, корп. 1
Рижское ш, 41А, Волоколамск, МО
Ласточкин пр-д, 16, Балашиха, МО
Маршала Жукова пр, 49, Москва
Рязанский пр, 71к1, Москва