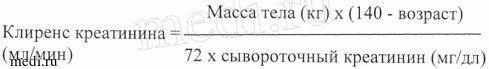ОДОБРЕНО
Совет по ветеринарным препаратам
протокол от «1» июля 2020 г. N 109.
ИНСТРУКЦИЯ
по применению ветеринарного препарата «Цефапик LA»
1 ОБЩИЕ СВЕДЕНИЯ
1.1 Цефапик LA (Сefapiсum LA).
Международное непатентованное наименование активной фармацевтической субстанции: цефтиофур.
1.2 Цефапик LA представляет собой суспензию белого или кремового цвета.
В 1,0 мл препарата содержится 100 мг цефтиофура (в форме кристаллической свободной цефтиофуровой кислоты), вспомогательные вещества: миглиол, хлопковое масло, стеариновая кислота, спирт бензиловый.
Лекарственная форма: суспензия для инъекций.
1.3 Препарат выпускают в стеклянных флаконах по 50, 100, 200 мл и полимерных флаконах по 100 мл.
1.4 Цефапик LA хранят по списку Б при температуре от плюс 5°С до плюс 25 °С в защищенном от света месте.
Срок годности – 2 (два) года от даты изготовления при соблюдении условий хранения. После вскрытия флакона препарат необходимо использовать в течение 28 дней. Не применять по истечению срока годности. Хранить в местах, недоступных для детей.
2 ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА
2.1 Цефапик LA – антибактериальный препарат из группы цефалоспоринов третьего поколения. Препарат активен в отношении многих грамположительных и грамотрицательных микроорганизмов, включая некоторые анаэробные бактерии и штаммы, продуцирующие β-лактамазу, и некоторых анаэробных бактерий: Escherichia coli, Pasteurella multocida, Mannheimia haemolytica, Haemophilus somnus, Actinobacillus pleuropneumoniae, Haemophilus parasuis, Salmonella spp., Streptococcus spp., Pasteurella spp., Staphylococcus spp., Actinomyces (Truepella) pyogenes, Klebsiela spp., Citrobacter spp., Enterobacter spp., Bacillus spp., Proteus spp., Fusobacterium necrophorum и Porphyromonas asaccharolytica, Porphlromonas levii. .
2.2 Цефтиофур обладает антибактериальным действием. Механизм действия заключается в ингибировании фермента транспептидазы и нарушении синтеза пептидогликана – мукопептида клеточной оболочки, что приводит к нарушению роста клеточной стенки микроорганизма и лизису бактерий.
2.3 После введения Цефапик LA быстро резорбируется с места инъекции. Цефтиофур в организме метаболизируется с образованием десфуроилцефтиофура, который оказывает антибактериальное действие.
У свиней максимальная концентрация антибиотика в плазме крови наблюдается через 22 часа после введения препарата и сохраняется не менее 7 суток. Выделение препарата из организма происходит главным образом с мочой (около 60 %) и с фекалиями (около 15 %) в течение 10 дней после введения.
У крупного рогатого скота максимальная концентрация препарата в плазме крови достигается через 12 часов после введения препарата и сохраняется на терапевтическом уровне не менее 7 суток. Выделение препарата из организма происходит главным образом с мочой (свыше 70 %) и с фекалиями (12-15 %).
3 ПОРЯДОК ПРИМЕНЕНИЯ
3.1 Цефапик LA применяют свиньям при респираторных инфекциях бактериальной этиологии, септицемии, полиартритах, сальмонеллезе, гемофилезном полисерозите, пастереллезе; крупному рогатому скоту – при респираторных инфекциях бактериальной этиологии, некробактериозе, послеродовом метрите, а также при других болезнях, вызванных микроорганизмами, чувствительными к цефтиофуру.
3.2 Перед применением флакон с препаратом встряхивают до получения однородной суспензии (максимальный объем для введения в одно место не должен превышать 15 мл).
Цефапик LA применяют однократно:
– свиньям: внутримышечно, в дозе 1 мл препарата на 20 кг массы тела животного (5 мг цефтиофура на 1 кг массы тела животного);
– крупному рогатому скоту: подкожно, в дозе 1 мл на 15 кг массы тела животного (6,6 мг цефтиофура на 1 кг массы тела животного).
Допускается применять Цефапик LA крупному рогатому скоту внутримышечно, в дозе 1 мл на 100 кг массы тела животного (1 мг цефтиофура на 1 кг массы тела животного) в течение 3-5 дней.
3.3 Запрещается применять препарат при индивидуальной чувствительности животных к компонентам препарата.
3.4 Симптомы передозировки препарата не установлены.
3.5 При применении препарата в соответствии с инструкцией побочных явлений и осложнений, как правило, не отмечается. В отдельных случаях возможно образование припухлости в месте введения препарата, которое исчезает самопроизвольно. В случае появления аллергических реакций использование препарата прекращают и назначают симптоматическое лечение.
3.6 Не рекомендуется применять Цефапик LA совместно с бактериостатическими антибактериальными лекарственными средствами.
3.7 Убой свиней, крупного рогатого скота на мясо разрешается не ранее, чем через 20 суток после введения препарата. В случае вынужденного убоя ранее установленного срока, мясо может быть использовано для кормления плотоядных животных.
Молоко продуктивных животных разрешается использовать для пищевых целей без ограничения.
4 МЕРЫ ПРОФИЛАКТИКИ
4.1 При работе с препаратом следует соблюдать правила личной гигиены и техники безопасности.
5 ПОРЯДОК ПРЕДЪЯВЛЕНИЯ РЕКЛАМАЦИЙ
5.1 В случае возникновения осложнений после применения препарата, его использование прекращают, и потребитель обращается в Государственное ветеринарное учреждение, на территории которого он находится. Ветеринарными специалистами этого учреждения производится изучение соблюдения всех правил по применению препарата в соответствии с инструкцией. При подтверждении не эффективности или несоответствия препарата по внешнему виду, ветеринарными специалистами отбираются пробы в необходимом количестве для проведения лабораторных испытаний, составляется акт отбора проб и направляется в Государственное учреждение «Белорусский государственный ветеринарный центр» (220005, г. Минск, ул. Красная, 19А) для подтверждения соответствия препарата нормативной документации.
6 ПОЛНОЕ НАИМЕНОВАНИЕ ПРОИЗВОДИТЕЛЯ
6.1 ООО «Промветсервис» (юридический адрес): 220034, Республика Беларусь, г. Минск, ул. З. Бядули, 12/2а, тел./факс: +375 17 503 53 67.
Производитель: Филиал «Промветсервис-Альба», 222603, Республика Беларусь, Минская область, Несвижский район, пос. Альба, ул. Заводская ½, тел./факс: +375 1770 27081.
Инструкция подготовлена сотрудниками РУП «Институт экспериментальной ветеринарии им. С.Н. Вышелесского» (Высоцкий А.Э.) и ООО “Промветсервис” (Дмитриева А.А.).
Один флакон содержит: действующего вещества – цефепима –1 г (в виде цефепима гидрохлорида и L-аргинина).
Порошок от белого до светло-желтого цвета.
Прочие β-лактамные антибиотики. Цефалоспорины IV поколения.
Код АТХ: J01DЕ01.
Фармакодинамика
Механизм действия
цефепима основан на нарушении синтеза бактериальной клеточной стенки (в фазе роста) путём ингибирования пенициллин-связывающих протонов (ПСП) таких как транспептидазы. Это приводит к бактерицидному эффекту.
Активен в отношении грамположительных аэробов:
Staphylococcus aureus и Staphylococcus epidermidis (только метициллиночувствительные штаммы)
Staphylococcus saprophyticus
Streptococcus pyogenes (группа A)
Streptococcus agalactiae (группа В)
Streptococcus pneumoniae
Streptococcus viridans
Грамотрицательных аэробов
Enterobacter spp. (в т.ч. Enterobacter cloacae, Enterobacter aerogenes, Enterobacter agglomerans и Enterobacter sakazakii)
Proteus mirabilis
Proteus vulgaris
Acinetobacter calcoaceticus подгруппа Iwoffii
Acinetobacter pittii
Citrobacter diversus
Citrobacter freundii
Haemophilus ducreyi
Haemophilus influenzae (включая штаммы, продуцирующие β-лактамазу)
Hafnia alvei
Morganella morganii
Moraxella catarrhalis (включая штаммы, продуцирующие β-лактамазы)
Providencia rettgeri
Providencia stuartii
Serratia marcescens
Serralia liquifaciens.
Виды микроорганизмов, которые могут приобретать устойчивость
Аэробные грамположительные микроорганизмы
Staphylococcus aureus*
Staphylococcus epidermidis+
Staphylococcus haemolyticus+
Staphylococcus hominis+
Аэробные грамотрицательные микроорганизмы
Acinetobacter baumannii
Enterobacter cloacae
Escherichia coli%
Klebsiella oxytoca%
Klebsiella pneumonia%
Pseudomonas aeruginosa
Устойчивые виды
Аэробные грамположительные микроорганизмы
Enterococcus spp.
Listeria monocytogenes
Staphylococcus aureus (метициллин-резистентный)
Аэробные грамотрицательные микроорганизмы
Legionella spp.
Stenotrophomonas maltophilia
Анаэробные микроорганизмы
Bacteroides fragilis
Clostridium difficile
Другие микроорганизмы
Chlamydia spp.
Chlamydophila spp.
Mycoplasma spp.
Примечания:
*— в амбулаторной практике уровень резистентности составляет <10%;
+ — по меньшей мере, в одной области, уровень резистентности составляет более 50%;
% — все штаммы, продуцирующие бета-лактамазы расширенного спектра, устойчивы.
Большинство изолятов энтерококков, например, Enterococcus faecalis и устойчивых к метициллину стафилококков, устойчивы к цефепиму. Цефепим неактивен против многих изолятов Stenotrophomonas maltophilia.
Фармакокинетика
Фармакокинетика цефепима линейная в диапазоне от 250 мг до 2 г. Кумуляции препарата у здоровых взрослых добровольцев мужского пола при применении средних терапевтических доз в течение 9 дней не наблюдалось.
Абсорбция
Средние концентрации цефепима в плазме у здоровых взрослых добровольцев мужского пола после однократной 30-минутной инфузии (в/в) цефепима 500 мг, 1 г и 2 г наблюдались в разное время (см. Таблицу 1).
После внутримышечного применения цефепим полностью абсорбируется. Средние концентрации цефепима в плазме в разное время после однократной внутримышечной инъекции приведены в Таблице 2. Фармакокинетика линейна в диапазоне от 500 мг до 2 г внутримышечно и остается неизменной вне зависимости от продолжительности лечения.
Таблица 1
|
Средние концентрации цефепима в плазме в мкг/мл и фармакокинетические параметры (± стандартное отклонение) после внутривенного введения |
|||
|
Параметры |
Цефепим (в мкг/мл) после внутривенного введения |
||
|
500 мг |
1000 мг |
2000 мг |
|
|
0,5 ч |
38,2 |
78,7 |
163,1 |
|
1,0 ч |
21,6 |
44,5 |
85,8 |
|
2,0 ч |
11,6 |
24,3 |
44,8 |
|
4,2 ч |
5,0 |
10,5 |
19,2 |
|
8,0 ч |
1,4 |
2,4 |
3,9 |
|
12,0 ч |
0,2 |
0,6 |
1,1 |
|
Сmax, мкг/мл |
39,1 (3,5) |
81,7 (5,1) |
163,9 (25,2) |
|
AUC, ч·мкг/мл |
70,8 (6,7) |
148,5 (15,1) |
284,8 (30,3) |
Таблица 2
|
Средние концентрации цефепима в плазме в мкг/мл и фармакокинетические параметры (± стандартное отклонение) после внутримышечного введения |
|||
|
Параметры |
Цефепим (в мкг/мл) после внутримышечного введения |
||
|
500 мг |
1000 мг |
2000 мг |
|
|
0,5 ч |
8,2 |
14,8 |
36,1 |
|
1,0 ч |
12,5 |
25,9 |
49,9 |
|
2,0 ч |
12,0 |
26,3 |
51,3 |
|
4,2 ч |
6,9 |
16 |
31,5 |
|
8,0 ч |
1,9 |
4,5 |
8,7 |
|
12,0 ч |
0,7 |
1,4 |
2,3 |
|
Сmax, мкг/мл |
13,9 (3,4) |
29,6 (4,4) |
57,5 (9,5) |
|
Тmax, мкг/мл |
1,4 (0,9) |
1,6 (0,4) |
1,5 (0,4) |
|
AUC, ч·мкг/мл |
60,0 (8,0) |
137,0 (11,0) |
262,0 (23,3) |
Распределение
Объем распределения цефепима в равновесном состоянии составляет 18 (±2) л. Связывание с белками сыворотки крови составляет около 20% и не зависит от концентрации цефепима в сыворотке крови. Цефепим выделяется с грудным молоком. Новорожденный на грудном вскармливании, потребляющий примерно 1000 мл грудного молока в день, может получить примерно 0,5 мг цефепима в день.
Цефепим проникает через воспаленный гематоэнцефалический барьер. В настоящее время клиническая значимость этих данных является неопределённой.
Метаболизм и выведение
Цефепим метаболизируется до N-метилпирролидина (NMP), который быстро преобразовывается в N-оксид (NMP-N-оксид). Примерно 85 % дозы выводится с мочой в неизменном виде. Менее 1% дозы – в виде
N-метилпирролидина, 6,8 % — NMP-N-оксида и 2,5 % в виде эпимера цефепима. Выведение цефепима осуществляется путем почечной экскреции со средним (± SD) периодом полувыведения 2 (± 0,3) часа и общим клиренсом
120 (± мл/мин у здоровых добровольцев. Поскольку почечная экскреция является основным способом выведения, у пациентов с нарушением функции почек и пациентов, находящихся на гемодиализе, требуется коррекция дозы.
Почечная недостаточность: средний период полувыведения у пациентов, нуждающихся в гемодиализе, составил 13,5 (± 2,7) часов и у пациентов, нуждающихся в непрерывном перитонеальном диализе, 19 (± 2) часов. Общий клиренс цефепима снижался пропорционально клиренсу креатинина у пациентов с нарушенной функцией почек, что служит основанием для коррекции дозы в этой группе пациентов.
Печеночная недостаточность: фармакокинетика цефепима не изменяется у пациентов с печеночной недостаточностью при применении разовой дозы в 1 г.
Пациенты пожилого возраста: фармакокинетика цефепима у пациентов пожилого возраста (65 лет и старше) мужского и женского пола, у которых средний (SD) клиренс креатинина был 74 (± 15) мл/мин характеризуется снижением общего клиренса цефепима в зависимости от клиренса креатинина. Таким образом, доза цефепима у пациентов пожилого возраста должна быть скорректирована по мере необходимости, если клиренс креатинина составляет 50 мл/мин или менее.
Дети: фармакокинетика цефепима у детей в возрасте от 1 месяца до 11 лет: после применения разовой и многократной дозы каждые 8 часов и каждые 12 часов общий клиренс и объем распределения в равновесном состоянии составляли в среднем 3,3 (± 1) мл/мин/кг и 0,3 (± 0,1) л/кг, соответственно. Выведение с мочой в неизмененном виде составило 60,4 (± 30,4) % от дозы, а средний почечный клиренс 2 (± 1,1) мл/мин/кг. Ни возраст, ни пол на общий клиренс и объем распределения с поправкой на массу тела не влияли. Кумуляции препарата не наблюдалось при применении 50 мг/кг каждые 12 часов, в то время как Cmax, AUC и Тmах увеличились примерно на 15 % в равновесном состоянии после применения 50 мг на кг каждые 8 часов. Доза в 50 мг/кг внутривенно у детей сравнима с дозой в 2 г внутривенно у взрослых. Абсолютная биодоступность цефепима после применения дозы в 50 мг/кг внутримышечно составила 82,3 (± 15) % у восьми пациентов.
Взрослые
Лечение инфекций, вызванных чувствительными штаммами соответствующих микроорганизмов:
— пневмония (от умеренной до тяжелой), вызванная Streptococcus pneumoniae, включая случаи с одновременной бактериемией, Pseudomonas aeruginosa, Klebsiella pneumonia или Enterobacter species;
— эмпирическая терапия пациентов с нейтропенической лихорадкой. Цефепим в качестве монотерапии показан для эмпирического лечения пациентов с фебрильной нейтропенией. У пациентов с высоким риском тяжелой инфекции (в том числе у пациентов с недавно перенесённой трансплантацией костного мозга в анамнезе (данных в поддержку эффективности монотерапии цефепимом у этих пациентов недостаточно; если необходимо, рекомендуется комбинированная терапия с антибиотиками из группы аминогликозидов или гликопептидов с учётом индивидуального профиля риска пациента), гипотонией, гематологической злокачественной опухолью, тяжелой или длительной нейтропенией) — в составе комбинированной терапии;
— неосложненные и осложненные инфекции мочевыводящих путей (в том числе пиелонефрит), вызванные Escherichia coli или Klebsiella pneumoniae, любой степени тяжести, а также легкие и умеренно тяжелые инфекции, вызванные Proteus mirabilis, включая случаи, связанные с одновременной бактериемией этими микроорганизмами;
— неосложнённые инфекции кожи и ее структур, вызванные Staphylococcus aureus (только метициллин-чувствительные штаммы) или Streptococcus pyogenes;
— осложнённые интраабдоминальные инфекции (в сочетании с метронидазолом), вызванные Echerichia coli, стрептококками группы viridens, Pseudomonas aeruginosa, Klebsiella pneumoniae, Enterobacter species или Bacteroides fragilis.
Дети
Инфекции, вызванные микроорганизмами, чувствительными к цефепиму:
— бактериемия, связанная с одной из упомянутых инфекций, или предположительно связанная;
— тяжёлая пневмония;
— тяжёлые инфекции мочевыводящих путей;
— бактериальный менингит;
— эмпирическое лечение фебрильных эпизодов у пациентов с умеренной (нейтрофилы < 1000/мм3) или тяжёлой (нейтрофилы ≤ 500/мм3) нейтропенией. У пациентов с высоким риском серьёзной инфекции (например, у пациентов с недавней трансплантацией костного мозга, низким начальным артериальным давлением, онкогематологическими заболеваниями или тяжёлой, или длительной нейтропенией) антимикробная монотерапия не применима. Имеющиеся данные по эффективности монотерапии цефепимом у таких пациентов недостаточны. Если необходимо, рекомендуется комбинированная терапия с антибиотиком из группы аминогликозидов или гликопептидов с учётом индивидуального профиля риска пациента.
Чтобы уменьшить развитие лекарственноустойчивых бактерий и поддерживать эффективность Цефепима и других антибактериальных препаратов, лекарственное средство следует использовать только для лечения инфекций, которые вызваны чувствительными бактериями. Когда информация о культуре и восприимчивости доступна, препарат следует использовать только для лечения инфекций, которые вызваны чувствительными бактериями. При отсутствии таких данных выбору эмпирической терапии могут способствовать эпидемиологические данные.
Повышенная чувствительность к цефепиму или L-аргинину, а также к цефалоспориновым антибиотикам, пенициллинам или другим β-лактамным антибиотикам. Детский возраст до 1 месяца.
Дозы и способ введения препарата зависят от чувствительности возбудителя, тяжести инфекции, функции почек и общего состояния пациента.
Рекомендации относительно дозирования лекарственного средства приведены в таблице 1.
Таблица 1. Дозирование у пациентов с нормальной функцией почек (клиренс креатинина (КК) более 50 мл/мин)
|
Локализация и тип инфекции |
Доза |
Частота |
Продолжитель-ность2 (дни) |
|
Взрослые и дети старше 12 лет (с массой тела более 40 кг) |
|||
|
Пневмония умеренной или тяжелой степени, вызванная S. pneumoniae*, P. aeruginosa1, К. pneumoniae или Enterobacter spp. |
1-2 г в/в |
Каждые 12 ч |
10 |
|
Эмпирическая терапия пациентов с фебрильной нейтропенией |
2 г в/в |
Каждые 8 ч |
7** |
|
Неосложненные или осложненные инфекции мочевых путей, включая пиелонефрит |
0,5-1 г в/в или в/м*** |
Каждые 12 ч |
7-10 |
|
Тяжелые неосложнённые или осложненные инфекции мочевых путей, в том числе пиелонефрит |
2 г в/в |
Каждые 12 ч |
10 |
|
Инфекции кожи и ее структур, вызываемые S. aureus или S.pyogens. |
2 г в/в |
Каждые 12 ч |
10 |
|
Осложнённые интраабдоминальные инфекции (в сочетании с метронидазолом) |
2 г в/в |
8-12 ч |
7-10 |
|
Дети в возрасте от 1 месяца до 12 лет (с массой тела ≤ 40 кг): |
|||
|
Возраст |
пневмония, осложнённые инфекции мочевыводящих путей. |
Очень тяжёлые инфекции: сепсис, бактериальный менингит, эмпирическое лечение эпизодов фебрильной нейтропении. |
|
|
2 месяца – 12 лет (с массой тела ≤ 40 кг) |
50 мг/кг массы тела каждые 12 часов Серьёзные инфекции: 50 мг/кг массы тела каждые 8 часов |
50 мг/кг массы тела каждые 8 часов |
|
|
Продолжительность: 10 дней 7-10 дней |
|||
|
От 1 до 2 месяцев |
30 мг/кг массы тела каждые 12 часов Серьёзные инфекции: 30 мг/кг массы тела каждые 8 часов |
30 мг/кг массы тела каждые 8 часов |
|
|
Продолжительность: 10 дней 7-10 дней |
* В том числе случаи, связанные с одновременной бактериемией.
** Или до окончания нейтропении. У пациентов со снижением температуры, но нейтропенией более 7 дней, должна быть пересмотрена необходимость продолжения антибактериальной терапии.
*** Внутримышечный путь введения показан только для легкой и умеренной неосложненной или осложненной инфекции мочевыводящих путей, вызванной E. coli.
1 При лечении пневмонии, вызванной P. aeruginosa: 2 г вводить в/в каждые 8 часов.
2 Продолжительность лечения, как правило, составляет от 7 до 10 дней. Максимальная продолжительность в целом – не менее 7, но не более 14 дней. Продолжительность эмпирического лечения фебрильной нейтропении: от 7 дней до исчезновения нейтропении.
Опыт применения у детей в возрасте до 1 месяца ограничен и основывается на расчете доз, исходя из опыта применения дозы 50 мг/кг массы тела, полученной на основании фармакокинетических данных у пациентов старше 1 месяца, что соответствует дозе 30 мг/кг массы тела каждые 12 или 8 часов для детей в возрасте от 1 до 2 месяцев. Дети этого возраста должны тщательно контролироваться во время введения препарата.
У детей с массой тела более 40 кг рекомендуется доза, как для взрослых (смотрите таблицу). У детей старше 12 лет с массой тела менее 40 кг рекомендуется доза, как для детей с массой тела ≤ 40 кг. Максимальная доза у детей не должна превышать максимальную дозу для взрослых (2,0 г каждые 8 часов).
Продолжительность лечения, как правило, составляет от 7 до 10 дней. В целом цефепим рекомендуется применять не менее 7, но не более 14 дней.
При эмпирическом лечении фебрильной нейтропении продолжительность лечения обычно составляет до 7 дней или до окончания нейтропении.
Пациенты с нарушенной функцией почек. Цефепим выводится почками путем клубочковой фильтрации, поэтому больным с нарушениями функции почек (клиренс креатинина (КК) менее 50 мл/мин) дозу Цефепима необходимо откорректировать. У этих пациентов рекомендуемая начальная доза цефепима должна быть такой же, как у пациентов с КК более 50 мл/мин, за исключением пациентов, подвергающихся гемодиализу (таблица 2).
Таблица 2. Рекомендуемые дозы Цефепима для взрослых.
|
КК (мл/мин) |
Интервал приема доз (часы) |
||
|
24 часа |
12 часов |
8 часов |
|
|
> 50 |
500-2000 мг |
2000 мг |
|
|
Коррекция дозы не требуется |
|||
|
30-50 |
500-2000 мг |
500 мг |
|
|
11-29 |
500-1000 мг |
||
|
≤ 10 |
250-500 мг |
||
|
Гемодиализ * |
1000 мг 1 доза, затем по 500 мг |
500 мг |
* В день проведения диализа инъекцию лекарственного средства необходимо выполнять после окончания процедуры диализа.
Если известна только концентрация креатинина в сыворотке крови, тогда КК можно определять по нижеуказанным формулам.
Мужчины: КК (мл/мин) = масса тела (кг)×(140 – возраст) : 72×креатинин плазмы крови (мг/дл).
Женщины: КК (мл/мин) = показатель у мужчин×0,85.
При гемодиализе за 3 ч удаляется приблизительно 68 % дозы препарата. При непрерывном амбулаторном перитонеальном диализе препарат можно применять в исходных рекомендованных дозах – 500 мг, 1 г или 2 г в зависимости от тяжести инфекции с интервалом 48 ч.
У детей при нарушении функции почек рекомендуются изменения режима дозирования, пропорциональные тем, которые принимаются у взрослых, в соответствии с приведённой ниже таблицей.
|
Дети в возрасте от 1 месяца до 12 лет (с массой тела ≤ 40 кг): |
||
|
Клиренс креатинина (мл/мин) |
Тяжёлые инфекции: пневмония, осложнённые инфекции мочевыводящих путей. |
Очень тяжёлые инфекции: сепсис, бактериальный менингит, эмпирическое лечение эпизодов фебрильной нейтропении. |
|
˃ 50 |
50 мг/кг массы тела каждые 12 часов |
50 мг/кг массы тела каждые 8 часов |
|
Регулировка дозы не требуется |
||
|
30 — 50 |
50 мг/кг массы тела каждые 24 часа |
50 мг/кг массы тела каждые 12 часов |
|
11 — 29 |
25 мг/кг массы тела каждые 24 часа |
50 мг/кг массы тела каждые 24 часа |
|
≤ 10 |
12,5 мг/кг массы тела каждые 24 часа |
25 мг/кг массы тела каждые 24 часа |
Расчет показателей КК у детей
КК (мл/мин/1,73 м2) = 0,55×рост (см): креатинин плазмы крови (мг/дл) или
КК (мл/мин/1,73 м2) = 0,52×рост (см): креатинин плазмы крови (мг/дл) −3,6.
Цефепим после восстановления вводят внутримышечно, внутривенно струйно медленно в течение 3-5 мин либо капельно путём инфузии в течение не менее 30 мин.
Приготовление раствора для внутривенного введения
Цефепим восстанавливают одним из следующих растворителей: стерильная вода для инъекций; 0,9 % раствор хлорида натрия для инъекций; 5 % раствор декстрозы для инъекций; стерильная бактериостатическая вода для инъекций с парабенами или бензиловым спиртом в количествах, указанных в таблице 3.
Восстановленный раствор разбавляют одним из следующих совместимых инфузионных растворов для внутривенного введения: 0,9 % раствор хлорида натрия; 5 % и 10 % раствор декстрозы; 5% раствор декстрозы с 0,9 % раствором хлорида натрия; 1/6 М раствор натрия лактата; раствор Рингера лактата; раствор Рингера лактата с 5 % раствором глюкозы.
Приготовление раствора для внутримышечного введения
Цефепим восстанавливают одним из следующих растворителей: стерильная вода для инъекций; 0,9 % раствор хлорида натрия для инъекций; 5 % раствор декстрозы для инъекций; стерильная бактериостатическая вода для инъекций с парабенами или бензиловым спиртом в количествах, указанных в таблице 3.
|
Путь введения |
Объем раствора для разведения (мл) |
Приблизительный объем полученного раствора (мл) |
Приблизительная концентрация Цефепима (мг/мл) |
|
В/в введение: |
|||
|
1 г/флакон |
10 |
11,4 |
90 |
|
В/м введение: |
|||
|
1 г/флакон |
3 |
4,4 |
230 |
Восстановленный раствор лекарственного средства может быть от светло-жёлтого до янтарно-жёлтого цвета.
Перед введением приготовленного раствора лекарственного средства необходимо убедиться, что раствор является прозрачным и не содержит нерастворённых частиц.
Имеются литературные данные о физико-химической несовместимости цефепима с метронидазолом, ванкомицином, гентамицином, тобрамицином, нетилмицином и аминофиллином. В связи с отсутствием собственных иссследований совместимости, данное лекарственное средство не следует смешивать с другими лекарственными средствами.
Описанная ниже частота возникновения побочных реакций соответствует шкале: очень часто ≥ 1/10; часто: ≥1/100 и <1/10; нечасто: ≥ 1/1000 и <1/100; редко: ≥ 1/10000 и <1/1000; очень редко: <1/10000, частота неизвестна – невозможно оценить на основе имеющихся данных.
Инфекции и инвазии. Нечасто: оральный кандидоз. Редко: неспецифический кандидоз.
Нарушения со стороны крови и лимфатической системы. Очень часто: положительная реакция Кумбса. Часто: анемия. Редко: эозинофилия, нейтропения, тромбоцитопения, лейкопения, снижение гематокрита, панцитопения, пролонгация протромбинового времени и активированного частичного тромбопластинового времени, кровотечения. Частота неизвестна: апластическая анемия, гемолитическая анемия, агранулоцитоз.
Нарушения со стороны иммунной системы. Редко: аллергические реакции, зуд, крапивница и лихорадка. Частота неизвестна: анафилактический шок, ангионевротический отёк.
Нарушения метаболизма и питания. Частота неизвестна: ложноположительная реакция на глюкозу в моче.
Нарушения со стороны нервной системы. Нечасто: головная боль. Редко: судороги, парастезия, изменение вкуса, головокружение. Частота неизвестна: кома, ступор, энцефалопатия, нарушение сознания, миоклонус.
Нарушения со стороны органа слуха и лабиринта. Редко: тиннитус (звон в ушах).
Нарушения со стороны сердца. Очень редко: артериальная гипотензия.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения. Очень редко: одышка.
Нарушения со стороны сосудов. Очень редко: вазодилатация.
Желудочно-кишечные нарушения. Часто: диарея. Нечасто: тошнота, рвота, стоматит. Очень редко: боль в животе, колит, псевдомембранозный колит, запор, диспепсия, язвы в полости рта.
Нарушения со стороны печени и желчевыводящих путей. Редко: умеренное и преходящее повышение уровня трансаминаз (АсТ, АлТ), увеличение билирубина в сыворотке крови, нарушения функций печени, включая холестаз.
Нарушения со стороны кожи и подкожной клетчатки. Часто: сыпь. Нечасто: эритема, крапивница, кожный зуд. Редко: отек, аллергические реакции, эритема. Частота неизвестна: токсический эпидермальный некролиз, синдром Стивенса-Джонсона, эритема многоформная.
Нарушения со стороны костно-мышечной системы и соединительной ткани. Очень редко: боль в суставах.
Нарушения со стороны почек и мочевыводящей системы. Редко: увеличение мочевины, креатинина в сыворотке крови, токсическая нефропатия, почечная недостаточность.
Нарушения со стороны репродуктивной системы и молочной железы. Очень редко: вагинит.
Общие нарушения и реакции в месте введения. Нечасто: раздражение в месте введения, флебит и тромбофлебит, боль и воспаление в месте инъекции. Редко: озноб.
Лабораторные и инструментальные данные. Редко: ложноположительная реакция на глюкозу в моче. Очень редко: увеличение щелочной фосфатазы в сыворотке крови, фосфатов, кальция, калия, уменьшение концентрации кальция в сыворотке крови.
Сообщение о нежелательных реакциях. Важно сообщать о подозреваемых нежелательных реакциях после регистрации лекарственного средства с целью обеспечения непрерывного мониторинга соотношения «польза–риск» лекарственного средства. Медицинским работникам рекомендуется сообщать о любых подозреваемых нежелательных реакциях лекарственного средства через национальные системы сообщения.
Возможны случаи повышения активности пероральных антикоагулянтов у пациентов, получающих цефалоспорины.
Применяя высокие дозы аминогликозидов одновременно с Цефепимом, необходимо следить за функцией почек из-за потенциальной нефротоксичности и ототоксичности аминогликозидных антибиотиков. Нефротоксичность отмечалась после одновременного применения других цефалоспоринов с сильнодействующими диуретиками (такими как фуросемид).
Перед началом лечения Цефепимом следует тщательно собрать анамнез с целью определения наличия у пациента реакции гиперчувствительности к Цефепиму или любому другому препарату группы цефалоспоринов, пенициллинов или β-лактамных антибиотиков. При наличии сомнений необходимо присутствие врача при первом введении для принятия неотложных мер в случае возникновения анафилактической реакции. При возникновении аллергических реакций необходимо прекратить введение препарата. Рекомендуется соблюдать особую осторожность при необходимости введения цефепима пациентам с бронхиальной астмой или любыми аллергическими реакциями в анамнезе.
Нарушения функций почек
У пациентов с почечной недостаточностью (клиренс креатинина ≤ 50 мл/мин) или другими факторами, которые влияют на функцию почек, доза цефепима должна быть скорректирована, чтобы компенсировать более медленный клиренс лекарственного средства почками. Поскольку у пациентов с нарушениями функций почек или другими факторами, которые влияют на функции почек, при обычных дозах уровень цефепима в сыворотке может быть высоким и сохраняться длительно, у них поддерживающая доза должна быть уменьшена. Во время постмаркетинговых наблюдений были зарегистрированы серьёзные побочные эффекты в виде обратимой энцефалопатии (расстройства сознания со спутанностью сознания, галлюцинациями, ступором и комой), афазия, миоклонус, судороги и бессудорожный эпилептический статус и/или почечная недостаточность. В большинстве случаев энцефалопатия наблюдалась у пациентов с почечной недостаточностью, которые получали дозы цефепима выше рекомендуемых. Обычно нейротоксичсеике симптомы проходили после прекращения лечения цефепимом или после гемодиализа, но были случаи со смертельным исходом.
Если происходит нейротоксичность, связанная с терапией цефепимом, прекратите применение цефепима и примите соответствующие меры. При развитии суперинфекций во время лечения необходимо принять соответствующие меры.
Многие цефалоспорины, включая цефепим, были связаны с уменьшением активности протромбина. К группам риска относятся пациенты с почечной или печёночной недостаточностью или плохим состоянием питания, а также пациенты, получающие длительный курс антимикробной терапии. У пациентов с факторами риска следует контролировать протромбиновое время и применять экзогенный витамин К по мере надобности.
Влияние на результаты лабораторных исследований
При проведении анализа мочи на глюкозурию возможен ложноположительный результат. Цефалоспорины склонны абсорбироваться на поверхности эритроцитов и вступать в реакцию с антителами, направленными против препаратов, результатом чего является положительный тест Кумбса.
Пациентам, у которых развивается гемолитическая анемия, следует прекратить введение препарата и провести соответствующую терапию. Положительный тест Кумбса может наблюдаться у новорожденных, чьи матери получали антибиотики группы цефалоспоринов до родов.
Длительное применение Цефепима может приводить к колонизации нечувствительной микрофлорой. При развитии суперинфекций во время лечения необходимо принять соответствующие меры.
В случае появления диареи на фоне лечения, следует учитывать возможность развития антибиотик-ассоциированной диареи, в том числе псевдомембранозного колита, диагностика которого основывается на данных колоноскопии. Легкие формы колита не требуют назначения симптоматической терапии; умеренные или тяжелые случаи могут потребовать специального лечения. Антибиотик-ассоциированная диарея может наблюдаться в течение двух и более месяцев после применения антибактериальных препаратов. Если такой диагноз подозревается, следует прекратить терапию цефепимом и начать соответствующее лечение.
Целесообразно следить за функцией почек при одновременном применении Цефепима с потенциально нефротоксичными антибиотиками (особенно аминогликозидами) и сильными диуретиками.
Антибактериальная активность цефепима
Из-за относительно ограниченного спектра антибактериальной активности, цефепим не подходит для лечения некоторых видов инфекций, особенно когда возбудитель ещё не установлен и не определена чувствительность выявленных микроорганизмов к цефепиму. По крайней мере, должна быть очень высокая вероятность того, что цефепим подходит для лечения данной инфекции.
Исследования на животных не установили наличие прямого или косвенного вредного влияния на течение беременности, развитие эмбриона, плода и постнатальное развитие потомства. Потенциальный риск для людей не известен. Цефепим проникает через плацентарный барьер. Клинических данных о применении Цефепима женщинами в период беременности недостаточно. Цефепим беременным можно назначать только тогда, когда ожидаемая польза для матери превышает потенциальный риск для плода. В малых концентрациях Цефепим проникает в грудное молоко. Поэтому при назначении Цефепима кормление грудью необходимо прекратить.
Исследований о влиянии на способность управлять транспортными средствами и другими механизмами не проводилось. Следует иметь в виду потенциальные побочные эффекты, такие как нарушение сознания, головокружение, спутанность сознания или галлюцинации, которые могут повлиять на способность управлять транспортными средствами и другими механизмами. Пациентам рекомендуется соблюдать осторожность и не управлять транспортом или другими сложными механизмами.
Безопасность и эффективность цефепима при лечении неосложненных и осложненных инфекций мочевыводящих путей (включая пиелонефрит), неосложненных инфекций кожи и мягких тканей, пневмонии, а также при эмпирическом лечении пациентов с нейтропенической лихорадкой была подтверждена в отношении детей в возрасте от 1 месяца до 16 лет. Применение Цефепима в этих возрастных группах обосновано результатами адекватных и хорошо контролируемых исследований применения цефепима у взрослых и дополнительными данными касательно фармакокинетики и безопасности, полученными в ходе исследований с участием детей.
Безопасность и эффективность применения у детей в возрасте до 1 месяца не изучена. Существует недостаточное количество клинических данных, подтверждающих целесообразность применения Цефепима у детей в возрасте до 1 месяца или для лечения тяжелых инфекций у детей в случаях, где подозреваемым или установленным возбудителем является Haemophilus influenzae типа b.
У пациентов с менингитом, у которых инфекция распространяется из удаленного очага, или у пациентов с подозреваемым или диагностированным менингитом, должен применяться альтернативный препарат с доказанной клинической эффективностью.
В ходе клинических исследований Цефепим применяли у более 6400 взрослых пациентов (35 % старше 65 лет, и 16 % 75 лет и старше). При применении обычной рекомендуемой дозы для взрослых клиническая эффективность и безопасность препарата были сопоставимы с таковыми у взрослых пациентов, не относящихся к пожилому и старческому возрасту.
Серьезные нежелательные явления наблюдались у пациентов пожилого возраста с почечной недостаточностью, у которых коррекция доз цефепима не осуществлялась, в том числе сообщалось об опасных для жизни или смертельных случаях, включая: энцефалопатию, миоклонус и судороги.
Препарат, как известно, выводится, главным образом, почками, и риск возникновения токсических реакций может быть выше у пациентов с нарушенной функцией почек. В силу того, что у пациентов пожилого возраста ухудшение почечной функции более вероятно, чем у пациентов других групп, следует обратить особое внимание на выбор дозы. Также должен осуществляться постоянный контроль функции почек.
Симптомы. Проявляются в случаях существенного превышения рекомендуемых доз, особенно у больных с нарушенной функцией почек. Симптомы передозировки включают энцефалопатию (нарушения сознания, включая спутанность сознания, галлюцинации, ступор и кому), миоклонус, судороги, нервно-мышечную возбудимость и неконвульсивный эпилептический статус.
Лечение. Необходимо прекратить введение препарата, провести симптоматическую терапию. Применение гемодиализа ускоряет удаление Цефепима из организма; перитонеальный диализ малоэффективен. Тяжелые аллергические реакции немедленного типа требуют применения адреналина и других форм интенсивной терапии.
1,0 г во флаконах из стекла. 1 флакон вместе с листком-вкладышем помещают в пачку из картона (№1).
10 флаконов вместе с листком-вкладышем помещают в пачку из картона с картонным вкладышем (№10).
Для стационаров: 50 флаконов вместе с 2 инструкциями по применению помещают в коробку из картона (№50).
В защищенном от света месте, при температуре не выше 25°С. Хранить в недоступном для детей месте.
2 года. Не использовать по истечении срока годности.
По рецепту.
Информация о производителе
Открытое акционерное общество «Борисовский завод медицинских препаратов», Республика Беларусь, Минская обл., г. Борисов, ул. Чапаева, 64, тел/факс +375(177) 735612, 731156.
Цефепим — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-005926
Торговое наименование:
Цефепим
Международное непатентованное или группировочное наименование:
цефепим
Лекарственная форма:
порошок для приготовления раствора для внутривенного и внутримышечного введения
Состав
на 1 флакон:
| 0,5 г | 1,0 г | 2,0 г | |
|
Действующее вещество: |
|||
|
Цефепима гидрохлорида моногидрат |
0,5945 г |
1,1891 г |
2,3782 г |
|
(в пересчете на цефепим) |
0,5 г |
1,0 г |
2,0 г |
| Вспомогательное вещество: | |||
| L-аргинин |
0,3625 г |
0,725 г |
1,450 г |
Описание:
белый или белый с желтоватым оттенком кристаллический порошок
Фармакотерапевтическая группа:
антибиотик-цефалоспорин
Код ATX:
J01DE01
Фармакологические свойства
Фармакодинамика
Цефепим является цефалоспориновым антибиотиком широкого спектра действия. Цефепим подавляет синтез белков клеточной стенки бактерий, обладает широким спектром бактерицидного действия в отношении различных грамположительных и грамотрицательных бактерий, в том числе большинства штаммов, резистентных к аминогликозидам или цефалоспориновым антибиотикам третьего поколения, таким как цефтазидим. Цефепим высоко устойчив к гидролизу большинством бета-лактамаз, он имеет низкое сродство к бета-лактамазам и быстро проникает в клетки грамотрицательных бактерий. Доказано, что цефепим обладает очень высоким сродством к пенициллин-связывающему белку (ПСБ) типа 3, высоким сродством -к ПСБ типа 2 и умеренным сродством — к ПСБ типов 1а и 1б. Цефепим оказывает бактерицидное действие в отношении широкого спектра бактерий. Цефепим активен в отношении следующих микроорганизмов:
Грамположителъные аэробы:
Staphylococcus aureus (включая штаммы, продуцирующие бета-лактамазу);
Staphylococcus epidermidis (включая штаммы, продуцирующие бета-лактамазу);
другие штаммы Staphylococcus spp., включая Staphylococcus hominis, Staphylococcus saprophyticus;
Streptococcus pyogenes (стрептококки группы A);
Streptococcus agalactiae (стрептококки группы В);
Streptococcus pneumoniae (включая штаммы со средней устойчивостью к пенициллину — минимальная подавляющая концентрация от 0,1 до 1 мкг/мл);
другие бета-гемолитические Streptococcus spp. (группы С, G, F), Streptococcus bovis (группа D), Streptococcus spp. группы viridans.
Примечание: большинство штаммов энтерококков, например, Enterococcus faecalis, и стафилококки, резистентные к метициллину, устойчивы к действию большинства цефалоспориновых антибиотиков, включая цефепим.
Грамотрицательные аэробы:
Acinetobacter calcoaceticus (подштаммы anitratus, Iwoffii);
Aeromonas hydrophila;
Capnocytophaga spp.;
Citrobacter spp., включая Citrobacter diversus, Citrobacter freundii,
Campylоbасter jejuni;
Enterobacter spp., включая Enterobacter cloacae, Enterobacter aerogenes, Enterobacter sakazakii;
Escherichia coli;
Gardnerella vaginalis;
Haemophilus ducreyi;
Haemophilus influenzae (включая штаммы, продуцирующие бета-лактамазу);
Haemophilus parainfluenzae;
Hafnia alvei;
Klebsiella spp., включая Klebsiella pneumoniae, Klebsiella oxytoca, Klebsiella ozaenae;
Legionella spp.;
Morganella morganii;
Moraxella catarrhalis (Branhamella catarrhalis) (включая штаммы, продуцирующие бета-лактамазы);
Neisseria gonorrhoeae (включая штаммы, продуцирующие бета-лактамазу);
Neisseria meningitidis;
Pantoea agglomerans (ранее известный как Enterobacter agglomerans);
Proteus spp., включая Proteus mirabilis, Proteus vulgaris;
Providencia spp., включая Providencia rettgeri, Providencia stuartii;
Pseudomonas spp., включая Pseudomonas aeruginosa, Pseudomonas putida, Pseudomonas stutzeri, Salmonella spp.;
Serratia, включая Serratia marcescens, Serratia liquefaciens;
Shigella spp.;
Yersinia enterocolitica.
Примечание: цефепим неактивен в отношении многих штаммов Stenotrophomonas maltophilia, ранее известных как Xanthomonas maltophilia и Pseudomonas maltophilia).
Анаэробы:
Bacteroides spp.;
Clostridium perfringens;
Fusobacterium spp.;
Mobiluncus spp.;
Peptostreptococcus spp.;
Prevotella melaninogenica (известный как Bacteroides melaninogenicus);
Veillonella spp.
Примечание: цефепим неактивен в отношении Bacteroides fragilis и Clostridium difficile.
Фармакокинетика
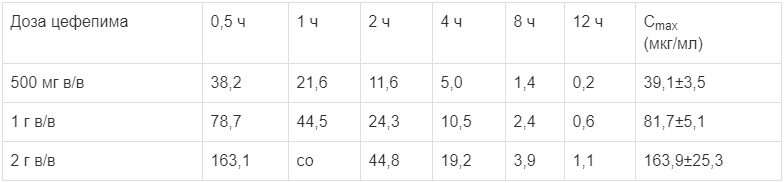
Средние концентрации цефепима в плазме крови взрослых здоровых мужчин в различные сроки после однократного внутривенного введения в течение 30 мин до 12 ч и максимальная концентрация (Сmах) приведены ниже в таблице.
Средние концентрации цефепима в плазме (мкг/мл) после внутривенного введения
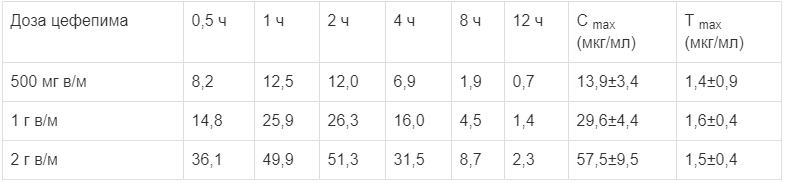
Сmах и время достижения максимальной концентрации (Тmах) после однократного внутримышечного введения приведены ниже в таблице.
Средние концентрации цефепима в плазме (мкг/мл) после внутримышечного введения
Цефепим метаболизируется в N-метилпирролидин, который быстро превращается в оксид N-метилпирролидина.
Цефепим выводится преимущественно почками, путем клубочковой фильтрации (почечный клиренс составляет в среднем 110 мл/мин). В моче обнаруживается приблизительно 85 % от введенной дозы неизмененного цефепима, менее 1 % N-метилпирролидина, около 6,8 % оксида N-метилпирролидина и около 2,5 % эпимера цефепима.
После введения доз от 250 мг до 2 г период полувыведения цефепима из организма составляет в среднем около 2 часов. Общий клиренс составляет в среднем 120 мл/мин. При внутривенном ведении препарата здоровым добровольцам в дозе 2 г каждые 8 часов в течение 9 дней кумуляции препарата не наблюдалось.
Пациенты с нарушениями функции почек
Период полувыведения из организма при почечной недостаточности увеличивается, при этом наблюдается линейная зависимость между общим клиренсом и клиренсом креатинина. При тяжёлых нарушениях функции почек, требующих проведения сеансов диализа, период полувыведения составляет в среднем 13 часов при гемодиализе и 19 часов при непрерывном перитонеальном диализе. При нарушенной функции почек требуется корректировка дозы.
Пациенты с нарушениями функции печени
Фармакокинетика цефепима у пациентов с нарушенной функцией печени не изменяется. Корректировки дозы для таких пациентов не требуется.
Пациенты старше 65 лет
После однократного внутривенного введения 1 г препарата здоровым добровольцам старше 65 лет отмечалось увеличение площади под кривой зависимости «концентрация-время» (AUC) и уменьшение почечного клиренса по сравнению с молодыми добровольцами. При нарушенной функции почек пациентам старшего возраста требуется корректировка дозы.
Дети
Фармакокинетика препарата исследовалась у детей в возрасте от 2 месяцев до 11 лет после однократного введения дозы 50 мг/кг массы тела внутривенно или внутримышечно, а также после повторного введения препарата (каждые 8-12 часов, в течение не менее 48 часов). После однократного внутривенного введения общий клиренс и объем распределения составляли 3,3 мл/мин/кг и 0,3 л/кг, соответственно. Период полувыведения из организма составлял в среднем 1,7 ч. Выведение цефепима в неизмененном виде почками составляло 60,4 % от введенной дозы, а почечный клиренс — в среднем 2,0 мл/мин/кг.
После многократного внутривенного введения концентрация цефепима в плазме крови в равновесном состоянии, а также другие фармакокинетические параметры не отличались от таковых после однократного введения. Возраст и пол пациентов не оказывали существенного влияния на общий клиренс и объем распределения с учетом поправки на массу тела. После внутримышечного введения максимальная концентрация цефепима в плазме крови в равновесном состоянии составляла в среднем 68 мкг/мл и достигалась в среднем за 0,75 ч. Через 8 ч после внутримышечного введения концентрации цефепима в плазме крови составляли в среднем 6 мкг/мл. Абсолютная биодоступность цефепима после внутримышечной инъекции составляла в среднем 82 %.
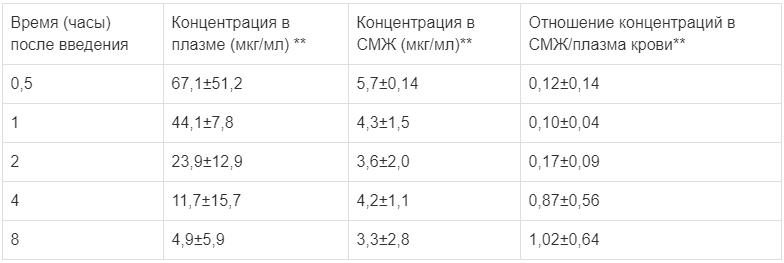
Концентрации препарата в спинномозговой жидкости (СМЖ) и в плазме крови у детей с бактериальным менингитом
Показания к применению
Инфекционно-воспалительные заболевания, вызванные чувствительными к цефепиму микроорганизмами, у взрослых:
— Инфекции нижних дыхательных путей, включая пневмонию и бронхит;
— Инфекции мочевыводящих путей, как осложнённые, включая пиелонефрит, так и неосложнённые;
— Инфекции кожи и мягких тканей;
— Инфекции брюшной полости, включая перитонит и инфекции желчных путей;
— Гинекологические инфекции;
— Септицемия;
— Фебрильная нейтропения.
Профилактика возможных инфекций при проведении полостных хирургических операций.
Инфекционно-воспалительные заболевания, вызванные чувствительными к цефепиму микроорганизмами, у детей:
— Пневмония;
— Инфекции мочевых путей, как осложнённые, включая пиелонефрит, так и неосложнённые;
— Инфекции кожи и мягких тканей;
— Септицемия;
— Фебрильная нейтропения;
— Бактериальный менингит.
Противопоказания
Гиперчувствительность к цефепиму или L-аргинину, а также к антибиотикам цефалоспориновой группы, пенициллинам или другим бета-лактамным антибиотикам.
Детский возраст до 2-х месяцев.
С осторожностью
Заболевания желудочно-кишечного тракта в анамнезе (особенно колит), почечная недостаточность (клиренс креатинина менее 60 мл/мин).
Применение при беременности и в период грудного вскармливания
Адекватных и контролируемых клинических исследований у беременных женщин не проводилось. При беременности следует применять препарат только в том случае, если предполагаемая польза для матери превышает потенциальный риск для плода.
Цефепим обнаруживается в грудном молоке в очень низких концентрациях.
В период грудного вскармливания следует применять препарат только в том случае, если предполагаемая польза для матери превышает потенциальный риск для ребенка.
Способ применения и дозы
Цефепим может вводиться внутривенно (в/в) или внутримышечно (в/м). Дозы и путь введения зависят от чувствительности возбудителей, тяжести инфекции, состояния функции почек и общего состояния пациента. Внутривенный путь введения рекомендуется для пациентов с тяжёлыми или угрожающими жизни инфекциями, особенно при угрозе возникновения септического шока. Внутримышечно доза до 1 г (объем <3,1 мл) может быть введена как однократная инъекция. Максимальную дозу (2 г/6,2 мл) следует вводить в виде двух инъекций в разные места.
Для детей доза не должна превышать максимальную рекомендуемую дозу для взрослых (2 г в/в каждые 8 часов). Опыт внутримышечного введения цефепима детям ограничен.
Взрослым и детям с массой тела более 40 кг при нормальной функции почек
|
Инфекции мочевых путей, легкой и средней тяжести |
0,5 г-1 г в/в или в/м |
Каждые 12 часов |
|
Другие инфекции, легкой и средней тяжести |
1 г в/в или в/м |
Каждые 12 часов |
|
Тяжелые инфекции |
2 г в/в |
Каждые 12 часов |
|
Очень тяжелые и угрожающие жизни инфекции |
2 г в/в |
Каждые 8 часов |
Обычная продолжительность лечения составляет 7-10 дней; тяжёлые инфекции могут потребовать более продолжительного лечения.
В случае лечения фебрильной нейтропении обычная продолжительность лечения составляет 7 дней или до исчезновения нейтропении.
Профилактика возможных инфекций при проведении хирургических операций
За 60 минут до начала хирургической операции вводится 2 г препарата внутривенно в виде инфузии в течение 30 минут. Сразу после окончания инфузии вводится 500 мг метронидазола внутривенно. Вследствие несовместимости метронидазола и цефепима их не следует вводить одновременно или смешивать. Инфузионную систему перед введением метронидазола следует промыть (см. «Внутривенное введение»). Раствор метронидазола следует приготовить в соответствии с инструкцией по применению метронидазола. Во время длительных (более 12 часов) хирургических операций через 12 часов после первой дозы рекомендуется повторное введение в той же дозе препарата Цефепим с последующим введением метронидазола.
Дети от 2 месяцев с массой тела до 40 кг
Обычная рекомендуемая доза при инфекциях мочевых путей, инфекциях кожи и мягких тканей, пневмонии составляет 50 мг/кг каждые 12 часов в течение 10 дней. В случае тяжелых инфекций — каждые 8 часов. Пациентам с фебрильной нейтропенией, септицемией, бактериальным менингитом следует вводить 50 мг/кг каждые 8 часов в течение 7-10 дней.
Пациенты с нарушением функции почек
Пациентам с нарушенной функцией почек требуется корректировка дозировки цефепима с целью компенсации уменьшенной скорости выведения препарата с мочой. Режим дозирования должен назначаться в зависимости от степени почечной недостаточности, тяжести инфекции и чувствительности микроорганизмов. У пациентов со слабым или умеренным нарушением функции почек исходная доза препарата должна быть такой же, как у пациентов с нормальной функцией почек.
Рекомендуемые поддерживающие дозы цефепима представлены в таблице. Клиренс креатинина для мужчин можно рассчитать исходя из концентрации сывороточного креатинина по следующей формуле:
Клиренс креатинина для женщин можно рассчитать, умножив полученное значение на 0,85.
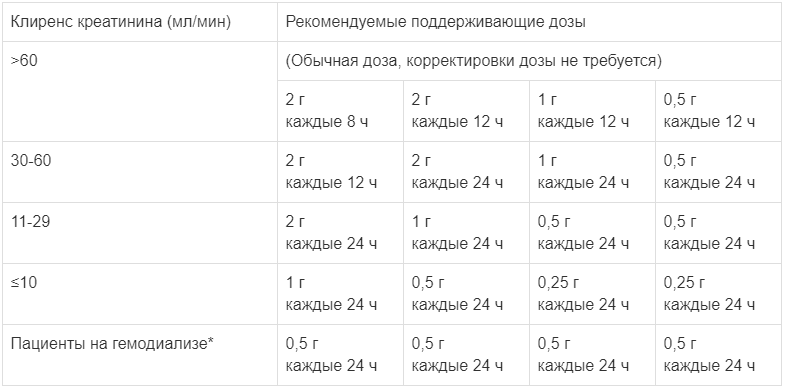
При гемодиализе за 3 часа удаляется из организма приблизительно 68 % введенной дозы препарата.
При непрерывном амбулаторном перитонеальном диализе препарат можно использовать в исходных рекомендованных дозах 0,5 г, 1 г или 2 г в зависимости от тяжести инфекции с интервалом между введением 48 часов.
Дети с нарушением функции почек
Детям при нарушенной функции почек рекомендуется уменьшение дозы или увеличение интервала между введениями, как указано выше в таблице. Клиренс креатинина вычисляется по следующим формулам:
Пациенты с нарушением функции печени
Коррекции дозы для пациентов с нарушением функции печени не требуется.
Внутривенное введение
Рекомендуется для пациентов с тяжёлыми или угрожающими жизни инфекциями, особенно при угрозе возникновения септического шока.
Приготовление раствора для внутривенного введения
Препарат растворяют в 5, 10 или 20 мл стерильной воды для инъекций, 5 % растворе декстрозы и 0,9 % растворе натрия хлорида для инъекций, как указано в приведенной ниже таблице, и вводят в течение 3-5 минут либо непосредственно в вену, либо в систему для внутривенного введения, через которую в организм пациента поступает совместимый раствор для внутривенного введения.
Приготовление раствора для внутривенной инфузии
Приготовленный раствор (см. выше) переносят в инфузионный сосуд с другими совместимыми растворам для внутривенных инфузий (см. ниже) и вводят в течение не менее 30 минут.

Внутримышечное введение: доза до 1 г (объем < 3,1 мл) может быть введена в виде однократной инъекции. Максимальную дозу (2 г/6,2 мл) следует вводить в виде двух инъекций в разные места.
Приготовление раствора для внутримышечного введения
Препарат растворяют в стерильной воде для инъекций, 5 % растворе декстрозы или 0,9 % растворе натрия хлорида для инъекций, бактериостатической воде для инъекций с парабенами или бензиловым спиртом, 0,5 % или 1 % растворе лидокаина, как указано ниже в таблице.

Приготовленные растворы препарата для внутримышечного и внутривенного введения стабильны в течение 24 часов при комнатной температуре или 7 дней при хранении в холодильнике (2-8°С).
Как и все растворы для парентерального применения, перед введением приготовленные растворы препарата следует проверить на отсутствие видимых механических включений. В противном случае запрещается использовать приготовленный раствор.
При хранении порошок и приготовленный раствор могут потемнеть, что не влияет на активность и качество препарата.
Побочное действие
Наиболее часто отмечаются побочные эффекты со стороны желудочно-кишечного тракта и аллергические реакции. Ниже перечислены побочные эффекты по органам и системам в соответствии с их частотой: очень часто (≥10 %); часто (≥1 % и <10 %); нечасто (≥0,1 % и <1 %); редко (≥0,01 % и <0,1 %); частота неизвестна (нет данных о частоте развития данного побочного эффекта).
Аллергические реакции
Часто — высыпания на коже;
Нечасто — эритема, крапивница, зуд;
Редко — анафилактические реакции;
Частота неизвестна — анафилактический шок, токсический эпидермальный некролиз, мультиформная эритема, синдром Стивенса-Джонсона, ангионевротический отек.
Инфекции
Нечасто — кандидоз слизистой оболочки полости рта, вагинальные инфекции;
Редко — кандидозы.
Со стороны центральной нервной системы
Нечасто — головная боль;
Редко — судороги, парестезии, дисгезии, головокружение;
Частота неизвестна (пострегистрационный опыт): энцефалопатия (нарушение сознания, включая спутанность сознания, галлюцинации, ступор и кома), миоклонус, судороги и бессудорожный эпилептический статус.
Несмотря на то, что большинство случаев отмечались у пациентов с почечной недостаточностью, которые получали цефепим в дозах, выше рекомендованных, в некоторых случаях нейротоксичность отмечалась у пациентов, которым проводилась коррекция дозы в зависимости от степени почечной недостаточности.
Со стороны мочевыделительной системы
Частота неизвестна — почечная недостаточность, токсическая нефропатия.
Со стороны пищеварительной системы
Часто — диарея;
Нечасто — тошнота, рвота, колит (включая псевдомембранозный колит);
Редко — абдоминальные боли, запор;
Частота неизвестна — нарушения пищеварения.
Со стороны дыхательной системы
Редко — одышка.
Со стороны сердечно-сосудистой системы
Редко — вазодилатация;
Частота неизвестна — кровотечения.
Общие реакции и реакции в месте введения
Часто — флебит в месте введения, боль в месте введения;
Нечасто — повышение температуры и воспаление в месте введения;
Редко — озноб.
Лабораторные показатели
Часто — повышение активности аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (ACT), щелочной фосфатазы (ЩФ), общего билирубина, анемия, эозинофилия, увеличение протромбинового времени или частичного тромбопластинового времени;
Нечасто — повышение азота мочевины крови, креатинина сыворотки, тромбоцитопения, лейкопения и нейтропения;
Частота неизвестна — апластическая анемия, гемолитическая анемия, агранулоцитоз.
Прочие
Редко — генитальный зуд, изменение вкуса, вагинит, эритема, ложноположительная проба Кумбса без гемолиза.
Передозировка
Симптомы: энцефалопатия (спутанность сознания, галлюцинации, ступор, кома), миоклонические судороги, повышенная нервно-мышечная возбудимость.
Лечение: симптоматическая и поддерживающая терапия. В случае значительного превышения рекомендованных доз, особенно у пациентов с нарушением функции почек, показан гемодиализ.
Взаимодействие с другими лекарственными средствами
Раствор препарата фармацевтически несовместим с растворами метронидазола, ванкомицина, гентамицина, тобрамицина сульфата, нетилмицина сульфата, поэтому их нельзя смешивать. Однако при одновременном назначении цефепима и вышеуказанных препаратов каждый из них можно вводить раздельно.
Данные по совместимости растворов цефепима и других лекарственных препаратов, а также их по их стабильности приведены в таблице ниже.
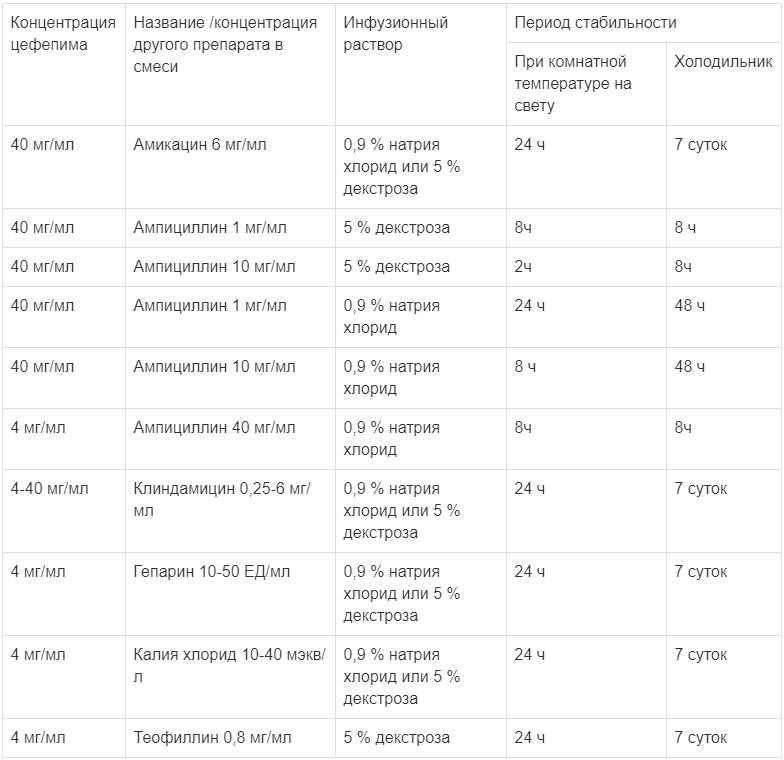
Особые указания
При наличии факторов, могущих вызвать нарушение функции почек, требуется корректировка дозы цефепима с целью компенсации уменьшенной скорости выведения препарата с мочой. Режим дозирования зависит от степени почечной недостаточности, тяжести инфекции и чувствительности микроорганизмов. При слабых или умеренных нарушениях функции почек начальная доза препарата такая же, как при нормальной функции почек. Риск развития токсических реакций особенно увеличивается у пожилых пациентов с нарушенной функцией почек.
Во время пострегистрационного наблюдения были зарегистрированы следующие серьезные нежелательные реакции, в том числе угрожающие жизни или приводящие к летальному исходу: энцефалопатия (нарушение сознания, включая спутанность сознания, галлюцинации, ступор и кома), миоклонус, судороги и бессудорожный эпилептический статус.
Большинство случаев отмечалось у пациентов с почечной недостаточностью, которым не проводилась коррекция дозы. Тем не менее, в некоторых случаях нейротоксичность отмечалась у пациентов, которым проводилась коррекция дозы в зависимости от степени почечной недостаточности. В большинстве случаев симптомы нейротоксичности были обратимы и исчезали после отмены препарата и/или после проведения гемодиализа. Если нейротоксичность связана с применением цефепима, следует рассмотреть вопрос о прекращении терапии цефепимом или корректировать дозу у пациентов с почечной недостаточностью. Перед началом лечения следует установить наличие в анамнезе у пациента аллергических реакций на цефепим, другие цефалоспориновые антибиотики, пенициллины и другие бета-лактамные антибиотики, а также других форм аллергии. При применении всех видов бета-лактамных антибиотиков отмечались случаи развития тяжелых реакций гиперчувствительности, иногда с летальным исходом.
Антибиотики группы цефалоспоринов могут быть причиной ложноположительной реакции на глюкозу в моче в тестах, основанных на восстановлении ионов меди (с растворами Бенедикта или Фелинга или с таблетками Клинитест), но не в ферментных тестах (с глюкозоксидазой). В связи с этим для определения глюкозы в моче рекомендуется применять ферментные тесты с глюкозоксидазой.
При развитии аллергической реакции следует прекратить лечение препаратом и предпринять соответствующие меры. При развитии тяжелой аллергической реакции (например, анафилактической реакции) непосредственно во время введения препарата может потребоваться применение эпинефрина и другой поддерживающей терапии.
При назначении эмпирического лечения необходимо принимать во внимание данные о приобретенной устойчивости микроорганизмов-возбудителей.
Устойчивость микроорганизмов может изменяться с течением времени и географического положения. Для идентификации микроорганизма-возбудителя и определения чувствительности к цефепиму следует провести соответствующие тесты. Цефепим может применяться в виде монотерапии даже до идентификации микроорганизма-возбудителя, так как он обладает широким спектром антибактериального действия в отношении грамположительных и грамотрицательных микроорганизмов. При риске смешанной аэробно/анаэробной инфекции (особенно, когда могут присутствовать нечувствительные к цефепиму микроорганизмы) лечение препаратом цефепим в комбинации с препаратом, действующим на анаэробы, можно начинать до идентификации возбудителя.
После идентификации возбудителя и определения чувствительности к антибиотикам лечение следует проводить в соответствии с результатами тестов.
Как и при применении других антибиотиков, лечение препаратом Цефепим может приводить к колонизации нечувствительной микрофлоры. При развитии суперинфекций во время лечения необходимо принятие соответствующих мер.
В исследованиях на крысах не было отмечено влияния на фертильность. Данные о влиянии на фертильность у людей при применении цефепима отсутствуют.
Clostridium difficile — ассоциированная диарея
При применении практически всех антибиотиков широкого спектра действия возможно возникновение диареи, ассоциированной с Clostridium difficile (CDAD — Clostridium difficile-associated diarrhea), которая может протекать как в легкой форме, так и в тяжелой, вплоть до летального исхода.
При возникновении диареи во время лечения препаратом необходимо подтвердить диагноз CDAD. Следует тщательно наблюдать за пациентом на предмет развития CDAD, поскольку регистрировались случаи ее возникновения спустя более двух месяцев после прекращения применения антибиотиков. При подозрении на CDAD или подтверждении данного диагноза необходимо прекратить применение антибиотиков, кроме тех, которые назначены для подавления Clostridium difficile. Нельзя применять лекарственные средства, тормозящие перистальтику кишечника.
Влияние на способность управлять транспортными средствами, механизмами
Изучение влияние препарата на способность к концентрации внимания не проводилось, однако, учитывая возможность развития побочных эффектов со стороны центральной нервной системы, во время лечения препаратом следует воздержаться от управления транспортными средствами и занятий другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Форма выпуска
Порошок для приготовления раствора для внутривенного и внутримышечного введения 0,5 г; 1,0 г; 2,0 г.
0,5 г или 1,0 г или 2,0 г действующего вещества во флаконы из трубки стеклянной для лекарственных средств вместимостью 10 мл, герметично укупоренные резиновыми пробками, обжатые колпачками алюминиевыми или комбинированными.
1; 5; 10 флаконов вместе с инструкцией по медицинскому применению укладывают в индивидуальную пачку из картона.
50 флаконов с приложением равного количества инструкций укладывают в коробку из картона (для стационаров).
Упаковка в комплекте с растворителем — водой для инъекций или 0,9 % раствором натрия хлорида. В комплект входят:
а) 1 флакон с препаратом по 0,5 г и 1 ампула с растворителем на 5 мл или 1 флакон с препаратом по 1,0 г или 2,0 г и 2 ампулы с растворителем на 5 мл;
б) 5 флаконов с препаратом по 0,5 г и 5 ампул с растворителем на 5 мл или 5 флаконов с препаратом по 1,0 г или 2,0 г и 10 ампул с растворителем на 5 мл;
в) 10 флаконов с препаратом по 0,5 г и 10 ампул с растворителем на 5 мл или 10 флаконов с препаратом по 1,0 г или 2,0 г и 20 ампул с растворителем на 5 мл.
Комплект укладывают в индивидуальную пачку из картона вместе с инструкцией по медицинскому применению, скарификатором ампульным.
При использовании ампул с надсечкой, кольцом излома или точкой излома скарификатор ампульный не вкладывают.
Условия хранения
В защищенном от света месте при температуре не выше 30°С.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности.
Условия отпуска
Отпускают по рецепту.
Владелец регистрационного удостоверения
ООО «ПРОМОМЕД РУС», Россия.
105005, г. Москва, ул. Почтовая М., дом 2/2, строение 1, пом I ком. 2.
Производитель
АО «Биохимик», Россия.
Юридический адрес: 430030, Республика Мордовия, г. Саранск, ул. Васенко, д. 15 А.
Адрес места производства: 430030, Республика Мордовия, г. Саранск, ул. Васенко, д. 15 А.
Организация, принимающая претензии потребителей
ООО «ПРОМОМЕД РУС», Россия.
129090, г. Москва, пр-т Мира, д.13, стр. 1.
Купить Цефепим в planetazdorovo.ru
*Цена в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Лекарственная форма
|
|
ЦЕФТОНИТ® |
Суспензия для инъекций рег. 44-3-3.17-3703№ПВР-3-29.11/02820 |
Форма выпуска, состав и упаковка
Суспензия для инъекций от белого до темно-кремового цвета.
Вспомогательные вещества: бутилгидрокситолуол (ионол), кремния диоксид коллоидный безводный (аэросил 300), триглицериды насыщенных жирных кислот (миритол 318).
Расфасована по 100 мл в стеклянные флаконы, герметично укупоренные резиновыми пробками, укрепленными алюминиевыми колпачками с клипсами контроля первого вскрытия. Флаконы с препаратом допускается упаковывать в индивидуальные пачки из картона. Каждая потребительская упаковка снабжена инструкцией по применению препарата.
Фармакологические (биологические) свойства и эффекты
Антибиотик группы цефалоспоринов.
Цефтиофура гидрохлорид, входящий в состав препарата, цефалоспориновый антибиотик III поколения, широкого спектра действия, оказывающий бактерицидное действие. Активен в отношении грамотрицательных и грамположительных бактерий, включая штаммы, продуцирующие β-лактамазы, и некоторые анаэробные бактерии: Actinobacillus spp., Actinobacillus pleuropneumoniae, Actinomyces spp., Actinomyces pyogenes, Bacillus spp., Citrobacter spp., Enterobacter spp., Escherichia spp., Escherichia coli, Fusobacterium spp, Fusobacterium necrophorum, Histophilus somni (Haemophilus somnus), Haemophilus spp., Haemophilus parasuis, Klebsiella spp., Pasteurella spp., в т.ч. Pasteurella (Mannheimia) haemolytica, Pasteurella multocida, Porphyromonas spp., Porphyromonas assacharolytica (Bacteroides melaninogenicus), Porphyromonas levii, Proteus spp., Salmonella spp., Salmonella choleraesuis, Salmonella typhimurium, Staphylococcus aureus, Staphylococcus spp.,Streptococcus suis, Streptococcus zooepidemicus, Streptococcus equi, Streptococcus agalactiae, Streptococcus dysgalactiae, Streptococcus uberis и Streptococcus bovis.
Механизм бактерицидного действия цефтиофура заключается в ингибировании функциональной активности бактериальных ферментов транспептидаз, участвующих в связывании основного компонента клеточной стенки микроорганизмов — пептидогликана, что приводит к нарушению осмотического баланса и разрушению бактериальной клетки.
После парентерального введения препарата цефтиофур поступает в системный кровоток, быстро метаболизируется с образованием десфуроилцефтиофура, который обладает эквивалентной цефтиофуру антибактериальной активностью, обратимо связывается с белками плазмы и концентрируется в местах воспаления. Cmax цефтиофура и его метаболитов в крови достигается через 0.5-2 ч и сохраняется на терапевтическом уровне не менее 20 ч. Выводится из организма, главным образом, с мочой (свыше 55%) и частично с фекалиями.
Цефтонит® по степени воздействия на организм относится к малоопасным веществам (4 класс опасности по ГОСТ 12.1.007-76).
Показания к применению препарата ЦЕФТОНИТ®
Крупному рогатому скоту для лечения заболеваний бактериальной этиологии, возбудители которых чувствительны к цефтиофуру, в т.ч.
- инфекции органов дыхания, вызываемые Pasteurella haemolytica, Pasteurella multocida, Haemophilus somnus;
- некробактериоз, вызываемый Fusobacterium necrophorum и Porphyromonas assacharolytica (Bacteroides melaninogenicus);
- острый эндометрит.
Свиньям для лечения заболеваний, возбудители которых чувствительны к цефтиофуру, в т.ч.:
- инфекции органов дыхания, вызываемые Pasteurella haemolytica, Pasteurella multocida, Actinobacillus pleuropneumoniae и Streptococcus suis.
Порядок применения
Цефтонит® вводят крупному рогатому скоту 1 раз/сут п/к в дозе 1 мл на 50 кг массы животного (1 мг цефтиофура на 1 кг). Курс лечения при заболеваниях дыхательных путей составляет 3-5 дней, при некробактериозе — 3 дня, при эндометрите — 5 дней.
Свиньям при заболеваниях органов дыхания препарат вводяи в/м 1 раз/сут в дозе 1 мл на 16 кг массы животного (3 мг цефтиофура на 1 кг) в течение 3 дней.
Перед каждым использованием флакон с препаратом следует тщательно встряхнуть.
Особенностей действия при первом применении и отмене лекарственного препарата не выявлено.
Следует избегать пропусков при введении очередной дозы препарата, т.к. это может привести к снижению терапевтической эффективности. При пропуске одной или нескольких доз препарата курс применения необходимо возобновить в предусмотренном режиме дозирования. Не следует превышать рекомендуемую дозу для компенсации пропущенной.
Побочные эффекты
При использовании препарата Цефтонит® согласно инструкции по применению побочных явлений и осложнений, как правило, не наблюдается. В редких случаях в месте инъекции возможно развитие отека, который рассасывается самопроизвольно в течение нескольких суток. При повышенной индивидуальной чувствительности животного к антибиотикам группы цефалоспоринов и возникновении аллергических реакций использование препарата прекращают, животному назначают антигистаминные препараты и симптоматическую терапию.
При передозировке препарата у животного может наблюдаться снижение аппетита, воспалительная реакция в месте инъекции.
Противопоказания к применению препарата ЦЕФТОНИТ®
- индивидуальная повышенная чувствительность животных к цефтиофуру и другим бета-лактамным антибиотикам.
Особые указания и меры личной профилактики
Цефтонит® не следует применять одновременно с антибиотиками группы тетрациклина и левомицетином в связи с возможным снижением его бактерицидной активности, с антибиотиками группы аминогликозидов, фуросемидом и этакриновой кислотой из-за возможного усиления нефротоксического эффекта.
Особенности применения препарата самкам во время беременности и лактации не установлены.
Убой на мясо крупного рогатого скота разрешается не ранее чем через 8 суток, свиней — не ранее чем через 5 суток после последнего введения лекарственного препарата. Мясо животных, вынужденно убитых до истечения указанного срока, может быть использовано для кормления пушных зверей. Молоко дойных коров в период применения препарата разрешается использовать в пищевых целях без ограничений.
Меры личной профилактики
При применении препарата Цефтонит® следует соблюдать общие правила личной гигиены и техники безопасности, предусмотренные при работе с лекарственными препаратами. Во время работы с препаратом запрещается пить, курить и принимать пищу. По окончании работы с препаратом руки следует вымыть теплой водой с мылом.
Людям с гиперчувствительностью к компонентам препарата следует избегать прямого контакта с препаратом Цефтонит®. При случайном контакте лекарственного препарата с кожей или слизистыми оболочками глаз их необходимо промыть большим количеством воды. В случае появления аллергических реакций или при случайном попадании препарата в организм человека следует немедленно обратиться в медицинское учреждение (при себе иметь инструкцию по применению препарата или этикетку).
Пустую тару из-под лекарственного препарата запрещается использовать для бытовых целей; она подлежит утилизации с бытовыми отходами.
Условия хранения ЦЕФТОНИТ®
Препарат следует хранить в закрытой упаковке производителя, отдельно от продуктов питания и кормов, в защищенном от прямых солнечных лучей, недоступном для детей месте при температуре от 5° до 25°С.
Неиспользованный лекарственный препарат утилизируют в соответствии с требованиями действующего законодательства.
Срок годности ЦЕФТОНИТ®
Срок годности при соблюдении условий хранения в закрытой упаковке производителя — 3 года со дня производства; после первого вскрытия первичной упаковки — не более 28 суток. Запрещается применять Цефтонит® по истечении срока годности.
Условия отпуска
Препарат отпускают без рецепта.
Контакты для обращений
|
|
410010 Саратов, |
ЦЕФТОНИТ® отзывы
Помогите другим с выбором, оставьте отзыв об ЦЕФТОНИТ®
Оставить отзыв
Выбор описания
| Лек. форма | Дозировка |
|---|---|
|
порошок для приготовления раствора для внутривенного и внутримышечного введения |
0.5 г 1 г 2 г 1000 мг |
|
порошок для приготовления раствора для внутримышечного введения |
0.5 г 1 г |
порошок для приготовления раствора для внутривенного и внутримышечного введения
порошок для приготовления раствора для внутримышечного введения
Цефепим (порошок для приготовления раствора для внутривенного и внутримышечного введения, 1000 мг), инструкция по медицинскому применению РУ № ЛС-002441
Дата последнего изменения: 10.02.2021
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Фармакологическая группа
- Лекарственная форма
- Состав
- Описание лекарственной формы
- Фармакокинетика
- Фармакодинамика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Аналоги (синонимы) препарата Цефепим
- Заказ в аптеках Москвы
Действующее вещество
ATX
Фармакологическая группа
Лекарственная форма
Порошок
для приготовления раствора для внутривенного и внутримышечного введения.
Состав
На
1 флакон
Действующее вещество:
Цефепима
гидрохлорида моногидрат — 1,19 г, в пересчете на цефепим — 1,0 г.
Вспомогательное вещество:
L-аргинин
— 0,73 г.
Примечание.
Масса содержимого флакона зависит от активности цефепима.
Описание лекарственной формы
Порошок
белого или белого с желтоватым оттенком цвета.
Фармакокинетика
Биодоступность
— 100%. Время достижения максимальной концентрации после внутривенного и
внутримышечного введения в дозе 0,5 г — к концу инфузии 1–2 часа
соответственно. Максимальная концентрация при внутримышечном введении в дозах
0,5, 1 и 2 г — 14, 30 и 57 мкг/мл соответственно; при внутривенном
введении в дозах 0,25, 0,5, 1 и 2 г — 18, 39, 82 и 164 мкг/мл
соответственно; время достижения средней терапевтической концентрации в плазме
— 12 часов; средняя терапевтическая концентрация при внутримышечном введении
— 0,2 мкг/мл, при внутривенном введении — 0,7 мкг/мл. Высокие
концентрации определяются в моче, желчи, перитонеальной жидкости, экссудате
волдыря, слизистом секрете бронхов, мокроте, предстательной железе, аппендиксе
и желчном пузыре. Объем распределения — 0,25 л/кг, у детей от 2 месяцев до
16 лет — 0,33 л/кг. Связь с белками плазмы — 20%. Метаболизируется в
печени и почках на 15%. Период полувыведения — 2 часа, общий клиренс —
120 мл/мин, почечный клиренс — 110 мл/мин. Выводится почками (путем
гломерулярной фильтрации в неизмененном виде — 85%), с грудным молоком. Период
полувыведения при гемодиализе — 13 часов, при непрерывном перитонеальном
диализе — 19 часов.
Фармакодинамика
Антибактериальное
средство из группы цефалоспоринов IV поколения. Действует бактерицидно, нарушая
синтез клеточной стенки микроорганизмов. Обладает широким спектром действия в
отношении грамположительных и грамотрицательных бактерий, штаммов, резистентных
к аминогликозидам и/или цефалоспориновым антибиотикам III поколения.
Высокоустойчив к гидролизу большинства бета-лактамаз и быстро проникает в
грамотрицательные бактериальные клетки. Внутри бактериальной клетки
молекулярной мишенью является пенициллинсвязывающие белки.
Активен
in vivo и in vitro в отношении грамположительных
аэробов: Staphylococcus aureus
(только метициллинчувствительные штаммы), Streptococcus
pneumoniae, Streptococcus pyogenes (группа A), Streptococcus группы viridans;
грамотрицательных
аэробов: Enterobacter spp., Escherichia
coli, Klebsiella pneumoniae, Proteus mirabilis, Pseudomonas aeruginosa.
In vitro активен (но
клиническая значимость неизвестна) в отношении грамположительных аэробов: Staphylococcus epidermidis (только
метициллинчувствительные штаммы), Staphylococcus
saprophyticus, Streptococcus agalactiae (группа В);
грамотрицательных
аэробов: Acinetobacter Iwoffii, Citrobacter
diversus, Citrobacter freundii, Enterobacter agglomerans, Haemophilus
influenzae (включая штаммы, продуцирующие бета‑лактамазу), Hafnia alvei, Klebsiella oxytoca, Moraxella
catarrhalis (включая штаммы, продуцирующие бета‑лактамазы), Morganella morganii, Proteus vulgaris, Providencia
rettgeri, Providencia stuartii, Serratia marcescens.
Большинство
штаммов Enterococcus spp., в том
числе Enterococcus faecalis,
метициллинрезистентные стафилококки, Stenotrophomonas
maltophilia (ранее известная как Xanthomonas
maltophilia и Pseudomonas
maltophilia), Clostridium
difficile не чувствительны к цефепиму.
Показания
Инфекционно-воспалительные
заболевания, вызванные чувствительными к цефепиму микроорганизмами: пневмония
(среднетяжелая и тяжелая), вызванная Streptococcus
pneumoniae (в том числе случаи ассоциации с сопутствующей
бактериемией), Pseudomonas aeruginosa,
Klebsiella pneumoniae или Enterobacter spp.;
Фебрильная
нейтропения (эмпирическая терапия);
Осложненные
и неосложненные инфекции мочевыводящих путей (включая пиелонефрит), вызванные Escherichia coli, Klebsiella pneumoniae, Proteus
mirabilis;
Неосложненные
инфекции кожи и мягких тканей, вызванные Staphylococcus
aureus (только метициллинчувствительные штаммы), Streptococcus pyogenes;
Осложненные
интраабдоминальные инфекции (в комбинации с метронидазолом), вызванные Escherichia coli, Klebsiella pneumoniae, Pseudomonas
aeruginosa, Enterobacter spp.
Противопоказания
Гиперчувствительность
к цефепиму, компонентам препарата, другим цефалоспоринам, пенициллинам, другим
бета-лактамным антибиотикам, детский возраст до 2 месяцев (для
внутривенного введения), детский возраст до 12 лет (для внутримышечного
введения), период лактации.
С осторожностью
Заболевания
желудочно-кишечного тракта (в том числе в анамнезе), особенно колит,
региональный энтерит или антибиотико-ассоциированный колит, тяжелая хроническая
почечная недостаточность.
Применение при беременности и кормлении грудью
Применение
препарата во время беременности возможно только в тех случаях, когда
потенциальная польза для матери превышает риск для плода.
При
необходимости назначения препарата в период лактации грудное вскармливание
следует приостановить.
Способ применения и дозы
Реклама: ООО «РЛС-Патент», ИНН 5044031277, erid=4CQwVszH9pUkpHxmQQo
Препарат
применяется внутривенно (в/в), внутримышечно (в/м). Дозы и путь введения
зависят от чувствительности возбудителей, тяжести инфекции, состояния функции
почек и общего состояния пациента.
Режимы дозирования цефепима в зависимости от заболевания,
массы тела и возраста пациента
Доза
для детей не должна превышать максимальную рекомендуемую дозу для взрослых
(2 г в/в, каждые 8 часов). Опыт внутримышечного введения препарата
детям ограничен.
Взрослые и дети с массой тела более 40 кг при
нормальной функции почек
|
Инфекции |
500 мг–1 г в/в |
каждые 12 |
|
Другие |
1 г в/в или |
каждые 12 |
|
Тяжелые |
2 г в/в |
каждые 12 |
|
Очень |
2 г в/в |
каждые 8 часов |
Обычная
продолжительность лечения составляет 7–10 дней; при тяжелых инфекциях может
потребоваться более продолжительное лечение.
В
случае лечения фебрильной нейтропении обычная продолжительность лечения
составляет 7 дней или до исчезновения нейтропении.
Профилактика инфекций при проведении хирургических операций
За
60 минут до начала хирургической операции вводят 2 г препарата в/в в
виде инфузии в течение 30 минут. Сразу после окончания инфузии пациенту
вводят 500 мг метронидазола внутривенно. Раствор метронидазола готовят в
соответствии с инструкцией по его применению. Вследствие фармацевтической
несовместимости метронидазола и цефепима их не следует смешивать в одном
сосуде. Инфузионную систему перед введением метронидазола следует промыть. Во
время длительных (более 12 ч) хирургических операций через 12 ч после
первой дозы рекомендуется повторное введение цефепима в той же дозе с последующим
введением метронидазола.
Дети от 2 месяцев с массой тела до 40 кг
При
инфекциях мочевых путей, инфекциях кожи и мягких тканей, пневмонии
рекомендуемая доза составляет 50 мг/кг каждые 12 часов в течение 10
дней. В случае тяжелых инфекций — каждые 8 часов.
Пациентам
с фебрильной нейтропенией, септицемией, бактериальным менингитом следует
вводить 50 мг/кг каждые 8 часов в течение 7–10 дней.
Пациенты с нарушением функции почек
Больным
с нарушением функции почек требуется корректировка дозировки цефепима с целью
компенсации уменьшенной скорости выведения препарата с мочой. Режим дозирования
зависит от степени нарушения функции почек, тяжести инфекции и чувствительности
микроорганизмов. При слабых или умеренных нарушениях функции почек начальная
доза препарата такая же, как при нормальной функции почек.
Рекомендуемые поддерживающие дозы цефепима в зависимости от
клиренса креатинина представлены в таблице ниже.
Клиренс
креатинина для мужчин рассчитывают, исходя из концентрации сывороточного
креатинина по следующей формуле:
Клиренс
креатинина для женщины рассчитывают по той же формуле, используя фактор 0,85.
|
Клиренс |
Рекомендуемые |
|||
|
(Обычная доза, |
||||
|
>60 |
2 г каждые 8 ч |
2 г каждые 12 |
1 г каждые 12 |
500 мг каждые |
|
30–60 |
2 г каждые 12 |
2 г каждые 24 |
1 г каждые 24 |
500 мг каждые |
|
11–29 |
2 г каждые 24 |
1 г каждые 24 |
500 мг каждые |
500 мг каждые |
|
≤10 |
1 г каждые 24 |
500 мг каждые |
250 мг каждые |
250 мг каждые |
|
Пациенты |
500 мг каждые |
500 мг каждые |
500 мг каждые |
500 мг каждые |
*
Для пациентов на гемодиализе рекомендуется уменьшение дозы препарата: 1 г
в первый день лечения и затем по 500 мг в день при всех инфекциях, за
исключением фебрильной нейтропении, где доза составляет 1 г в день. В дни
диализа препарат следует вводить по окончании диализа. По возможности препарат
следует вводить в одно и то же время каждый день.
При
гемодиализе в течение 3 ч из организма удаляется приблизительно 68%
введенной дозы препарата.
При
непрерывном амбулаторном перитонеальном диализе препарат можно использовать в
исходных рекомендованных дозах 500 мг, 1 г или 2 г, в
зависимости от тяжести инфекции, с интервалами между введениями —
48 часов.
Дети с нарушением функции почек
Детям
при нарушенной функции почек рекомендуется уменьшение дозы или увеличение
интервала между введениями, как указано выше в таблице.
Клиренс
креатинина вычисляют по следующим формулам:
или
Пациенты с нарушением функции печени
Коррекция
дозы для пациентов с нарушением функции печени не требуется.
Приготовление инъекционных растворов
Для
приготовления раствора для внутривенного введения препарат (1,0 г)
растворяют в 10 мл стерильной воды для инъекций, 5% растворе декстрозы или
0,9% растворе натрия хлорида для инъекций и вводят в течение 3–5 минут
непосредственно в вену. Для внутривенной инфузии приготовленный раствор (см.
выше) совмещают с другими растворами для внутривенных инфузий (0,9% раствор натрия
хлорида, 5% или 10% раствор декстрозы, Рингера лактата раствор; максимальная
концентрация 40 мг/мл) и вводят в течение не менее 30 минут.
Для
приготовления раствора для внутримышечного введения препарат (1,0 г)
растворяют в 3,0 мл стерильной воды для инъекций, 0,9% раствора натрия
хлорида, бактериостатической воды для инъекций с парабеном или бензиловым
спиртом, в 0,5% или 1% раствора лидокаина гидрохлорида. Доза 1 г может
быть введена за 1 инъекцию, максимальная доза (2 г) — в виде двух инъекций
в разные места.
Побочные действия
Наиболее
часто отмечаются побочные эффекты со стороны желудочно-кишечного тракта и
аллергические реакции. Ниже перечислены побочные эффекты по органам и системам
в соответствии с их частотой: очень частые (≥10%); частые (≥1% и
<10%); нечастые (≥0,1% и <1%); редкие (≥0,01% и <0,1%);
частота неизвестна (нет данных о частоте развития данного побочного эффекта).
Инфекционные и паразитарные заболевания:
Нечасто — кандидоз
слизистой оболочки полости рта, вагинальные инфекции; редко — кандидозы.
Со стороны иммунной системы:
Редко —
анафилактические реакции; частота неизвестна
— анафилактический шок, токсический эпидермальный некролиз, мультиформная
эритема, синдром Стивенса‑Джонсона, ангионевротический отек.
Со стороны нервной системы:
Нечасто — головная
боль; редко — судороги,
парестезии, дисгевзия, головокружение, изменение вкуса; частота неизвестна — пострегистрационный
опыт: энцефалопатия (нарушение сознания, включая спутанность сознания,
галлюцинации, ступор и кома), миоклонус, судороги и бессудорожный
эпилептический статус. Несмотря на то, что большинство случаев отмечались у
пациентов с почечной недостаточностью, которые получали цефепим в дозах, выше
рекомендованных, в некоторых случаях нейротоксичность отмечалась у пациентов, которым
проводилась коррекция дозы в зависимости от степени почечной недостаточности.
Со стороны сосудов:
Редко —
вазодилатация; частота неизвестна —
кровотечения.
Со стороны дыхательной системы, органов грудной клетки и
средостения:
Редко — одышка.
Со стороны желудочно-кишечного тракта:
Часто — диарея; нечасто — тошнота, рвота, колит (включая
псевдомембранозный колит); редко
— абдоминальные боли, запор; частота неизвестна — нарушение пищеварения.
Со стороны кожи и подкожных тканей:
Часто — высыпания на
коже; нечасто — эритема,
крапивница, зуд.
Со стороны почек и мочевыводящих путей:
Частота неизвестна
— почечная недостаточность, токсическая нефропатия.
Общие расстройства и нарушения в месте введения:
Часто — флебит в
месте введения, боль в месте введения; нечасто
— повышение температуры и воспаление в месте введения; редко — озноб.
Со стороны половых органов и молочной железы:
Редко — генитальный
зуд, вагинит.
Изменения со стороны лабораторных показателей:
Часто — повышение
активности аланинаминотрансферазы, аспартатаминотрансферазы, щелочной
фосфатазы, общего билирубина, анемия, эозинофилия, увеличение протромбинового
времени или частичного тромбопластинового времени; нечасто — повышение азота мочевины крови, креатинина
сыворотки, тромбоцитопения, лейкопения и нейтропения; редко — ложноположительная проба Кумбса
без гемолиза; частота неизвестна
— апластическая анемия, гемолитическая анемия, агранулоцитоз.
Взаимодействие
Реклама: ООО «ВЕДАНТА», ИНН 7714886235, erid 4CQwVszH9pUkKJ7jUDd
Реклама: ООО «РЛС-Библиомед» ИНН 7714758963
Реклама: ООО «ВЕДАНТА», ИНН 7714886235, erid 4CQwVszH9pUkKJ7jUDd
Реклама: ООО «РЛС-Библиомед» ИНН 7714758963
Фармацевтически
несовместим с другими противомикробными лекарственными средствами и гепарином.
Диуретики
снижают канальцевую секрецию цефепима и повышают его концентрацию в сыворотке
крови, удлиняют период полувыведения, усиливают нефротоксичность (повышается
риск развития нефронекроза).
Нестероидные
противовоспалительные препараты, замедляя выведение цефалоспоринов, повышают
риск развития кровотечения.
Несовместим
с раствором метронидазола (перед введением раствора метронидазола для
профилактики инфекций при проведении хирургических вмешательств следует промыть
инфузионную систему от раствора цефепима).
Повышает
нефро- и ототоксичность аминогликозидов.
Передозировка
Симптомы (чаще
возникают у больных с хронической почечной недостаточностью)
Судороги,
энцефалопатия, нервно-мышечное возбуждение.
Лечение
Гемодиализ
и симптоматическая терапия.
Особые указания
При
наличии факторов, которые могут вызвать нарушение функции почек, требуется
корректировка дозы цефепима с целью компенсации уменьшенной скорости выведения
препарата с мочой. Режим дозирования зависит от степени почечной
недостаточности, тяжести инфекции и чувствительности микроорганизмов. При
слабых или умеренных нарушениях функции почек начальная доза препарата такая
же, как при нормальной функции почек. Риск развития токсических реакций
особенно увеличивается у пожилых пациентов с нарушенной функцией почек.
Как
и при использовании других представителей этого класса, в практике применения
цефепима отмечались случаи развития у пациентов энцефалопатии (обычно
обратимой) (спутанность сознания, галлюцинации, ступор, кома), миоклонуса,
судорог (в том числе бессудорожный эпилептический статус) и/или почечной
недостаточности. Большинство случаев отмечалось у пациентов с нарушениями
функции почек, которым назначались дозы выше рекомендованных. Обычно симптомы
нейротоксичности исчезали после проведения гемодиализа, однако иногда они
заканчивались летальным исходом. У пациентов с нарушениями функции почек или
при наличии других факторов, могущих приводить к замедлению выведения цефепима,
следует скорректировать его дозу.
Перед
началом лечения следует установить наличие в анамнезе у больного аллергических
реакций на цефепим, другие цефалоспориновые антибиотики, пенициллины и другие
бета‑лактамные антибиотики, а также других форм аллергии.
При
применении всех видов бета-лактамных антибиотиков отмечались случаи развития
тяжелых реакций гиперчувствительности, иногда с летальным исходом. При развитии
аллергической реакции следует прекратить лечение препаратом и предпринять
соответствующие меры. При развитии тяжелой аллергической реакции (например,
анафилактической реакции) непосредственно во время введения препарата может
потребоваться применение эпинефрина и другой поддерживающей терапии.
Антибиотики
группы цефалоспоринов могут быть причиной ложноположительной реакции на глюкозу
в моче в тестах, основанных на восстановлении ионов меди (с растворами
Бенедикта или Фелинга или с таблетками Клинитест), но не в ферментных тестах (с
глюкозоксидазой). В связи с этим для определения глюкозы в моче рекомендуется
применять ферментные тесты с глюкозоксидазой.
В
исследованиях на крысах не было отмечено влияния на фертильность. Данные о
влиянии на фертильность у людей при применении цефепима отсутствуют.
При
назначении эмпирического лечения необходимо принимать во внимание данные о
приобретенной устойчивости микроорганизмов-возбудителей. Устойчивость
микроорганизмов может изменяться с течением времени и географического
положения. Для идентификации микроорганизма‑возбудителя и определения
чувствительности к цефепиму следует провести соответствующие тесты. Цефепим
может применяться в виде монотерапии даже до идентификации
микроорганизма-возбудителя, так как он обладает широким спектром
антибактериального действия в отношении грамположительных и грамотрицательных
микроорганизмов. При риске смешанной аэробно/анаэробной инфекции (особенно,
когда могут присутствовать нечувствительные к цефепиму микроорганизмы) лечение
препаратом цефепим в комбинации с препаратом, действующим на анаэробы, можно
начинать до идентификации возбудителя.
После
идентификации возбудителя и определения чувствительности к антибиотикам лечение
следует проводить в соответствии с результатами тестов.
Как
и при применении других антибиотиков, лечение препаратом цефепим может
приводить к колонизации нечувствительной микрофлоры. При развитии суперинфекций
во время лечения необходимо принятие соответствующих мер.
Clostridium difficile
ассоциированная диарея.
При
применении практически всех антибиотиков широкого спектра действия возможно
возникновение диареи, ассоциированной с Clostridium difficile (CDAD
— Clostridium difficile‑associated diarrhea),
которая может протекать как в легкой форме, так и в тяжелой, вплоть до
летального исхода. При возникновении диареи во время лечения препаратом
необходимо подтвердить диагноз CDAD.
Следует тщательно наблюдать за больным на предмет развития CDAD,
поскольку регистрировались случаи ее возникновения спустя более двух месяцев
после прекращения применения антибиотиков. При подозрении или подтверждении CDAD
необходимо прекратить применение антибиотиков, кроме тех, которые назначены для
подавления Clostridium difficile. Нельзя применять
лекарственные средства, тормозящие перистальтику кишечника.
Влияние на способность управлять
транспортными средствами, механизмами
В
период лечения необходимо воздержаться от вождения автотранспорта и занятий
потенциально опасными видами деятельности, требующими повышенной концентрации
внимания и быстроты психомоторных реакций.
Форма выпуска
Порошок
для приготовления раствора для внутривенного и внутримышечного введения
1,0 г.
По
1,0 г действующего вещества во флаконы стеклянные из нейтрального стекла
марок НС‑1, НС‑3 или стекла 1-го гидролитического класса
вместимостью 10 мл, герметично укупоренные резиновыми пробками, обжатые
колпачками алюминиевыми или колпачками комбинированными.
1. По
1 флакону с препаратом и инструкцией по применению препарата помещают в пачку
из картона.
2. Для
стационаров. По 10, 14, 25, 50 флаконов с препаратом с равным количеством
инструкций по применению препарата помещают в коробку (с перегородками или без
перегородок) из картона.
Условия отпуска из аптек
Условия хранения
В
защищенном от света месте при температуре не выше 25 °С.
Хранить
в недоступном для детей месте.
Срок годности
2
года.
Не
применять по истечении срока годности, указанного на упаковке.
Дата обновления: 09.08.2023
Аналоги (синонимы) препарата Цефепим
Заказ в аптеках
Выбор региона:
| Название препарата | Цена за упак., руб. | Аптеки |
|---|---|---|
|
Цефепим, порошок для приготовления раствора для внутривенного и внутримышечного введения, |
||
|
20.50 |
|
|
|
130.00 |
|
|
|
Цефепим, порошок для приготовления раствора для внутривенного и внутримышечного введения, |
||
|
82.00 |
|
|
|
Цефепим, порошок для приготовления раствора для внутривенного и внутримышечного введения, |
||
|
103.00 |
|
|
|
Цефепим, порошок для приготовления раствора для внутривенного и внутримышечного введения, |
||
|
134.00 |
|
|
|
Цефепим, порошок для приготовления раствора для внутривенного и внутримышечного введения, |
||
|
218.00 |
|
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
Перед применением флакон с препаратом тщательно встряхивают до получения гомогенной суспензии. Применяют парентерально один раз в сутки в следующих дозах:
— крупному рогатому скоту подкожно
1 мл на 50 кг массы тела (1,1 мг цефтиофура на 1 кг массы):
при остром межпальцевом некробактериозе в течение 3 дней;
при респираторных заболеваниях в течение 3-5 дней;
2 мл на 50 кг массы тела (2,2 мг цефтиофура на 1 кг массы)
при остром послеродовом эндометрите (первые 10 дней послеотельного периода) в течение 5 дней;
— свиньям внутримышечно
1 мл на 16 кг массы животного (3 мг цефтиофура на 1 кг массы) в течение 3-5 дней.
Следует избегать пропусков при введении очередной дозы препарата, так как это может привести к снижению терапевтической эффективности. В случае пропуска одной дозы необходимо ввести её как можно скорее, далее интервал между введениями препарата не изменяется.