Медикамент запрещен для реализации в аптеках.
|
||
|
||
|
||
|
||
|
||
|
||
|
||
|
||
|
||
|
||
|

Информация о лекарственных препаратах, размещенная на AptekaMos.ru, не должна использоваться неспециалистами для самостоятельного принятия решения об их покупке и применении без консультации врача.
Свидетельство о регистрации средства массовой информации ЭЛ № ФС77-44705 выдано Федеральной службой по надзору в сфере связи, информационных технологий и массовых коммуникаций (Роскомнадзор) 21 апреля 2011 года.
• Инструкция по применению Ацикловир-Акри суспензия д/вн приема 4% 100мл.
• Способ применения и дозировка, состав, побочное действие и взаимодействие Ацикловир-Акри суспензия д/вн приема 4% 100мл
Acyclovir Oral Suspension Prescribing Information
Package insert / product label
Dosage form: oral suspension
Drug class: Purine nucleosides
Medically reviewed by Drugs.com. Last updated on Sep 5, 2022.
On This Page
- Description
- Clinical Pharmacology
- Drug Interactions
- Clinical Studies
- Indications and Usage
- Contraindications
- Warnings
- Precautions
- Adverse Reactions/Side Effects
- Overdosage
- Dosage and Administration
- How Supplied/Storage and Handling
Acyclovir Oral Suspension Description
Acyclovir is a synthetic nucleoside analogue active against herpes viruses. Acyclovir Oral Suspension is a formulation for oral administration.
Each teaspoonful (5 mL) of Acyclovir Oral Suspension contains 200 mg of acyclovir and the inactive ingredients methylparaben 0.1% and propylparaben 0.01% (added as preservatives), microcrystalline cellulose, sodium carboxymethylcellulose, Banana Flavor NAT & ART 805.0079U, glycerin, and sorbitol.
Acyclovir, USP is a white to off-white, crystalline powder with the molecular formula C
8H
11N
5O
3 and a molecular weight of 225. The maximum solubility in water at 37°C is 2.5 mg/mL. The pka’s of acyclovir are 2.16 and 9.04.
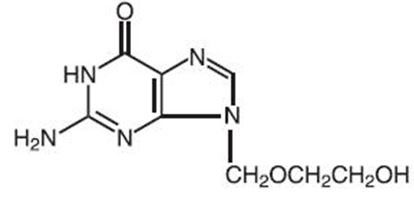
The chemical name of acyclovir is 2-amino-1,9-dihydro-9-[(2-hydroxyethoxy)methyl]-6
H-purin-6-one; it has the following structural formula:
VIROLOGY
Mechanism of Antiviral Action
Acyclovir is a synthetic purine nucleoside analogue with
in vitro and
in vivo inhibitory activity against herpes simplex virus types 1 (HSV-1), 2 (HSV-2), and varicella-zoster virus (VZV).
The inhibitory activity of acyclovir is highly selective due to its affinity for the enzyme thymidine kinase (TK) encoded by HSV and VZV. This viral enzyme converts acyclovir into acyclovir monophosphate, a nucleotide analogue. The monophosphate is further converted into diphosphate by cellular guanylate kinase and into triphosphate by a number of cellular enzymes.
In vitro, acyclovir triphosphate stops replication of herpes viral DNA. This is accomplished in 3 ways: 1) competitive inhibition of viral DNA polymerase, 2) incorporation into and termination of the growing viral DNA chain, and 3) inactivation of the viral DNA polymerase. The greater antiviral activity of acyclovir against HSV compared with VZV is due to its more efficient phosphorylation by the viral TK.
Antiviral Activities
The quantitative relationship between the
in vitro susceptibility of herpes viruses to antivirals and the clinical response to therapy has not been established in humans, and virus sensitivity testing has not been standardized. Sensitivity testing results, expressed as the concentration of drug required to inhibit by 50% the growth of virus in cell culture (IC
50), vary greatly depending upon a number of factors. Using plaque-reduction assays, the IC
50 against herpes simplex virus isolates ranges from 0.02 to13.5 mcg/mL for HSV-1 and from 0.01 to 9.9mcg/mL for HSV-2. The IC
50 for acyclovir against most laboratory strains and clinical isolates of VZV ranges from 0.12 to 10.8 mcg/mL. Acyclovir also demonstrates activity against the Oka vaccine strain of VZV with a mean IC
50 of1.35 mcg/mL.
Drug Resistance
Resistance of HSV and VZV to acyclovir can result from qualitative and quantitative changes in the viral TK and/or DNA polymerase. Clinical isolates of HSV and VZV with reduced susceptibility to acyclovir have been recovered from immunocompromised patients, especially with advanced HIV infection. While most of the acyclovir-resistant mutants isolated thus far from immunocompromised patients have been found to be TK-deficient mutants, other mutants involving the viral TK gene (TK partial and TK altered) and DNA polymerase have been isolated. TK-negative mutants may cause severe disease in infants and immunocompromised adults. The possibility of viral resistance to acyclovir should be considered in patients who show poor clinical response during therapy.
Acyclovir Oral Suspension — Clinical Pharmacology
Pharmacokinetics
The pharmacokinetics of acyclovir after oral administration have been evaluated in healthy volunteers and in immunocompromised patients with herpes simplex or varicella-zoster virus infection. Acyclovir pharmacokinetic parameters are summarized in Table 1.
|
* Bioavailability decreases with increasing dose. |
|
|
Parameter |
Range |
|
Plasma protein binding |
9% to 33% |
|
Plasma elimination half-life |
2.5 to 3.3 hr |
|
Average oral bioavailability |
10% to 20%* |
In one multiple-dose, crossover study in healthy subjects (n = 23), it was shown that increases in plasma acyclovir concentrations were less than dose proportional with increasing dose, as shown in Table 2. The decrease in bioavailability is a function of the dose and not the dosage form.
|
Parameter |
200 mg |
400 mg |
800 mg |
|
Cmax SS |
0.83 mcg/mL |
1.21 mcg/mL |
1.61 mcg/mL |
|
Ctrough SS |
0.46 mcg/mL |
0.63 mcg/mL |
0.83 mcg/mL |
There was no effect of food on the absorption of acyclovir (n = 6); therefore, Acyclovir Oral Suspension may be administered with or without food.
The only known urinary metabolite is 9-[(carboxymethoxy)methyl]guanine.
Special Populations
Adults with Impaired Renal Function
The half-life and total body clearance of acyclovir are dependent on renal function. A dosage adjustment is recommended for patients with reduced renal function (see
DOSAGE AND ADMINISTRATION).
Geriatrics
Acyclovir plasma concentrations are higher in geriatric patients compared with younger adults, in part due to age-related changes in renal function. Dosage reduction may be required in geriatric patients with underlying renal impairment (see
PRECAUTIONS: Geriatric Use).
Pediatrics
In general, the pharmacokinetics of acyclovir in pediatric patients is similar to that of adults.
Mean half- life after oral doses of 300 mg/m
2 and 600 mg/m
2 in pediatric patients aged 7 months to 7 years was 2.6 hours (range 1.59 to 3.74 hours).
Drug Interactions
Coadministration of probenecid with intravenous acyclovir has been shown to increase the mean acyclovir half-life and the area under the concentration-time curve. Urinary excretion and renal clearance were correspondingly reduced.
Clinical Trials
Initial Genital Herpes
Double-blind, placebo-controlled studies have demonstrated that orally administered acyclovir significantly reduced the duration of acute infection and duration of lesion healing. The duration of pain and new lesion formation was decreased in some patient groups.
Recurrent Genital Herpes
Double-blind, placebo-controlled studies in patients with frequent recurrences (6 or more episodes per year) have shown that orally administered acyclovir given daily for 4 months to 10 years prevented or reduced the frequency and/or severity of recurrences in greater than 95% of patients.
In a study of patients who received acyclovir 400 mg twice daily for 3 years, 45%, 52%, and 63% of patients remained free of recurrences in the first, second, and third years, respectively. Serial analyses of the 3-month recurrence rates for the patients showed that 71% to 87% were recurrence free in each quarter.
Herpes Zoster Infections
In a double-blind, placebo-controlled study of immunocompetent patients with localized cutaneous zoster infection, acyclovir (800 mg 5 times daily for 10 days) shortened the times to lesion scabbing, healing, and complete cessation of pain, and reduced the duration of viral shedding and the duration of new lesion formation.
In a similar double-blind, placebo-controlled study, acyclovir (800 mg 5 times daily for 7 days) shortened the times to complete lesion scabbing, healing, and cessation of pain; reduced the duration of new lesion formation; and reduced the prevalence of localized zoster-associated neurologic symptoms (paresthesia, dysesthesia, or hyperesthesia).
Treatment was begun within 72 hours of rash onset and was most effective if started within the first 48 hours.
Adults greater than 50 years of age showed greater benefit.
Chickenpox
Three randomized, double-blind, placebo-controlled trials were conducted in 993 pediatric patients aged 2 to 18 years with chickenpox. All patients were treated within 24 hours after the onset of rash. In 2 trials, acyclovir was administered at 20 mg/kg 4 times daily (up to 3,200 mg per day) for 5 days. In the third trial, doses of 10, 15, or 20 mg/kg were administered 4 times daily for 5 to 7 days. Treatment with acyclovir shortened the time to 50% healing; reduced the maximum number of lesions; reduced the median number of vesicles; decreased the median number of residual lesions on day 28; and decreased the proportion of patients with fever, anorexia, and lethargy by day 2. Treatment with acyclovir did not affect varicella-zoster virus-specific humoral or cellular immune responses at 1 month or 1 year following treatment.
Indications and Usage for Acyclovir Oral Suspension
Herpes Zoster Infections
Acyclovir is indicated for the acute treatment of herpes zoster (shingles).
Genital Herpes
Acyclovir is indicated for the treatment of initial episodes and the management of recurrent episodes of genital herpes.
Chickenpox
Acyclovir is indicated for the treatment of chickenpox (varicella).
Contraindications
Acyclovir is contraindicated for patients who develop hypersensitivity to acyclovir or valacyclovir.
Warnings
Acyclovir Oral Suspension is intended for oral ingestion only. Renal failure, in some cases resulting in death, has been observed with acyclovir therapy (see
ADVERSE REACTIONS: Observed During Clinical Practice and
OVERDOSAGE). Thrombotic thrombocytopenic purpura/hemolytic uremic syndrome (TTP/HUS), which has resulted in death, has occurred in immunocompromised patients receiving acyclovir therapy.
Precautions
Dosage adjustment is recommended when administering acyclovir to patients with renal impairment (see
DOSAGE AND ADMINISTRATION). Caution should also be exercised when administering acyclovir to patients receiving potentially nephrotoxic agents since this may increase the risk of renal dysfunction and/or the risk of reversible central nervous system symptoms such as those that have been reported in patients treated with intravenous acyclovir. Adequate hydration should be maintained.
Information for Patients
Patients are instructed to consult with their physician if they experience severe or troublesome adverse reactions, they become pregnant or intend to become pregnant, they intend to breastfeed while taking orally administered acyclovir, or they have any other questions.Patients should be advised to maintain adequate hydration.
Herpes Zoster
There are no data on treatment initiated more than 72 hours after onset of the zoster rash. Patients should be advised to initiate treatment as soon as possible after a diagnosis of herpes zoster.
Genital Herpes Infections
Patients should be informed that acyclovir is not a cure for genital herpes. There are no data evaluating whether acyclovir will prevent transmission of infection to others. Because genital herpes is a sexually transmitted disease, patients should avoid contact with lesions or intercourse when lesions and/or symptoms are present to avoid infecting partners. Genital herpes can also be transmitted in the absence of symptoms through asymptomatic viral shedding. If medical management of a genital herpes recurrence is indicated, patients should be advised to initiate therapy at the first sign or symptom of an episode.
Chickenpox
Chickenpox in otherwise healthy children is usually a self-limited disease of mild to moderate severity. Adolescents and adults tend to have more severe disease. Treatment was initiated within 24 hours of the typical chickenpox rash in the controlled studies, and there is no information regarding the effects of treatment begun later in the disease course.
Drug Interactions
See
CLINICAL PHARMACOLOGY: Pharmacokinetics.
Carcinogenesis, Mutagenesis, Impairment of Fertility
The data presented below include references to peak steady-state plasma acyclovir concentrations observed in humans treated with 800 mg given orally 5 times a day (dosing appropriate for treatment of herpes zoster) or 200 mg given orally 5 times a day (dosing appropriate for treatment of genital herpes). Plasma drug concentrations in animal studies are expressed as multiples of human exposure to acyclovir at the higher and lower dosing schedules (see
CLINICAL PHARMACOLOGY: Pharmacokinetics).
Acyclovir was tested in lifetime bioassays in rats and mice at single daily doses of up to 450 mg/kg administered by gavage. There was no statistically significant difference in the incidence of tumors between treated and control animals, nor did acyclovir shorten the latency of tumors. Maximum plasma concentrations were 3 to 6 times human levels in the mouse bioassay and 1 to 2 times human levels in the rat bioassay.
Acyclovir was tested in 16
in vitro and
in vivo genetic toxicity assays. Acyclovir was positive in 5 of the assays.
Acyclovir did not impair fertility or reproduction in mice (450 mg/kg/day, p.o.) or in rats (25 mg/kg/day, s.c.). In the mouse study, plasma levels were 9 to 18 times human levels, while in the rat study, they were 8 to 15 times human levels. At higher doses (50 mg/kg/day, s.c.) in rats and rabbits (11 to 22 and 16 to 31 times human levels, respectively) implantation efficacy, but not litter size, was decreased. In a rat peri- and post-natal study at 50 mg/kg/day, s.c., there was a statistically significant decrease in group mean numbers of corpora lutea, total implantation sites, and live fetuses.
No testicular abnormalities were seen in dogs given 50 mg/kg/day, IV for 1 month (21 to 41 times human levels) or in dogs given 60 mg/kg/day orally for 1 year (6 to 12 times human levels). Testicular atrophy and aspermatogenesis were observed in rats and dogs at higher dose levels.
Pregnancy
Acyclovir administered during organogenesis was not teratogenic in the mouse (450 mg/kg/day, p.o.), rabbit (50 mg/kg/day, s.c. and IV), or rat (50 mg/kg/day, s.c.). These exposures resulted in plasma levels 9 and 18, 16 and 106, and 11 and 22 times, respectively, human levels.
There are no adequate and well-controlled studies in pregnant women. A prospective epidemiologic registry of acyclovir use during pregnancy was established in 1984 and completed in April 1999.There were 749 pregnancies followed in women exposed to systemic acyclovir during the first trimester of pregnancy resulting in 756 outcomes. The occurrence rate of birth defects approximates that found in the general population. However, the small size of the registry is insufficient to evaluate the risk for less common defects or to permit reliable or definitive conclusions regarding the safety of acyclovir in pregnant women and their developing fetuses. Acyclovir should be used during pregnancy only if the potential benefit justifies the potential risk to the fetus.
Nursing Mothers
Acyclovir concentrations have been documented in breast milk in 2 women following oral administration of acyclovir and ranged from 0.6 to 4.1 times corresponding plasma levels. These concentrations would potentially expose the nursing infant to a dose of acyclovir up to 0.3 mg/kg/day. Acyclovir should be administered to a nursing mother with caution and only when indicated.
Pediatric Use
Safety and effectiveness of oral formulations of acyclovir in pediatric patients younger than 2 years of age have not been established.
Geriatric Use
Of 376 subjects who received acyclovir in a clinical study of herpes zoster treatment in immunocompetent subjects≥50 years of age, 244 were 65 and over while 111 were 75 and over. No overall differences in effectiveness for time to cessation of new lesion formation or time to healing were reported between geriatric subjects and younger adult subjects. The duration of pain after healing was longer in patients 65 and over. Nausea, vomiting, and dizziness were reported more frequently in elderly subjects. Elderly patients are more likely to have reduced renal function and require dose reduction. Elderly patients are also more likely to have renal or CNS adverse events. With respect to CNS adverse events observed during clinical practice, somnolence, hallucinations, confusion, and coma were reported more frequently in elderly patients (see
CLINICAL PHARMACOLOGY,
ADVERSE REACTIONS: Observed During Clinical Practice, and
DOSAGE AND ADMINISTRATION).
Adverse Reactions/Side Effects
Herpes Simplex
Short-Term Administration
The most frequent adverse events reported during clinical trials of treatment of genital herpes with acyclovir 200 mg administered orally 5 times daily every 4 hours for 10 days were nausea and/or vomiting in 8 of 298 patient treatments (2.7%). Nausea and/or vomiting occurred in 2 of 287 (0.7%) patients who received placebo.
Long-Term Administration
The most frequent adverse events reported in a clinical trial for the prevention of recurrences with continuous administration of 400 mg (two 200-mg capsules) 2 times daily for 1 year in 586 patients treated with acyclovir were nausea (4.8%) and diarrhea (2.4%). The 589 control patients receiving intermittent treatment of recurrences with acyclovir for 1 year reported diarrhea (2.7%), nausea (2.4%), and headache (2.2%).
Herpes Zoster
The most frequent adverse event reported during 3 clinical trials of treatment of herpes zoster (shingles) with 800 mg of oral acyclovir 5 times daily for 7 to 10 days in 323 patients was malaise (11.5%). The 323 placebo recipients reported malaise (11.1%).
Chickenpox
The most frequent adverse event reported during 3 clinical trials of treatment of chickenpox with oral acyclovir at doses of 10 to 20 mg/kg 4 times daily for 5 to 7 days or 800 mg 4 times daily for 5 days in 495 patients was diarrhea (3.2%). The 498 patients receiving placebo reported diarrhea (2.2%).
Observed During Clinical Practice
In addition to adverse events reported from clinical trials, the following events have been identified during post-approval use of acyclovir. Because they are reported voluntarily from a population of unknown size, estimates of frequency cannot be made. These events have been chosen for inclusion due to either their seriousness, frequency of reporting, potential causal connection to acyclovir, or a combination of these factors.
General: Anaphylaxis, angioedema, fever, headache, pain, peripheral edema.
Nervous: Aggressive behavior, agitation, ataxia, coma, confusion, decreased consciousness, delirium, dizziness, dysarthria, encephalopathy, hallucinations, paresthesia, psychosis, seizure, somnolence, tremors. These symptoms may be marked, particularly in older adults or in patients with renal impairment (see
PRECAUTIONS).
Digestive: Diarrhea, gastrointestinal distress, nausea.
Hematologic and Lymphatic: Anemia, leukocytoclastic vasculitis, leukopenia, lymphadenopathy, thrombocytopenia.
Hepatobiliary Tract and Pancreas: Elevated liver function tests, hepatitis, hyperbilirubinemia, jaundice.
Musculoskeletal: Myalgia.
Skin: Alopecia, erythema multiforme, photosensitive rash, pruritus, rash, Stevens-Johnson syndrome, toxic epidermal necrolysis, urticaria.
Special Senses: Visual abnormalities.
Urogenital: Renal failure, renal pain (may be associated with renal failure), elevated blood urea nitrogen, elevated creatinine, hematuria (see
WARNINGS).
Overdosage
Overdoses involving ingestion of up to 100 capsules (20 g) have been reported. Adverse events that have been reported in association with overdosage include agitation, coma, seizures, and lethargy.Precipitation of acyclovir in renal tubules may occur when the solubility (2.5 mg/mL) is exceeded in the intratubular fluid. Overdosage has been reported following bolus injections or inappropriately high doses and in patients whose fluid and electrolyte balance were not properly monitored. This has resulted in elevated BUN and serum creatinine and subsequent renal failure. In the event of acute renal failure and anuria, the patient may benefit from hemodialysis until renal function is restored (see
DOSAGE AND ADMINISTRATION).
Acyclovir Oral Suspension Dosage and Administration
Acute Treatment of Herpes Zoster
800 mg every 4 hours orally, 5 times daily for 7 to 10 days.
Genital Herpes
Treatment of Initial Genital Herpes
200 mg every 4 hours, 5 times daily for 10 days.
Chronic Suppressive Therapy for Recurrent Disease
400 mg 2 times daily for up to 12 months, followed by re-evaluation. Alternative regimens have included doses ranging from 200 mg 3 times daily to 200 mg 5 times daily.
The frequency and severity of episodes of untreated genital herpes may change over time. After 1 year of therapy, the frequency and severity of the patient’s genital herpes infection should be re-evaluated to assess the need for continuation of therapy with acyclovir.
Intermittent Therapy
200 mg every 4 hours, 5 times daily for 5 days. Therapy should be initiated at the earliest sign or symptom (prodrome) of recurrence.
Treatment of Chickenpox
Children (2 years of age and older)
20 mg/kg per dose orally 4 times daily (80 mg/kg/day) for 5 days. Children over 40 kg should receive the adult dose for chickenpox.
Adults and Children over 40 kg
800 mg 4 times daily for 5 days.
Intravenous acyclovir is indicated for the treatment of varicella-zoster infections in immunocompromised patients.
When therapy is indicated, it should be initiated at the earliest sign or symptom of chickenpox. There is no information about the efficacy of therapy initiated more than 24 hours after onset of signs and symptoms.
Patients with Acute or Chronic Renal Impairment
In patients with renal impairment, the dose of Acyclovir Capsules, Tablets, or Oral Suspension should be modified as shown in Table 3.
| Normal Dosage Regimen |
Creatinine
Clearance (mL/min/1.73 m 2) |
Adjusted Dosage Regimen | |
| Dose (mg) | Dosing Interval | ||
| 200 mg every 4 hours | > 10
0-10 |
200
200 |
every 4 hours, 5x daily every 12 hours |
| 400 mg every 12 hours | > 10
0-10 |
400
200 |
every 12 hours
every 12 hours |
| 800 mg every 4 hours | > 25
10-25 0-10 |
800
800 800 |
every 4 hours, 5x daily
every 8 hours every 12 hours |
Hemodialysis
For patients who require hemodialysis, the mean plasma half-life of acyclovir during hemodialysis is approximately 5 hours. This results in a 60% decrease in plasma concentrations following a 6-hour dialysis period. Therefore, the patient’s dosing schedule should be adjusted so that an additional dose is administered after each dialysis.
Peritoneal Dialysis
No supplemental dose appears to be necessary after adjustment of the dosing interval.
Bioequivalence of Dosage Forms
Acyclovir Oral Suspension was shown to be bioequivalent to Acyclovir Capsules (n = 20) and 1 Acyclovir 800-mg tablet was shown to be bioequivalent to 4 Acyclovir 200-mg capsules (n = 24).
How is Acyclovir Oral Suspension supplied
Acyclovir Oral Suspension contains 200 mg of acyclovir, USP in each teaspoonful (5 mL). White to off-white, banana flavored suspension is available as follows:
NDC 72888-079-17
HDPE bottle (473 mL)
Store at 15° to 25°C (59° to 77°F). Protect from light.
All trademarks are the property of their respective owners.
Distributed by:
Advagen Pharma Ltd
666 Plainsboro Road
Suite 605 Plainsboro, NJ 08536, USA.
Revision: 01/2021
PRINCIPAL DISPLAY PANEL
Acyclovir Oral Suspension,USP 200 mg — NDC 72888-079-17 — 473mL Bottle
| ACYCLOVIR acyclovir suspension |
|||||||||||||||||
|
|||||||||||||||||
|
|||||||||||||||||
|
|||||||||||||||||
|
|||||||||||||||||
|
|||||||||||||||||
|
Labeler — Advagen Pharma Limited
(051627256)
| Establishment | |||
| Name | Address | ID/FEI | Business Operations |
|---|---|---|---|
| Delpharm Montreal Inc. | 203565379 | manufacture(72888-079) , analysis(72888-079) , label(72888-079) , pack(72888-079) |
Frequently asked questions
- Can you drink alcohol while taking acyclovir?
- What would be the benefits of taking valacyclovir vs acyclovir?
Medical Disclaimer
Ацикловир Дж (Aciclovir J)
💊 Состав препарата Ацикловир Дж
✅ Применение препарата Ацикловир Дж
Описание активных компонентов препарата
Ацикловир Дж
(Aciclovir J)
Приведенная научная информация является обобщающей и не может быть использована для принятия
решения о возможности применения конкретного лекарственного препарата.
Дата обновления: 2021.05.20
Владелец регистрационного удостоверения:
Лекарственные формы
| Ацикловир Дж |
Лиофилизат д/пригот. р-ра д/инф. 250 мг: фл. 1, 5 или 10 шт. рег. №: ЛП-006384 |
|
|
Лиофилизат д/пригот. р-ра д/инф. 500 мг: фл. 1, 5 или 10 шт. рег. №: ЛП-006384 |
||
|
Лиофилизат д/пригот. р-ра д/инф. 1000 мг: фл. 1, 5 или 10 шт. рег. №: ЛП-006384 |
Форма выпуска, упаковка и состав
препарата Ацикловир Дж
Лиофилизат для приготовления раствора для инфузий от белого до светло-желтого цвета; комкование порошка допускается.
Вспомогательные вещества: натрия гидроксид — от 41.25 до 48.75 мг.
флаконы — пачки картонные.
флаконы (5) — пачки картонные.
флаконы (10) — пачки картонные.
Лиофилизат для приготовления раствора для инфузий от белого до светло-желтого цвета; комкование порошка допускается.
Вспомогательные вещества: натрия гидроксид — от 41.25 до 48.75 мг.
флаконы — пачки картонные.
флаконы (5) — пачки картонные.
флаконы (10) — пачки картонные.
Лиофилизат для приготовления раствора для инфузий от белого до светло-желтого цвета; комкование порошка допускается.
Вспомогательные вещества: натрия гидроксид — от 41.25 до 48.75 мг.
флаконы — пачки картонные.
флаконы (5) — пачки картонные.
флаконы (10) — пачки картонные.
Фармакологическое действие
Противовирусное средство, синтетический аналог пуринового нуклеозида.
Обладает способностью ингибировать in vitro и in vivo вирус Herpes simplex типов 1 и 2, вирус Varicella zoster, вирус Эпштейна-Барр, цитомегаловирус. В культуре клеток ацикловир обладает наиболее выраженной противовирусной активностью в отношении вируса Herpes simplex типа 1, далее в порядке убывания активности следуют: вирус Herpes типа 2, вирус Varicella zoster, вирус Эпштейна-Барр и цитомегаловирус. Ингибирующее действие ацикловира на данные вирусы характеризуется высокой избирательностью.
Ацикловир не является субстратом для фермента тимидинкиназы неинфицированных клеток, поэтому ацикловир малотоксичен для клеток млекопитающих. Высокая избирательность действия и низкая токсичность для человека обусловлены отсутствием необходимого фермента для образования ацикловира трифосфата в интактных клетках макроорганизма.
Тимидинкиназа клеток, инфицированных вирусами Herpes simplex типов 1 и 2, вирус Varicella zoster, вирус Эпштейна-Барр или цитомегаловирусом, превращает ацикловир в ацикловир монофосфат — аналог нуклеозида, который затем последовательно превращается в дифосфат и трифосфат над действием клеточных ферментов. Ацикловира трифосфат встраивается в цепочку вирусной ДНК и блокирует ее синтез посредством конкурентного ингибирования вирусной ДНК-полимеразы. Таким образом, формируется «дефектная» вирусная ДНК, что приводит к подавлению репликации новых поколений вирусов.
Фармакокинетика
Ацикловир широко распределяется в тканях и жидких средах организма. Связывание с белками плазмы составляет 9-33%. Концентрация в спинномозговой жидкости составляет около 50% соответствующей концентрации в плазме крови в равновесном состоянии. У взрослых после в/в введения конечный Т1/2 составляет около 2.9 ч. У новорожденных (от 0 до 3 месяцев) при введении ацикловира в дозе 10 мг/кг в виде инфузии в течение 1 ч каждые 8 ч конечный Т1/2 — около 3.8 ч. Выводится преимущественно с мочой в неизмененном виде. Единственным известным метаболитом в моче является 9-[(карбоксиметокси)метил]гуанин, который составляет 10-15% выделяемой с мочой дозы.
Показания активных веществ препарата
Ацикловир Дж
Лечение инфекций, вызванных вирусом Herpes simplex типов 1 и 2; профилактика инфекций, вызванных вирусом вирусом Herpes simplex типов 1 и 2, у пациентов с иммунодефицитом; лечение инфекций, вызванных вирусом Varicella zoster, в т.ч ветряной оспы и опоясывающего герпеса; лечение инфекций, вызванных вирусом Herpes simplex типов 1 и 2, у новорожденных; профилактика цитомегаловирусной инфекции у реципиентов трансплантатов костного мозга.
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Вводят в виде медленной в/в инфузии. Режим дозирования подбирают в зависимости от диагноза, тяжести течения заболевания, возраста и массы тела пациента. Длительность курса лечения может изменяться в зависимости от локализации инфекции, состояния пациента и ответа на терапию.
Побочное действие
Со стороны системы кроветворения: нечасто — анемия, лейкопения, тромбоцитопения.
Со стороны иммунной системы: очень редко — анафилаксия.
Со стороны нервной системы: очень редко — головная боль, головокружение, возбуждение, спутанность сознания, тремор, атаксия, дизартрия, галлюцинации, психотические симптомы, судороги, сонливость, энцефалопатия, кома.
Со стороны сердечно-сосудистой системы: часто — флебит.
Со стороны дыхательной системы: очень редко — одышка.
Со стороны пищеварительной системы: часто — тошнота, рвота; очень редко — диарея, боль в животе.
Со стороны печени: часто — преходящее повышение активности печеночных трансаминаз; очень редко — преходящее повышение концентрации билирубина, желтуха, гепатит.
Со стороны кожи и подкожных тканей: часто — зуд, крапивница, сыпь (в т.ч. фотосенсибилизация); очень редко — ангионевротический отек.
Со стороны мочевыделительной системы: часто — повышение концентрации мочевины и креатинина в крови; очень редко — нарушение функции почек, острая почечная недостаточность, почечная колика.
Прочие: очень редко — общая слабость, лихорадка, местные воспалительные реакции. При случайном введении ацикловира во внеклеточное пространство при в/в инфузии были выявлены тяжелые местные воспалительные реакции, что может привести к деструктивным изменениям кожи.
Противопоказания к применению
Повышенная чувствительность к ацикловиру, валацикловиру.
С осторожностью: беременность, период грудного вскармливания, пожилой возраст, почечная недостаточность, дегидратация, одновременное применение с другими нефротоксичными препаратами.
Применение при беременности и кормлении грудью
При беременности возможно применение в тех случаях, когда предполагаемая польза для матери превышает потенциальный риск для плода.
Следует соблюдать осторожность при применении ацикловира у кормящих женщин.
Применение при нарушениях функции почек
С осторожностью следует назначать ацикловир пациентам с почечной недостаточностью.
Применение у детей
Возможно применение у детей строго по показаниям, в рекомендуемых соответственно возрасту дозах и схемах.
Применение у пожилых пациентов
Необходимо учитывать вероятность нарушения функции почек у пациентов пожилого возраста, доза должна быть скорректирована в соответствии со степенью нарушения функции почек.
Особые указания
Следует поддерживать надлежащий уровень гидратации организма у пациентов, получающих ацикловир внутривенно.
Риск развития почечной недостаточности увеличивается при одновременном применении с другими нефротоксичными препаратами.
Ацикловир выводится с мочой, поэтому у пациентов с нарушением функции почек следует применять сниженные дозы ацикловира. У пожилых пациентов возможно снижение функции почек, поэтому следует оценивать необходимость уменьшения дозы ацикловира для данной группы пациентов. Как у пациентов пожилого возраста, так и у пациентов с нарушением функции почек повышается риск развития нежелательных реакций со стороны ЦНС, поэтому такие пациенты должны находиться под тщательным медицинским контролем для своевременного выявления соответствующих симптомов.
У пациентов, получающих более высокие дозы ацикловира (например, при герпетическом энцефалите), следует тщательно контролировать функцию почек, особенно на фоне обезвоживания или уже имеющегося нарушения функции почек.
Длительные или повторные курсы лечения ацикловиром у пациентов с выраженным иммунодефицитом могут привести к появлению штаммов вируса с пониженной чувствительностью к ацикловиру, которые не ответят на продолжение терапии ацикловиром.
Лекарственное взаимодействие
Следует соблюдать осторожность при совместном назначении с препаратами, конкурирующими с ацикловиром за путь выведения, вследствие возможного повышения в плазме крови концентрации одного или обоих препаратов, либо их метаболитов.
Увеличение AUC ацикловира и неактивного метаболита микофенолата мофетила — иммуносупрессивного средства, применяемого у пациентов после трансплантации, наблюдалось при одновременном применении лекарственных препаратов, содержащих данные вещества.
Необходимо соблюдать осторожность (и проводить мониторинг изменения функции почек) при в/в инфузии ацикловира совместно с лекарственными препаратами, которые влияют на другие аспекты физиологии почек (например, циклоспорин, такролимус).
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Лекарственная форма Ацикловир: суспензия для приема внутрь
Лекарственная форма суспензия для приема внутрь Ацикловир
Описание лекарственной формы суспензия для приема внутрь Ацикловир
Фармакологическое действие суспензия для приема внутрь Ацикловир
Противовирусный препарат — синтетический аналог нуклеозида тимидина. В инфицированных клетках, содержащих вирусную тимидинкиназу, происходит фосфорилирование и превращение в ацикловира монофосфат. Под влиянием гуанилатциклазы ацикловира монофосфат преобразуется в дифосфат и под действием нескольких клеточных ферментов — в трифосфат. Высокая избирательность действия и низкая токсичность для человека обусловлены отсутствием необходимого фермента для образования ацикловира трифосфата в интактных клетках макроорганизма.
Ацикловира трифосфат, «встраиваясь» в синтезируемую вирусом ДНК, блокирует размножение вируса. Специфичность и весьма высокая селективость действия также обусловлены преимущественным его накоплением в клетках, пораженных вирусом герпеса. Высокоактивен в отношении вируса Herpes simplex 1 и 2 типа; вируса, вызывающего ветряную оспу и опоясывающий лишай (Varicella zoster); вируса Эпштейна-Барр (виды вирусов указаны в порядке возрастания величины МПК ацикловира). Умеренно активен в отношении ЦМВ.
При герпесе предупреждает образование новых элементов сыпи, снижает вероятность кожной диссеминации и висцеральных осложнений, ускоряет образование корок, снижает боль в острой фазе опоясывающего герпеса. Оказывает иммуностимулирующее действие.
Фармакокинетика суспензия для приема внутрь Ацикловир
После приема внутрь частично всасывается в кишечнике, из-за низкой липофильности абсорбция после перорального приема 200 мг — 20% (15-30%), однако при этом создаются дозозависимые концентрации, достаточные для эффективного лечения вирусных заболеваний. Пища не оказывает значительного влияния на всасывание ацикловира.
Cmax после назначения внутрь 200 мг 5 раз в сутки — 0.7 мкг/мл, Cmin — 0.4 мкг/мл. TCmax — 1.5-2 ч.
Cmax после в/в капельного введения в течение 1 ч в дозе 2.5, 5 и 10 мг/кг — 5.1, 9.8 и 20.7 мкг/мл соответственно; Cmin через 7 ч — 0.5, 0.7 и 2.3 мкг/мл соответственно.
Cmax и Cmin при назначении ацикловира детям старше 1 года в дозе 250 и 500 мг/кв.м такие же, как у взрослых при назначении в дозе 5 и 10 мг/кг.
У новорожденных и младенцев в возрасте до 3 мес при введении ацикловира в дозе 10 мг/кг в/в капельно в течение 1 ч 3 раза в сутки Cmax — 13.8 мкг/мл, Cmin — 2.3 мкг/мл.
Проникает через ГЭБ и плацентарный барьер, выделяется с грудным молоком. Хорошо проникает в органы и ткани (в т.ч. головной мозг, почки, легкие, печень, водянистую влагу, слезную жидкость, кишечник, мышцы, селезенку, грудное молоко, матку, слизистую оболочку и секрет влагалища, сперму, амниотическую жидкость, содержимое герпетических пузырьков); концентрация в СМЖ — 50% от таковой в крови. После приема внутрь 1 г/сут концентрация в грудном молоке — 60-410% от его концентрации в плазме (в организм ребенка с молоком матери ацикловир поступает в дозе 0.3 мг/кг/сут).
Связь с белками плазмы — 9-33%.
Метаболизируется в печени с образованием метаболита — 9-карбоксиметоксиметилгуанина. Выводится почками путем клубочковой фильтрации и канальцевой секреции: при приеме внутрь — 14% в неизмененном виде, при в/в введении — 45-79% в неизмененном виде. Менее 2% выводятся через ЖКТ; следовые количества определяются в выдыхаемом воздухе.
При однократном сеансе гемодиализа в течение 6 ч концентрация ацикловира в плазме уменьшается примерно на 60%; при перитонеальном диализе клиренс ацикловира значительно не изменяется. Скорость выведения с возрастом замедляется, но T1/2 активного препарата увеличивается незначительно.
T1/2 при приеме внутрь у взрослых — 3.3 ч. T1/2 после в/в введения у взрослых — 2.9 ч, у детей до 3 мес — 3.8 ч (при введении в/в капельно 10 мг/кг в течение 1 ч 3 раза в сутки), у детей и подростков от 1 года до 18 лет — 2.6 ч.
У больных с тяжелой ХПН T1/2 — 20 ч, при гемодиализе — 5.7 ч (при этом концентрация ацикловира в плазме уменьшается до 60% от исходного значения).
T1/2 при почечной недостаточности (у взрослых в зависимости от значений КК): при КК 80 мл/мин — 2.5 ч, 50-80 мл/мин — 3 ч, 15-50 мл/мин — 3.5 ч; при анурии — 19.5 ч, во время проведения гемодиализа — 5.7, при постоянном амбулаторном перитонеальном диализе — 14-18 ч.
С осторожностью суспензия для приема внутрь Ацикловир
Беременность, период лактации.
Для в/в введения (дополнительно) — почечная недостаточность (риск нефротоксического действия), дегидратация, неврологические нарушения или неврологические реакции на прием цитотоксичных ЛС (в т.ч. в анамнезе).
Режим дозирования суспензия для приема внутрь Ацикловир
Внутрь, в/в капельно.
Для профилактики рецидивов Herpes simplex пациентам с иммунодефицитом назначают по 200 мг 4 раза в сутки каждые 6 ч. В случае выраженного иммунодефицита (после трансплантации костного мозга или при нарушении всасывания из кишечника) — 400 мг 5 раз в сутки.
Детям старше 6 лет — по 800 мг 4 раза в сутки; 2-6 лет — по 400 мг 4 раза в сутки; младше 2 лет — по 200 мг 4 раза в сутки. Более точно дозу можно определить из расчета 20 мг/кг, но не более чем по 800 мг 4 раза в сутки. Курс лечения — 5 дней.
Детям от 3 мес до 12 лет дозу для в/в введения определяют исходя из площади тела: инфекции, вызванные вирусом Herpes simplex, — 250 мг/кв.м поверхности тела каждые 8 ч; сниженный иммунитет, герпетический энцефалит, ветряная оспа, опоясывающий лишай — 500 мг/кв.м.
Внутрь. Генитальный герпес: начальная терапия — по 200 мг каждые 4 ч в период бодрствования, 5 раз в сутки в течение 10 дней;
рецидивирующий генитальный герпес (менее 6 эпизодов в год), прерывистая терапия — по 200 мг каждые 4 ч в период бодрствования, 5 раз в сутки в течение 5 дней;
рецидивирующий генитальный герпес (более 6 эпизодов в год), длительная подавляющая терапия — по 400 мг 2 раза в день или по 200 мг 3-5 раз в сутки.
Простой герпес кожи и слизистых оболочек (лечение): по 200-400 мг 5 раз в сутки в течение 10 дней у пациентов с нарушением иммунитета.
Простой герпес кожи и слизистых оболочек (профилактика): по 400 мг каждые 12 ч.
Опоясывающий герпес: по 800 мг каждые 4 ч в период бодрствования, 5 раз в сутки в течение 7-10 дней.
Ветряная оспа: по 800 мг 4 раза в сутки, в течение 5 дней. Лечение необходимо начинать при появлении самых ранних признаков или симптомов ветряной оспы.
При ХПН необходима коррекция дозы в зависимости от величины КК и необходимого режима дозирования при нормальной функции почек: нормальная функция почек и ХПН с КК более 10 мл/мин — 200 мг каждые 4 ч, 5 раз в день КК менее 10 мл/мин — 200 мг каждые 12 ч;
нормальная функция почек, ХПН с КК более 10 мл/мин — 400 мг каждые 12 ч, при КК менее 10 мл/мин — 200 мг каждые 12 ч;
нормальная функция почек, ХПН с КК более 25 мл/мин — 800 мг каждые 4 ч в период бодрствования, 5 раз в сутки, Кк 10-25 мл/мин — 800 мг каждые 8 ч, КК менее 10 мл/мин — 800 мг каждые 12 ч.
Дети до 2 лет — доза не определена. Однако при изучении препарата никакого необычного токсического действия или специфических педиатрических проблем у детей, получавших ацикловир в дозах до 3 г/кв.м и 80 мг/кг в сутки, не выявлено.
Дети 2-12 лет, с массой тела до 40 кг, при ветряной оспе: внутрь, по 20 мг/кг, до 800 мг на дозу, 4 раза в сутки в течение 5 дней.
Дети 2-12 лет, с массой тела 40 кг и более, при ветряной оспе: доза для взрослых.
В/в капельно (вводят с постоянной скоростью по крайней мере в течение 1 ч).
Тяжелый генитальный герпес, начальная терапия: взрослые и дети старше 12 лет — по 5 мг/кг каждые 8 ч в течение 5 дней; дети до 12 лет — по 250 мг/кв.м каждые 8 ч в течение 5 дней.
Простой герпес кожи и слизистых оболочек у больных с нарушением иммунитета: взрослые и дети старше 12 лет — по 5-10 мг/кг каждые 8 ч в течение 7 дней; дети до 12 лет — 250 мг/кв.м каждые 8 ч в течение 7 дней.
Энцефалит, вызываемый вирусом Herpes simplex: взрослые и дети старше 12 лет — по 10 мг/кг каждые 8 ч в течение 10 дней; дети с 3 мес до 12 лет — 20 мг/кг каждые 8 ч в течение 10 дней.
Опоясывающий герпес у больных с нарушением иммунитета: взрослые и дети старше 12 лет — по 10 мг/кг каждые 8 ч в течение 7 дней; дети до 12 лет — по 20 мг/кг каждые 8 ч в течение 7 дней.
Генерализованная инфекция у новорожденных, вызываемая вирусом Herpes simplex: новорожденные и дети до 3 мес — по 10 мг/кг каждые 8 ч в течение 10 дней. Может быть использована доза 15-20 мг/кг каждые 8 ч, однако эффективность и безопасность применения таких доз не установлены.
При ХПН у взрослых и детей требуется снижение дозы и/или изменение интервала между введением: КК более 50 мл/мин, доза — 100%, интервал — 8 ч; КК 25-50 мл/мин, доза — 100%, интервал — 12 ч; КК 10-25 мл/мин, доза — 100%, интервал — 24 ч; КК менее 10 мл/мин, доза — 50%, интервал — 24 ч.
Максимальные дозы для взрослых при в/в введении — 30 мг/кг или 1.5 г/кв.м/сут.
Противопоказания суспензия для приема внутрь Ацикловир
Гиперчувствительность (в т.ч. к валацикловиру), детский возраст до 3 лет (для твердых ЛФ).
Показания к применению суспензия для приема внутрь Ацикловир
Лечение первичного и рецидивирующего тяжелого генитального герпеса (в т.ч. у пациентов с нарушением иммунитета) — внутрь и парентерально;
профилактика часто рецидивирующего (6 и более случаев в год) генитального герпеса (в т.ч. у пациентов с нарушением иммунитета) — внутрь;
лечение первичного и рецидивирующего простого герпеса с поражением кожи и слизистых оболочек, вызываемого вирусом Herpes simplex 1 и 2 типа, у больных с нарушением иммунитета — внутрь, парентерально;
профилактика простого герпеса у больных с нарушением иммунитета (в т.ч. после трансплантации и приеме иммуносупрессивных ЛС, ВИЧ-инфицированные пациенты, на фоне химиотерапии) — внутрь;
энцефалит, вызываемый вирусом Herpes simplex 1 и 2 типа — парентерально;
лечение опоясывающего герпеса, вызываемого вирусом Varicella zoster, у взрослых — внутрь; у больных с нарушением иммунитета и при генерализованном опоясывающем герпесе у больных с ненарушенным иммунитетом — парентерально;
профилактика опоясывающего герпеса, вызываемого вирусом Varicella zoster, после начального периода использования ацикловира для парентерального применения у всех больных с нарушением иммунитета (в т.ч. после трансплантации и при приеме иммуносупрессивных ЛС, ВИЧ-инфицированные пациенты, на фоне химиотерапии) — внутрь;
опоясывающий герпес с поражением глаз — внутрь, парентерально;
генерализованная инфекция у новорожденных, вызываемая вирусом Herpes simplex — парентерально;
ветряная оспа у больных с ненарушенным иммунитетом в течение 24 ч после появления типичной сыпи — внутрь, у больных с нарушением иммунитета — парентерально.
Побочное действие суспензия для приема внутрь Ацикловир
Анафилактические реакции, кожные аллергические реакции (зуд, сыпь, синдром Лайелла, крапивница, мультиформная экссудативная эритема, в т.ч. синдром Стивенса-Джонсона), спутанность сознания, повышение активности “печеночных” трансаминаз, лихорадка, галлюцинации, лейкопения, лимфоаденопатия, периферические отеки, нарушение зрения, головная боль.
Только для парентерального введения: флебит или воспаление в месте введения, острая почечная недостаточность, признаки энцефалопатии (кома, спутанность сознания, галлюцинации, судороги, тремор), гематологические нарушения (анемия, лейкоцитоз, нейтропения или нейтрофилез, тромбоцитопения или тромбоцитоз), гематурия, ДВС-синдром, гемолиз, снижение АД, психические расстройства (в т.ч. делирий), угнетенное состояние или психоз, нарушение функции ЖКТ (снижение аппетита, тошнота, рвота), повышение азота мочевины и гиперкреатининемия (в связи с обструкцией почечных канальцев; обычно при правильно подобранной дозе и адекватном поступлении жидкости повышения не отмечается).
Только при приеме внутрь: недомогание, нарушение функции ЖКТ (тошнота, рвота, диарея, абдоминальные боли), ажитация, алопеция, головокружение, миалгия, парестезия, сонливость.
Передозировка суспензия для приема внутрь Ацикловир
Пероральный прием 20 г ацикловира не приводил к развитию специфических симптомов.
При парентеральном применении (при болюсном введении, или использовании в высоких дозах, или у пациентов, у которых должным образом не контролировался водно-электролитный баланс): повышение азота мочевины, гиперкреатининемия, нарушение функции почек, летаргия, судороги, кома.
Лечение: поддержание жизненно важных функций, гемодиализ.
Особые указания суспензия для приема внутрь Ацикловир
Длительное или повторное лечение ацикловиром больных со сниженным иммунитетом может привести к появлению штаммов вирусов, нечувствительных к его действию. У большинства выделенных штаммов вирусов, нечувствительных к ацикловиру, обнаруживается относительная нехватка вирусной тимидинкиназы; были выделены штаммы с измененной тимидинкиназой или с измененной ДНК-полимеразой. In vitro действие ацикловира на изолированные штаммы вируса Herpes simplex может вызвать появление менее чувствительных штаммов.
Адекватных и строго контролируемых клинических исследований безопасности применения препарата в период беременности не проведено. Применение показано только в тех случаях, когда предполагаемая польза для матери превышает потенциальный риск для плода.
В ходе терапии высокими пероральными дозами препарата следует обеспечить достаточное поступление жидкости в организм пациента.
При необходимости назначения препарата в период лактации следует прекратить грудное вскармливание.
Ацикловир не предупреждает передачу герпеса половым путем, поэтому в период лечения необходимо воздерживаться от половых контактов, даже при отсутствии клинических проявлений.
Взаимодействие суспензия для приема внутрь Ацикловир
При смешивании растворов необходимо учитывать щелочную реакцию ацикловира для в/в введения (pH 11).
Усиление эффекта отмечается при одновременном назначении иммуностимуляторов.
Блокаторы канальцевой секреции снижают канальцевую секрецию в/в вводимого ацикловира, что может приводить к повышению концентрации ацикловира в сыворотке крови и СМЖ, замедлению выведения ацикловира (увеличение T1/2) из крови и СМЖ, усилению токсического действия.
Др. нефротоксические ЛС — повышение риска нефротоксического действия.